第2章 第2节 课时3 化学反应速率与化学平衡图像课件(共18张PPT)2023-2024学年上学期高二化学人教版(2019)选择性必修1
文档属性
| 名称 | 第2章 第2节 课时3 化学反应速率与化学平衡图像课件(共18张PPT)2023-2024学年上学期高二化学人教版(2019)选择性必修1 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-13 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
第二节 化学平衡
能力课时3 化学反应速率与化学平衡图像
第二章 化学反应速率与化学平衡
Ⅱ
Ⅲ
Ⅰ
T2>T1
T↑,生成物C的含量↓,平衡逆向(吸热)移动。说明正反应为放热反应。
Ⅰ
P2>P1
P↑,反应物A的转化率↓,平衡逆向(n气↓)移动。说明正反应为n气↑的反应。
Ⅱ
Ⅲ
va > vb
生成物含量不变,平衡不移动。va>vb,说明a使用了催化剂,
或反应前后n气不变的反应增大了压强。
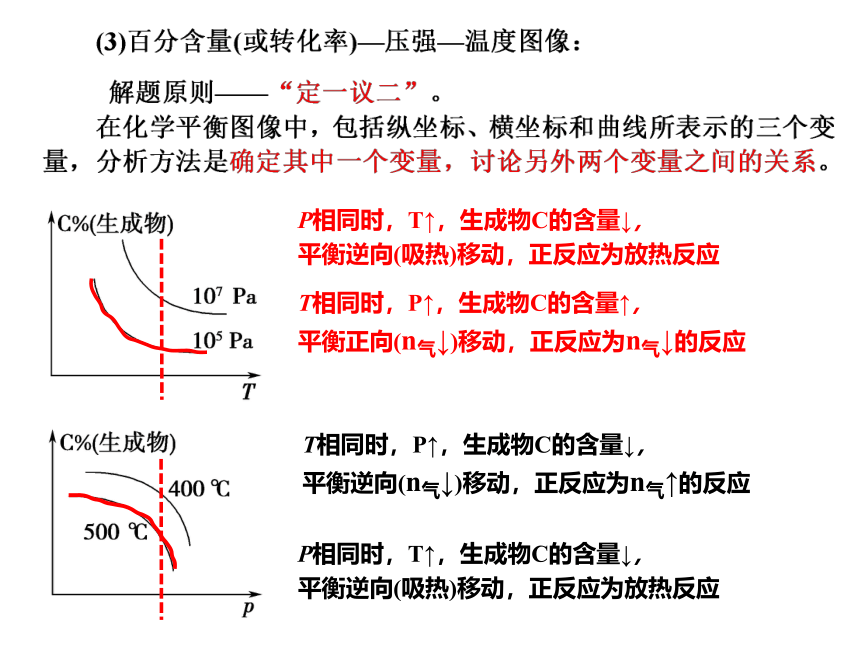
P相同时,T↑,生成物C的含量↓,
平衡逆向(吸热)移动,正反应为放热反应
T相同时,P↑,生成物C的含量↑,
平衡正向(n气↓)移动,正反应为n气↓的反应
T相同时,P↑,生成物C的含量↓,
平衡逆向(n气↓)移动,正反应为n气↑的反应
P相同时,T↑,生成物C的含量↓,
平衡逆向(吸热)移动,正反应为放热反应
T1>T2
P2>P1
mA(g)+nB(g) pC(g)+qD(g)
1.分析下列图像对应可逆反应焓变特点、计量数m+n和p+q的大小。
T
v
v逆
v正
T1
T2
T
v
v正
v逆
C%
450℃
P
A%
P1
正反应
★
正反应
★
正反应
★
m+n p+q
达标检测
T
吸热
放热
<
吸热
看图技巧:可逆反应的最大程度即化学平衡状态
0
下图是在其它条件一定时,反应2NO+O2 2NO2 △H 0 中NO 的最大转化率与温度的关系曲线。图中坐标A、B、C、D、E 5点,其中表示未达平衡状态且V正>V逆的点是 。
A
B
C
D
C点
T
NO转化率
线为平衡点
线外未平衡点
达标检测
线上所有的点都是平衡点。右上方(A点),NO转化率大于此压强时平衡体系中的NO转化率,必须逆向移动才能达到平衡状态,故A点v逆<v正;则左下方(C点)v正>v逆
交点、最高点、最低点、与x轴的平行线往往代表平衡状态
v逆
v正
C
A
P↑,生成物含量增加,平衡正向(n气↓)移动,正反应是n气↓的反应。
T↑,生成物含量减少,平衡逆向(吸热)移动,正反应是放热反应;
H2O都在生成物中
T2>T1
p1>p2
A
T1>T2 P1>P2
P↑,B%↓,平衡正向(n气↓)移动,m+n>p
T↑,B%↓,平衡正向(吸热)移动,ΔH>0
随堂评估自测
C
D
T↑,平衡逆向移动,AB%↓,v逆>v正
不符合先拐先平
P↑,平衡正向移动,AB%↑
C
使用催化剂,缩短到达平衡的时间
D
X
5.下列叙述与下图相对应的是( )
① ② ③ ④
B
v正渐变
Z
谢谢观看 THANK YOU!
第二节 化学平衡
能力课时3 化学反应速率与化学平衡图像
第二章 化学反应速率与化学平衡
Ⅱ
Ⅲ
Ⅰ
T2>T1
T↑,生成物C的含量↓,平衡逆向(吸热)移动。说明正反应为放热反应。
Ⅰ
P2>P1
P↑,反应物A的转化率↓,平衡逆向(n气↓)移动。说明正反应为n气↑的反应。
Ⅱ
Ⅲ
va > vb
生成物含量不变,平衡不移动。va>vb,说明a使用了催化剂,
或反应前后n气不变的反应增大了压强。
P相同时,T↑,生成物C的含量↓,
平衡逆向(吸热)移动,正反应为放热反应
T相同时,P↑,生成物C的含量↑,
平衡正向(n气↓)移动,正反应为n气↓的反应
T相同时,P↑,生成物C的含量↓,
平衡逆向(n气↓)移动,正反应为n气↑的反应
P相同时,T↑,生成物C的含量↓,
平衡逆向(吸热)移动,正反应为放热反应
T1>T2
P2>P1
mA(g)+nB(g) pC(g)+qD(g)
1.分析下列图像对应可逆反应焓变特点、计量数m+n和p+q的大小。
T
v
v逆
v正
T1
T2
T
v
v正
v逆
C%
450℃
P
A%
P1
正反应
★
正反应
★
正反应
★
m+n p+q
达标检测
T
吸热
放热
<
吸热
看图技巧:可逆反应的最大程度即化学平衡状态
0
下图是在其它条件一定时,反应2NO+O2 2NO2 △H 0 中NO 的最大转化率与温度的关系曲线。图中坐标A、B、C、D、E 5点,其中表示未达平衡状态且V正>V逆的点是 。
A
B
C
D
C点
T
NO转化率
线为平衡点
线外未平衡点
达标检测
线上所有的点都是平衡点。右上方(A点),NO转化率大于此压强时平衡体系中的NO转化率,必须逆向移动才能达到平衡状态,故A点v逆<v正;则左下方(C点)v正>v逆
交点、最高点、最低点、与x轴的平行线往往代表平衡状态
v逆
v正
C
A
P↑,生成物含量增加,平衡正向(n气↓)移动,正反应是n气↓的反应。
T↑,生成物含量减少,平衡逆向(吸热)移动,正反应是放热反应;
H2O都在生成物中
T2>T1
p1>p2
A
T1>T2 P1>P2
P↑,B%↓,平衡正向(n气↓)移动,m+n>p
T↑,B%↓,平衡正向(吸热)移动,ΔH>0
随堂评估自测
C
D
T↑,平衡逆向移动,AB%↓,v逆>v正
不符合先拐先平
P↑,平衡正向移动,AB%↑
C
使用催化剂,缩短到达平衡的时间
D
X
5.下列叙述与下图相对应的是( )
① ② ③ ④
B
v正渐变
Z
谢谢观看 THANK YOU!
