化学人教版(2019)选择性必修1 4.3.2金属的腐蚀(共17张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修1 4.3.2金属的腐蚀(共17张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 32.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-14 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
第1课时 金属的腐蚀
选择性必修1(人教版2019)
2023-2024学年
第四章 ·化学反应与电能
第三节 金属的腐蚀与防护
使用说明:本产品一接触空气,即开始发热。
讨论:猜测暖贴的发热原理?
与空气中的氧气反应
主要成分:铁粉、水、食盐、活性炭、蛭石(保温)。
设计实验:证明暖贴发热过程中氧气参加了反应。
活动探究一
1、气密性检验:向烧杯中加适量水浸没导管口,用双手紧握锥形瓶,若烧杯中导管口有气泡冒出,松开手后形成一小段水柱,则气密性好,否则气密性不好。
2、装入药品,连接装置,开始反应。
3、观察实验现象,并用手触摸锥形瓶底部感受温度有无变化。
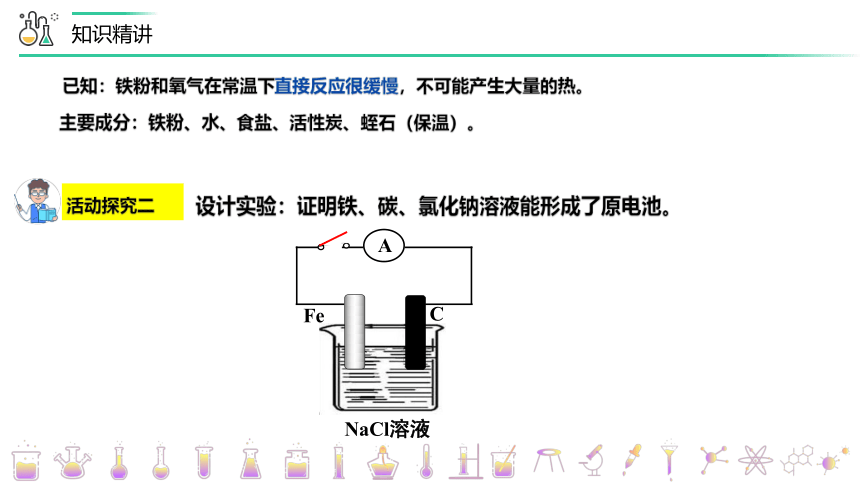
设计实验:证明铁、碳、氯化钠溶液能形成了原电池。
活动探究二
NaCl溶液
C
Fe
A
主要成分:铁粉、水、食盐、活性炭、蛭石(保温)。
已知:铁粉和氧气在常温下直接反应很缓慢,不可能产生大量的热。
写出电极反应式及总反应
Fe - 2e- === Fe2+
负极反应
正极反应
总反应式
O2 + 2H2O + 4e- === 4OH-
2Fe + O2 + 2H2O === 2Fe(OH)2
K3[Fe(CN)6] 3Fe2++ 2[Fe(CN)6]3- =Fe3 [Fe(CN)6]2 (蓝色)
酚酞 溶液有无色变为红色
,并思考如何检验产物?
Fe2+
OH-
疑惑:活动探究二的实验中O2在正极得电子放电,溶液中的H+为什么没有得电子放电生成H2?
NaCl溶液
C
Fe
A
活动探究三
如何设计实验来证明?
向正极区加入适量的稀盐酸,观察电流表的指针偏转情况有无变化。
负极(Fe):Fe - 2e- = Fe2+
正极(C):2H+ + 2e- = H2↑
总反应:Fe + 2H+ = Fe2+ + H2↑
写出电极反应式和总反应式
正极是O2放电还是H+放电由什么决定?
H+和O2在正极都想得电子放电,二者为竞争关系,当溶液中H+浓度较大即溶液显酸性时H+优先放电,当溶液中H+浓度较小即溶液显中性或碱性时O2优先放电。
将用过的暖宝宝贴片打开,可以看到其中混有红棕色的物质,你也许还看到了这些
红棕色的物质是什么?
铁锈的主要成分是
Fe2O3 xH2O
铁生锈即铁被腐蚀。
金属腐蚀的概念:金属或合金与周围接触的气体或液体进行氧化还原反应而损耗的现象。
实质:M(金属 ) ne-→Mn+(氧化反应) 如:Fe - 2e- === Fe2+
金属腐蚀的类型
(1)化学腐蚀:金属接触氧化剂(如O2、Cl2、等)而直接被氧化腐蚀的过程。
(2)电化学腐蚀:不纯的金属(或合金)接触到电解质溶液形成原电池发生原电池反应,比较活泼的金属原子失去电子而被氧化所引起的腐蚀。
两种腐蚀哪种更普遍?
两种往往同时发生,但电化学腐蚀更普遍
根据已学知识写出铁变成铁锈的主要反应式:
负极(氧化):Fe -2e- = Fe2+
正极(还原):O2 + 2H2O + 4e- = 4OH- (吸氧腐蚀)
总反应: 2Fe + O2 + 2H2O === 2Fe(OH)2 Fe + 2H+ = Fe2+ + H2↑
4Fe(OH)2+O2 +2H2O = 4Fe(OH)3
2Fe(OH)3 = Fe2O3·xH2O +(3-x)H2O
2H+ + 2e- === H2↑ (析氢腐蚀)
Fe生锈:
Fe2+
Fe2O3·xH2O
电化学
腐蚀
生活中吸氧腐蚀更普遍
武汉大学汪振道教授首创以铝—空气—海水电池为能源的新型海水标志灯已研制成功。只要把灯放入海水中,数分钟后就会发出耀眼的闪光,其能量比干电池高20—50倍。试推测此种新型电池电极反应式:
负极:_____________________________;
正极:______________________________ 。
总反应:______________________________ 。
Al -3e- = Al3+
O2 + 2H2O + 4e- = 4OH-
4Al+ 3O2 + 6H2O = 4Al(OH)3
练习:
【例1】(2021·四川郫都·高二期中)下列有关金属腐蚀的说法,正确的是
A.化学腐蚀比电化学腐蚀要普遍得多
B.化学腐蚀和电化学腐蚀不可能同时发生
C.化学腐蚀比电化学腐蚀的腐蚀速度要快得多
D.电化学腐蚀过程伴随有电流产生,而化学腐蚀过程没有
D
题型一:金属的化学腐蚀与电化学腐蚀
【例2】(2021·福建·泉州现代中学高二阶段练习)利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间,下列说法不正确的是
A.a管发生吸氧腐蚀,b管发生析氢腐蚀
B.一段时间后,a管液面高于b管液面
C.a、b处溶液的pH增大
D.a、b两处具有相同的电极反应式:Fe-3e-=Fe3+
D
题型二:析氢腐蚀与吸氧腐蚀
将所学的化学知识合理利用,可以方便生活,服务社会:
同时我们也应该认识到,化学给我们的生活也带来了很多的麻烦:
辛吉飞:“那必是科技与狠活!”
·
化学是一把双刃剑!
不仅要学好化学,更要利用好化学!
课后思考:
1、利用你所学的化学知识,怎样防止或减缓铁的腐蚀?
2、金属都会被腐蚀吗?
化学人类进步的关键!
完成知识梳理及课后练习
第1课时 金属的腐蚀
选择性必修1(人教版2019)
2023-2024学年
第四章 ·化学反应与电能
第三节 金属的腐蚀与防护
使用说明:本产品一接触空气,即开始发热。
讨论:猜测暖贴的发热原理?
与空气中的氧气反应
主要成分:铁粉、水、食盐、活性炭、蛭石(保温)。
设计实验:证明暖贴发热过程中氧气参加了反应。
活动探究一
1、气密性检验:向烧杯中加适量水浸没导管口,用双手紧握锥形瓶,若烧杯中导管口有气泡冒出,松开手后形成一小段水柱,则气密性好,否则气密性不好。
2、装入药品,连接装置,开始反应。
3、观察实验现象,并用手触摸锥形瓶底部感受温度有无变化。
设计实验:证明铁、碳、氯化钠溶液能形成了原电池。
活动探究二
NaCl溶液
C
Fe
A
主要成分:铁粉、水、食盐、活性炭、蛭石(保温)。
已知:铁粉和氧气在常温下直接反应很缓慢,不可能产生大量的热。
写出电极反应式及总反应
Fe - 2e- === Fe2+
负极反应
正极反应
总反应式
O2 + 2H2O + 4e- === 4OH-
2Fe + O2 + 2H2O === 2Fe(OH)2
K3[Fe(CN)6] 3Fe2++ 2[Fe(CN)6]3- =Fe3 [Fe(CN)6]2 (蓝色)
酚酞 溶液有无色变为红色
,并思考如何检验产物?
Fe2+
OH-
疑惑:活动探究二的实验中O2在正极得电子放电,溶液中的H+为什么没有得电子放电生成H2?
NaCl溶液
C
Fe
A
活动探究三
如何设计实验来证明?
向正极区加入适量的稀盐酸,观察电流表的指针偏转情况有无变化。
负极(Fe):Fe - 2e- = Fe2+
正极(C):2H+ + 2e- = H2↑
总反应:Fe + 2H+ = Fe2+ + H2↑
写出电极反应式和总反应式
正极是O2放电还是H+放电由什么决定?
H+和O2在正极都想得电子放电,二者为竞争关系,当溶液中H+浓度较大即溶液显酸性时H+优先放电,当溶液中H+浓度较小即溶液显中性或碱性时O2优先放电。
将用过的暖宝宝贴片打开,可以看到其中混有红棕色的物质,你也许还看到了这些
红棕色的物质是什么?
铁锈的主要成分是
Fe2O3 xH2O
铁生锈即铁被腐蚀。
金属腐蚀的概念:金属或合金与周围接触的气体或液体进行氧化还原反应而损耗的现象。
实质:M(金属 ) ne-→Mn+(氧化反应) 如:Fe - 2e- === Fe2+
金属腐蚀的类型
(1)化学腐蚀:金属接触氧化剂(如O2、Cl2、等)而直接被氧化腐蚀的过程。
(2)电化学腐蚀:不纯的金属(或合金)接触到电解质溶液形成原电池发生原电池反应,比较活泼的金属原子失去电子而被氧化所引起的腐蚀。
两种腐蚀哪种更普遍?
两种往往同时发生,但电化学腐蚀更普遍
根据已学知识写出铁变成铁锈的主要反应式:
负极(氧化):Fe -2e- = Fe2+
正极(还原):O2 + 2H2O + 4e- = 4OH- (吸氧腐蚀)
总反应: 2Fe + O2 + 2H2O === 2Fe(OH)2 Fe + 2H+ = Fe2+ + H2↑
4Fe(OH)2+O2 +2H2O = 4Fe(OH)3
2Fe(OH)3 = Fe2O3·xH2O +(3-x)H2O
2H+ + 2e- === H2↑ (析氢腐蚀)
Fe生锈:
Fe2+
Fe2O3·xH2O
电化学
腐蚀
生活中吸氧腐蚀更普遍
武汉大学汪振道教授首创以铝—空气—海水电池为能源的新型海水标志灯已研制成功。只要把灯放入海水中,数分钟后就会发出耀眼的闪光,其能量比干电池高20—50倍。试推测此种新型电池电极反应式:
负极:_____________________________;
正极:______________________________ 。
总反应:______________________________ 。
Al -3e- = Al3+
O2 + 2H2O + 4e- = 4OH-
4Al+ 3O2 + 6H2O = 4Al(OH)3
练习:
【例1】(2021·四川郫都·高二期中)下列有关金属腐蚀的说法,正确的是
A.化学腐蚀比电化学腐蚀要普遍得多
B.化学腐蚀和电化学腐蚀不可能同时发生
C.化学腐蚀比电化学腐蚀的腐蚀速度要快得多
D.电化学腐蚀过程伴随有电流产生,而化学腐蚀过程没有
D
题型一:金属的化学腐蚀与电化学腐蚀
【例2】(2021·福建·泉州现代中学高二阶段练习)利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间,下列说法不正确的是
A.a管发生吸氧腐蚀,b管发生析氢腐蚀
B.一段时间后,a管液面高于b管液面
C.a、b处溶液的pH增大
D.a、b两处具有相同的电极反应式:Fe-3e-=Fe3+
D
题型二:析氢腐蚀与吸氧腐蚀
将所学的化学知识合理利用,可以方便生活,服务社会:
同时我们也应该认识到,化学给我们的生活也带来了很多的麻烦:
辛吉飞:“那必是科技与狠活!”
·
化学是一把双刃剑!
不仅要学好化学,更要利用好化学!
课后思考:
1、利用你所学的化学知识,怎样防止或减缓铁的腐蚀?
2、金属都会被腐蚀吗?
化学人类进步的关键!
完成知识梳理及课后练习
