生物人教版(2019)必修1 2.4蛋白质是生命活动的主要承担者(共30张ppt)
文档属性
| 名称 | 生物人教版(2019)必修1 2.4蛋白质是生命活动的主要承担者(共30张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2023-10-15 00:00:00 | ||
图片预览




文档简介
(共30张PPT)
复习提问:
1、主要的能源物质 植物体内的储能物质?动物体内的储能物质?良好的储能物质?
2、组成DNA、RNA的单糖分别是什么?
3、常见的二糖的组成成分?哪些糖是还原糖?
4、组成多糖的基本单位?
5、糖原的种类及分布?
6、几丁质的化学本质?广泛分布在哪里?作用?
7、脂肪由什么形成的酯?脂肪的作用?为什么脂肪含有的能量高?
8、植物脂肪、动物脂肪分别含有哪种类型的脂肪酸?室温呈什么状态?
9、磷脂的作用?固醇包括哪些?作用分别是什么?
10、糖类与脂肪之间转化程度的差异?
11、含有C、H、O的化合物? 含有C、H、O、N、P的化合物?
2.4 蛋白质是生命活动的主要承担者
第二章 组成细胞的分子
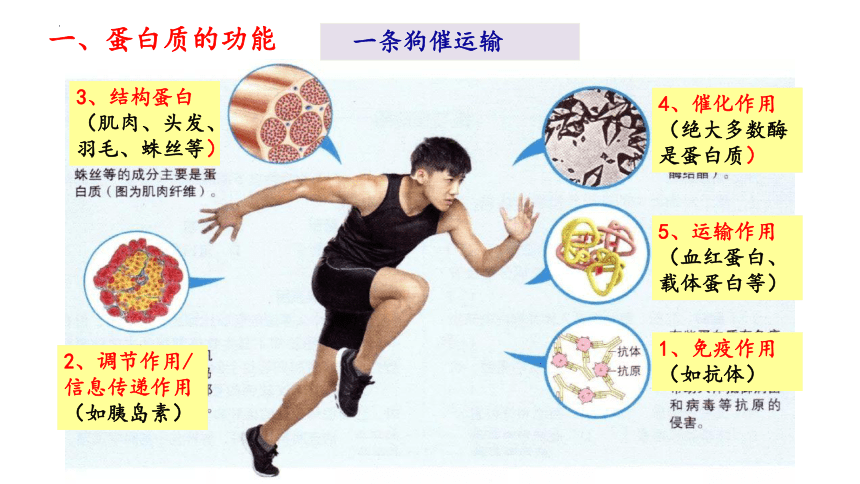
一、蛋白质的功能
3、结构蛋白(肌肉、头发、羽毛、蛛丝等)
4、催化作用(绝大多数酶是蛋白质)
5、运输作用(血红蛋白、载体蛋白等)
2、调节作用/信息传递作用(如胰岛素)
1、免疫作用(如抗体)
一条狗催运输
蛋白质分子的主要功能:
一切生命活动都离不开蛋白质,蛋白质是生命活动的主要承担者
①结构蛋白:是构成细胞和生物体的重要物质,
如肌球蛋白、肌动蛋白等
②催化蛋白:起生物催化作用,如绝大多数酶
③运输蛋白:如血红蛋白、细胞膜上的载体
④调节蛋白:如胰岛素和生长激素等
⑤免疫蛋白:免疫过程中产生的抗体
组成蛋白质的氨基酸大约有____ 种。
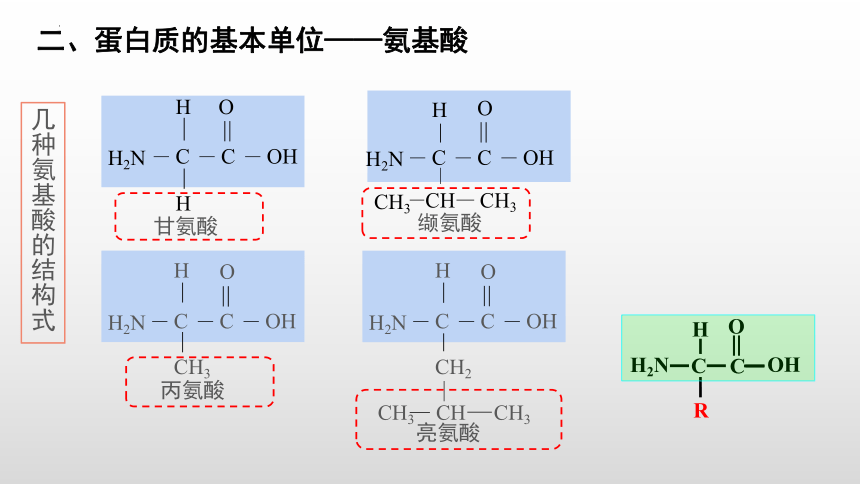
二、蛋白质的基本单位——氨基酸
2.种类:
21
必需氨基酸(8种):不能合成
非必需氨基酸(13种):能合成
3. 分类:
根据人体细胞能否合成
必须从外界获取
1.元素组成:
C、H、O、N (S、P)
巧记“8种必需氨基酸”
甲(甲硫氨酸)来(赖氨酸)写(缬氨酸)一(异亮氨酸)本(苯丙氨酸)亮(亮氨酸)色(色氨酸)书(苏氨酸)
注:评价蛋白质食品营养价值主要依据其必需氨基酸的种类和含量。
C
H
C
H
H2N
OH
O
C
H
C
H2N
OH
O
CH3
CH3
CH
C
H
C
H2N
OH
O
CH3
C
H
C
H2N
OH
O
CH2
CH3
CH3
CH
甘氨酸
缬氨酸
丙氨酸
亮氨酸
几种氨基酸的结构式
二、蛋白质的基本单位——氨基酸
C
C
O
OH
H
H2N
R
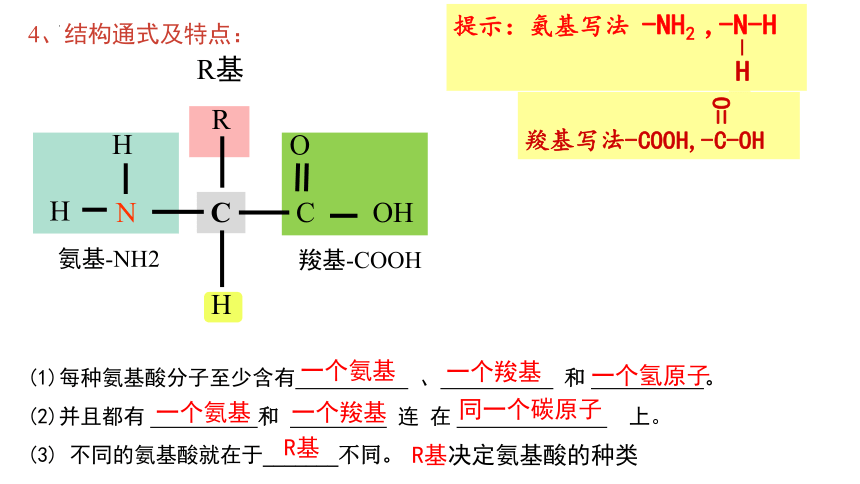
4、结构通式及特点:
氨基-NH2
R基
羧基-COOH
每种氨基酸分子至少含有 、 和 。
并且都有 和 连 在 上。
(3) 不同的氨基酸就在于_______不同。
一个氨基
一个羧基
一个氨基
同一个碳原子
R基
H
C
C OH
N
R
H
H
O
一个羧基
一个氢原子
R基决定氨基酸的种类
羧基写法-COOH,-C-OH
O=
提示:氨基写法 -NH2 ,-N-H
H
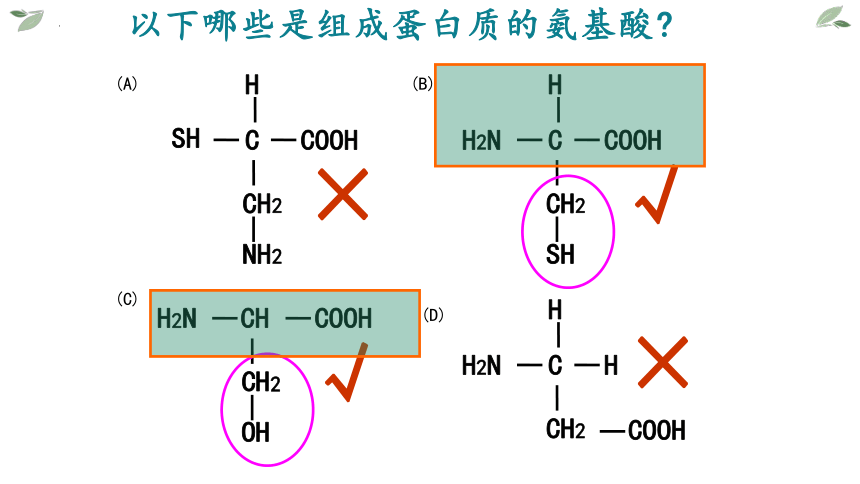
以下哪些是组成蛋白质的氨基酸
C
H
H2N
COOH
CH2
SH
C
H
NH2
COOH
CH2
SH
CH
H2N
COOH
CH2
OH
C
H
H2N
H
CH2
COOH
√
√
×
×
(A)
(B)
(C)
(D)
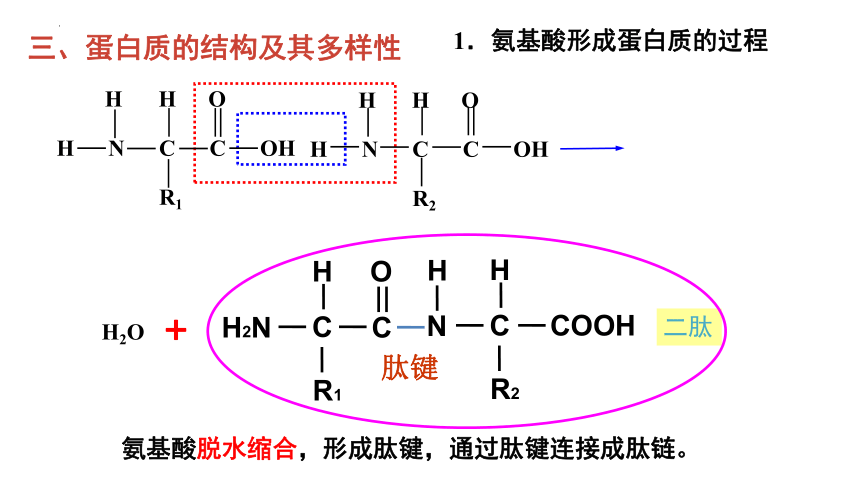
1.氨基酸形成蛋白质的过程
氨基酸脱水缩合,形成肽键,通过肽键连接成肽链。
H2O
H H O
H N C C OH
R1
H H O
H N C C OH
R2
二肽
+
C
H
R1
H2N
C
O
C
H
COOH
R2
H
N
肽键
三、蛋白质的结构及其多样性
C
H
R1
H2N
OH
C
O
H2O
C
H
COOH
R2
H
N
H
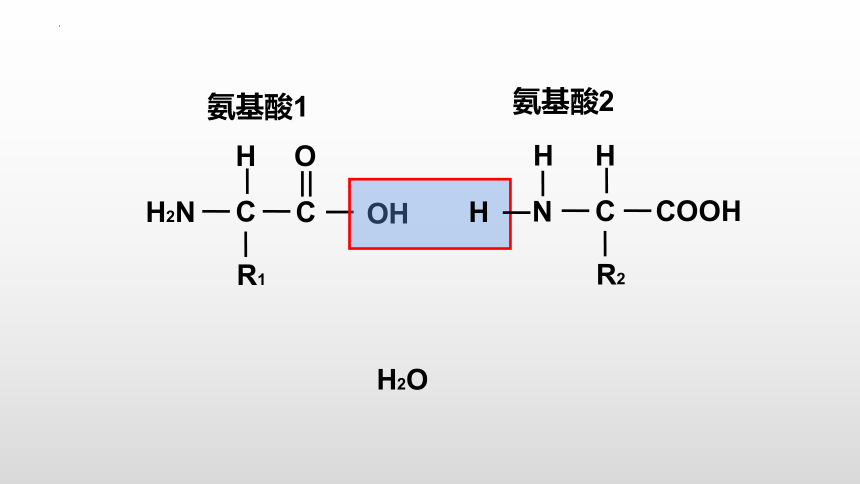
氨基酸1
氨基酸2
C
H
R1
H2N
C
O
H2O
C
H
COOH
R2
H
N
肽键
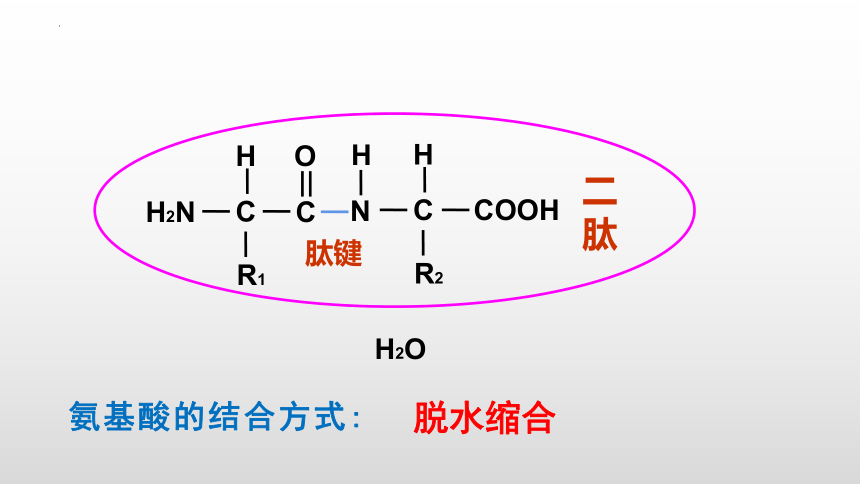
二肽
氨基酸的结合方式:
脱水缩合
肽键
OH
H
二肽
H2O
H2O
C
C
H
R1
NH2
C
O
C
H
R2
H
N
O
C
H
COOH
R2
H
N
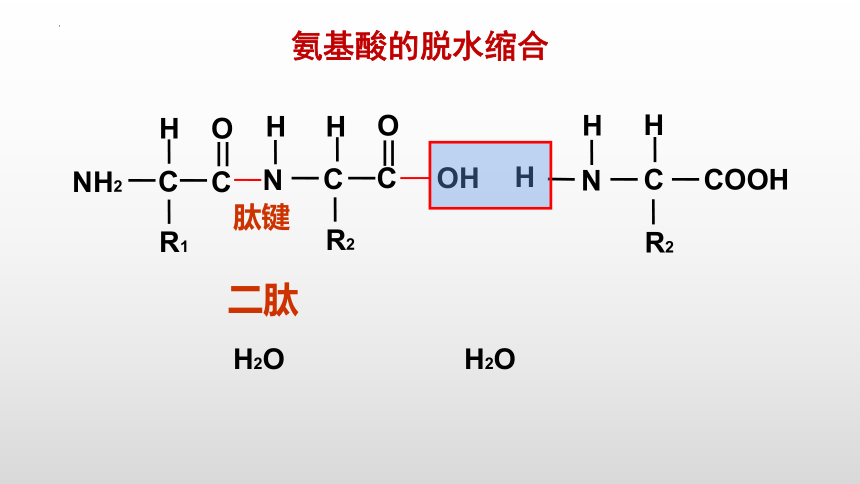
氨基酸的脱水缩合
C
H
COOH
R2
H
N
C
C
H
R1
NH2
C
O
C
H
R2
H
N
O
肽键
C
H
COOH
R2
H
N
H2O
肽键
三肽
H2O
以此类推,由多个氨基酸分子缩合而成的含有多个肽键的化合物,叫多肽。
氨基酸的脱水缩合
二肽
肽键数 =脱水数
= 氨基酸数-肽链数
复习提问:
1、蛋白质的功能?举例说明?
2、组成蛋白质的氨基酸有多少种?蛋白质的元素组成?
3、氨基酸的结构通试?氨基、羧基的写法?分子式?
4、氨基酸的结构特点?
5、什么是必需氨基酸?哪些氨基酸是必需氨基酸?
6、什么是脱水缩合?生成的水中H、O的来源分别是哪里?
7、默写二肽的形成过程?
8、连接两个氨基酸之间的化学键?连接两个氨基酸之间的化学键的有关结构?
9、三肽含是由几个氨基酸脱水缩合形成的?含有几个肽键?
10、蛋白质具有多样性的原因?肽链具有多样性的原因?
11、哪些因素可以导致蛋白质变性?
12、与蛋白计算有关的公式?
氨基酸
二肽
三肽
多肽
几条多肽链折
叠形成蛋白质
折叠盘曲成
空间结构
一条多肽链折
叠形成蛋白质
三、蛋白质的结构及其多样性
氨基酸形成血红蛋白示意图
氨基酸
多肽链
蛋白质
总结:
脱水缩合
盘区折叠
三、蛋白质的结构及其多样性
2.蛋白质的多样性
氨基酸种数不同
氨基酸数目不同
氨基酸序列不同
肽链空间结构不同
蛋白质结构
多种多样
蛋白质种类
多种多样
结构多样性决定了功能多样性!
三、蛋白质的结构及其多样性
蛋白质具有多样性的原因:
氨基酸的种类、数目、排列顺序不同,肽链(蛋白质)的空间结构不同。
肽链具有多样性的原因:
氨基酸的种类、数目、排列顺序不同。
蛋白质空间结构的重要性
血红蛋白β链第6位氨基酸谷氨酸被缬氨酸代替,形成了异常的血红蛋白S(HbS),取代了正常血红蛋白(HbA),氧分压下降时血红蛋白S分子之间相互作用,聚合成为螺旋形多聚体,使红细胞扭曲成镰状细胞(即镰变现象),导致运输氧的能力大为削弱。
左下为镰状红细
2.蛋白质的多样性
三、蛋白质的结构及其多样性
(盐析现象)
(蛋白质变性)
高温、强酸、强碱、重金属
盐析:向鸡蛋清中加入食盐溶液看到白色絮状物,加水后白色絮状物消失。盐析属于物理变化,能复原。
四、盐析和变性
变性: 高温、强酸、强碱、重金属盐等,可以使蛋白质的空间结构变得伸展、松散,失去活性。变性属于化学反应,不能复原。
1.蛋白质分子质量、氨基酸数、肽链数、肽键数和失去水分子数的关系
(1)肽键数=失去水分子数=氨基酸数-肽链数;
(2)蛋白质相对分子质量=氨基酸数目×氨基酸平均相对分子质量-脱去水分子数×18。
蛋白质的相关计算问题
肽链 数目 氨基酸数 肽键数目 脱去水分子数 多肽链相对 分子质量 氨基数目 羧基数目
1条 n n-1 n-1 na-18(n-1) 至少1个 至少1个
m条 n n-m n-m na-18(n-m) 至少m个 至少m个
2.蛋白质中游离氨基或羧基数目的计算
(1)至少含有的游离氨基或羧基数=肽链数。
(2)游离氨基或羧基数目=肽链数+R基中含有的氨基或羧基数。
3.蛋白质中含有N、O原子数的计算
(1)N原子数=肽链数+肽键数+R基上的N原子数=各氨基酸中N原子总数。
(2)O原子数=肽链数×2+肽键数+R基上的O原子数=各氨基酸中O原子总数-脱去水分子数。
【易混必明】
(4)在多肽相对分子质量计算时,还要考虑一些其他化学变化过程,如二硫键(—S—S—)的形成,每形成一个二硫键,脱去2个—H,故相对分子质量减少2。
(5)多肽≠蛋白质
项目 多肽 蛋白质
有无空 间结构 无 有
联系 蛋白质可由一条或几条肽链形成 提醒 翻译的直接产物——多肽,不叫蛋白质,必须经加工,形成一定的空间结构才叫蛋白质 组成蛋白质的氨基酸种类不同
氨基酸的数目不同
氨基酸排列顺序不同
多肽的空间结构不同
组成元素
C、H、O、N
氨基酸
种类:21种
必需氨基酸:8种
非必需氨基酸:13种
通式:
特点:至少一个-NH2和一个-COOH,连在且都有一
个连在同一个C原子上
脱水缩合
多肽
折叠盘曲
蛋白质
结构多样性
功能多样性
组成
O
C
H
C
H2N
OH
R
1.下列关于蛋白质功能的举例合理的是( )
A.催化—抗体 B.运输—唾液淀粉酶
C.调节—胰岛素 D.免疫—血红蛋白
C
2.催产素、牛加压素、血管舒缓素等多肽化合物的氨基酸数量相同,但其生理功能却不同,原因有( )
①氨基酸种类不同 ②合成的场所不同
③氨基酸的排列顺序不同 ④肽链的折叠盘曲方式不同
A.①②③ B.①③④ C.②③④ D.①②③④
B
课堂练习
3.下列物质中,不是构成蛋白质的氨基酸( )
D
A.
B.
C.
D.
4.有关下图中某蛋白质的叙述,正确的是( )
B
A.形成该蛋白质时共脱掉126个水分子
B.该蛋白质含有两条肽链
C.该蛋白质的R基中共含16个氨基
D.该蛋白质共有111个肽键
5.如图表示有关蛋白质分子的简要概念图,下列对图示分析正确的是( )
B
A.A中肯定含有S元素
B.①过程发生伴随着水的生成
C.多肽中B的数目等于C的数目
D.蛋白质结构和功能的多样性是细胞多样性的根本原因
6. 某一多肽链内共有肽键109个,则此分子中含有—NH2和—COOH的数目至少为( )
A. 110、110 B. 109、109
C. 9、9 D. 1、1
D
7. 20种氨基酸的平均分子量是128,由280个氨基酸、4条多肽组成的蛋白质,其分子量约为( )
A. 31432 B. 30872
C. 31378 D. 36382
B
复习提问:
1、主要的能源物质 植物体内的储能物质?动物体内的储能物质?良好的储能物质?
2、组成DNA、RNA的单糖分别是什么?
3、常见的二糖的组成成分?哪些糖是还原糖?
4、组成多糖的基本单位?
5、糖原的种类及分布?
6、几丁质的化学本质?广泛分布在哪里?作用?
7、脂肪由什么形成的酯?脂肪的作用?为什么脂肪含有的能量高?
8、植物脂肪、动物脂肪分别含有哪种类型的脂肪酸?室温呈什么状态?
9、磷脂的作用?固醇包括哪些?作用分别是什么?
10、糖类与脂肪之间转化程度的差异?
11、含有C、H、O的化合物? 含有C、H、O、N、P的化合物?
2.4 蛋白质是生命活动的主要承担者
第二章 组成细胞的分子
一、蛋白质的功能
3、结构蛋白(肌肉、头发、羽毛、蛛丝等)
4、催化作用(绝大多数酶是蛋白质)
5、运输作用(血红蛋白、载体蛋白等)
2、调节作用/信息传递作用(如胰岛素)
1、免疫作用(如抗体)
一条狗催运输
蛋白质分子的主要功能:
一切生命活动都离不开蛋白质,蛋白质是生命活动的主要承担者
①结构蛋白:是构成细胞和生物体的重要物质,
如肌球蛋白、肌动蛋白等
②催化蛋白:起生物催化作用,如绝大多数酶
③运输蛋白:如血红蛋白、细胞膜上的载体
④调节蛋白:如胰岛素和生长激素等
⑤免疫蛋白:免疫过程中产生的抗体
组成蛋白质的氨基酸大约有____ 种。
二、蛋白质的基本单位——氨基酸
2.种类:
21
必需氨基酸(8种):不能合成
非必需氨基酸(13种):能合成
3. 分类:
根据人体细胞能否合成
必须从外界获取
1.元素组成:
C、H、O、N (S、P)
巧记“8种必需氨基酸”
甲(甲硫氨酸)来(赖氨酸)写(缬氨酸)一(异亮氨酸)本(苯丙氨酸)亮(亮氨酸)色(色氨酸)书(苏氨酸)
注:评价蛋白质食品营养价值主要依据其必需氨基酸的种类和含量。
C
H
C
H
H2N
OH
O
C
H
C
H2N
OH
O
CH3
CH3
CH
C
H
C
H2N
OH
O
CH3
C
H
C
H2N
OH
O
CH2
CH3
CH3
CH
甘氨酸
缬氨酸
丙氨酸
亮氨酸
几种氨基酸的结构式
二、蛋白质的基本单位——氨基酸
C
C
O
OH
H
H2N
R
4、结构通式及特点:
氨基-NH2
R基
羧基-COOH
每种氨基酸分子至少含有 、 和 。
并且都有 和 连 在 上。
(3) 不同的氨基酸就在于_______不同。
一个氨基
一个羧基
一个氨基
同一个碳原子
R基
H
C
C OH
N
R
H
H
O
一个羧基
一个氢原子
R基决定氨基酸的种类
羧基写法-COOH,-C-OH
O=
提示:氨基写法 -NH2 ,-N-H
H
以下哪些是组成蛋白质的氨基酸
C
H
H2N
COOH
CH2
SH
C
H
NH2
COOH
CH2
SH
CH
H2N
COOH
CH2
OH
C
H
H2N
H
CH2
COOH
√
√
×
×
(A)
(B)
(C)
(D)
1.氨基酸形成蛋白质的过程
氨基酸脱水缩合,形成肽键,通过肽键连接成肽链。
H2O
H H O
H N C C OH
R1
H H O
H N C C OH
R2
二肽
+
C
H
R1
H2N
C
O
C
H
COOH
R2
H
N
肽键
三、蛋白质的结构及其多样性
C
H
R1
H2N
OH
C
O
H2O
C
H
COOH
R2
H
N
H
氨基酸1
氨基酸2
C
H
R1
H2N
C
O
H2O
C
H
COOH
R2
H
N
肽键
二肽
氨基酸的结合方式:
脱水缩合
肽键
OH
H
二肽
H2O
H2O
C
C
H
R1
NH2
C
O
C
H
R2
H
N
O
C
H
COOH
R2
H
N
氨基酸的脱水缩合
C
H
COOH
R2
H
N
C
C
H
R1
NH2
C
O
C
H
R2
H
N
O
肽键
C
H
COOH
R2
H
N
H2O
肽键
三肽
H2O
以此类推,由多个氨基酸分子缩合而成的含有多个肽键的化合物,叫多肽。
氨基酸的脱水缩合
二肽
肽键数 =脱水数
= 氨基酸数-肽链数
复习提问:
1、蛋白质的功能?举例说明?
2、组成蛋白质的氨基酸有多少种?蛋白质的元素组成?
3、氨基酸的结构通试?氨基、羧基的写法?分子式?
4、氨基酸的结构特点?
5、什么是必需氨基酸?哪些氨基酸是必需氨基酸?
6、什么是脱水缩合?生成的水中H、O的来源分别是哪里?
7、默写二肽的形成过程?
8、连接两个氨基酸之间的化学键?连接两个氨基酸之间的化学键的有关结构?
9、三肽含是由几个氨基酸脱水缩合形成的?含有几个肽键?
10、蛋白质具有多样性的原因?肽链具有多样性的原因?
11、哪些因素可以导致蛋白质变性?
12、与蛋白计算有关的公式?
氨基酸
二肽
三肽
多肽
几条多肽链折
叠形成蛋白质
折叠盘曲成
空间结构
一条多肽链折
叠形成蛋白质
三、蛋白质的结构及其多样性
氨基酸形成血红蛋白示意图
氨基酸
多肽链
蛋白质
总结:
脱水缩合
盘区折叠
三、蛋白质的结构及其多样性
2.蛋白质的多样性
氨基酸种数不同
氨基酸数目不同
氨基酸序列不同
肽链空间结构不同
蛋白质结构
多种多样
蛋白质种类
多种多样
结构多样性决定了功能多样性!
三、蛋白质的结构及其多样性
蛋白质具有多样性的原因:
氨基酸的种类、数目、排列顺序不同,肽链(蛋白质)的空间结构不同。
肽链具有多样性的原因:
氨基酸的种类、数目、排列顺序不同。
蛋白质空间结构的重要性
血红蛋白β链第6位氨基酸谷氨酸被缬氨酸代替,形成了异常的血红蛋白S(HbS),取代了正常血红蛋白(HbA),氧分压下降时血红蛋白S分子之间相互作用,聚合成为螺旋形多聚体,使红细胞扭曲成镰状细胞(即镰变现象),导致运输氧的能力大为削弱。
左下为镰状红细
2.蛋白质的多样性
三、蛋白质的结构及其多样性
(盐析现象)
(蛋白质变性)
高温、强酸、强碱、重金属
盐析:向鸡蛋清中加入食盐溶液看到白色絮状物,加水后白色絮状物消失。盐析属于物理变化,能复原。
四、盐析和变性
变性: 高温、强酸、强碱、重金属盐等,可以使蛋白质的空间结构变得伸展、松散,失去活性。变性属于化学反应,不能复原。
1.蛋白质分子质量、氨基酸数、肽链数、肽键数和失去水分子数的关系
(1)肽键数=失去水分子数=氨基酸数-肽链数;
(2)蛋白质相对分子质量=氨基酸数目×氨基酸平均相对分子质量-脱去水分子数×18。
蛋白质的相关计算问题
肽链 数目 氨基酸数 肽键数目 脱去水分子数 多肽链相对 分子质量 氨基数目 羧基数目
1条 n n-1 n-1 na-18(n-1) 至少1个 至少1个
m条 n n-m n-m na-18(n-m) 至少m个 至少m个
2.蛋白质中游离氨基或羧基数目的计算
(1)至少含有的游离氨基或羧基数=肽链数。
(2)游离氨基或羧基数目=肽链数+R基中含有的氨基或羧基数。
3.蛋白质中含有N、O原子数的计算
(1)N原子数=肽链数+肽键数+R基上的N原子数=各氨基酸中N原子总数。
(2)O原子数=肽链数×2+肽键数+R基上的O原子数=各氨基酸中O原子总数-脱去水分子数。
【易混必明】
(4)在多肽相对分子质量计算时,还要考虑一些其他化学变化过程,如二硫键(—S—S—)的形成,每形成一个二硫键,脱去2个—H,故相对分子质量减少2。
(5)多肽≠蛋白质
项目 多肽 蛋白质
有无空 间结构 无 有
联系 蛋白质可由一条或几条肽链形成 提醒 翻译的直接产物——多肽,不叫蛋白质,必须经加工,形成一定的空间结构才叫蛋白质 组成蛋白质的氨基酸种类不同
氨基酸的数目不同
氨基酸排列顺序不同
多肽的空间结构不同
组成元素
C、H、O、N
氨基酸
种类:21种
必需氨基酸:8种
非必需氨基酸:13种
通式:
特点:至少一个-NH2和一个-COOH,连在且都有一
个连在同一个C原子上
脱水缩合
多肽
折叠盘曲
蛋白质
结构多样性
功能多样性
组成
O
C
H
C
H2N
OH
R
1.下列关于蛋白质功能的举例合理的是( )
A.催化—抗体 B.运输—唾液淀粉酶
C.调节—胰岛素 D.免疫—血红蛋白
C
2.催产素、牛加压素、血管舒缓素等多肽化合物的氨基酸数量相同,但其生理功能却不同,原因有( )
①氨基酸种类不同 ②合成的场所不同
③氨基酸的排列顺序不同 ④肽链的折叠盘曲方式不同
A.①②③ B.①③④ C.②③④ D.①②③④
B
课堂练习
3.下列物质中,不是构成蛋白质的氨基酸( )
D
A.
B.
C.
D.
4.有关下图中某蛋白质的叙述,正确的是( )
B
A.形成该蛋白质时共脱掉126个水分子
B.该蛋白质含有两条肽链
C.该蛋白质的R基中共含16个氨基
D.该蛋白质共有111个肽键
5.如图表示有关蛋白质分子的简要概念图,下列对图示分析正确的是( )
B
A.A中肯定含有S元素
B.①过程发生伴随着水的生成
C.多肽中B的数目等于C的数目
D.蛋白质结构和功能的多样性是细胞多样性的根本原因
6. 某一多肽链内共有肽键109个,则此分子中含有—NH2和—COOH的数目至少为( )
A. 110、110 B. 109、109
C. 9、9 D. 1、1
D
7. 20种氨基酸的平均分子量是128,由280个氨基酸、4条多肽组成的蛋白质,其分子量约为( )
A. 31432 B. 30872
C. 31378 D. 36382
B
同课章节目录
- 第1章 走近细胞
- 第1节 细胞是生命活动的基本单位
- 第2节 细胞的多样性和统一性
- 第2章 组成细胞的分子
- 第1节 细胞中的元素和化合物
- 第2节 细胞中的无机物
- 第3节 细胞中的糖类和脂质
- 第4节 蛋白质是生命活动的主要承担者
- 第5节 核酸是遗传信息的携带者
- 第3章 细胞的基本结构
- 第1节 细胞膜的结构和功能
- 第2节 细胞器之间的分工合作
- 第3节 细胞核的结构和功能
- 第4章 细胞的物质输入和输出
- 第1节 被动运输
- 第2节 主动运输与胞吞、胞吐
- 第5章 细胞的能量供应和利用
- 第1节 降低化学反应活化能的酶
- 第2节 细胞的能量“货币”ATP
- 第3节 细胞呼吸的原理和应用
- 第4节 光合作用与能量转化
- 第6章 细胞的生命历程
- 第1节 细胞的增殖
- 第2节 细胞的分化
- 第3节 细胞的衰老和死亡
