酸和碱的复习(25张ppt)
图片预览





文档简介
课件24张PPT。 酸和碱的复习讨论1:找出下列物质中的纯净物与混合物,并说出你的判断依据。
①空气 ②氯化钠 ③液氧 ④氢氧化钠
⑤铁 ⑥稀盐酸 ⑦干冰 ⑧铝合金
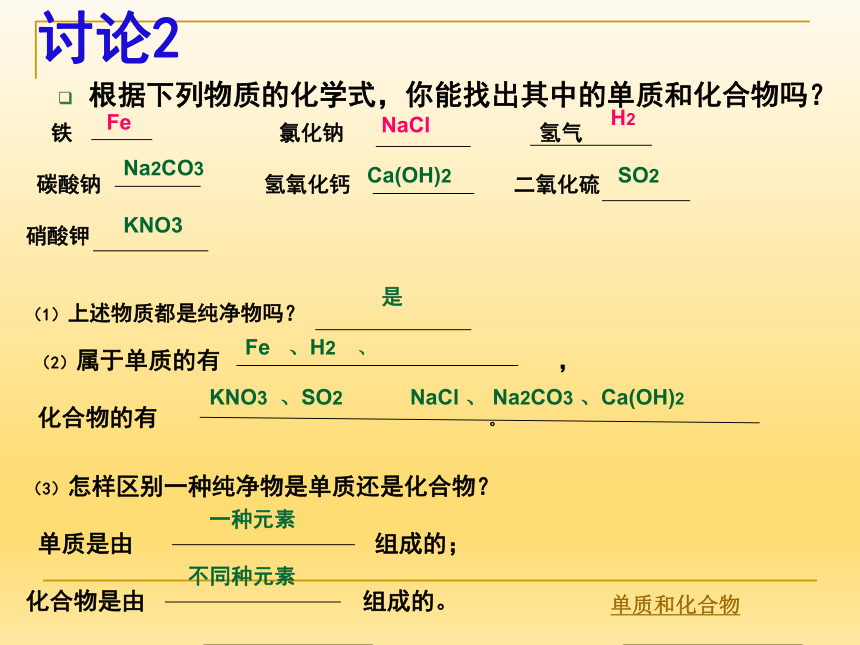
同一种物质 属于纯净物的有 ②③④⑤⑦①⑥⑧属于混合物的有你的判断依据:纯净物由 组成,不同种的物质 纯净物与混合物讨论2根据下列物质的化学式,你能找出其中的单质和化合物吗?
铁 氯化钠 氢气
碳酸钠 氢氧化钙 二氧化硫
硝酸钾
(1)上述物质都是纯净物吗?
(2)属于单质的有 ,
化合物的有 。
(3)怎样区别一种纯净物是单质还是化合物?
单质是由 组成的;
化合物是由 组成的。
FeH2Na2CO3Ca(OH)2NaCl Fe 、H2 、NaCl 、 Na2CO3 、Ca(OH)2一种元素 KNO3SO2是不同种元素KNO3 、SO2单质和化合物讨论3:请先写出下列物质的化学式,分析它们的元素组成特点,并进行归纳总结规律。
水 氧化钙 四氧化三铁
氧化镁 五氧化二磷
总结:这些物质都是 (化合物、混合物),
它们都是由 种元素组成的,其中都含有一种相
同的 元素,所以它们都属于
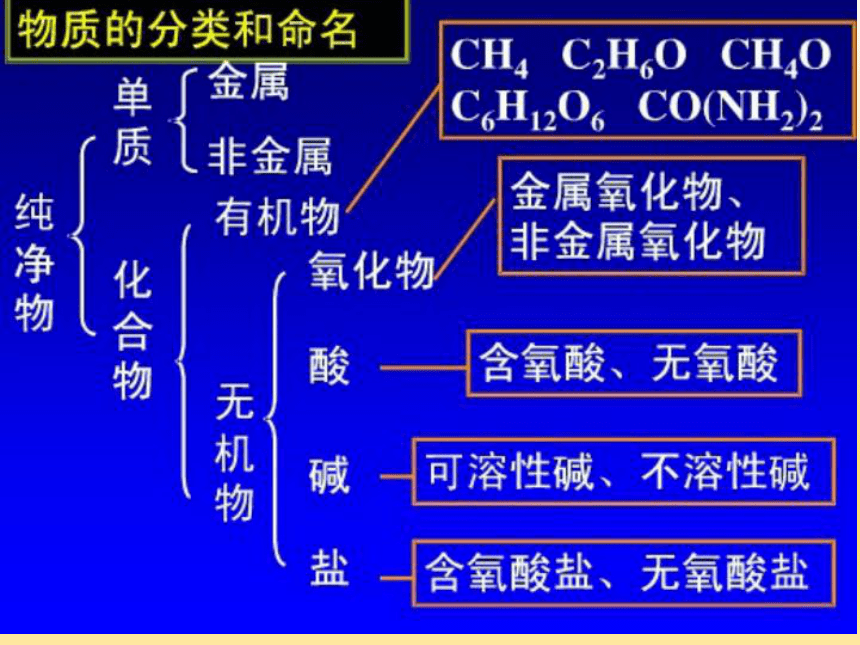
化合物两氧氧化物。H2OCaOFe3O4MgOP2O5氧化物讨论4:给下列纯净物分类,并说出分类依据。
①盐酸 ②氯化钠 ③熟石灰 ④氢氧化钠
⑤硫酸铜 ⑥硫酸 ⑦氯化钾 ⑧碳酸
属于酸的有 ①⑥⑧③④属于碱的有你的判断依据:酸是由 组成,②⑤⑦酸=H++酸根离子碱=金属离子+OH-酸碱盐属于盐的有具体物质物质所属类别。联想一种物质提示2:酸提示1:无色溶液提示3:挥发提示4:胃液答案:盐酸无色黏稠油状液体无气味有刺激性气味无明显现象瓶口附近有白雾出现不易挥发易挥发无色液体一、盐酸和硫酸性质的比较有吸水性、脱水性、 氧化性和强腐蚀性有强烈的腐蚀性二、酸的化学性质1:酸能与指示剂反应。遇酸溶液变红色,遇碱溶液变蓝色溶液变红色不变色溶液变蓝色不变色不变色溶液变红色二、酸的化学性质2:酸能与多种活泼金属反应,生成盐和氢气Mg+2HCl=MgCl2+H2↑ Zn+2HCl=ZnCl2+H2↑ Mg+H2SO4=MgSO4+H2↑ Zn+H2SO4=ZnSO4+H2↑ Fe+2HCl=FeCl2+H2↑ Fe+H2SO4=FeSO4+H2↑ ★注意:金属活动性在H以前二、酸的化学性质3:酸能与某些金属氧化物反应,生成盐和水。Fe2O3+6HCl=2FeCl3+3H2OFe2O3+3H2SO4=Fe2(SO4)3+3H2O CuO+2HCl=CuCl2+H2OCuO+H2SO4=CuSO4+H2O 二、酸的化学性质4:酸和碱发生中和反应,生成盐和水。
注意:酸与碱作用生成盐和水的反应,叫中和反应。
5.盐+酸 →新盐+新酸(产物符合复分解反应发生的条件)
实验室用大理石和稀盐酸反应制二氧化碳
_________________________________
碳酸钡与稀盐酸反应
_________________________________
纯碱中加入稀盐酸
__________________________________
稀盐酸中滴入硝酸银溶液
_______________________________
稀硫酸中滴入氯化钡溶液
_______________________________常见沉淀有:BaSO4 、 BaCO3 、 AgCl 、 CaCO3 、 Mg(OH)2
Fe(OH)3 、Cu(OH)2 、红褐色沉淀蓝色沉淀CaCO3 + 2HCl = CaCl2 + H2O + CO2 ↑BaCO3 + 2HCl = BaCl2 + H2O + CO2 ↑Na2CO3 + 2HCl = 2NaCl + H2O + CO2 ↑AgNO3 + HCl = AgCl ↓ + HNO3BaCl2 + H2SO4 = BaSO4 ↓ + 2HCl二、酸的化学性质HClCuCO2NaCl Fe2O3FeCuCO2H2SO4NaClCuNaOHH2SO4CO2NaClCaCO3H2SO4NaClCuCO2H2SO4入口出口小羊选择哪条路才不会羊入狼口呢?
并找出其他几条路中谁是狼?
酸的化学性质1、酸能使紫色石蕊试液变红,使无色酚酞不变色。
2、酸与金属反应生成盐和氢气。
3、酸与金属氧化物反应生成盐和水。
4、酸与碱反应生成盐和水。
5、酸与某些盐反应生成新酸和新盐。三、碱的化学性质2:碱能与某些非金属氧化物反应,生成盐和水。3:酸和碱发生中和反应,生成盐和水。4:碱与某些盐在溶液中发生反应,生成另一种盐和碱。黄色溶液逐渐变浅,生成红褐色沉淀。蓝色溶液逐渐变浅,生成蓝色沉淀。FeCl3+3NaOH =Fe(OH)3↓ +3NaCl
CuSO4+2NaOH =Cu(OH)2 ↓ +2NaCl三、碱的化学性质黄色溶液逐渐变浅,生成红褐色沉淀。蓝色溶液逐渐变浅,生成蓝色沉淀。FeCl3+3NaOH =Fe(OH)3↓ +3NaCl
CuSO4+2NaOH =Cu(OH)2 ↓ +2NaCl三、碱的化学性质4:碱与某些盐在溶液中发生反应,生成另一种盐和碱。Fe2O3NaOH NaClCuCO2NaOHNaClHCl CuNaClNaOHCuFe2O3NaClCuSO4CuFe2O3碱的化学性质
1、碱能使紫色石蕊试液变蓝,使无色酚酞试液变红。
2、碱与非金属氧化物反应生成盐和水。
3、碱与酸反应生成盐和水。
4、碱与某些盐反应生成新碱和新盐。
只给你酚酞请鉴别出NaOH、H2SO4、NaCl三种无色溶液?无色酚酞ABC装入C试管内液
体是NaOH溶液AB装入A试管内的 液体是NaCl装入B试管内的液体是H2SO4
①空气 ②氯化钠 ③液氧 ④氢氧化钠
⑤铁 ⑥稀盐酸 ⑦干冰 ⑧铝合金
同一种物质 属于纯净物的有 ②③④⑤⑦①⑥⑧属于混合物的有你的判断依据:纯净物由 组成,不同种的物质 纯净物与混合物讨论2根据下列物质的化学式,你能找出其中的单质和化合物吗?
铁 氯化钠 氢气
碳酸钠 氢氧化钙 二氧化硫
硝酸钾
(1)上述物质都是纯净物吗?
(2)属于单质的有 ,
化合物的有 。
(3)怎样区别一种纯净物是单质还是化合物?
单质是由 组成的;
化合物是由 组成的。
FeH2Na2CO3Ca(OH)2NaCl Fe 、H2 、NaCl 、 Na2CO3 、Ca(OH)2一种元素 KNO3SO2是不同种元素KNO3 、SO2单质和化合物讨论3:请先写出下列物质的化学式,分析它们的元素组成特点,并进行归纳总结规律。
水 氧化钙 四氧化三铁
氧化镁 五氧化二磷
总结:这些物质都是 (化合物、混合物),
它们都是由 种元素组成的,其中都含有一种相
同的 元素,所以它们都属于
化合物两氧氧化物。H2OCaOFe3O4MgOP2O5氧化物讨论4:给下列纯净物分类,并说出分类依据。
①盐酸 ②氯化钠 ③熟石灰 ④氢氧化钠
⑤硫酸铜 ⑥硫酸 ⑦氯化钾 ⑧碳酸
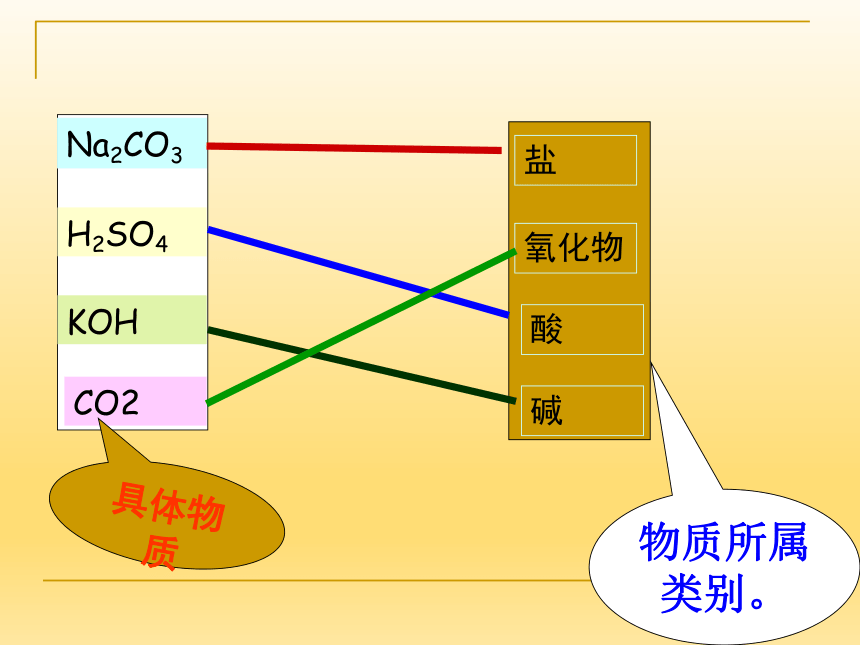
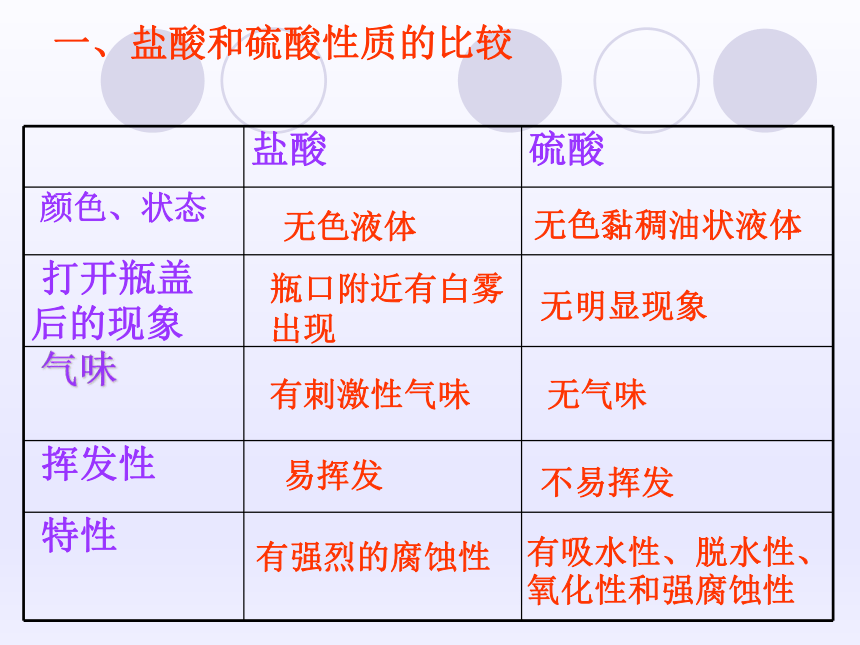
属于酸的有 ①⑥⑧③④属于碱的有你的判断依据:酸是由 组成,②⑤⑦酸=H++酸根离子碱=金属离子+OH-酸碱盐属于盐的有具体物质物质所属类别。联想一种物质提示2:酸提示1:无色溶液提示3:挥发提示4:胃液答案:盐酸无色黏稠油状液体无气味有刺激性气味无明显现象瓶口附近有白雾出现不易挥发易挥发无色液体一、盐酸和硫酸性质的比较有吸水性、脱水性、 氧化性和强腐蚀性有强烈的腐蚀性二、酸的化学性质1:酸能与指示剂反应。遇酸溶液变红色,遇碱溶液变蓝色溶液变红色不变色溶液变蓝色不变色不变色溶液变红色二、酸的化学性质2:酸能与多种活泼金属反应,生成盐和氢气Mg+2HCl=MgCl2+H2↑ Zn+2HCl=ZnCl2+H2↑ Mg+H2SO4=MgSO4+H2↑ Zn+H2SO4=ZnSO4+H2↑ Fe+2HCl=FeCl2+H2↑ Fe+H2SO4=FeSO4+H2↑ ★注意:金属活动性在H以前二、酸的化学性质3:酸能与某些金属氧化物反应,生成盐和水。Fe2O3+6HCl=2FeCl3+3H2OFe2O3+3H2SO4=Fe2(SO4)3+3H2O CuO+2HCl=CuCl2+H2OCuO+H2SO4=CuSO4+H2O 二、酸的化学性质4:酸和碱发生中和反应,生成盐和水。
注意:酸与碱作用生成盐和水的反应,叫中和反应。
5.盐+酸 →新盐+新酸(产物符合复分解反应发生的条件)
实验室用大理石和稀盐酸反应制二氧化碳
_________________________________
碳酸钡与稀盐酸反应
_________________________________
纯碱中加入稀盐酸
__________________________________
稀盐酸中滴入硝酸银溶液
_______________________________
稀硫酸中滴入氯化钡溶液
_______________________________常见沉淀有:BaSO4 、 BaCO3 、 AgCl 、 CaCO3 、 Mg(OH)2
Fe(OH)3 、Cu(OH)2 、红褐色沉淀蓝色沉淀CaCO3 + 2HCl = CaCl2 + H2O + CO2 ↑BaCO3 + 2HCl = BaCl2 + H2O + CO2 ↑Na2CO3 + 2HCl = 2NaCl + H2O + CO2 ↑AgNO3 + HCl = AgCl ↓ + HNO3BaCl2 + H2SO4 = BaSO4 ↓ + 2HCl二、酸的化学性质HClCuCO2NaCl Fe2O3FeCuCO2H2SO4NaClCuNaOHH2SO4CO2NaClCaCO3H2SO4NaClCuCO2H2SO4入口出口小羊选择哪条路才不会羊入狼口呢?
并找出其他几条路中谁是狼?
酸的化学性质1、酸能使紫色石蕊试液变红,使无色酚酞不变色。
2、酸与金属反应生成盐和氢气。
3、酸与金属氧化物反应生成盐和水。
4、酸与碱反应生成盐和水。
5、酸与某些盐反应生成新酸和新盐。三、碱的化学性质2:碱能与某些非金属氧化物反应,生成盐和水。3:酸和碱发生中和反应,生成盐和水。4:碱与某些盐在溶液中发生反应,生成另一种盐和碱。黄色溶液逐渐变浅,生成红褐色沉淀。蓝色溶液逐渐变浅,生成蓝色沉淀。FeCl3+3NaOH =Fe(OH)3↓ +3NaCl
CuSO4+2NaOH =Cu(OH)2 ↓ +2NaCl三、碱的化学性质黄色溶液逐渐变浅,生成红褐色沉淀。蓝色溶液逐渐变浅,生成蓝色沉淀。FeCl3+3NaOH =Fe(OH)3↓ +3NaCl
CuSO4+2NaOH =Cu(OH)2 ↓ +2NaCl三、碱的化学性质4:碱与某些盐在溶液中发生反应,生成另一种盐和碱。Fe2O3NaOH NaClCuCO2NaOHNaClHCl CuNaClNaOHCuFe2O3NaClCuSO4CuFe2O3碱的化学性质
1、碱能使紫色石蕊试液变蓝,使无色酚酞试液变红。
2、碱与非金属氧化物反应生成盐和水。
3、碱与酸反应生成盐和水。
4、碱与某些盐反应生成新碱和新盐。
只给你酚酞请鉴别出NaOH、H2SO4、NaCl三种无色溶液?无色酚酞ABC装入C试管内液
体是NaOH溶液AB装入A试管内的 液体是NaCl装入B试管内的液体是H2SO4
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
