2024届高三化学一轮专题复习 寻踪觅迹,多维度探究 SO2的性质与应用 教学设计
文档属性
| 名称 | 2024届高三化学一轮专题复习 寻踪觅迹,多维度探究 SO2的性质与应用 教学设计 |

|
|
| 格式 | docx | ||
| 文件大小 | 765.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-16 00:00:00 | ||
图片预览

文档简介
寻踪觅迹,多维度探究SO2性质与应用
—依托元素化学,运用科学探究,提升化学素养
教学设计
课 题 寻踪觅迹,多维度探究SO2性质与应用 科 目 化学 年级 高三
授课教师 课 型 复习课 日期
教学内容分析 本节课建立在完成硫元素性质梳理的课时后,借助价类二维模型和化学学科特征对硫元素家族中的重要成员——二氧化硫的性质展开具体讨论,同时有对实验探究方案的提出以及原理知识的理解。
学习目标 以硫元素“物质家族”重要成员—二氧化硫为依托,进一步认识和掌握从“化学学科的任务与特征”、“价类二维图”等维度构建元素化合物知识体系的认知模型; 通过对二氧化硫性质及其实际应用的多维度探究,提升获取信息、独立思考、整合及运用元素化合物知识与化学反应原理分析问题解决问题的能力; 通过理论及实验探索,培养科学探究精神与创新意识,进一步认识“定性与定量结合”的科学态度,能对食品安全等社会热点问题做出正确的价值判断,认识化学学科的价值。
学习者特征分析 本课时的教学对象为高三,他们思维敏捷、活跃,比较喜欢动手做实验并且已经具备了一定的操作能力。而且在此之前学生已硫元素家族基本概念的梳理,回顾了二氧化硫的基本性质,但是对SO2 性质的探究可能缺乏深层次的分析。
教学过程
教学环节 教师活动 学生活动 设计意图
课前环节:评价课前学案 要学会借助价类二维图对元素化合物进行定位和定性的认识。从类别和化合价角度分析二氧化硫的氧化性、还原性、酸性氧化物通性以及漂白性。 学生完善课前学案,自我诊断 (
f
),学会与原理、结构等关联。 帮助学生明确无机物的复习模型。
任务一:定性检验SO2 任务二:定量检验SO2 素材一、酒瓶里的二氧化硫 现场展示葡萄酒瓶。 资料卡展示葡萄酒中二氧化硫的作用。 学生根据葡萄酒瓶标签总结SO2的性质。 帮助学生认识到性质决定用途。
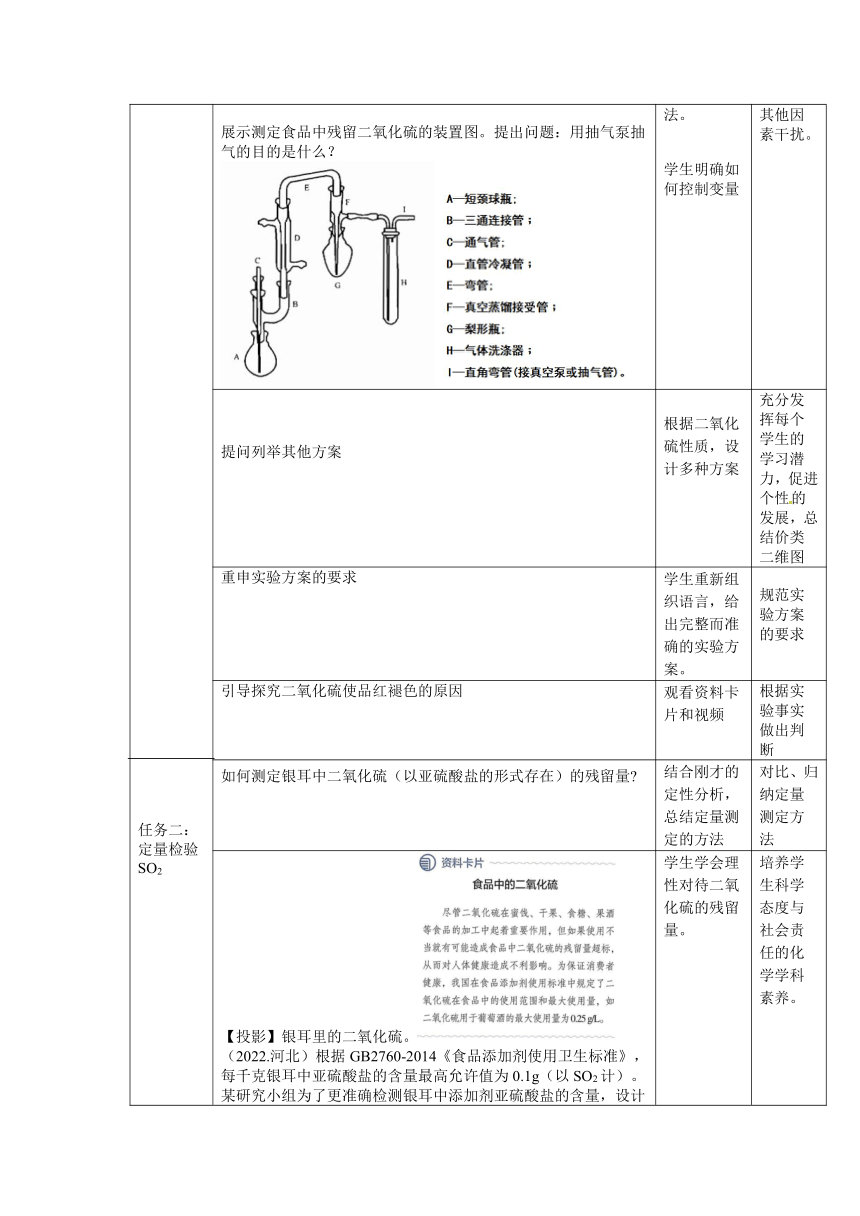
如何定量检测葡萄酒中的二氧化硫? 展示测定食品中残留二氧化硫的装置图。提出问题:用抽气泵抽气的目的是什么? 学生讨论总结定量检测葡萄酒中二氧化硫的方法。 学生明确如何控制变量 强化学生控制变量思想,排除其他因素干扰。
提问列举其他方案 根据二氧化硫性质,设计多种方案 充分发挥每个学生的学习潜力,促进个性的发展,总结价类二维图
重申实验方案的要求 学生重新组织语言,给出完整而准确的实验方案。 规范实验方案的要求
引导探究二氧化硫使品红褪色的原因 观看资料卡片和视频 根据实验事实做出判断
如何测定银耳中二氧化硫(以亚硫酸盐的形式存在)的残留量 结合刚才的定性分析,总结定量测定的方法 对比、归纳定量测定方法
【投影】银耳里的二氧化硫。 (2022.河北)根据GB2760-2014《食品添加剂使用卫生标准》,每千克银耳中亚硫酸盐的含量最高允许值为0.1g(以SO2计)。某研究小组为了更准确检测银耳中添加剂亚硫酸盐的含量,设计实验如下: ①三颈烧瓶中加入10.00g银耳样品和400mL水;锥形瓶中加入125mL水、1mL指示剂X,并预加0.30mL0.0100mol·L-1的碘标准溶液,搅拌。 ②以0.2L·min-1流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了0.70mL碘标准溶液。 1)若先加硫酸再通氮气,会使测定结果__________(填“偏高”、“偏低”或“无影响”)。 (2)该样品中亚硫酸盐含量为__________(以SO2计,结果保留三位有效数字)。该样品中二氧化硫的残留量是否超标? 已知: 回答下列问题: 解释加入H3PO4,能够生成SO2的原因: 学生学会理性对待二氧化硫的残留量。 分析通氮气的理由 利用关系式法测出含量 分析平衡对反应的影响 培养学生科学态度与社会责任的化学学科素养。 培养学生严谨的实验态度 培养学生分析与推测能力、探究与创新能力。 引导学生体会多重平衡的竞争
任务三:认识二氧化硫的应用 硫代硫酸钠(Na2S2O3)常用作纸浆漂白的脱氯剂以及感光工业中的定影剂等。实验室可用如下装置(略去部分加持仪器)模拟生成过程。 问题2:补充完整装置C中反应的化学方程式 (I)____________________________________ (体现SO2酸性) (II)___________________________________(体现SO2氧化性) (III)S + Na2SO3 Na2S2O3 问题3:为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为。 (2020·浙江卷节选)用下图装置制备Na2S2O3·5H2O(略去加热和加持仪器) 综合运用二氧化硫性质,分析烧瓶中的反应方程式 根据其综合性质,计算得出比例关系
体会高考题中仪器的相似性 理清计量关系 引导学生根据性质写方程式 综合体会酸性和还原性 引导学会迁移应用,举一反三。学会利用平衡思想理解二氧化硫到二氧化碳的转化
—依托元素化学,运用科学探究,提升化学素养
教学设计
课 题 寻踪觅迹,多维度探究SO2性质与应用 科 目 化学 年级 高三
授课教师 课 型 复习课 日期
教学内容分析 本节课建立在完成硫元素性质梳理的课时后,借助价类二维模型和化学学科特征对硫元素家族中的重要成员——二氧化硫的性质展开具体讨论,同时有对实验探究方案的提出以及原理知识的理解。
学习目标 以硫元素“物质家族”重要成员—二氧化硫为依托,进一步认识和掌握从“化学学科的任务与特征”、“价类二维图”等维度构建元素化合物知识体系的认知模型; 通过对二氧化硫性质及其实际应用的多维度探究,提升获取信息、独立思考、整合及运用元素化合物知识与化学反应原理分析问题解决问题的能力; 通过理论及实验探索,培养科学探究精神与创新意识,进一步认识“定性与定量结合”的科学态度,能对食品安全等社会热点问题做出正确的价值判断,认识化学学科的价值。
学习者特征分析 本课时的教学对象为高三,他们思维敏捷、活跃,比较喜欢动手做实验并且已经具备了一定的操作能力。而且在此之前学生已硫元素家族基本概念的梳理,回顾了二氧化硫的基本性质,但是对SO2 性质的探究可能缺乏深层次的分析。
教学过程
教学环节 教师活动 学生活动 设计意图
课前环节:评价课前学案 要学会借助价类二维图对元素化合物进行定位和定性的认识。从类别和化合价角度分析二氧化硫的氧化性、还原性、酸性氧化物通性以及漂白性。 学生完善课前学案,自我诊断 (
f
),学会与原理、结构等关联。 帮助学生明确无机物的复习模型。
任务一:定性检验SO2 任务二:定量检验SO2 素材一、酒瓶里的二氧化硫 现场展示葡萄酒瓶。 资料卡展示葡萄酒中二氧化硫的作用。 学生根据葡萄酒瓶标签总结SO2的性质。 帮助学生认识到性质决定用途。
如何定量检测葡萄酒中的二氧化硫? 展示测定食品中残留二氧化硫的装置图。提出问题:用抽气泵抽气的目的是什么? 学生讨论总结定量检测葡萄酒中二氧化硫的方法。 学生明确如何控制变量 强化学生控制变量思想,排除其他因素干扰。
提问列举其他方案 根据二氧化硫性质,设计多种方案 充分发挥每个学生的学习潜力,促进个性的发展,总结价类二维图
重申实验方案的要求 学生重新组织语言,给出完整而准确的实验方案。 规范实验方案的要求
引导探究二氧化硫使品红褪色的原因 观看资料卡片和视频 根据实验事实做出判断
如何测定银耳中二氧化硫(以亚硫酸盐的形式存在)的残留量 结合刚才的定性分析,总结定量测定的方法 对比、归纳定量测定方法
【投影】银耳里的二氧化硫。 (2022.河北)根据GB2760-2014《食品添加剂使用卫生标准》,每千克银耳中亚硫酸盐的含量最高允许值为0.1g(以SO2计)。某研究小组为了更准确检测银耳中添加剂亚硫酸盐的含量,设计实验如下: ①三颈烧瓶中加入10.00g银耳样品和400mL水;锥形瓶中加入125mL水、1mL指示剂X,并预加0.30mL0.0100mol·L-1的碘标准溶液,搅拌。 ②以0.2L·min-1流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了0.70mL碘标准溶液。 1)若先加硫酸再通氮气,会使测定结果__________(填“偏高”、“偏低”或“无影响”)。 (2)该样品中亚硫酸盐含量为__________(以SO2计,结果保留三位有效数字)。该样品中二氧化硫的残留量是否超标? 已知: 回答下列问题: 解释加入H3PO4,能够生成SO2的原因: 学生学会理性对待二氧化硫的残留量。 分析通氮气的理由 利用关系式法测出含量 分析平衡对反应的影响 培养学生科学态度与社会责任的化学学科素养。 培养学生严谨的实验态度 培养学生分析与推测能力、探究与创新能力。 引导学生体会多重平衡的竞争
任务三:认识二氧化硫的应用 硫代硫酸钠(Na2S2O3)常用作纸浆漂白的脱氯剂以及感光工业中的定影剂等。实验室可用如下装置(略去部分加持仪器)模拟生成过程。 问题2:补充完整装置C中反应的化学方程式 (I)____________________________________ (体现SO2酸性) (II)___________________________________(体现SO2氧化性) (III)S + Na2SO3 Na2S2O3 问题3:为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为。 (2020·浙江卷节选)用下图装置制备Na2S2O3·5H2O(略去加热和加持仪器) 综合运用二氧化硫性质,分析烧瓶中的反应方程式 根据其综合性质,计算得出比例关系
体会高考题中仪器的相似性 理清计量关系 引导学生根据性质写方程式 综合体会酸性和还原性 引导学会迁移应用,举一反三。学会利用平衡思想理解二氧化硫到二氧化碳的转化
同课章节目录
