第四单元从海洋到用户之计算工具篇——物质的量课件(共36张PPT)-2023-2024学年高一化学(人教版2019必修第一册)
文档属性
| 名称 | 第四单元从海洋到用户之计算工具篇——物质的量课件(共36张PPT)-2023-2024学年高一化学(人教版2019必修第一册) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-16 17:16:52 | ||
图片预览









文档简介
(共36张PPT)
大单元教学课件
新人教版 化学
必修第一册
第三单元
海水中的重要元素
——钠和氯
A
物质的量
从海洋到用户之计算工具篇
物质的量总结提升
学习目标
1,能基于物质的量认识物质组成及其化学变化,运用物质的量、摩尔质量、气体摩尔体积、物质的量浓度之间的相互关系进行简单计算
2,通过完成物质的量的学习,使学生了解科学的推理过程,理解微观粒子模型在化学研究中的重要作用。通过类比等方法学习物质的量的概念的过程,建立逻辑推理、归纳推理、模型认知能力。
3,通过对概念的透彻理解,锻炼严谨、认真的学习态度,体会定量研究的方法对研究和学习化学的重要作用。
从海洋到用户之计算工具
物质的量
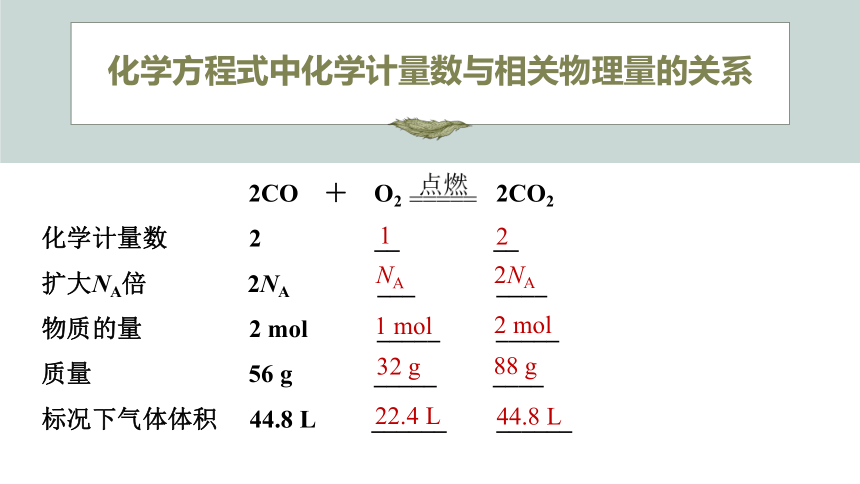
化学方程式中化学计量数与相关物理量的关系
2CO + O2 2CO2
化学计量数 2 __ __
扩大NA倍 2NA ___ ____
物质的量 2 mol _____ _____
质量 56 g _____ ____
标况下气体体积 44.8 L ______ ______
1
2
NA
2NA
1 mol
2 mol
32 g
88 g
22.4 L
44.8 L
结论:化学方程式中各物质的化学计量数之比等于其粒子数目之比,等于其物质的量之比,也等于同温同压下气体的体积之比
物质的量与其它物理量之间的联系
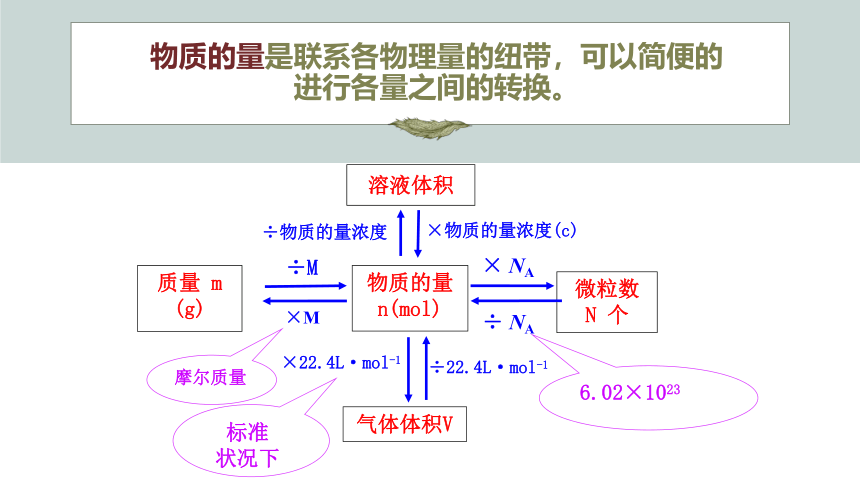
物质的量是联系各物理量的纽带,可以简便的进行各量之间的转换。
质量 m
(g)
微粒数
N 个
÷M
物质的量
n(mol)
×M
× NA
÷ NA
气体体积V
×22.4L·mol-1
6.02×1023
摩尔质量
溶液体积
×物质的量浓度(c)
÷物质的量浓度
÷22.4L·mol-1
标准
状况下
物质的量
宏观
粒子的
数目
微观
物质的
质量
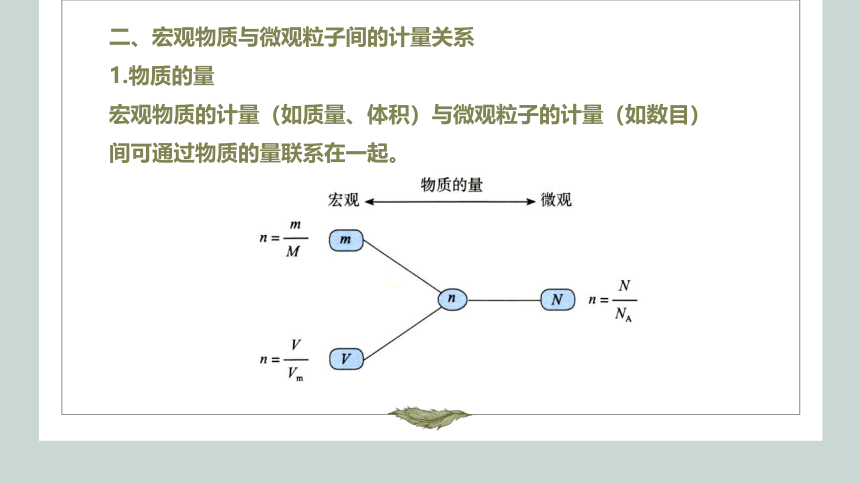
二、宏观物质与微观粒子间的计量关系
1.物质的量
宏观物质的计量(如质量、体积)与微观粒子的计量(如数目)间可通过物质的量联系在一起。
例1、(1)现有m g某气体,它由双原子分子构成,它的摩尔质量为
M g·mol-1。若阿伏加德罗常数值用NA表示,则:
①该气体的物质的量为 mol。
②该气体所含原子总数为 个。
③该气体在标准状况下的体积为 L。
(2)利用“化学计量在实验中的应用”的相关知识进行填空。
①含有6.02×1023个氧原子的H2SO4的物质的量是 mol。
②与标准状况下V L CO2所含氧原子数目相同的水的质量是________ (用分式表示)g。
③在一定的温度和压强下,1体积X2(g)跟3体积Y2(g)化合生成2体积化合
物,则该化合物的化学式是 。
m/M
2mNA/M
22.4m/M
0.25
45v/28
XY3
物质的量在化学方程式计算中的应用
物质的量在化学方程式计算中的应用
模型建构
2Na + 2H2O === 2NaOH + H2↑
化学方程式中化学计量数与相关物理量的关系
2
∶
∶
∶
2
2
1
化学计量数之比:
2 mol
物质的量之比:
∶
∶
∶
2 mol
2 mol
1 mol
2 NA
扩大NA倍:
∶
∶
∶
2 NA
2 NA
1 NA
∶
∶
∶
扩大6.02×1023倍:
2×6.02×1023
2×6.02×1023
2×6.02×1023
1×6.02×1023
实验模拟工业上用CO与氧化铁反应炼铁,若参加反应的一氧化碳为56 g,则生成的铁的物质的量为多少?
解:
28×3 g
56×2 g
56 g
m(Fe)
m(Fe)=56×4/3 g
n(Fe)=56×4/3 g÷56 g/mol=1.3 mol
答:
生成的铁的物质的量为1.3 mol。
实验模拟工业上用CO与氧化铁反应炼铁,若参加反应的一氧化碳为56 g,则生成的铁的物质的量为多少?
解:
n(Fe)=56 g×2 mol/(28×3 g)=1.3 mol
28×3 g
2 mol
56 g
n(Fe)
答:
生成的铁的物质的量为1.3 mol。
实验模拟工业上用CO与氧化铁反应炼铁,若参加反应的一氧化碳为56 g,则生成的铁的物质的量为多少?
解:
56 g一氧化碳的物质的量为2 mol
3 mol
2 mol
2 mol
n(Fe)
n(Fe)=2 mol×2 mol/3 mol=1.3 mol
答:
生成的铁的物质的量为1.3 mol。
物质的量在化学方程式计算中的应用
进行物质的量应用于化学方程式的计算时,须按以下步骤进行:
①写出有关反应方程式
②找出相关物质的化学计量数之比
③对应化学计量数,找出相关物质的物质的量的关系
④根据物质的量的关系,按照比例相等的模式进行计算
物质的量浓度及物质的量浓度溶液的配制
物质的量浓度及物质的量浓度溶液的配制
例2、某品牌84消毒液,经折算,有效成分NaClO的含量为105 g/L。该消毒液NaClO的物质的量浓度是多少?
以1 L 消毒液为例进行计算
NaClO质量为 105 g
n
m
M
105 g
35.5 g/mol
1.41 mol
c
n
V(aq)
1 L
1.41 mol/L
1.41 mol
NaClO的物质的量为
分析过程:
NaClO的物质的量浓度为
物质的量浓度溶液的配制
5.4
10 mL量筒
500 mL容量瓶
向烧杯中加入一定量的水,
再将浓硫酸沿烧杯内壁慢慢倒入,并用玻璃棒不断搅拌
AC
①未采用玻璃棒引流;②未采用500 mL容量瓶
物质的量的思维导图
物质的量思维导图
物质的量
课堂评价
D
课堂评价
C
课堂评价
C
课堂评价
500
课堂评价
C
课堂评价
10.0
cd
c
课堂评价
偏低
无影响
课堂评价
A
课堂评价
C
大单元教学课件
新人教版 化学
必修第一册
第三单元
海水中的重要元素
——钠和氯
A
物质的量
从海洋到用户之计算工具篇
物质的量总结提升
学习目标
1,能基于物质的量认识物质组成及其化学变化,运用物质的量、摩尔质量、气体摩尔体积、物质的量浓度之间的相互关系进行简单计算
2,通过完成物质的量的学习,使学生了解科学的推理过程,理解微观粒子模型在化学研究中的重要作用。通过类比等方法学习物质的量的概念的过程,建立逻辑推理、归纳推理、模型认知能力。
3,通过对概念的透彻理解,锻炼严谨、认真的学习态度,体会定量研究的方法对研究和学习化学的重要作用。
从海洋到用户之计算工具
物质的量
化学方程式中化学计量数与相关物理量的关系
2CO + O2 2CO2
化学计量数 2 __ __
扩大NA倍 2NA ___ ____
物质的量 2 mol _____ _____
质量 56 g _____ ____
标况下气体体积 44.8 L ______ ______
1
2
NA
2NA
1 mol
2 mol
32 g
88 g
22.4 L
44.8 L
结论:化学方程式中各物质的化学计量数之比等于其粒子数目之比,等于其物质的量之比,也等于同温同压下气体的体积之比
物质的量与其它物理量之间的联系
物质的量是联系各物理量的纽带,可以简便的进行各量之间的转换。
质量 m
(g)
微粒数
N 个
÷M
物质的量
n(mol)
×M
× NA
÷ NA
气体体积V
×22.4L·mol-1
6.02×1023
摩尔质量
溶液体积
×物质的量浓度(c)
÷物质的量浓度
÷22.4L·mol-1
标准
状况下
物质的量
宏观
粒子的
数目
微观
物质的
质量
二、宏观物质与微观粒子间的计量关系
1.物质的量
宏观物质的计量(如质量、体积)与微观粒子的计量(如数目)间可通过物质的量联系在一起。
例1、(1)现有m g某气体,它由双原子分子构成,它的摩尔质量为
M g·mol-1。若阿伏加德罗常数值用NA表示,则:
①该气体的物质的量为 mol。
②该气体所含原子总数为 个。
③该气体在标准状况下的体积为 L。
(2)利用“化学计量在实验中的应用”的相关知识进行填空。
①含有6.02×1023个氧原子的H2SO4的物质的量是 mol。
②与标准状况下V L CO2所含氧原子数目相同的水的质量是________ (用分式表示)g。
③在一定的温度和压强下,1体积X2(g)跟3体积Y2(g)化合生成2体积化合
物,则该化合物的化学式是 。
m/M
2mNA/M
22.4m/M
0.25
45v/28
XY3
物质的量在化学方程式计算中的应用
物质的量在化学方程式计算中的应用
模型建构
2Na + 2H2O === 2NaOH + H2↑
化学方程式中化学计量数与相关物理量的关系
2
∶
∶
∶
2
2
1
化学计量数之比:
2 mol
物质的量之比:
∶
∶
∶
2 mol
2 mol
1 mol
2 NA
扩大NA倍:
∶
∶
∶
2 NA
2 NA
1 NA
∶
∶
∶
扩大6.02×1023倍:
2×6.02×1023
2×6.02×1023
2×6.02×1023
1×6.02×1023
实验模拟工业上用CO与氧化铁反应炼铁,若参加反应的一氧化碳为56 g,则生成的铁的物质的量为多少?
解:
28×3 g
56×2 g
56 g
m(Fe)
m(Fe)=56×4/3 g
n(Fe)=56×4/3 g÷56 g/mol=1.3 mol
答:
生成的铁的物质的量为1.3 mol。
实验模拟工业上用CO与氧化铁反应炼铁,若参加反应的一氧化碳为56 g,则生成的铁的物质的量为多少?
解:
n(Fe)=56 g×2 mol/(28×3 g)=1.3 mol
28×3 g
2 mol
56 g
n(Fe)
答:
生成的铁的物质的量为1.3 mol。
实验模拟工业上用CO与氧化铁反应炼铁,若参加反应的一氧化碳为56 g,则生成的铁的物质的量为多少?
解:
56 g一氧化碳的物质的量为2 mol
3 mol
2 mol
2 mol
n(Fe)
n(Fe)=2 mol×2 mol/3 mol=1.3 mol
答:
生成的铁的物质的量为1.3 mol。
物质的量在化学方程式计算中的应用
进行物质的量应用于化学方程式的计算时,须按以下步骤进行:
①写出有关反应方程式
②找出相关物质的化学计量数之比
③对应化学计量数,找出相关物质的物质的量的关系
④根据物质的量的关系,按照比例相等的模式进行计算
物质的量浓度及物质的量浓度溶液的配制
物质的量浓度及物质的量浓度溶液的配制
例2、某品牌84消毒液,经折算,有效成分NaClO的含量为105 g/L。该消毒液NaClO的物质的量浓度是多少?
以1 L 消毒液为例进行计算
NaClO质量为 105 g
n
m
M
105 g
35.5 g/mol
1.41 mol
c
n
V(aq)
1 L
1.41 mol/L
1.41 mol
NaClO的物质的量为
分析过程:
NaClO的物质的量浓度为
物质的量浓度溶液的配制
5.4
10 mL量筒
500 mL容量瓶
向烧杯中加入一定量的水,
再将浓硫酸沿烧杯内壁慢慢倒入,并用玻璃棒不断搅拌
AC
①未采用玻璃棒引流;②未采用500 mL容量瓶
物质的量的思维导图
物质的量思维导图
物质的量
课堂评价
D
课堂评价
C
课堂评价
C
课堂评价
500
课堂评价
C
课堂评价
10.0
cd
c
课堂评价
偏低
无影响
课堂评价
A
课堂评价
C
