2023-2024学年鲁科版高中化学选择性必修2 2.3配合物 课件(共19张PPT)
文档属性
| 名称 | 2023-2024学年鲁科版高中化学选择性必修2 2.3配合物 课件(共19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 49.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-17 00:00:00 | ||
图片预览


文档简介
(共19张PPT)
高二化学
鲁科版选择性必修2
第二章第三节
配合物
配合物
通过实验探究感受配合物的存在、制备和应用,形成“结构决定性质,性质决定应用”的观念。
通过介绍配合物在生物、医药领域的广泛应用,让学生了解无机化学的研究进程,树立社会责任感。
学科核心素养
通过分析NH4+中配位键的形成知道配位键的形成实质,了解配合物的广泛应用。
单击此处添加标题
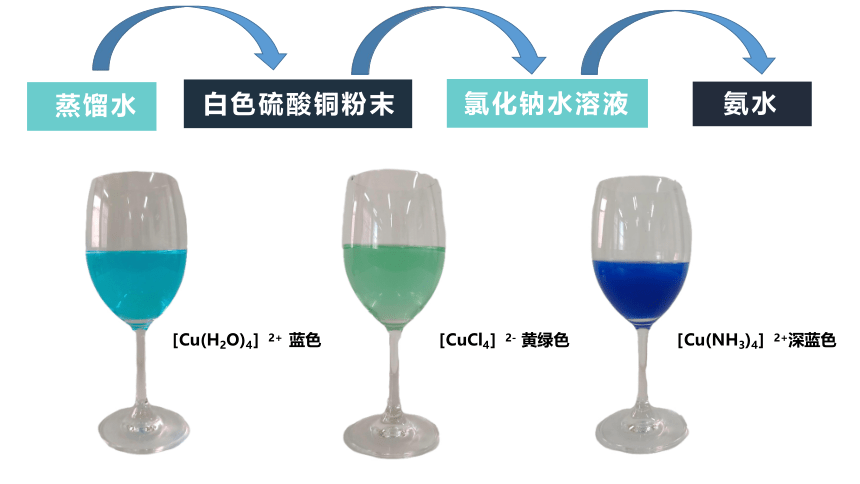
蒸馏水
白色硫酸铜粉末
氯化钠水溶液
氨水
[Cu(H2O)4]2+ 蓝色
[CuCl4]2- 黄绿色
[Cu(NH3)4]2+深蓝色
想一想
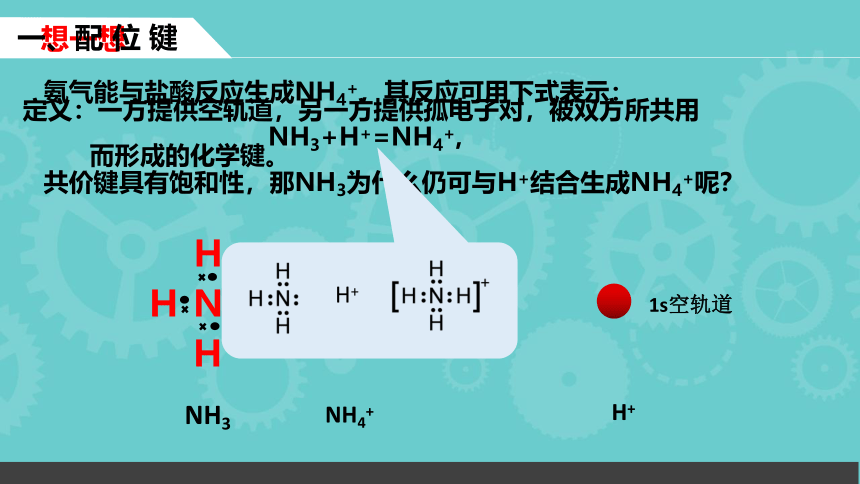
氨气能与盐酸反应生成NH4+,其反应可用下式表示:
NH3+H+=NH4+,
共价键具有饱和性,那NH3为什么仍可与H+结合生成NH4+呢?
NH3
H+
NH4+
1s空轨道
H
N
H
H
H+
一、配 位 键
定义:一方提供空轨道,另一方提供孤电子对,被双方所共用
而形成的化学键。
配位化合物的定义:
金属原子(或离子)
与含有孤电子对的分子
(或离子)以配位键结合形成的化合物,简称配合物。
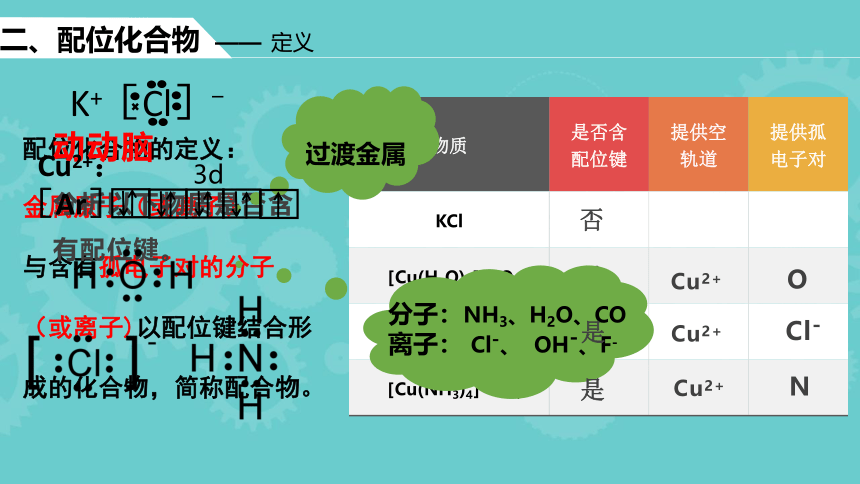
物质 是否含配位键 提供空轨道 提供孤电子对
KCl
[Cu(H2O)4]SO4
Na2[CuCl4]
[Cu(NH3)4]SO4
动动脑
分析以下物质是否含有配位键。
Cu2+
N
否
是
二、配位化合物 —— 定义
分子:NH3、H2O、CO
离子: Cl-、 OH-、F-
过渡金属
K+[Cl]-
3d
Cu2+:
[Ar]
是
是
Cu2+
Cu2+
Cl-
O
[Cu(H2O)4]SO4
内界(配离子)
外界
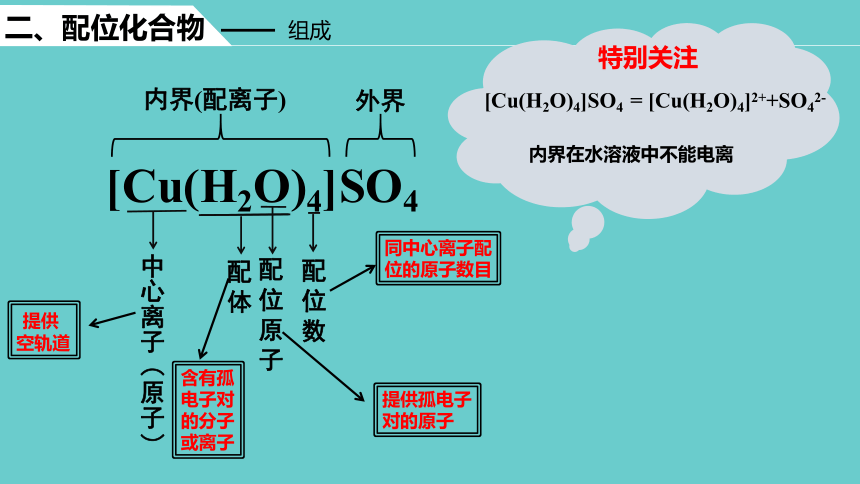
二、配位化合物 —— 组成
中心离子(原子)
提供
空轨道
配位原子
提供孤电子对的原子
配位数
同中心离子配
位的原子数目
配体
含有孤电子对 的分子或离子
特别关注
[Cu(H2O)4]SO4 = [Cu(H2O)4]2++SO42-
内界在水溶液中不能电离
2、配位数是直接同中心体配位的原子数目。 配位数不一定等于配体个数。
1、配位化合物一定含有配位键,但含有配位 键的化合物不一定是配位化合物。
3、电负性小的原子更容易提供孤电子对,作配位原子。
[Cu(H2O)4]2+ 蓝色
[CuCl4]2- 黄绿色
少量硫酸铜溶液
饱和氯化钠水溶液
概括提升
二、配位化合物 ——制备
设计方案
实施方案
成果展示
探究一:探究配合物的制备
任务1:探究CuCl2固体在溶解并稀释过程中溶液颜色的变化,根据信息支持从平衡移动的角度分析颜色变化的原因。
任务2:Fe(NO3)3、FeCl3溶液显黄色的原因。
配体种类
离子浓度
配合物的形成
溶液的酸碱性
平衡移动
配位能力
实验方案:
Fe(NO3)3溶液:向Fe(NO3)3溶液中加HNO3,若溶液黄色退去,则证明Fe3+和OH-配位。
实验方案:
FeCl3溶液:向FeCl3溶液中加HNO3,若溶液黄色退去,则证明Fe3+和OH-配位;
若溶液黄色不退去,则证明Fe3+和Cl-配位。
二、配 位 化 合 物 —— 应用
近几十年
新型配合物
1929
晶体场理论
1940
价键理论
1893
第一次提出
“配位理论”
配位化学的研究历程
二、配 位 化 合 物 —— 应用
二、配 位 化 合 物 —— 应用
探究二:体验配合物的应用
任务3:制备[Ag(NH3)2]OH溶液并用于和葡萄糖溶液反应制备银镜。
任务4:向CuSO4溶液中分别逐滴滴加氨水与NaOH溶液至过量,观察现象,根据信息支持分析原因。
信息支持
Cu(OH)2 + 2OH- [Cu(OH)4]2-
蓝色沉淀 深蓝色
Cu(OH)2 + 4NH3 =[Cu(NH3)4]2++2OH-
蓝色沉淀 深蓝色
实验任务
实施方案
成果展示
AgNO3+NH3·H2O = AgOH+NH4NO3
AgOH+2NH3 = [Ag(NH3)2]OH
Cu2+的检验
工业制镜
Cu2+ + 2NH3·H2O = Cu(OH)2 + 2NH4+
Cu(OH)2+4NH3 = [Cu(NH3)4]2++ 2OH-
深蓝色
Cu2+ + 2OH- = Cu(OH)2
Cu(OH)2 + 2OH- [Cu(OH)4]2-
深蓝色
当堂检测
1、下列配合物的水溶液中加入硝酸银
不能生成沉淀的是 ( )
A. [Co(NH3)4 Cl2]Cl B. [Co(NH3)3 Cl3]
C. [Co(NH3)6]Cl3 D. [Cu(NH3)4]Cl2
B
当堂检测
2、向盛有硫酸铜溶液的试管中滴加氨水,先生成
难溶物,继续滴加氨水,难溶物溶解,得到深蓝色透
明溶液。下列说法正确的是( )
A、反应后溶液不存在任何沉淀,所以反应前后Cu2+浓度不变
B、沉淀溶解后,生成深蓝色的配离子 [Cu(H2O)4 ]2+
C、该实验能证明 [Cu(NH3)4 ]2+比Cu(OH)2稳定
D、在配离子[Cu(NH3)4 ]2+中,Cu2+提供孤电子对,NH3提供空轨道
C
学以致用
中国疾控发布的数据显示,我国每年大约有6000多人急性一氧化碳中毒。
试用所学知识解释一氧化碳中毒的原理。
我们如何对一氧化碳中毒患者进行施救?
稀土之父—徐光宪
合成有特殊结构和性能的稀土配合物,引起稀土分离技术的全面革新。
量子化学之父— 唐敖庆
开展了配合化学模拟生
物固氮。
谢谢观看
高二化学
鲁科版选择性必修2
第二章第三节
配合物
配合物
通过实验探究感受配合物的存在、制备和应用,形成“结构决定性质,性质决定应用”的观念。
通过介绍配合物在生物、医药领域的广泛应用,让学生了解无机化学的研究进程,树立社会责任感。
学科核心素养
通过分析NH4+中配位键的形成知道配位键的形成实质,了解配合物的广泛应用。
单击此处添加标题
蒸馏水
白色硫酸铜粉末
氯化钠水溶液
氨水
[Cu(H2O)4]2+ 蓝色
[CuCl4]2- 黄绿色
[Cu(NH3)4]2+深蓝色
想一想
氨气能与盐酸反应生成NH4+,其反应可用下式表示:
NH3+H+=NH4+,
共价键具有饱和性,那NH3为什么仍可与H+结合生成NH4+呢?
NH3
H+
NH4+
1s空轨道
H
N
H
H
H+
一、配 位 键
定义:一方提供空轨道,另一方提供孤电子对,被双方所共用
而形成的化学键。
配位化合物的定义:
金属原子(或离子)
与含有孤电子对的分子
(或离子)以配位键结合形成的化合物,简称配合物。
物质 是否含配位键 提供空轨道 提供孤电子对
KCl
[Cu(H2O)4]SO4
Na2[CuCl4]
[Cu(NH3)4]SO4
动动脑
分析以下物质是否含有配位键。
Cu2+
N
否
是
二、配位化合物 —— 定义
分子:NH3、H2O、CO
离子: Cl-、 OH-、F-
过渡金属
K+[Cl]-
3d
Cu2+:
[Ar]
是
是
Cu2+
Cu2+
Cl-
O
[Cu(H2O)4]SO4
内界(配离子)
外界
二、配位化合物 —— 组成
中心离子(原子)
提供
空轨道
配位原子
提供孤电子对的原子
配位数
同中心离子配
位的原子数目
配体
含有孤电子对 的分子或离子
特别关注
[Cu(H2O)4]SO4 = [Cu(H2O)4]2++SO42-
内界在水溶液中不能电离
2、配位数是直接同中心体配位的原子数目。 配位数不一定等于配体个数。
1、配位化合物一定含有配位键,但含有配位 键的化合物不一定是配位化合物。
3、电负性小的原子更容易提供孤电子对,作配位原子。
[Cu(H2O)4]2+ 蓝色
[CuCl4]2- 黄绿色
少量硫酸铜溶液
饱和氯化钠水溶液
概括提升
二、配位化合物 ——制备
设计方案
实施方案
成果展示
探究一:探究配合物的制备
任务1:探究CuCl2固体在溶解并稀释过程中溶液颜色的变化,根据信息支持从平衡移动的角度分析颜色变化的原因。
任务2:Fe(NO3)3、FeCl3溶液显黄色的原因。
配体种类
离子浓度
配合物的形成
溶液的酸碱性
平衡移动
配位能力
实验方案:
Fe(NO3)3溶液:向Fe(NO3)3溶液中加HNO3,若溶液黄色退去,则证明Fe3+和OH-配位。
实验方案:
FeCl3溶液:向FeCl3溶液中加HNO3,若溶液黄色退去,则证明Fe3+和OH-配位;
若溶液黄色不退去,则证明Fe3+和Cl-配位。
二、配 位 化 合 物 —— 应用
近几十年
新型配合物
1929
晶体场理论
1940
价键理论
1893
第一次提出
“配位理论”
配位化学的研究历程
二、配 位 化 合 物 —— 应用
二、配 位 化 合 物 —— 应用
探究二:体验配合物的应用
任务3:制备[Ag(NH3)2]OH溶液并用于和葡萄糖溶液反应制备银镜。
任务4:向CuSO4溶液中分别逐滴滴加氨水与NaOH溶液至过量,观察现象,根据信息支持分析原因。
信息支持
Cu(OH)2 + 2OH- [Cu(OH)4]2-
蓝色沉淀 深蓝色
Cu(OH)2 + 4NH3 =[Cu(NH3)4]2++2OH-
蓝色沉淀 深蓝色
实验任务
实施方案
成果展示
AgNO3+NH3·H2O = AgOH+NH4NO3
AgOH+2NH3 = [Ag(NH3)2]OH
Cu2+的检验
工业制镜
Cu2+ + 2NH3·H2O = Cu(OH)2 + 2NH4+
Cu(OH)2+4NH3 = [Cu(NH3)4]2++ 2OH-
深蓝色
Cu2+ + 2OH- = Cu(OH)2
Cu(OH)2 + 2OH- [Cu(OH)4]2-
深蓝色
当堂检测
1、下列配合物的水溶液中加入硝酸银
不能生成沉淀的是 ( )
A. [Co(NH3)4 Cl2]Cl B. [Co(NH3)3 Cl3]
C. [Co(NH3)6]Cl3 D. [Cu(NH3)4]Cl2
B
当堂检测
2、向盛有硫酸铜溶液的试管中滴加氨水,先生成
难溶物,继续滴加氨水,难溶物溶解,得到深蓝色透
明溶液。下列说法正确的是( )
A、反应后溶液不存在任何沉淀,所以反应前后Cu2+浓度不变
B、沉淀溶解后,生成深蓝色的配离子 [Cu(H2O)4 ]2+
C、该实验能证明 [Cu(NH3)4 ]2+比Cu(OH)2稳定
D、在配离子[Cu(NH3)4 ]2+中,Cu2+提供孤电子对,NH3提供空轨道
C
学以致用
中国疾控发布的数据显示,我国每年大约有6000多人急性一氧化碳中毒。
试用所学知识解释一氧化碳中毒的原理。
我们如何对一氧化碳中毒患者进行施救?
稀土之父—徐光宪
合成有特殊结构和性能的稀土配合物,引起稀土分离技术的全面革新。
量子化学之父— 唐敖庆
开展了配合化学模拟生
物固氮。
谢谢观看
