第二节 物质的组成课件(共34张PPT)-2023-2024学年九年级化学上册同步精品课堂(鲁教版)
文档属性
| 名称 | 第二节 物质的组成课件(共34张PPT)-2023-2024学年九年级化学上册同步精品课堂(鲁教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-18 00:00:00 | ||
图片预览








文档简介
(共34张PPT)
第二节 物质的组成
第四章 我们周围的空气
学习目标
CONTENTS
1
掌握化学式及其含义,能用化学式表示某些常见物质的组成
3
了解相对分子质量的含义,能利用相对原子质量进行有关简单计算
2
了解化合价的含义,并熟记常见元素及原子团的化合价,并能利用化合价推求化学式
课堂导入
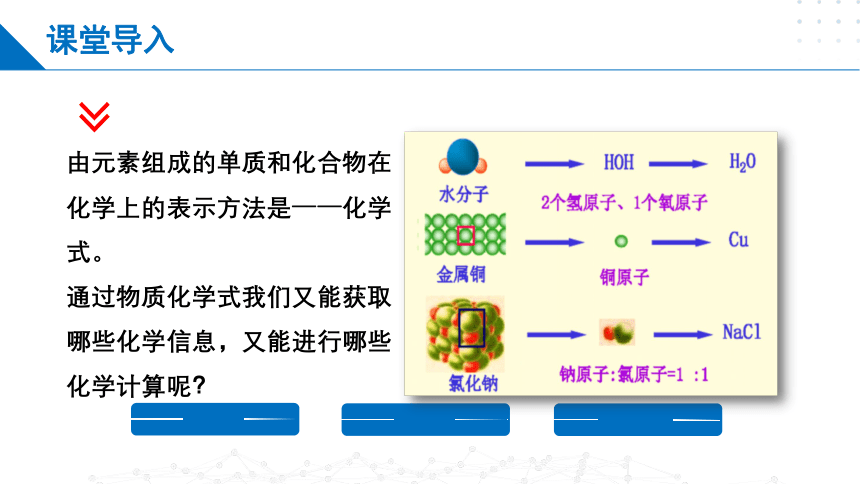
由元素组成的单质和化合物在化学上的表示方法是——化学式。
通过物质化学式我们又能获取哪些化学信息,又能进行哪些化学计算呢?
一、化学式反映物质的组成
化学式的定义
化学式是用元素符号和数字表示物质组成的式子。
任何纯净物都有固定的组成,不同的物质组成不同,
所以一种纯净物只用一个化学式来表示。因此,化学
式是对物质组成情况的真实反映。
水 H2O 二氧化碳 CO2 氧气 O2 氢气 H2
一、化学式反映物质的组成
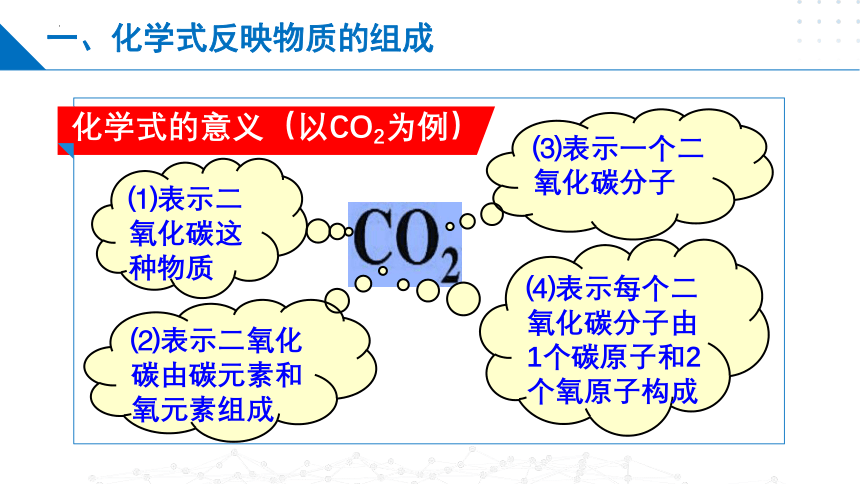
化学式的意义(以CO2为例)
⑶表示一个二氧化碳分子
⑴表示二氧化碳这种物质
⑷表示每个二氧化碳分子由1个碳原子和2个氧原子构成
⑵表示二氧化碳由碳元素和氧元素组成
一、化学式反映物质的组成
化学式的意义
宏观
微观
(1)表示一种物质
(2)表示该物质的元素组成
(1)若该物质由分子构成,还可表示该物质的一个分子
(2)表示该物质的各组成元素的原子个数比
一、化学式反映物质的组成
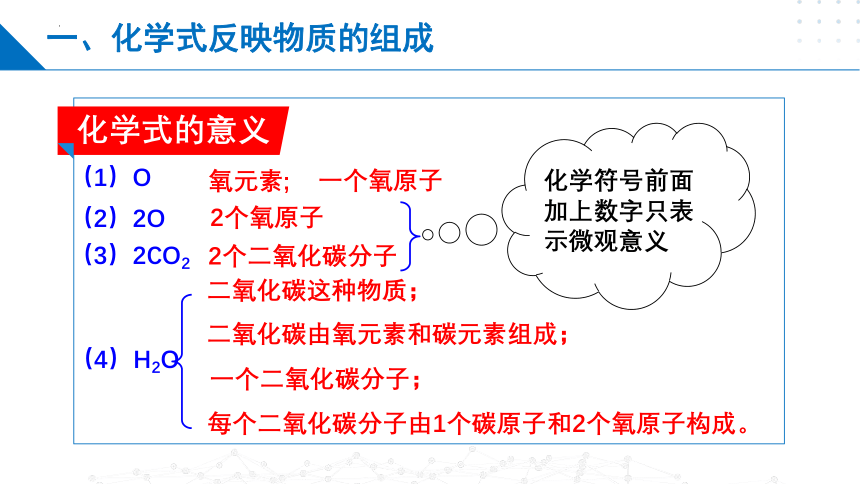
化学式的意义
(1)O
(2)2O
(4)H2O
(3)2CO2
2个二氧化碳分子
2个氧原子
氧元素;
一个氧原子
二氧化碳这种物质;
二氧化碳由氧元素和碳元素组成;
一个二氧化碳分子;
每个二氧化碳分子由1个碳原子和2个氧原子构成。
化学符号前面加上数字只表示微观意义
二、化学式的书写
1.单质
(1)原子型(直接用元素符号表示)
——金属、稀有气体、部分固态非金属:
如:Cu、Fe、He、Ne、Si、C
(2)分子型 (元素符号右下角标表示一个分子所含原子个数)——气态或液态非金属:
如:O2、N2、H2、Cl2、Br2、 O3
二、化学式的书写
2.化合物
(1)氧化物化学式写法:
一般氧元素在右, 另一元素在左。
如: H2O 、CO2 、HgO 。
(2)金属和非金属组成的化合物:
一般金属元素在左,非金属元素在右。
如: NaCl 、 KCl 、ZnS。
二、化学式的书写
3.化学式的读法
(1)单质:直接读物质名称。如:Fe 铁 O2 氧气
(2)化合物:
①两种元素组成的化合物从右到左读作“某化某”,有的把右下角的数字也读出。
如:NaCl 氯化钠 Fe3O4 四氧化三铁
②含有原子团的化合物读作:“某酸某”。
如:Na2CO3 碳酸钠 KMnO4 高锰酸钾
1.化合价定义
三、化合价
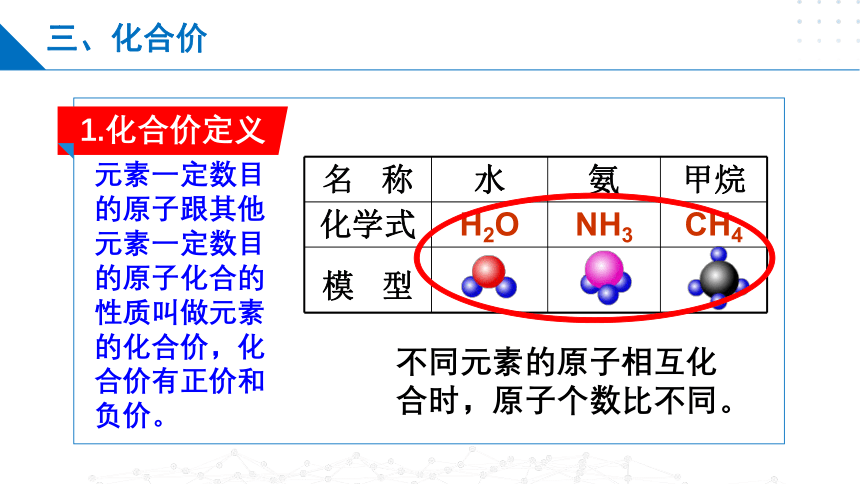
元素一定数目的原子跟其他元素一定数目的原子化合的性质叫做元素的化合价,化合价有正价和负价。
名 称 水 氨 甲烷
化学式 H2O NH3 CH4
模 型
不同元素的原子相互化合时,原子个数比不同。
2.原子团
三、化合价
一种或多种元素的原子结合在一起形成带电的离子,作为一个整体参加化学反应,这样的原子集合称为原子团。化学上常用“根”来命名。
如氢氧根(OH) 、碳酸根(CO3) 、硫酸根(SO4) 、硝酸根(NO3) 、 铵根(NH4)。
3.常见元素和原子团的主要化合价
三、化合价
名称 符号 化合价 名称 符号 化合价
钠 Na +1 碳 C +2 +4
钙 Ca +2 氯 Cl -1
钾 K +1 硫 S -2 +4 +6
镁 Mg +2 氮 N -3 +2 +4 +5
铝 Al +3 氢氧根 OH -1
锌 Zn +2 碳酸根 CO3 -2
铁 Fe +2 +3 硝酸根 NO3 -1
铜 Cu +2 硫酸根 SO4 -2
氢 H +1 铵 根 NH4 +1
氧 O -2
元素和原子团的主要化合价记忆口诀
三、化合价
元素化合价
钾 钠 银 氢 正 一 价,钙 镁 钡 锌 正 二 价;
铁 正 二 三 铜 一 二,三 铝 四 硅 二 四 碳;
氟 氯 溴 碘 氮 价 多,单 质 零 价 永 不 变。
原子团化合价
负 一 硝 酸 氢 氧 根,负 二 硫 酸 碳 酸 根;
负 三 记 住 磷 酸 根,正 一 价 的 是 铵 根。
4.化合价的一般规律
三、化合价
④化合物中各种元素化合价的代数和为零
⑤单质中元素的化合价为零
①通常,金属元素显正价,非金属元素显负价
②一些元素在不同物质中可显不同的化合价
③一些元素在同一物质中可显不同的化合价
例:FeO Fe2O3
+2
+3
例: NH4NO3
-3
+5
(氧化亚铁)
(氧化铁)
5.化合价与离子符号书写比较
三、化合价
化合价 离子符号
区别
联系 ⑴元素符号的正上方标注化合价
⑵符号在前,数字在后
⑶“1”不能省
⑴元素符号的右上角标注所带电荷
⑵数字在前,符号在后
⑶“1”必须省
同种元素(或原子团)的化合价和对应离子的电荷,通常数值相等,位置相反
6.化合价的应用
三、化合价
·写出组成该物质的元素符号,正价在前、负价在后。 Al O
·标上元素的化合价 Al O
·计算元素化合价的最小公倍数 2×3=6
·求出原子的个数 6÷3=2,6÷2=3
·将原子个数分别写在元素符号的右下方 Al2O3
·检验 (+3)×2 +(-2)×3=0
(1)已知化合价求化学式 例1:写出氧化铝的化学式
+3
-2
6.化合价的应用
三、化合价
·设铁元素的化合价为X
·明确氧元素的化合价为-2
·计算(化合物中各元素的代数和为零)
X×2 +(-2)×3=0
X=+3
·将化合价写在化学式中铁元素的上方Fe2O3
(2)已知化学式求化合价 例2:求Fe2O3中铁元素的化合价
+3
1.计算组成物质的各元素的质量比
四、纯净物中元素之间的质量关系
在化合物中,各元素质量之比就是各元素的相对原子质量与它的原子个数乘积之间的比值。
例1:计算CO2中各元素的质量比。
C:O =
(12×1)∶
(16×2)
相对原子质量
原子个数
2.计算物质中某元素的质量分数
四、纯净物中元素之间的质量关系
根据化合物的化学式,就可以确定组成物质的各种成分的质量在物质总质量中所占的质量分数。质量分数可以用百分数表示。
该元素的相对原子质量(Ar)× 原子个数
化合物的相对分子质量(Mr)
某元素的质量分数= ×100%
(ω)
2.计算物质中某元素的质量分数
四、纯净物中元素之间的质量关系
例2:计算NH4NO3中氮元素的质量分数。
氮元素的质量分数=
————————
14×2
14×2+1×4+16×3
×100%
=
14×2
80
×100%
=
35%
————————
氮元素的质量:
相对原子质量×原子个数
NH4NO3的相对分子质量:各元素原子的相对原子质量×原子个数之和
3.计算一定质量的物质中某元素的质量
四、纯净物中元素之间的质量关系
例2:求60gNH4NO3中含有氮的质量。
用物质的质量乘以各种元素在物质总质量中所占的质量分数,既可以得到物质中该元素的质量。
解:m(N)= m(NH4NO3)×ω(N)
= 60g×35%
= 21g
答:60g NH4NO3中氮的质量是21g。
NH4NO3的质量
NH4NO3中N的质量分数
典型例题
知识点一:化学式
【典例1】类推的思维方法在化学学习中有广泛的应用。
例如:
已知氧化钡的化学式为BaO, 由此可推断,过氧化钡的化学式为( )
A.Ba2O B.BaO2 C.Ba2O2 D.BaO3
B
典型例题
知识点二:化合价及化合价的应用
【典例2】下列关于化合价的说法,正确的是( )
A.非金属元素在化合物中既可显负价也可显正价 B.金属元素都只有一种化合价
C.N2、NH3、NH4+ 中N的化学价逐渐升高 D.氢气中氢元素的化合价为+1价
A
典型例题
知识点三:有关化学式的计算
【典例3】粮食的主要成分是淀粉,淀粉进入人体后,在酶的作用下转化为可被人体吸收的葡萄糖(葡萄糖的化学式为C6H12O6)。
(1)C6H12O6由_______种元素组成(填数字)。
(2)C6H12O6分子中C、H、O原子的个数比为__________。
(3)葡萄糖中碳元素的质量分数为__________。
3
6:12:6=1:2:1
————————
12×6
12×6+1×12+16×6
×100%
=
35%
课堂达标
(二)药理作用
1.下列物质的化学式书写正确的是( )
A.碳酸钠NaCO3 B.氢氧化钠Na(OH)2
C.氧化铁O3Fe2 D.硫酸钠Na2SO4
2.下列化学符号中关于数字“2”的意义说法不正确的是( )
A.2NO﹣﹣表示2个一氧化氮分子
B.P2O5﹣﹣表示五氧化二磷中含有2个磷原子
C.Cu2+﹣﹣表示1个铜离子带2个单位的正电荷
D. ﹣﹣表示氧化汞中汞元素的化合价为+2价
D
B
课堂达标
(二)药理作用
3.下列物质HCl、X、KClO3、KClO4是氯元素的化合价按一定规律排列的,则X代表的物质不可能是( )
A.NaCl B.Ca(ClO)2 C.Cl2 D.Cl2O3
4.下列有关化合价的叙述正确的是( )
A.化合价与原子最外层电子数有关 B.甲烷(CH4)中碳元素化合价为+4
C.氧气中氧元素的化合价为﹣2 D.氯元素化合价永远为-1
A
A
课堂达标
(二)药理作用
5. “芯片”是电子产品的核心部件,氮化镓是制造芯片的材料之一,如图是镓元素(Ga)的原子结构示意图及元素周期表的一部分。下列说法不正确的是( )
A.镓属于金属元素,m=3
B.氯化镓的化学式为GaCl2
C.镓元素的位置应该在Z处
D.镓的最外层电子数与A1相同
B
课堂达标
(二)药理作用
6.有些年轻人喜欢染发,染发时一般要用到一种着色剂﹣对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图所示。下列有关对苯二胺的说法不正确的是( )
A.对苯二胺的化学式为C6H8N2
B.对苯二胺的相对分子质量为108g
C.对苯二胺中碳、氢、氮元素的质量比为18:2:7
D.对苯二胺对人体有害
B
课堂达标
(二)药理作用
7.碘元素是人体必需的微量元素之,碘缺乏会引起甲状腺肿大,幼儿缺碘会影响生长发育,造成思维迟钝,过量也会引起甲状腺肿大。请根据图示回答下列问题。
(1)碘元素的相对原子质量为 _____。
(2)氯元素和碘元素的化学性质相似,原因是 _____。
(3)碘元素与镁元素形成的化合物的化学式为 _____。
(4)我国采用在食盐中添加碘酸钾(KIO3)的方法来防止人体缺碘,碘酸钾中碘元素的化合价 _____价。
126.9
最外层电子数相同
MgI2
+5
课堂达标
8.在江南,有句俗语叫做“清明螺赛肥鹅”,螺蛳之所以鲜美是因为螺肉内含有谷氨酸等多种增鲜物质,已知谷氨酸的化学式为C5H9NO4,请回答以下问题:
(1)该物质是由 ___种元素组成。
(2)该物质中碳、氧元素的质量比是 ___。
(3)14.7g谷氨酸中氧元素的质量与多少gCa(OH)2中氧元素的质量相等?(要求写出计算过程)
课堂达标
(二)药理作用
解:(1)有化学式可知,含有碳、氢、氮、氧4种元素。
(2)该物质中碳、氧元素的质量比是(12×5):(16×4)=15:16。
(3)设氢氧化钙的质量为x
14.7g× =x×
x=14.8g
答:14.7g谷氨酸中氧元素的质量与14.8gCa(OH)2中氧元素的质量相等。
——————————
16×4
12×5+1×9+14+16×4
×100%
———————
16×2
40+(16+1)×2
×100%
课堂小结
不良反应
1.化学式及化学式表示的意义。
2.化合价的含义及常见元素的化合价。
3.根据化合价正确书写物质的化学式及根据物质的化学式能判断某元素的化合价。
4.根据化学式计算物质的相对分子质量、物质各组成元素的质量比、物质中某元素质量分数及质量。
物质的组成
谢谢观看
THANKS
第二节 物质的组成
第四章 我们周围的空气
学习目标
CONTENTS
1
掌握化学式及其含义,能用化学式表示某些常见物质的组成
3
了解相对分子质量的含义,能利用相对原子质量进行有关简单计算
2
了解化合价的含义,并熟记常见元素及原子团的化合价,并能利用化合价推求化学式
课堂导入
由元素组成的单质和化合物在化学上的表示方法是——化学式。
通过物质化学式我们又能获取哪些化学信息,又能进行哪些化学计算呢?
一、化学式反映物质的组成
化学式的定义
化学式是用元素符号和数字表示物质组成的式子。
任何纯净物都有固定的组成,不同的物质组成不同,
所以一种纯净物只用一个化学式来表示。因此,化学
式是对物质组成情况的真实反映。
水 H2O 二氧化碳 CO2 氧气 O2 氢气 H2
一、化学式反映物质的组成
化学式的意义(以CO2为例)
⑶表示一个二氧化碳分子
⑴表示二氧化碳这种物质
⑷表示每个二氧化碳分子由1个碳原子和2个氧原子构成
⑵表示二氧化碳由碳元素和氧元素组成
一、化学式反映物质的组成
化学式的意义
宏观
微观
(1)表示一种物质
(2)表示该物质的元素组成
(1)若该物质由分子构成,还可表示该物质的一个分子
(2)表示该物质的各组成元素的原子个数比
一、化学式反映物质的组成
化学式的意义
(1)O
(2)2O
(4)H2O
(3)2CO2
2个二氧化碳分子
2个氧原子
氧元素;
一个氧原子
二氧化碳这种物质;
二氧化碳由氧元素和碳元素组成;
一个二氧化碳分子;
每个二氧化碳分子由1个碳原子和2个氧原子构成。
化学符号前面加上数字只表示微观意义
二、化学式的书写
1.单质
(1)原子型(直接用元素符号表示)
——金属、稀有气体、部分固态非金属:
如:Cu、Fe、He、Ne、Si、C
(2)分子型 (元素符号右下角标表示一个分子所含原子个数)——气态或液态非金属:
如:O2、N2、H2、Cl2、Br2、 O3
二、化学式的书写
2.化合物
(1)氧化物化学式写法:
一般氧元素在右, 另一元素在左。
如: H2O 、CO2 、HgO 。
(2)金属和非金属组成的化合物:
一般金属元素在左,非金属元素在右。
如: NaCl 、 KCl 、ZnS。
二、化学式的书写
3.化学式的读法
(1)单质:直接读物质名称。如:Fe 铁 O2 氧气
(2)化合物:
①两种元素组成的化合物从右到左读作“某化某”,有的把右下角的数字也读出。
如:NaCl 氯化钠 Fe3O4 四氧化三铁
②含有原子团的化合物读作:“某酸某”。
如:Na2CO3 碳酸钠 KMnO4 高锰酸钾
1.化合价定义
三、化合价
元素一定数目的原子跟其他元素一定数目的原子化合的性质叫做元素的化合价,化合价有正价和负价。
名 称 水 氨 甲烷
化学式 H2O NH3 CH4
模 型
不同元素的原子相互化合时,原子个数比不同。
2.原子团
三、化合价
一种或多种元素的原子结合在一起形成带电的离子,作为一个整体参加化学反应,这样的原子集合称为原子团。化学上常用“根”来命名。
如氢氧根(OH) 、碳酸根(CO3) 、硫酸根(SO4) 、硝酸根(NO3) 、 铵根(NH4)。
3.常见元素和原子团的主要化合价
三、化合价
名称 符号 化合价 名称 符号 化合价
钠 Na +1 碳 C +2 +4
钙 Ca +2 氯 Cl -1
钾 K +1 硫 S -2 +4 +6
镁 Mg +2 氮 N -3 +2 +4 +5
铝 Al +3 氢氧根 OH -1
锌 Zn +2 碳酸根 CO3 -2
铁 Fe +2 +3 硝酸根 NO3 -1
铜 Cu +2 硫酸根 SO4 -2
氢 H +1 铵 根 NH4 +1
氧 O -2
元素和原子团的主要化合价记忆口诀
三、化合价
元素化合价
钾 钠 银 氢 正 一 价,钙 镁 钡 锌 正 二 价;
铁 正 二 三 铜 一 二,三 铝 四 硅 二 四 碳;
氟 氯 溴 碘 氮 价 多,单 质 零 价 永 不 变。
原子团化合价
负 一 硝 酸 氢 氧 根,负 二 硫 酸 碳 酸 根;
负 三 记 住 磷 酸 根,正 一 价 的 是 铵 根。
4.化合价的一般规律
三、化合价
④化合物中各种元素化合价的代数和为零
⑤单质中元素的化合价为零
①通常,金属元素显正价,非金属元素显负价
②一些元素在不同物质中可显不同的化合价
③一些元素在同一物质中可显不同的化合价
例:FeO Fe2O3
+2
+3
例: NH4NO3
-3
+5
(氧化亚铁)
(氧化铁)
5.化合价与离子符号书写比较
三、化合价
化合价 离子符号
区别
联系 ⑴元素符号的正上方标注化合价
⑵符号在前,数字在后
⑶“1”不能省
⑴元素符号的右上角标注所带电荷
⑵数字在前,符号在后
⑶“1”必须省
同种元素(或原子团)的化合价和对应离子的电荷,通常数值相等,位置相反
6.化合价的应用
三、化合价
·写出组成该物质的元素符号,正价在前、负价在后。 Al O
·标上元素的化合价 Al O
·计算元素化合价的最小公倍数 2×3=6
·求出原子的个数 6÷3=2,6÷2=3
·将原子个数分别写在元素符号的右下方 Al2O3
·检验 (+3)×2 +(-2)×3=0
(1)已知化合价求化学式 例1:写出氧化铝的化学式
+3
-2
6.化合价的应用
三、化合价
·设铁元素的化合价为X
·明确氧元素的化合价为-2
·计算(化合物中各元素的代数和为零)
X×2 +(-2)×3=0
X=+3
·将化合价写在化学式中铁元素的上方Fe2O3
(2)已知化学式求化合价 例2:求Fe2O3中铁元素的化合价
+3
1.计算组成物质的各元素的质量比
四、纯净物中元素之间的质量关系
在化合物中,各元素质量之比就是各元素的相对原子质量与它的原子个数乘积之间的比值。
例1:计算CO2中各元素的质量比。
C:O =
(12×1)∶
(16×2)
相对原子质量
原子个数
2.计算物质中某元素的质量分数
四、纯净物中元素之间的质量关系
根据化合物的化学式,就可以确定组成物质的各种成分的质量在物质总质量中所占的质量分数。质量分数可以用百分数表示。
该元素的相对原子质量(Ar)× 原子个数
化合物的相对分子质量(Mr)
某元素的质量分数= ×100%
(ω)
2.计算物质中某元素的质量分数
四、纯净物中元素之间的质量关系
例2:计算NH4NO3中氮元素的质量分数。
氮元素的质量分数=
————————
14×2
14×2+1×4+16×3
×100%
=
14×2
80
×100%
=
35%
————————
氮元素的质量:
相对原子质量×原子个数
NH4NO3的相对分子质量:各元素原子的相对原子质量×原子个数之和
3.计算一定质量的物质中某元素的质量
四、纯净物中元素之间的质量关系
例2:求60gNH4NO3中含有氮的质量。
用物质的质量乘以各种元素在物质总质量中所占的质量分数,既可以得到物质中该元素的质量。
解:m(N)= m(NH4NO3)×ω(N)
= 60g×35%
= 21g
答:60g NH4NO3中氮的质量是21g。
NH4NO3的质量
NH4NO3中N的质量分数
典型例题
知识点一:化学式
【典例1】类推的思维方法在化学学习中有广泛的应用。
例如:
已知氧化钡的化学式为BaO, 由此可推断,过氧化钡的化学式为( )
A.Ba2O B.BaO2 C.Ba2O2 D.BaO3
B
典型例题
知识点二:化合价及化合价的应用
【典例2】下列关于化合价的说法,正确的是( )
A.非金属元素在化合物中既可显负价也可显正价 B.金属元素都只有一种化合价
C.N2、NH3、NH4+ 中N的化学价逐渐升高 D.氢气中氢元素的化合价为+1价
A
典型例题
知识点三:有关化学式的计算
【典例3】粮食的主要成分是淀粉,淀粉进入人体后,在酶的作用下转化为可被人体吸收的葡萄糖(葡萄糖的化学式为C6H12O6)。
(1)C6H12O6由_______种元素组成(填数字)。
(2)C6H12O6分子中C、H、O原子的个数比为__________。
(3)葡萄糖中碳元素的质量分数为__________。
3
6:12:6=1:2:1
————————
12×6
12×6+1×12+16×6
×100%
=
35%
课堂达标
(二)药理作用
1.下列物质的化学式书写正确的是( )
A.碳酸钠NaCO3 B.氢氧化钠Na(OH)2
C.氧化铁O3Fe2 D.硫酸钠Na2SO4
2.下列化学符号中关于数字“2”的意义说法不正确的是( )
A.2NO﹣﹣表示2个一氧化氮分子
B.P2O5﹣﹣表示五氧化二磷中含有2个磷原子
C.Cu2+﹣﹣表示1个铜离子带2个单位的正电荷
D. ﹣﹣表示氧化汞中汞元素的化合价为+2价
D
B
课堂达标
(二)药理作用
3.下列物质HCl、X、KClO3、KClO4是氯元素的化合价按一定规律排列的,则X代表的物质不可能是( )
A.NaCl B.Ca(ClO)2 C.Cl2 D.Cl2O3
4.下列有关化合价的叙述正确的是( )
A.化合价与原子最外层电子数有关 B.甲烷(CH4)中碳元素化合价为+4
C.氧气中氧元素的化合价为﹣2 D.氯元素化合价永远为-1
A
A
课堂达标
(二)药理作用
5. “芯片”是电子产品的核心部件,氮化镓是制造芯片的材料之一,如图是镓元素(Ga)的原子结构示意图及元素周期表的一部分。下列说法不正确的是( )
A.镓属于金属元素,m=3
B.氯化镓的化学式为GaCl2
C.镓元素的位置应该在Z处
D.镓的最外层电子数与A1相同
B
课堂达标
(二)药理作用
6.有些年轻人喜欢染发,染发时一般要用到一种着色剂﹣对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如图所示。下列有关对苯二胺的说法不正确的是( )
A.对苯二胺的化学式为C6H8N2
B.对苯二胺的相对分子质量为108g
C.对苯二胺中碳、氢、氮元素的质量比为18:2:7
D.对苯二胺对人体有害
B
课堂达标
(二)药理作用
7.碘元素是人体必需的微量元素之,碘缺乏会引起甲状腺肿大,幼儿缺碘会影响生长发育,造成思维迟钝,过量也会引起甲状腺肿大。请根据图示回答下列问题。
(1)碘元素的相对原子质量为 _____。
(2)氯元素和碘元素的化学性质相似,原因是 _____。
(3)碘元素与镁元素形成的化合物的化学式为 _____。
(4)我国采用在食盐中添加碘酸钾(KIO3)的方法来防止人体缺碘,碘酸钾中碘元素的化合价 _____价。
126.9
最外层电子数相同
MgI2
+5
课堂达标
8.在江南,有句俗语叫做“清明螺赛肥鹅”,螺蛳之所以鲜美是因为螺肉内含有谷氨酸等多种增鲜物质,已知谷氨酸的化学式为C5H9NO4,请回答以下问题:
(1)该物质是由 ___种元素组成。
(2)该物质中碳、氧元素的质量比是 ___。
(3)14.7g谷氨酸中氧元素的质量与多少gCa(OH)2中氧元素的质量相等?(要求写出计算过程)
课堂达标
(二)药理作用
解:(1)有化学式可知,含有碳、氢、氮、氧4种元素。
(2)该物质中碳、氧元素的质量比是(12×5):(16×4)=15:16。
(3)设氢氧化钙的质量为x
14.7g× =x×
x=14.8g
答:14.7g谷氨酸中氧元素的质量与14.8gCa(OH)2中氧元素的质量相等。
——————————
16×4
12×5+1×9+14+16×4
×100%
———————
16×2
40+(16+1)×2
×100%
课堂小结
不良反应
1.化学式及化学式表示的意义。
2.化合价的含义及常见元素的化合价。
3.根据化合价正确书写物质的化学式及根据物质的化学式能判断某元素的化合价。
4.根据化学式计算物质的相对分子质量、物质各组成元素的质量比、物质中某元素质量分数及质量。
物质的组成
谢谢观看
THANKS
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
