2.2.2 化学反应能量转化的重要应用——化学电池-2023-2024学年高一化学鲁科版必修第二册课件(共19张PPT)
文档属性
| 名称 | 2.2.2 化学反应能量转化的重要应用——化学电池-2023-2024学年高一化学鲁科版必修第二册课件(共19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-19 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
第2节 化学反应与能量转化
第2课时 化学反应能量转化的重要
应用——化学电池
第2章
化学键 化学反应规律
【自主学习】
1.氧化还原反应中概念间的关系
2.人们常常利用化学反应将化学能转化为 、 等其他形式的能量,用于生产、生活和科研
3.化学电池:根据 原理制成的电池
4.原电池:利用 反应将 能直接转化成 能的装置
热能
电能
原电池
氧化还原
化学
电
形
形
色
色
的
电
池
二、化学反应能量转化的重要应用——化学电池
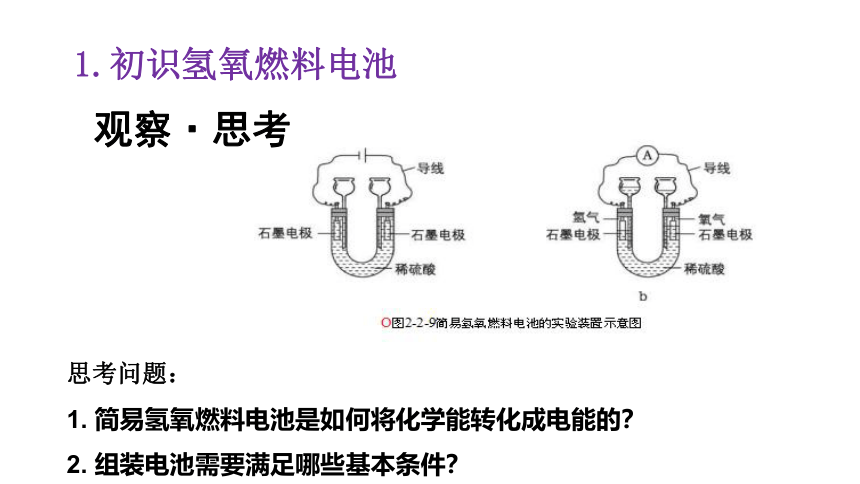
观察·思考
1.初识氢氧燃料电池
思考问题:
1. 简易氢氧燃料电池是如何将化学能转化成电能的?
2. 组装电池需要满足哪些基本条件?
负极
正极
还原剂失电子
氧化剂得电子
电子流出
电子流入
离子
导体
e-
导体
导线
电解质溶液
发生氧化反应
发生还原反应
+
-
e-
负极反应物
失电子氧化反应
正极反应物
得电子还原反应
电解质溶液
传导电子
(1)原电池基本工作原理
闭合回路
原电池
的构成
2.两个电极
3.电子导体
1.电极反应物
——导线
——传导电荷的电解质
——导电的固体
——在两极上自发进行氧化还原反应
闭合
回路
4.离子导体
(2)原电池构成要素
例1 下列图示能形成原电池的有哪些?
稀硫酸
稀硫酸
稀硫酸
稀硫酸
稀硫酸
酒精
CuSO4溶液
√
√
√
√
×
×
×
认识锌锰干电池——
锌锰干电池分为酸性锌锰干电池和碱性锌锰干电池两种。酸性锌锰干电池的组成如右图所示。
在酸性锌锰干电池中,负极反应物和正极反应物分别是什么?正负极材料分别是什么?离子导体是什么?
负极反应物和负极材料
正极反应物
离子导体
正极材料
身边的化学
【交流·研讨】
2.设计简单原电池
活动·探究(课本P51页)
利用所给用品设计装置并进行实验,将下列反应所释放的能量转化为电能。
实验原理:Zn + 2H+ = Zn2+ + H2↑
实验用品: 锌片,铜片,石墨棒,稀硫酸,稀盐酸;
烧杯,导线,电流表,开关。
(或石墨)
设计思路及依据 实验装置 实验现象与电极反应
Zn+2H+====Zn2++H2↑ 负极:_____________;电极反应为
___________________
正极:铜片或石墨棒表面___________;电极反应为_________________
确定 负极 选择负极反应物:
选择负极材料:
确定 正极 选择正极反应物:
选择正极材料:
构成闭 合回路 选择离子导体:
选择电子导体:
锌片
锌片
氢离子
铜片(或石墨)
稀硫酸
导线
2H++2e-=H2↑
有气泡产生
思考
1. 分析下图所示原电池的工作原理。
2. 锌片、铜片与稀硫酸,哪些可以替换为其他物质却同样能产生电流?
铜锌原电池工作原理
正极
负极
氧化反应
电极反应式:
Zn-2e-=Zn2+
还原反应
电极反应式:
2H++2e-=H2↑
电解质溶液
不
断
溶
解
阳
离
子
移
向
e- 沿导线传递、有电流产生
阴离子移向
正极材料(导电)
电解质溶液
含有正极反应物H+
电子导体
负极材料(导电)
负极反应物
稀盐酸
活动性比锌弱的金属或石墨
替换
替换
总结
负极材料选择
正极材料选择
离子导体选择
不与正极反应物和离子导体发生反应且能导电的固体
金属(活动性比负极弱)或石墨
一般是能电离出正极反应物离子的电解质溶液
(燃料电池正极反应物为O2,电解质不做反应物)
负极反应物为金属时,用负极反应物做负极材料(活动性比正极强)
负极反应物不导电时,负极材料用惰性导电材料(如石墨)
原电池正负极材料和离子导体的选择
化学电池的分类
干电池
(一次电池)
充电电池
(二次电池)
燃料电池
例2 利用生活或实验室中的常用物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池。填写下列空白:
(1)实验原理:Fe+2H+===Fe2++H2↑。
(2)实验用品:电极( 、 )、稀硫酸、 、 (填写所缺的实验用品)、耳机(或者电流表)。
(3)实验装置(如图)
铁钉(或铁条)
铜钉(或铅笔芯、碳棒)
烧杯
导线
(4)原理分析
①按如图所示连接好实验仪器,注意观察(耳朵听)耳机
是否有声音发出,如果没有,可将原电池的两个电极中
的一极接触耳机插头上的一极(注意:接触的同时耳机的另一极是连接在原电池的另一个电极上的),这时可以听见耳机发出“嚓嚓嚓”的声音。其原因是在原电池中,由化学能转化为 。
②如果将装置中的耳机改为电流表,则铁钉应该接电流表的 极,电极反应: ;另一极应该接电流表的 极,电极发生了 反应。
电能
负
Fe-2e-===Fe2+
正
还原
课堂小结
化学电池
原电池
工作原理
构成
设计
电极
离子导体(电解质溶液)
电子导体(导线)
自发氧化还原反应
找电极材料、找电解质溶液、形成闭合回路
第2节 化学反应与能量转化
第2课时 化学反应能量转化的重要
应用——化学电池
第2章
化学键 化学反应规律
【自主学习】
1.氧化还原反应中概念间的关系
2.人们常常利用化学反应将化学能转化为 、 等其他形式的能量,用于生产、生活和科研
3.化学电池:根据 原理制成的电池
4.原电池:利用 反应将 能直接转化成 能的装置
热能
电能
原电池
氧化还原
化学
电
形
形
色
色
的
电
池
二、化学反应能量转化的重要应用——化学电池
观察·思考
1.初识氢氧燃料电池
思考问题:
1. 简易氢氧燃料电池是如何将化学能转化成电能的?
2. 组装电池需要满足哪些基本条件?
负极
正极
还原剂失电子
氧化剂得电子
电子流出
电子流入
离子
导体
e-
导体
导线
电解质溶液
发生氧化反应
发生还原反应
+
-
e-
负极反应物
失电子氧化反应
正极反应物
得电子还原反应
电解质溶液
传导电子
(1)原电池基本工作原理
闭合回路
原电池
的构成
2.两个电极
3.电子导体
1.电极反应物
——导线
——传导电荷的电解质
——导电的固体
——在两极上自发进行氧化还原反应
闭合
回路
4.离子导体
(2)原电池构成要素
例1 下列图示能形成原电池的有哪些?
稀硫酸
稀硫酸
稀硫酸
稀硫酸
稀硫酸
酒精
CuSO4溶液
√
√
√
√
×
×
×
认识锌锰干电池——
锌锰干电池分为酸性锌锰干电池和碱性锌锰干电池两种。酸性锌锰干电池的组成如右图所示。
在酸性锌锰干电池中,负极反应物和正极反应物分别是什么?正负极材料分别是什么?离子导体是什么?
负极反应物和负极材料
正极反应物
离子导体
正极材料
身边的化学
【交流·研讨】
2.设计简单原电池
活动·探究(课本P51页)
利用所给用品设计装置并进行实验,将下列反应所释放的能量转化为电能。
实验原理:Zn + 2H+ = Zn2+ + H2↑
实验用品: 锌片,铜片,石墨棒,稀硫酸,稀盐酸;
烧杯,导线,电流表,开关。
(或石墨)
设计思路及依据 实验装置 实验现象与电极反应
Zn+2H+====Zn2++H2↑ 负极:_____________;电极反应为
___________________
正极:铜片或石墨棒表面___________;电极反应为_________________
确定 负极 选择负极反应物:
选择负极材料:
确定 正极 选择正极反应物:
选择正极材料:
构成闭 合回路 选择离子导体:
选择电子导体:
锌片
锌片
氢离子
铜片(或石墨)
稀硫酸
导线
2H++2e-=H2↑
有气泡产生
思考
1. 分析下图所示原电池的工作原理。
2. 锌片、铜片与稀硫酸,哪些可以替换为其他物质却同样能产生电流?
铜锌原电池工作原理
正极
负极
氧化反应
电极反应式:
Zn-2e-=Zn2+
还原反应
电极反应式:
2H++2e-=H2↑
电解质溶液
不
断
溶
解
阳
离
子
移
向
e- 沿导线传递、有电流产生
阴离子移向
正极材料(导电)
电解质溶液
含有正极反应物H+
电子导体
负极材料(导电)
负极反应物
稀盐酸
活动性比锌弱的金属或石墨
替换
替换
总结
负极材料选择
正极材料选择
离子导体选择
不与正极反应物和离子导体发生反应且能导电的固体
金属(活动性比负极弱)或石墨
一般是能电离出正极反应物离子的电解质溶液
(燃料电池正极反应物为O2,电解质不做反应物)
负极反应物为金属时,用负极反应物做负极材料(活动性比正极强)
负极反应物不导电时,负极材料用惰性导电材料(如石墨)
原电池正负极材料和离子导体的选择
化学电池的分类
干电池
(一次电池)
充电电池
(二次电池)
燃料电池
例2 利用生活或实验室中的常用物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池。填写下列空白:
(1)实验原理:Fe+2H+===Fe2++H2↑。
(2)实验用品:电极( 、 )、稀硫酸、 、 (填写所缺的实验用品)、耳机(或者电流表)。
(3)实验装置(如图)
铁钉(或铁条)
铜钉(或铅笔芯、碳棒)
烧杯
导线
(4)原理分析
①按如图所示连接好实验仪器,注意观察(耳朵听)耳机
是否有声音发出,如果没有,可将原电池的两个电极中
的一极接触耳机插头上的一极(注意:接触的同时耳机的另一极是连接在原电池的另一个电极上的),这时可以听见耳机发出“嚓嚓嚓”的声音。其原因是在原电池中,由化学能转化为 。
②如果将装置中的耳机改为电流表,则铁钉应该接电流表的 极,电极反应: ;另一极应该接电流表的 极,电极发生了 反应。
电能
负
Fe-2e-===Fe2+
正
还原
课堂小结
化学电池
原电池
工作原理
构成
设计
电极
离子导体(电解质溶液)
电子导体(导线)
自发氧化还原反应
找电极材料、找电解质溶液、形成闭合回路
