鲁教版化学九上同步课件:3.1 溶液的形成第2课时 饱和溶液与不饱和溶液(共20张PPT)
文档属性
| 名称 | 鲁教版化学九上同步课件:3.1 溶液的形成第2课时 饱和溶液与不饱和溶液(共20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-19 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
鲁教版化学九年级(上)
1.溶液的形成
第三单元 溶液
第2课时 饱和溶液与不饱和溶液
教学目标
重点难点
1.理解并掌握饱和溶液与不饱和溶液的概念。(重点)
2.学会判断溶液是否达到饱和;知道饱和溶液与不饱和溶液互相转化的方法。(难点)
忆一忆
教学过程
温故知新
2.溶液具有什么特征?
1.什么叫溶液?
议一议
教学过程
新课引入
观察下面两杯食盐水溶液,一杯里面看不到食盐,另一杯里还有食盐没有溶解。这两杯食盐溶液由什么不同?
看一看
教学过程
新知新授
饱和溶液与不饱和溶液
活动天地3——3
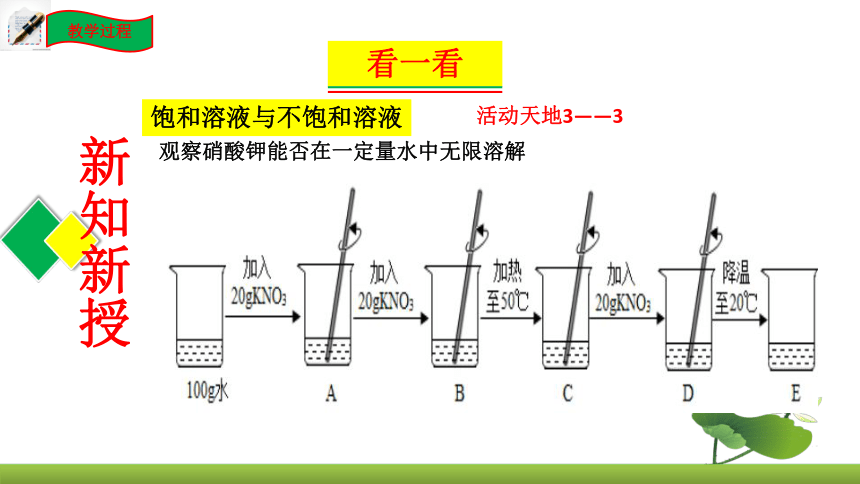
观察硝酸钾能否在一定量水中无限溶解
做一做
教学过程
新知新授
饱和溶液与不饱和溶液
活动天地3——3
观察硝酸钾能否在一定量水中无限溶解
实验操作:(1)在盛有20mL水的烧杯中,加入5g硝酸钾,充分搅拌
实验操作:(2)在上述得到的溶液中,再加入5g硝酸钾,充分搅拌
实验现象:硝酸钾全部溶解
实验现象:硝酸钾部分溶解
实验结论:硝酸钾在一定量的水中不能无限地溶解
记一记
教学过程
新知新授
饱和溶液与不饱和溶液
活动天地3——3
饱和溶液与不饱和溶液的概念
在一定温度下,在一定量的溶剂里,某种溶质不能继续溶解时,所得到的溶液,称为这种溶质的饱和溶液。
在一定温度下,在一定量的溶剂里,某种溶质还能继续溶解该种溶质时,所得到的溶液,称为这种溶质的不饱和溶液。
注意:
(1)必须要指明一定温度、一定量的溶剂。因为改变温度或容剂的量,饱和溶液与不饱和溶液可以相互转化。
(2)必须指明是何种溶质的饱和溶液或不饱和溶液,也可能是对应溶质的饱和溶液。因为对于某温度下的某物质的饱和溶友,仅是指不能再继续溶解此种物质,但还能溶解其他物质。如消酸钾的饱和溶液不能继续溶解硝酸钾,但能溶解氯化钠。
记一记
教学过程
新知新授
饱和溶液与不饱和溶液
活动天地3——3
饱和溶液与不饱和溶液的判断
(1)在一定温度下,若有不能继续溶解的溶质存在,则是对应溶质的饱和溶液。
(2)在一定温度下,若没有相应的未溶解溶质,则可能是对应溶质的不饱和溶液,也可能是对应溶质的饱和溶液。此时可向溶液中加入少量相应溶质固体,若溶解表明溶液不饱和,若不溶解表明溶液饱和。
(3)在一定温度下,析出溶质(常是晶体)后的剩余溶液,一定是相应溶质的饱和溶液。
做一做
教学过程
新知新授
饱和溶液与不饱和溶液
实验探究3——2
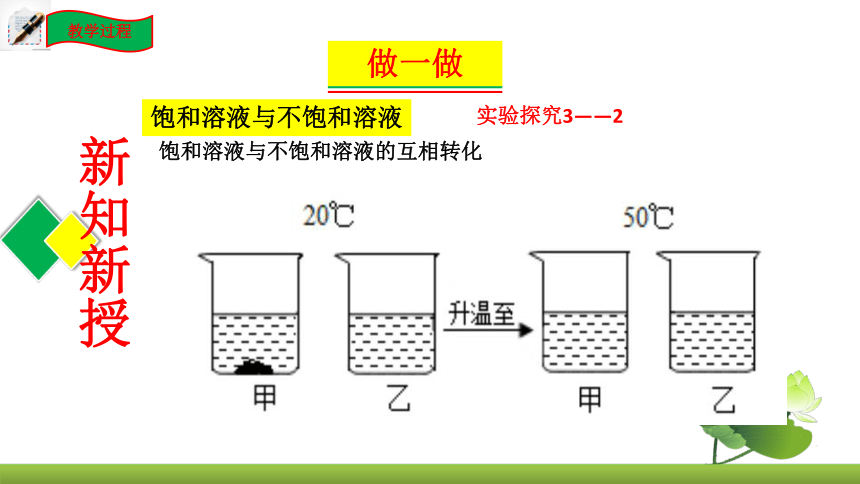
饱和溶液与不饱和溶液的互相转化
做一做
教学过程
新知新授
饱和溶液与不饱和溶液
实验探究3——2
实验操作
1.在盛有10mL水的小烧杯中,加入5g硝酸硝酸钾,充分搅拌。
实验现象
硝酸钾不能全部溶解,烧杯底部还有剩余的固体。
实验操作
2.将上述得到的液体静置后,取少量上层清液于试管中,加入少量硝酸钾固体,充分振荡,观察现象。然后将该试管加热,观察现象。待试管冷却后观察,又有什么现象?
实验用品
大烧杯、小烧杯、试管、酒精灯、石棉网、铁架台、玻璃棒;硝酸钾、蒸馏水。
饱和溶液与不饱和溶液的互相转化
记一记
教学过程
新知新授
饱和溶液与不饱和溶液
实验探究3——2
实验操作
实验现象
实验结论
3.在步骤1的小烧杯中再加入10 mL水并充分搅拌。
烧杯底部的硝酸钾固体继续溶解,直至全部溶解
升高温度、增加溶剂可使硝酸钾的饱和溶液变成不饱和溶液;降低温度可使硝酸钾的不饱和溶液变成饱和溶液转化不饱和溶液。
实验现象
当加入少量硝酸钾固体时,这些固体不能再溶解;将该试管加热,硝酸钾固体会继续溶解,持续加热,硝酸钾固体会全部溶解;待试管冷却,试管底部又会出现硝酸钾固体
饱和溶液与不饱和溶液的互相转化
记一记
教学过程
新知新授
饱和溶液与不饱和溶液
实验探究3——2
饱和溶液与不饱和溶液的互相转化
饱和溶液 不饱和溶液
增加溶剂、减少溶质、改变温度
增加溶质、减少溶剂、改变温度
饱和溶液、不饱和溶液与浓溶液、稀溶液的关系
溶液是否饱和,取决于溶质在一定条件下能否继续溶解
溶液的浓与稀,取决于在一定量的溶液里含溶质的多少
溶液是否饱和与溶液的浓或稀没有必然的关系
饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液。反之亦然
在一定温度下,同种溶质、同种溶剂的饱和溶液一定比不
饱和溶液浓。
记一记
教学过程
新知新授
饱和溶液与不饱和溶液
实验探究3——2
常见物质的溶解与温度的关系
①大多数固体物质在一定量水中溶解的最大量随温度的升高而增大,如硝酸钾(KNO3)、硝酸铵(NH4NO3)等。若将它们的饱和溶液转化为不饱和溶液,可升高温度;若将它们的不饱和溶液转化为饱和溶液,可降低温度。
②熟石灰[Ca(OH)2]在一定量水中溶解的最大量随温度的升高而降低。因此,升高温度可以将熟石灰的不饱和溶液转化为饱和溶液,降低温度可以将熟石灰的饱和溶液转化为不饱和溶液。
③对于任何固体溶质来讲,将其不饱和溶液转化为饱和溶液,最可靠的方法是增加溶质;将其饱和溶液转化为不饱和溶液来讲,最可靠的方法是增加溶剂。
典例解析
教学过程
学以致用
【典例1】
20℃时,100g水中最多溶解氯化钾 34 g。下列是四位同学在20℃时配制的氯化钾溶液,其中一定达到饱和的是( )
A
B
C
D
C
典例解析
教学过程
学以致用
【典例2】保证其他条件不变,欲使接近饱和的澄清石灰水变为饱和溶液,下列方法不可行的是( )
A.蒸发溶剂 B.升高温度
C.降低温度 D.加入氢氧化钙固体
B
【典例3】25 ℃时向一定量不饱和硝酸钾溶液中逐渐加入硝酸钾固体,则下列图象中能正确表示此过程溶液中溶质质量变化规律的是( )
C
典例解析
教学过程
学以致用
【典例4】在一定温度下,对一定量的氯化钠饱和溶液作适当处理,试分析溶质或溶液质量的变化。用“不变”“增加”“减少”填空。
(1)若向其中加入少量氯化钠固体,则溶液的质量 。
(2)若向其中加入少量水,则溶质的质量质量 ,溶液的质量 。
(3)若温度不变蒸发掉少量水,则溶质的质量 液的质量 。
不变
不变
增加
减少
减少
记一记
教学过程
课堂小结
1.什么是饱和溶液?什么是不饱和溶液?
2.饱和溶液和不饱和溶液这样转化?
记一记
教学过程
长话短说
1.溶解就是在溶剂分子的作用下,溶质分子或离子均匀分散到溶剂中的过程。物质的溶解通常伴随着能量的变化。
2.乳化是使不易溶于水的液体以细小液滴的形态分散到水中,形成不易分层、比较稳定的混合物的过程。溶解和乳化都能使物质混合得更为均匀。
3.溶液是溶质的粒子分散在溶剂中形成的均一、稳定的混合物。均一、稳定是溶液的重要特征。
4.水是最重要的溶剂,酒精、汽油等也是常见的溶剂。溶液对于生命活动、工农业生产、科学研究和我们的日常生活都具有重要意义。
5.溶液的饱和与不饱和是有条件的,改变条件可以使饱和溶液与不饱和溶液相互转化。
分层作业
教学过程
课后巩固
完成相关作业
教学过程
结束新课
感谢聆听
鲁教版化学九年级(上)
1.溶液的形成
第三单元 溶液
第2课时 饱和溶液与不饱和溶液
教学目标
重点难点
1.理解并掌握饱和溶液与不饱和溶液的概念。(重点)
2.学会判断溶液是否达到饱和;知道饱和溶液与不饱和溶液互相转化的方法。(难点)
忆一忆
教学过程
温故知新
2.溶液具有什么特征?
1.什么叫溶液?
议一议
教学过程
新课引入
观察下面两杯食盐水溶液,一杯里面看不到食盐,另一杯里还有食盐没有溶解。这两杯食盐溶液由什么不同?
看一看
教学过程
新知新授
饱和溶液与不饱和溶液
活动天地3——3
观察硝酸钾能否在一定量水中无限溶解
做一做
教学过程
新知新授
饱和溶液与不饱和溶液
活动天地3——3
观察硝酸钾能否在一定量水中无限溶解
实验操作:(1)在盛有20mL水的烧杯中,加入5g硝酸钾,充分搅拌
实验操作:(2)在上述得到的溶液中,再加入5g硝酸钾,充分搅拌
实验现象:硝酸钾全部溶解
实验现象:硝酸钾部分溶解
实验结论:硝酸钾在一定量的水中不能无限地溶解
记一记
教学过程
新知新授
饱和溶液与不饱和溶液
活动天地3——3
饱和溶液与不饱和溶液的概念
在一定温度下,在一定量的溶剂里,某种溶质不能继续溶解时,所得到的溶液,称为这种溶质的饱和溶液。
在一定温度下,在一定量的溶剂里,某种溶质还能继续溶解该种溶质时,所得到的溶液,称为这种溶质的不饱和溶液。
注意:
(1)必须要指明一定温度、一定量的溶剂。因为改变温度或容剂的量,饱和溶液与不饱和溶液可以相互转化。
(2)必须指明是何种溶质的饱和溶液或不饱和溶液,也可能是对应溶质的饱和溶液。因为对于某温度下的某物质的饱和溶友,仅是指不能再继续溶解此种物质,但还能溶解其他物质。如消酸钾的饱和溶液不能继续溶解硝酸钾,但能溶解氯化钠。
记一记
教学过程
新知新授
饱和溶液与不饱和溶液
活动天地3——3
饱和溶液与不饱和溶液的判断
(1)在一定温度下,若有不能继续溶解的溶质存在,则是对应溶质的饱和溶液。
(2)在一定温度下,若没有相应的未溶解溶质,则可能是对应溶质的不饱和溶液,也可能是对应溶质的饱和溶液。此时可向溶液中加入少量相应溶质固体,若溶解表明溶液不饱和,若不溶解表明溶液饱和。
(3)在一定温度下,析出溶质(常是晶体)后的剩余溶液,一定是相应溶质的饱和溶液。
做一做
教学过程
新知新授
饱和溶液与不饱和溶液
实验探究3——2
饱和溶液与不饱和溶液的互相转化
做一做
教学过程
新知新授
饱和溶液与不饱和溶液
实验探究3——2
实验操作
1.在盛有10mL水的小烧杯中,加入5g硝酸硝酸钾,充分搅拌。
实验现象
硝酸钾不能全部溶解,烧杯底部还有剩余的固体。
实验操作
2.将上述得到的液体静置后,取少量上层清液于试管中,加入少量硝酸钾固体,充分振荡,观察现象。然后将该试管加热,观察现象。待试管冷却后观察,又有什么现象?
实验用品
大烧杯、小烧杯、试管、酒精灯、石棉网、铁架台、玻璃棒;硝酸钾、蒸馏水。
饱和溶液与不饱和溶液的互相转化
记一记
教学过程
新知新授
饱和溶液与不饱和溶液
实验探究3——2
实验操作
实验现象
实验结论
3.在步骤1的小烧杯中再加入10 mL水并充分搅拌。
烧杯底部的硝酸钾固体继续溶解,直至全部溶解
升高温度、增加溶剂可使硝酸钾的饱和溶液变成不饱和溶液;降低温度可使硝酸钾的不饱和溶液变成饱和溶液转化不饱和溶液。
实验现象
当加入少量硝酸钾固体时,这些固体不能再溶解;将该试管加热,硝酸钾固体会继续溶解,持续加热,硝酸钾固体会全部溶解;待试管冷却,试管底部又会出现硝酸钾固体
饱和溶液与不饱和溶液的互相转化
记一记
教学过程
新知新授
饱和溶液与不饱和溶液
实验探究3——2
饱和溶液与不饱和溶液的互相转化
饱和溶液 不饱和溶液
增加溶剂、减少溶质、改变温度
增加溶质、减少溶剂、改变温度
饱和溶液、不饱和溶液与浓溶液、稀溶液的关系
溶液是否饱和,取决于溶质在一定条件下能否继续溶解
溶液的浓与稀,取决于在一定量的溶液里含溶质的多少
溶液是否饱和与溶液的浓或稀没有必然的关系
饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液。反之亦然
在一定温度下,同种溶质、同种溶剂的饱和溶液一定比不
饱和溶液浓。
记一记
教学过程
新知新授
饱和溶液与不饱和溶液
实验探究3——2
常见物质的溶解与温度的关系
①大多数固体物质在一定量水中溶解的最大量随温度的升高而增大,如硝酸钾(KNO3)、硝酸铵(NH4NO3)等。若将它们的饱和溶液转化为不饱和溶液,可升高温度;若将它们的不饱和溶液转化为饱和溶液,可降低温度。
②熟石灰[Ca(OH)2]在一定量水中溶解的最大量随温度的升高而降低。因此,升高温度可以将熟石灰的不饱和溶液转化为饱和溶液,降低温度可以将熟石灰的饱和溶液转化为不饱和溶液。
③对于任何固体溶质来讲,将其不饱和溶液转化为饱和溶液,最可靠的方法是增加溶质;将其饱和溶液转化为不饱和溶液来讲,最可靠的方法是增加溶剂。
典例解析
教学过程
学以致用
【典例1】
20℃时,100g水中最多溶解氯化钾 34 g。下列是四位同学在20℃时配制的氯化钾溶液,其中一定达到饱和的是( )
A
B
C
D
C
典例解析
教学过程
学以致用
【典例2】保证其他条件不变,欲使接近饱和的澄清石灰水变为饱和溶液,下列方法不可行的是( )
A.蒸发溶剂 B.升高温度
C.降低温度 D.加入氢氧化钙固体
B
【典例3】25 ℃时向一定量不饱和硝酸钾溶液中逐渐加入硝酸钾固体,则下列图象中能正确表示此过程溶液中溶质质量变化规律的是( )
C
典例解析
教学过程
学以致用
【典例4】在一定温度下,对一定量的氯化钠饱和溶液作适当处理,试分析溶质或溶液质量的变化。用“不变”“增加”“减少”填空。
(1)若向其中加入少量氯化钠固体,则溶液的质量 。
(2)若向其中加入少量水,则溶质的质量质量 ,溶液的质量 。
(3)若温度不变蒸发掉少量水,则溶质的质量 液的质量 。
不变
不变
增加
减少
减少
记一记
教学过程
课堂小结
1.什么是饱和溶液?什么是不饱和溶液?
2.饱和溶液和不饱和溶液这样转化?
记一记
教学过程
长话短说
1.溶解就是在溶剂分子的作用下,溶质分子或离子均匀分散到溶剂中的过程。物质的溶解通常伴随着能量的变化。
2.乳化是使不易溶于水的液体以细小液滴的形态分散到水中,形成不易分层、比较稳定的混合物的过程。溶解和乳化都能使物质混合得更为均匀。
3.溶液是溶质的粒子分散在溶剂中形成的均一、稳定的混合物。均一、稳定是溶液的重要特征。
4.水是最重要的溶剂,酒精、汽油等也是常见的溶剂。溶液对于生命活动、工农业生产、科学研究和我们的日常生活都具有重要意义。
5.溶液的饱和与不饱和是有条件的,改变条件可以使饱和溶液与不饱和溶液相互转化。
分层作业
教学过程
课后巩固
完成相关作业
教学过程
结束新课
感谢聆听
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
