化学(人教版)九上提升练:6.3 二氧化碳和一氧化碳(含解析)
文档属性
| 名称 | 化学(人教版)九上提升练:6.3 二氧化碳和一氧化碳(含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-19 00:00:00 | ||
图片预览





文档简介
第六单元 碳和碳的氧化物
课题3 二氧化碳和一氧化碳
夯基知识梳理
知识点1 二氧化碳的性质和用途
1.关于二氧化碳的用途,下列说法错误的是 ( )
A.灭火 B.生产汽水 C.气体肥料 D.供给呼吸
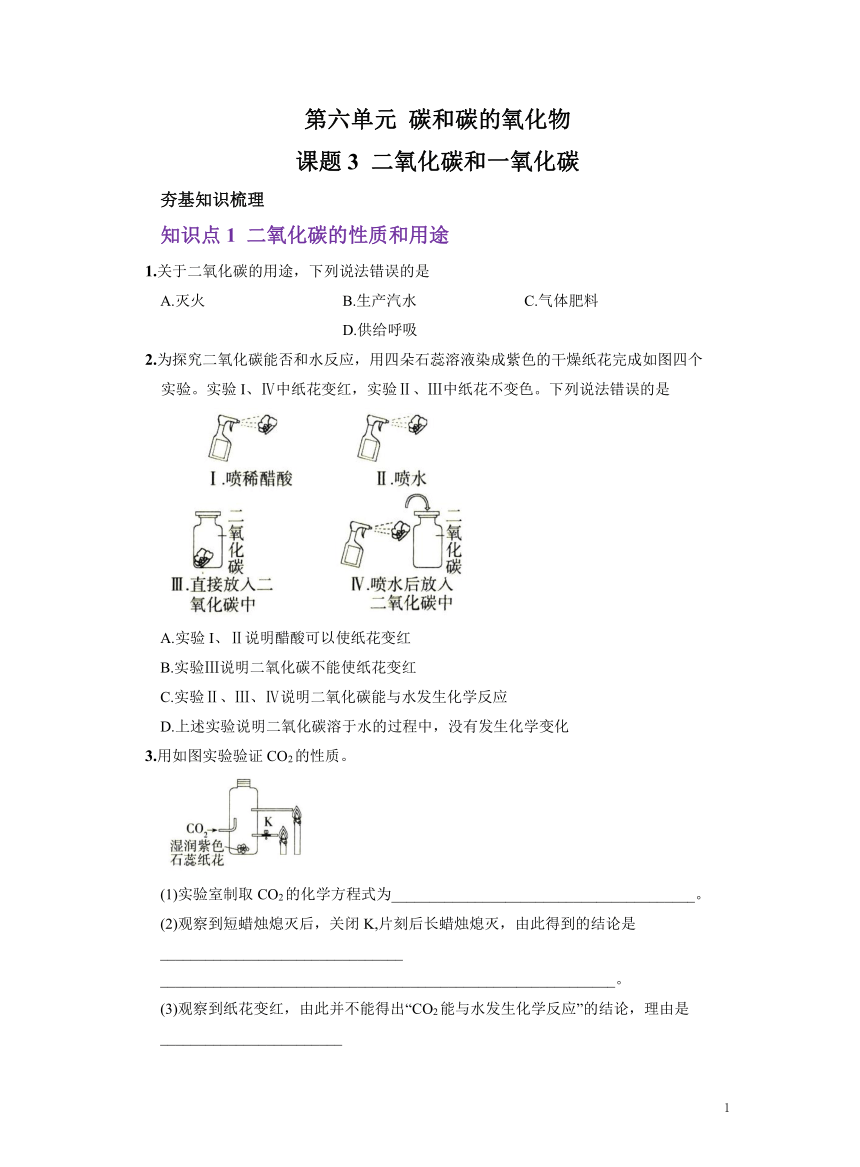
2.为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥纸花完成如图四个实验。实验I、Ⅳ中纸花变红,实验Ⅱ、Ⅲ中纸花不变色。下列说法错误的是 ( )
A.实验I、Ⅱ说明醋酸可以使纸花变红
B.实验Ⅲ说明二氧化碳不能使纸花变红
C.实验Ⅱ、Ⅲ、Ⅳ说明二氧化碳能与水发生化学反应
D.上述实验说明二氧化碳溶于水的过程中,没有发生化学变化
3.用如图实验验证CO2的性质。
(1)实验室制取CO2的化学方程式为________________________________________。
(2)观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,由此得到的结论是________________________________
____________________________________________________________。
(3)观察到纸花变红,由此并不能得出“CO2能与水发生化学反应”的结论,理由是________________________
____________________________________________________________。
4.用如图装置验证二氧化碳的性质。
(1)通入二氧化碳后,观察到澄清石灰水变浑浊,反应的化学方程式为____________________.
(2)实验中,得出“二氧化碳能与水发生化学反应”的结论,依据的现象为____________________________。
(3)实验后,取出湿润的石蕊纸条,一段时间后纸条变为紫色,其原因为________________________________
(用化学方程式解释)。
知识点2 二氧化碳对人体和环境的影响
5. 2022年1月29日,我国首个百万吨级碳捕集、利用与封存项目全面建成,每年可减排二氧化碳100万吨,实现了生产过程低碳化。生活中下列做法,不符合“低碳”要求的是 ( )
A.垃圾分类处理,加强资源回收利用 B.打印资料时纸张双面使用
C.生活中提倡使用节能产品 D.为了方便快速,多采用自驾车出行
6.温室效应加剧引起的气候异常变化是人类面临的全球性问题。我国由此提出“碳达峰”和“碳中和”目标,并将其写入政府工作报告,体现了中国的大国责任与担当。
(1)“碳达峰”与“碳中和”中的“碳”指的物质是____________________。
(2)植树造林是完成“碳中和”目标的重要途径,其原理是利用绿色植物的________作用,以减少大气中的温室气体。
(3)生活中,良好的行为习惯也有助于完成目标。下列做法不合理的是________(填字母)。
A.不用电器时及时关闭电源 B.外出时多步行或骑自行车
C.产生纸质垃圾时焚烧处理
知识点3 一氧化碳的性质和用途
7.科学研究发现,金星大气层的成分之一是三氧化二碳(C2O3),实验证明三氧化二碳的化学性质与一氧化碳相似,下列关于三氧化二碳的说法中不正确的是 ( )
A.C2O3中碳的化合价为+3价 B.C2O3具有可燃性,可以用作燃料
C.C2O3在一定条件下能还原氧化铜 D.C2O3能使澄清石灰水变浑浊
8.如图是CO与CuO反应的实验装置,下列关于该实验的说法正确的是 ( )
①玻璃管中黑色固体变成了红色 ②CO被还原为CO2
③玻璃管中发生的反应为化合反应 ④既有效地防止了CO对空气的污染,又充分利用了能源
A.①② B.①④ C.②④ D.③④
9.一氧化碳在工业上有重要作用。
(1)作燃料:一氧化碳在空气中燃烧的化学方程式________________________________________;
(2)作还原剂:一氧化碳还原氧化铜的化学方程式________________________________________。
提优强化练习
10.下列实验现象既能体现二氧化碳的物理性质,又能体现其化学性质的是 ( )
A.蜡烛自下而上熄灭 B.软塑料瓶变瘪 C.石蕊溶液变红 D.气球上浮
11.今年的政府工作报告,把“碳达峰”“碳中和”工作列为重点任务之一,提出“二氧化碳排放力争于2O30年前达到峰值,努力争取2060年前实现碳中和”。如图形象解读了“碳达峰”和“碳中和”。下列措施不符合上述发展理念的是 ( )
A.优先选乘公共交通 B.随手关闭电源 C.尽量用一次性餐具 D.使用节能灯泡
12.下列关于二氧化碳和一氧化碳的描述,完全正确的是 ( )
A.组成:CO2、CO均由碳元素和氧元素组成 B.性质:CO2、CO密度均大于空气
C.用途:CO2可用于人工降雨;CO可用作气体肥料 D.危害:CO2会引起中毒;CO会引起雾霾
13.某实验小组计划利用甲酸(HCOOH)与浓硫酸制备CO,并利用氧化铜(CuO)能够被还原成单质铜的性质,验证CO的还原性。装置如图所示。已知:HCOOHH2O+CO↑,下列说法错误的是 ( )
A.操作时,先点燃酒精灯,再滴加HCOOH B.甲处的现象是固体由黑色变为红色
C.澄清石灰水变浑浊是因为甲处生成了二氧化碳 D.气球的作用:收集尾气,防止CO污染空气
14.有甲、乙、丙三种纯净物,甲为黑色固体,乙、丙为无色气体。点燃时,甲既能生成乙,也能生成丙;丙点燃也能生成乙。以下关于这三种物质推断的叙述中,正确的是 ( )
A.甲是一种化合物 B.乙是一氧化碳 C.丙是一氧化碳 D.丙是二氧化碳
15.按如图所示装置探究二氧化碳的性质并填空:
(1)A中的实验现象说明CO2具有的化学性质是____________________。
(2)B中的现象是____________________,写出反应的化学方程式:________________________________________。
(3)C装置中干石蕊纸花不变色,湿石蕊纸花由紫色变红色的原因是____________________
素养能力培优
16.[科学探究与创新意识]同学们对“二氧化碳溶于水是否与水反应”进行实验探究,请参与探究并回答下列问题。
【探究思路】(1)判断物质间是否发生化学反应的根本依据是________________________________________,观察到的可以作为判断依据的宏观实验现象有________________________________________。
(2)CO2溶于水无明显现象,________(填“能”或“不能”)用观察的方法判断是否发生反应。
(3)利用“实验”的方法探究物质间是否反应的设计依据是:生成物和反应物的性质差异。
【提出猜想】猜想一:二氧化碳溶于水不与水反应;猜想二:________________________。
【实验设计】用四朵石蕊溶液染成紫色的干燥纸花设计如下实验:
序号 实验设计
① 向第一朵纸花喷稀醋酸
② ____________________
③ 将第三朵纸花直接放入盛有二氧化碳的集气瓶中
④ 将第四朵纸花喷水后放入盛有二氧化碳的集气瓶中
(1)“实验设计①”中的稀醋酸还可用____________________(填物质名称)代替;
(2)“实验设计②”的具体内容是________________________________________。
(3)“实验设计③”的目的是________________________________________。
【进行实验】进行实验探究,观察记录实验现象。
【实验结论】猜想二成立,支持猜想二成立的实验现象是________________________________________。
【反思交流】实验探究“无明显实验现象时是否发生化学反应”的核心思路有________(填字母序号)。
A.设计对比实验 B.控制实验条件 C.获取事实证据 D.逻辑推理判断
17.[科学态度与社会责任]我国“十四五”规划已经明确“2O30年前实现碳达峰”的目标。碳达峰是指二氧化碳的排放达到峰值,不再增长。如图为自然界中CO2的循环图,图中箭头指向表示产生(排放)或消耗CO2的途径。回答下列问题:
(1)途径①需要消耗空气中的________。
(2)途径②中,枯枝败叶中的纤维素[化学式为(C6H10O5)n]在微生物作用下彻底转化为CO2和H2O,该转化中消耗O2与产生的CO2分子个数比为________。
(3)途径④通过光合作用吸收CO2的量白天________夜晚(填“大于”或“小于”)。
(4)降碳的一种途径是在合适的催化剂条件下,将二氧化碳与氢气反应使碳全部转化为乙烯(C2H4),同时生成另一种化合物。请写出反应的化学方程式:________________________________________。
(5)某年通过不同途径产生或消耗碳量的相对值如下表所示:
途径 ① ② ③ ④ ⑤ ⑥ ⑦
相对值 0.6 60 60 121.8 5.5 92 90
据表可知,这一年大气中碳量增加了____(用表中相对值计算)。为达成“2O30年前实现碳达峰”的目标,下列措施不可行的是________。
A.开发新能源 B.植树造林 C.禁止使用化石燃料
进一步分析上表回答:人口增多是否是大气中碳量增加的主要因素,并说明理由_________________________
________________________________________。
【参考答案及解析】
夯基知识梳理
1.D 氧气能供给呼吸,二氧化碳不能供给呼吸。
2.D Ⅱ中纸花不变色,说明水不能使石蕊变色;Ⅲ中纸花不变色,说明二氧化碳不能使石蕊变红;而Ⅳ中纸花变红,说明二氧化碳溶于水的过程中与水发生了化学反应,生成的物质能使石蕊变红。
3.【答案】
(1)CaCO3+2HCl=CaCl2+CO2↑+H2O
(2)二氧化碳密度比空气大,不燃烧也不支持燃烧
(3)没有验证二氧化碳不能使干燥的紫色石蕊变红
【解析】
(1)实验室制取二氧化碳的反应原理是碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳。
(2)蜡烛由下至上依次熄灭,说明二氧化碳具有不能燃烧、不支持燃烧,且密度比空气大的性质。
4.【答案】
(1)CO2+Ca(0H)2=CaCO3↓+H2O
(2)干燥的石蕊纸条不变色,湿润的石蕊纸条由紫色变为红色
(3)H2CO3=H2O+CO2↑
【解析】
(1)二氧化碳与澄清的石灰水反应生成碳酸钙沉淀和水。
(2)二氧化碳与水反应生成的碳酸能使紫色石蕊纸条变为红色。
(3)碳酸不稳定,易分解生成二氧化碳和水,所以取出湿润的石蕊纸条,一段时间后纸条变为紫色。
5.D 多采用自驾车出行,增加了燃油、燃气的使用,从而增加了二氧化碳的排放,不符合“低碳”要求。
6.【答案】(1)二氧化碳 (2)光合 (3)C
【解析】
(3)焚烧处理纸质垃圾时会产生大量的二氧化碳。
7.D 三氧化二碳的化学性质与一氧化碳相似,一氧化碳不能与澄清石灰水反应,由此判断三氧化二碳不能与澄清石灰水反应。
8.B 一氧化碳具有还原性,能与氧化铜反应生成铜和二氧化碳,会观察到玻璃管中黑色固体变成了红色,①正确;一氧化碳夺取了氧化铜中的氧,CO被氧化为CO2,②错误;两种物质反应生成两种新的物质,不属于化合反应,③错误;一氧化碳燃烧生成二氧化碳,利用一氧化碳燃烧产生的热量给玻璃管加热,既有效地防止了CO对空气的污染,又充分利用了能源,④正确,故选B。
9.【答案】(1)2CO+O22CO2 (2)CuO+COCu+CO2
提优强化练习
10.A 蜡烛自下而上熄灭,体现了二氧化碳不燃烧也不支持燃烧的化学性质,也体现了密度比空气大的物理性质。
11.C 尽量用一次性餐具会浪费资源,增加了二氧化碳的排放,不符合题述发展理念。
12.A CO的密度比空气略小;CO不能作气体肥料;CO2不会引起中毒。
13.A 应先滴加HCOOH,再点燃酒精灯,目的是排尽装置中的空气,防止加热时发生爆炸;一氧化碳与氧化铜反应生成铜和二氧化碳,甲处的现象是固体由黑色变为红色;澄清石灰水变浑浊是因为甲处生成了二氧化碳;一氧化碳有毒,直接排放到空气中会污染环境,气球的作用是收集尾气,防止污染空气。
14.C 甲为黑色固体,常见的黑色固体有碳、氧化铜、四氧化三铁、二氧化锰等,甲可以被点燃,因此甲为碳;乙和丙为无色气体,甲既能生成乙,也能生成丙,丙点燃也能生成乙,因此乙为二氧化碳,丙为一氧化碳。
15.【答案】
(1)不燃烧也不支持燃烧
(2)澄清石灰水变浑浊 CO2+Ca(OH)2=CaCO3↓+H2O
(3)二氧化碳与水反应生成碳酸,碳酸使石蕊纸花变为红色
【解析】
(1)蜡烛熄灭,说明二氧化碳具有不燃烧也不支持燃烧的化学性质。
(2)二氧化碳与澄清石灰水反应生成碳酸钙沉淀与水,看到的现象是澄清石灰水变浑浊。
(3)二氧化碳不能使干燥的石蕊纸花变色,二氧化碳与水反应生成的碳酸能使石蕊纸花变为红色。
素养能力培优
16.【答案】【探究思路】
(1)是否有新物质生成 颜色变化、放出气体、生成沉淀等并伴有吸热、放热、发光等能量变化(前三种体现物质变化的宏观现象答出一种即可,后三种体现能量变化的宏观现象不写也可)
(2)不能
【提出猜想】二氧化碳溶于水与水反应
【实验设计】
(1)稀盐酸(或稀硫酸等)
(2)向第二朵纸花喷水
(3)验证CO2能否使紫色石蕊变色
【实验结论】②③不变红,④变红
【反思交流】ABCD
【解析】【提出猜想】根据猜想一的内容知猜想二为二氧化碳溶于水与水反应。
【实验设计】(1)酸溶液能使石蕊变红,因此“实验设计①”中的稀醋酸还可用稀硫酸等代替。
【实验结论】②③中纸花不变色,说明水、二氧化碳都不能使纸花变色,④中纸花变红色,说明二氧化碳和水反应生成了新物质。
17.【答案】(1)氧气 (2)1∶1 (3)大于 (4)2CO2+6H2C2H4+4H2O
(5)2.3 C 是,人口增多需要消耗更多的化石燃料,呼吸作用会产生二氧化碳
【解析】
(1)途径①是呼吸作用,需要消耗空气中的氧气。
(2)转化的化学方程式为(C6H10O5)n+6nO26nCO2+5nH2O,该转化中消耗O2与产生的CO2分子个数比为6n:6n=1:1。
(3)光合作用需要太阳能,所以途径④通过光合作用吸收CO2的量白天大于夜晚。
(4)根据化学反应前后元素的种类不变可知,生成的另一种化合物是水。
(5)根据排放和吸收二氧化碳的量可知,这一年大气中碳量增加了0.6+60+60+5.5+90-121.8-92=2.3;化石燃料是当前人类获取能量的主要来源,不能禁止使用。
1
课题3 二氧化碳和一氧化碳
夯基知识梳理
知识点1 二氧化碳的性质和用途
1.关于二氧化碳的用途,下列说法错误的是 ( )
A.灭火 B.生产汽水 C.气体肥料 D.供给呼吸
2.为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥纸花完成如图四个实验。实验I、Ⅳ中纸花变红,实验Ⅱ、Ⅲ中纸花不变色。下列说法错误的是 ( )
A.实验I、Ⅱ说明醋酸可以使纸花变红
B.实验Ⅲ说明二氧化碳不能使纸花变红
C.实验Ⅱ、Ⅲ、Ⅳ说明二氧化碳能与水发生化学反应
D.上述实验说明二氧化碳溶于水的过程中,没有发生化学变化
3.用如图实验验证CO2的性质。
(1)实验室制取CO2的化学方程式为________________________________________。
(2)观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,由此得到的结论是________________________________
____________________________________________________________。
(3)观察到纸花变红,由此并不能得出“CO2能与水发生化学反应”的结论,理由是________________________
____________________________________________________________。
4.用如图装置验证二氧化碳的性质。
(1)通入二氧化碳后,观察到澄清石灰水变浑浊,反应的化学方程式为____________________.
(2)实验中,得出“二氧化碳能与水发生化学反应”的结论,依据的现象为____________________________。
(3)实验后,取出湿润的石蕊纸条,一段时间后纸条变为紫色,其原因为________________________________
(用化学方程式解释)。
知识点2 二氧化碳对人体和环境的影响
5. 2022年1月29日,我国首个百万吨级碳捕集、利用与封存项目全面建成,每年可减排二氧化碳100万吨,实现了生产过程低碳化。生活中下列做法,不符合“低碳”要求的是 ( )
A.垃圾分类处理,加强资源回收利用 B.打印资料时纸张双面使用
C.生活中提倡使用节能产品 D.为了方便快速,多采用自驾车出行
6.温室效应加剧引起的气候异常变化是人类面临的全球性问题。我国由此提出“碳达峰”和“碳中和”目标,并将其写入政府工作报告,体现了中国的大国责任与担当。
(1)“碳达峰”与“碳中和”中的“碳”指的物质是____________________。
(2)植树造林是完成“碳中和”目标的重要途径,其原理是利用绿色植物的________作用,以减少大气中的温室气体。
(3)生活中,良好的行为习惯也有助于完成目标。下列做法不合理的是________(填字母)。
A.不用电器时及时关闭电源 B.外出时多步行或骑自行车
C.产生纸质垃圾时焚烧处理
知识点3 一氧化碳的性质和用途
7.科学研究发现,金星大气层的成分之一是三氧化二碳(C2O3),实验证明三氧化二碳的化学性质与一氧化碳相似,下列关于三氧化二碳的说法中不正确的是 ( )
A.C2O3中碳的化合价为+3价 B.C2O3具有可燃性,可以用作燃料
C.C2O3在一定条件下能还原氧化铜 D.C2O3能使澄清石灰水变浑浊
8.如图是CO与CuO反应的实验装置,下列关于该实验的说法正确的是 ( )
①玻璃管中黑色固体变成了红色 ②CO被还原为CO2
③玻璃管中发生的反应为化合反应 ④既有效地防止了CO对空气的污染,又充分利用了能源
A.①② B.①④ C.②④ D.③④
9.一氧化碳在工业上有重要作用。
(1)作燃料:一氧化碳在空气中燃烧的化学方程式________________________________________;
(2)作还原剂:一氧化碳还原氧化铜的化学方程式________________________________________。
提优强化练习
10.下列实验现象既能体现二氧化碳的物理性质,又能体现其化学性质的是 ( )
A.蜡烛自下而上熄灭 B.软塑料瓶变瘪 C.石蕊溶液变红 D.气球上浮
11.今年的政府工作报告,把“碳达峰”“碳中和”工作列为重点任务之一,提出“二氧化碳排放力争于2O30年前达到峰值,努力争取2060年前实现碳中和”。如图形象解读了“碳达峰”和“碳中和”。下列措施不符合上述发展理念的是 ( )
A.优先选乘公共交通 B.随手关闭电源 C.尽量用一次性餐具 D.使用节能灯泡
12.下列关于二氧化碳和一氧化碳的描述,完全正确的是 ( )
A.组成:CO2、CO均由碳元素和氧元素组成 B.性质:CO2、CO密度均大于空气
C.用途:CO2可用于人工降雨;CO可用作气体肥料 D.危害:CO2会引起中毒;CO会引起雾霾
13.某实验小组计划利用甲酸(HCOOH)与浓硫酸制备CO,并利用氧化铜(CuO)能够被还原成单质铜的性质,验证CO的还原性。装置如图所示。已知:HCOOHH2O+CO↑,下列说法错误的是 ( )
A.操作时,先点燃酒精灯,再滴加HCOOH B.甲处的现象是固体由黑色变为红色
C.澄清石灰水变浑浊是因为甲处生成了二氧化碳 D.气球的作用:收集尾气,防止CO污染空气
14.有甲、乙、丙三种纯净物,甲为黑色固体,乙、丙为无色气体。点燃时,甲既能生成乙,也能生成丙;丙点燃也能生成乙。以下关于这三种物质推断的叙述中,正确的是 ( )
A.甲是一种化合物 B.乙是一氧化碳 C.丙是一氧化碳 D.丙是二氧化碳
15.按如图所示装置探究二氧化碳的性质并填空:
(1)A中的实验现象说明CO2具有的化学性质是____________________。
(2)B中的现象是____________________,写出反应的化学方程式:________________________________________。
(3)C装置中干石蕊纸花不变色,湿石蕊纸花由紫色变红色的原因是____________________
素养能力培优
16.[科学探究与创新意识]同学们对“二氧化碳溶于水是否与水反应”进行实验探究,请参与探究并回答下列问题。
【探究思路】(1)判断物质间是否发生化学反应的根本依据是________________________________________,观察到的可以作为判断依据的宏观实验现象有________________________________________。
(2)CO2溶于水无明显现象,________(填“能”或“不能”)用观察的方法判断是否发生反应。
(3)利用“实验”的方法探究物质间是否反应的设计依据是:生成物和反应物的性质差异。
【提出猜想】猜想一:二氧化碳溶于水不与水反应;猜想二:________________________。
【实验设计】用四朵石蕊溶液染成紫色的干燥纸花设计如下实验:
序号 实验设计
① 向第一朵纸花喷稀醋酸
② ____________________
③ 将第三朵纸花直接放入盛有二氧化碳的集气瓶中
④ 将第四朵纸花喷水后放入盛有二氧化碳的集气瓶中
(1)“实验设计①”中的稀醋酸还可用____________________(填物质名称)代替;
(2)“实验设计②”的具体内容是________________________________________。
(3)“实验设计③”的目的是________________________________________。
【进行实验】进行实验探究,观察记录实验现象。
【实验结论】猜想二成立,支持猜想二成立的实验现象是________________________________________。
【反思交流】实验探究“无明显实验现象时是否发生化学反应”的核心思路有________(填字母序号)。
A.设计对比实验 B.控制实验条件 C.获取事实证据 D.逻辑推理判断
17.[科学态度与社会责任]我国“十四五”规划已经明确“2O30年前实现碳达峰”的目标。碳达峰是指二氧化碳的排放达到峰值,不再增长。如图为自然界中CO2的循环图,图中箭头指向表示产生(排放)或消耗CO2的途径。回答下列问题:
(1)途径①需要消耗空气中的________。
(2)途径②中,枯枝败叶中的纤维素[化学式为(C6H10O5)n]在微生物作用下彻底转化为CO2和H2O,该转化中消耗O2与产生的CO2分子个数比为________。
(3)途径④通过光合作用吸收CO2的量白天________夜晚(填“大于”或“小于”)。
(4)降碳的一种途径是在合适的催化剂条件下,将二氧化碳与氢气反应使碳全部转化为乙烯(C2H4),同时生成另一种化合物。请写出反应的化学方程式:________________________________________。
(5)某年通过不同途径产生或消耗碳量的相对值如下表所示:
途径 ① ② ③ ④ ⑤ ⑥ ⑦
相对值 0.6 60 60 121.8 5.5 92 90
据表可知,这一年大气中碳量增加了____(用表中相对值计算)。为达成“2O30年前实现碳达峰”的目标,下列措施不可行的是________。
A.开发新能源 B.植树造林 C.禁止使用化石燃料
进一步分析上表回答:人口增多是否是大气中碳量增加的主要因素,并说明理由_________________________
________________________________________。
【参考答案及解析】
夯基知识梳理
1.D 氧气能供给呼吸,二氧化碳不能供给呼吸。
2.D Ⅱ中纸花不变色,说明水不能使石蕊变色;Ⅲ中纸花不变色,说明二氧化碳不能使石蕊变红;而Ⅳ中纸花变红,说明二氧化碳溶于水的过程中与水发生了化学反应,生成的物质能使石蕊变红。
3.【答案】
(1)CaCO3+2HCl=CaCl2+CO2↑+H2O
(2)二氧化碳密度比空气大,不燃烧也不支持燃烧
(3)没有验证二氧化碳不能使干燥的紫色石蕊变红
【解析】
(1)实验室制取二氧化碳的反应原理是碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳。
(2)蜡烛由下至上依次熄灭,说明二氧化碳具有不能燃烧、不支持燃烧,且密度比空气大的性质。
4.【答案】
(1)CO2+Ca(0H)2=CaCO3↓+H2O
(2)干燥的石蕊纸条不变色,湿润的石蕊纸条由紫色变为红色
(3)H2CO3=H2O+CO2↑
【解析】
(1)二氧化碳与澄清的石灰水反应生成碳酸钙沉淀和水。
(2)二氧化碳与水反应生成的碳酸能使紫色石蕊纸条变为红色。
(3)碳酸不稳定,易分解生成二氧化碳和水,所以取出湿润的石蕊纸条,一段时间后纸条变为紫色。
5.D 多采用自驾车出行,增加了燃油、燃气的使用,从而增加了二氧化碳的排放,不符合“低碳”要求。
6.【答案】(1)二氧化碳 (2)光合 (3)C
【解析】
(3)焚烧处理纸质垃圾时会产生大量的二氧化碳。
7.D 三氧化二碳的化学性质与一氧化碳相似,一氧化碳不能与澄清石灰水反应,由此判断三氧化二碳不能与澄清石灰水反应。
8.B 一氧化碳具有还原性,能与氧化铜反应生成铜和二氧化碳,会观察到玻璃管中黑色固体变成了红色,①正确;一氧化碳夺取了氧化铜中的氧,CO被氧化为CO2,②错误;两种物质反应生成两种新的物质,不属于化合反应,③错误;一氧化碳燃烧生成二氧化碳,利用一氧化碳燃烧产生的热量给玻璃管加热,既有效地防止了CO对空气的污染,又充分利用了能源,④正确,故选B。
9.【答案】(1)2CO+O22CO2 (2)CuO+COCu+CO2
提优强化练习
10.A 蜡烛自下而上熄灭,体现了二氧化碳不燃烧也不支持燃烧的化学性质,也体现了密度比空气大的物理性质。
11.C 尽量用一次性餐具会浪费资源,增加了二氧化碳的排放,不符合题述发展理念。
12.A CO的密度比空气略小;CO不能作气体肥料;CO2不会引起中毒。
13.A 应先滴加HCOOH,再点燃酒精灯,目的是排尽装置中的空气,防止加热时发生爆炸;一氧化碳与氧化铜反应生成铜和二氧化碳,甲处的现象是固体由黑色变为红色;澄清石灰水变浑浊是因为甲处生成了二氧化碳;一氧化碳有毒,直接排放到空气中会污染环境,气球的作用是收集尾气,防止污染空气。
14.C 甲为黑色固体,常见的黑色固体有碳、氧化铜、四氧化三铁、二氧化锰等,甲可以被点燃,因此甲为碳;乙和丙为无色气体,甲既能生成乙,也能生成丙,丙点燃也能生成乙,因此乙为二氧化碳,丙为一氧化碳。
15.【答案】
(1)不燃烧也不支持燃烧
(2)澄清石灰水变浑浊 CO2+Ca(OH)2=CaCO3↓+H2O
(3)二氧化碳与水反应生成碳酸,碳酸使石蕊纸花变为红色
【解析】
(1)蜡烛熄灭,说明二氧化碳具有不燃烧也不支持燃烧的化学性质。
(2)二氧化碳与澄清石灰水反应生成碳酸钙沉淀与水,看到的现象是澄清石灰水变浑浊。
(3)二氧化碳不能使干燥的石蕊纸花变色,二氧化碳与水反应生成的碳酸能使石蕊纸花变为红色。
素养能力培优
16.【答案】【探究思路】
(1)是否有新物质生成 颜色变化、放出气体、生成沉淀等并伴有吸热、放热、发光等能量变化(前三种体现物质变化的宏观现象答出一种即可,后三种体现能量变化的宏观现象不写也可)
(2)不能
【提出猜想】二氧化碳溶于水与水反应
【实验设计】
(1)稀盐酸(或稀硫酸等)
(2)向第二朵纸花喷水
(3)验证CO2能否使紫色石蕊变色
【实验结论】②③不变红,④变红
【反思交流】ABCD
【解析】【提出猜想】根据猜想一的内容知猜想二为二氧化碳溶于水与水反应。
【实验设计】(1)酸溶液能使石蕊变红,因此“实验设计①”中的稀醋酸还可用稀硫酸等代替。
【实验结论】②③中纸花不变色,说明水、二氧化碳都不能使纸花变色,④中纸花变红色,说明二氧化碳和水反应生成了新物质。
17.【答案】(1)氧气 (2)1∶1 (3)大于 (4)2CO2+6H2C2H4+4H2O
(5)2.3 C 是,人口增多需要消耗更多的化石燃料,呼吸作用会产生二氧化碳
【解析】
(1)途径①是呼吸作用,需要消耗空气中的氧气。
(2)转化的化学方程式为(C6H10O5)n+6nO26nCO2+5nH2O,该转化中消耗O2与产生的CO2分子个数比为6n:6n=1:1。
(3)光合作用需要太阳能,所以途径④通过光合作用吸收CO2的量白天大于夜晚。
(4)根据化学反应前后元素的种类不变可知,生成的另一种化合物是水。
(5)根据排放和吸收二氧化碳的量可知,这一年大气中碳量增加了0.6+60+60+5.5+90-121.8-92=2.3;化石燃料是当前人类获取能量的主要来源,不能禁止使用。
1
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
