7.2.乙烯与有机高分子材料(含解析) 能力提升 2023-2024学年高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 7.2.乙烯与有机高分子材料(含解析) 能力提升 2023-2024学年高一下学期化学人教版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 508.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-19 00:00:00 | ||
图片预览



文档简介
7.2.乙烯与有机高分子材料能力提升-2023-2024学年高一下学期化学人教版(2019)必修第二册
一、单选题
1.下列有关化学用语的表述正确的是( )
A.37Cl-的结构示意图: B.中子数为7的碳原子:C
C.NH3的结构式: D.次氯酸的电子式:
2.建国以来我国的化学工业发展迅速,为提高我们的国际地位和改善人民群众的生产生活做出了突出贡献,下列说法正确的是
A.北京冬奥会吉祥物“冰墩墩”的材质中有聚氯乙烯,聚氯乙烯是纯净物
B.中国承建卡塔尔世界杯“大金碗”球场采用聚四氟乙烯材料的单体是不饱和烃
C.空间站天和核心舱的太阳电池翼的氮化硼陶瓷涂层属于新型无机非金属材料
D.北斗卫星导航系统由中国自主研发、独立运行,其所用芯片的主要成分为
3.下列化学用语表达正确的是
A.二氧化碳: B.氮气:
C.氯化镁: D.氯化氢的形成过程:
4.三层复合石头纸是一种新型纸张,其结构如图所示:上下两层为聚乙烯,中间层为碳酸钙。下列关于它的叙述错误的是
A.易生物降解 B.可替代木浆纸以减少树木砍伐
C.与普通纸相比难以燃烧 D.具有防水防油的特性
5.相同物质的量的下列各烃,完全燃烧消耗O2的量最大的是
A.CH4 B.C2H4
C.C3H4 D.C2H6
6.下列化学用语表达正确的是
A.乙烯的结构简式:
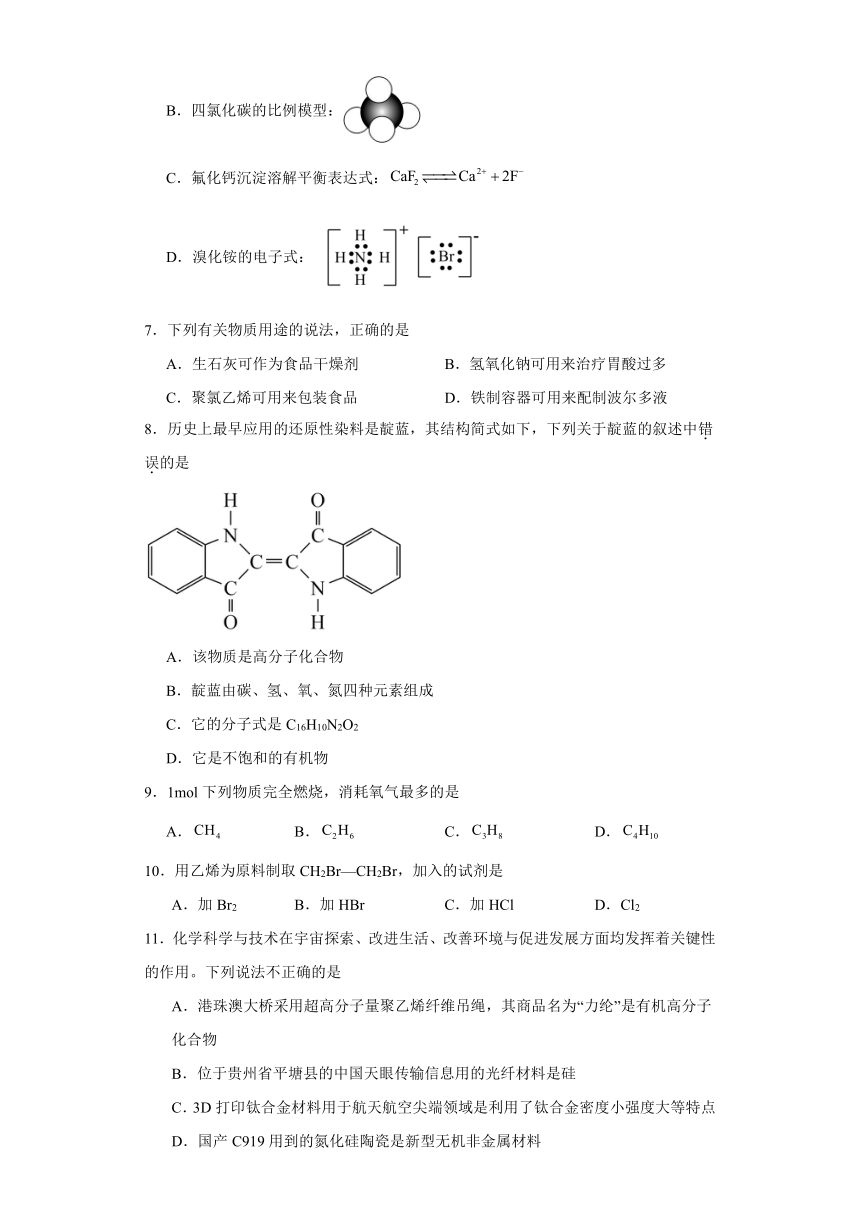
B.四氯化碳的比例模型:
C.氟化钙沉淀溶解平衡表达式:
D.溴化铵的电子式:
7.下列有关物质用途的说法,正确的是
A.生石灰可作为食品干燥剂 B.氢氧化钠可用来治疗胃酸过多
C.聚氯乙烯可用来包装食品 D.铁制容器可用来配制波尔多液
8.历史上最早应用的还原性染料是靛蓝,其结构简式如下,下列关于靛蓝的叙述中错误的是
A.该物质是高分子化合物
B.靛蓝由碳、氢、氧、氮四种元素组成
C.它的分子式是C16H10N2O2
D.它是不饱和的有机物
9.1mol下列物质完全燃烧,消耗氧气最多的是
A. B. C. D.
10.用乙烯为原料制取CH2Br—CH2Br,加入的试剂是
A.加Br2 B.加HBr C.加HCl D.Cl2
11.化学科学与技术在宇宙探索、改进生活、改善环境与促进发展方面均发挥着关键性的作用。下列说法不正确的是
A.港珠澳大桥采用超高分子量聚乙烯纤维吊绳,其商品名为“力纶”是有机高分子化合物
B.位于贵州省平塘县的中国天眼传输信息用的光纤材料是硅
C.3D打印钛合金材料用于航天航空尖端领域是利用了钛合金密度小强度大等特点
D.国产C919用到的氮化硅陶瓷是新型无机非金属材料
12.已知次氯酸具有强氧化性,可将S2﹣氧化,其反应为HClO+S2﹣+H+=Cl﹣+S↓+H2O。下列表示相关微粒的化学用语不正确的是
A.中子数为18的氯原子:35Cl B.H2O的电子式:H:O:H
C.HClO的结构式:H﹣O﹣Cl D.S2﹣的结构示意图:
13.近年我国在载人飞船、北斗卫星、5G技术、能源开发等领域取得了举世瞩目的成就,它们都与化学有着密切联系,下列判断错误的是
A.“天和”核心舱电推进系统中使用的氮化硼陶瓷材料属于新型无机非金属材料
B.北斗三号卫星搭载了精密计时的铷原子钟,铷(Rb)是碱金属元素
C.天问一号探测器着陆火星过程中使用了芳纶制作的降落伞,芳纶是高分子材料
D.大量开发可燃冰作为新能源有利于实现碳达峰、碳中和
14.下列有关微粒的化学用语正确的是
A.中子数为18的氯原子: B.乙醇的结构式:
C.的结构示意图: D.的电子式:
15.降冰片二烯在紫外线照射下可以发生下列转化。
下列说法错误的是
A.降冰片二烯与四环烷互为同分异构体
B.降冰片二烯能使酸性高锰酸钾溶液褪色
C.四环烷的一氯代物超过三种(不考虑立体异构)
D.降冰片二烯分子中位于同一平面的碳原子不超过4个
16.食品保鲜膜按材质分为聚乙烯(PE)、聚氯乙烯(PVC)、聚偏二氯乙烯(PVDC)等种类。PVC被广泛地用于食品、蔬菜外包装,它对人体有潜在危害。下列有关叙述不正确的是
A.等质量的聚乙烯和乙烯燃烧消耗的氧气相等
B.PVC保鲜膜属于链状聚合物,在加热时易熔化,能溶于氯仿
C.鉴别PE和PVC,可把其放入试管中加强热,在试管口放置一湿润的蓝色石蕊试纸,如果试纸变红,则是PVC;不变红,则为PE
D.PVC单体可由PE的单体与氯化氢加成制得
17.下图是锂离子电池的一种电解质电离出来的阴离子,该阴离子是由同周期元素X、Y、Z、R构成(如图所示),Y是构成物质种类最多的元素,Z的最外层电子数等于Y的核外电子数,四种元素的最外层电子数之和为20。下列说法正确的是
A.Y、Z、R三种元素形成的简单氢化物中,R的氢化物沸点最高
B.Y与Z形成的化合物均有毒
C.原子半径X>Y>Z>R
D.R分别与另外三种元素形成的二元化合物,各原子最外层均满足8电子稳定结构
18.下列表示物质结构的化学用语或模型正确的是
A.氯化钠的分子式: B.次氯酸的结构式:
C.甲烷的球棍模型: D.二氯甲烷的结构简式:
19.下列说法不正确的是( )
A.在光照条件下,甲苯能与Cl2发生取代反应
B.乙炔和乙烯都能使溴水褪色,其褪色原理相同
C.总质量一定的甲苯和甘油混合物完全燃烧时生成水的质量一定
D.对二氯苯只有一种结构,说明苯环结构中不存在单双建交替的结构
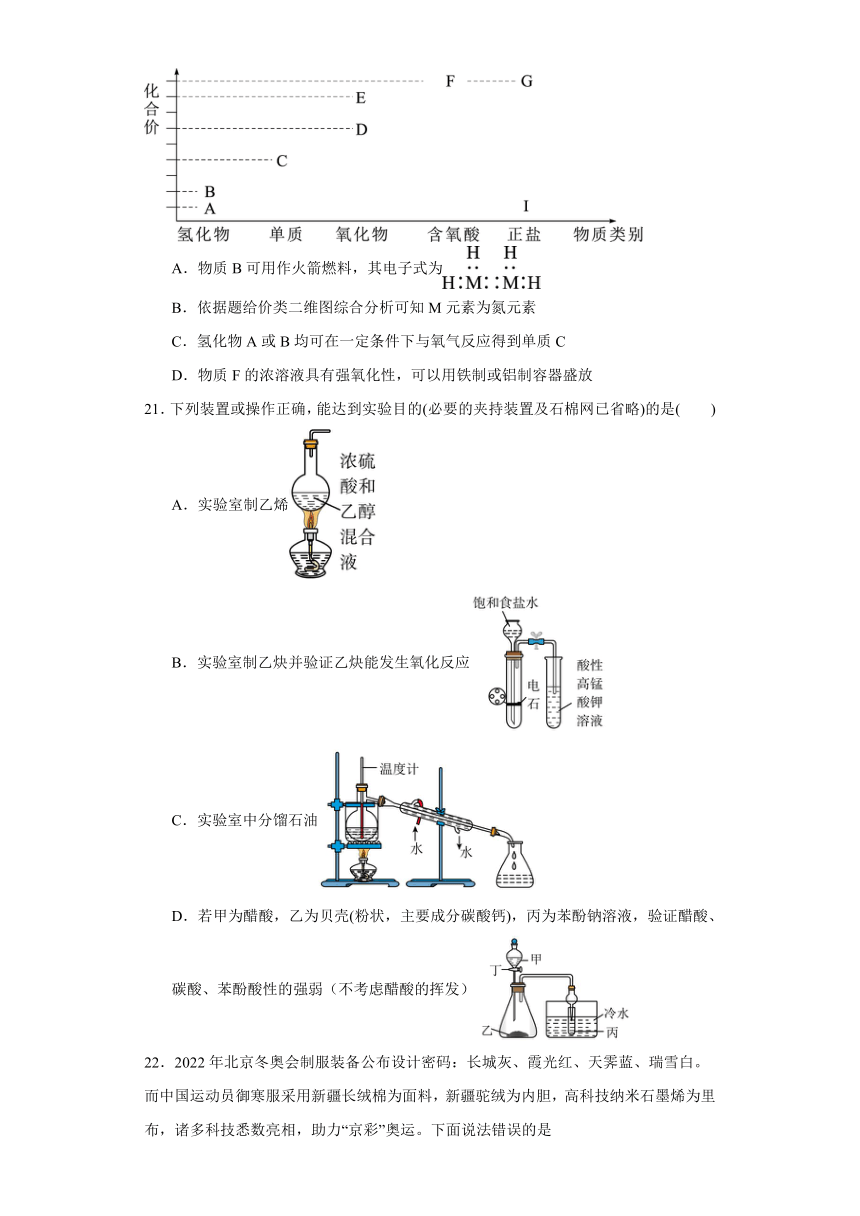
20.如图是M元素高中常见物质的价类二维图。其中A到D、D到E的转化都可加同一种物质实现,且E的相对分子质量比D的相对分子质量大16,则下列说法不正确的是
A.物质B可用作火箭燃料,其电子式为
B.依据题给价类二维图综合分析可知M元素为氮元素
C.氢化物A或B均可在一定条件下与氧气反应得到单质C
D.物质F的浓溶液具有强氧化性,可以用铁制或铝制容器盛放
21.下列装置或操作正确,能达到实验目的(必要的夹持装置及石棉网已省略)的是( )
A.实验室制乙烯
B.实验室制乙炔并验证乙炔能发生氧化反应
C.实验室中分馏石油
D.若甲为醋酸,乙为贝壳(粉状,主要成分碳酸钙),丙为苯酚钠溶液,验证醋酸、碳酸、苯酚酸性的强弱(不考虑醋酸的挥发)
22.2022年北京冬奥会制服装备公布设计密码:长城灰、霞光红、天霁蓝、瑞雪白。而中国运动员御寒服采用新疆长绒棉为面料,新疆驼绒为内胆,高科技纳米石墨烯为里布,诸多科技悉数亮相,助力“京彩”奥运。下面说法错误的是
A.长城青砖的“青”是由于含铁的氧化物
B.云蒸霞蔚中所说的霞光是胶体的丁达尔效应
C.驼绒与长绒棉主体化学成分相同,属于有机高分子
D.石墨烯可从石墨中剥离,具有导电性
23.下列分子中,所有原子都满足最外层8电子结构的是( )
A.PCl5 B.H2O C.CO2 D.LiF
24.下列表示正确的是
A.硝基苯的结构简式: B.Cl-的结构示意图:
C.NH3的电子式: D.乙炔分子的球棍模型:
25.人们发现生产人造羊毛和聚氯乙烯(PVC)可以用煤作为原料,合成路线如下。下列说法正确的是
A.PVC塑料制品可以直接用于盛放食物
B.A生成C、D的反应类型分别为加成反应、取代反应
C.实验室制备A的过程中,常用CuSO4溶液净化气体
D.与D互为同分异构体且可发生碱性水解的物质有5种(不包括环状化合物和D本身)
二、填空题
26.物理性质:乙烯是一种 ,稍有气味, 溶于水,密度比空气 的气体。
27.根据系统命名法,天然橡胶应称为聚2-甲基-1,3-丁二烯,其结构简式为,单体为2-甲基-1,3-丁二烯。该反应的化学方程式为。合成橡胶就是根据以上原理制成的。
(1)以为单体可生成氯丁橡胶,试写出该反应的化学方程式: 。
(2)丁腈橡胶的结构简式为,形成该橡胶的单体为 。
28.回答下列问题
(1)烷烃的通式是: ,烷烃分子中的碳原子数目每增加一个,其相对分子质量增加 。
(2)乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请问:乙烯的结构式 ,鉴别甲烷和乙烯的试剂是 (填序号)。
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列反应中,属于取代反应的是 ,属于加成反应的是 ,属于氧化反应的是 。(填序号
A.工业由乙烯制乙醇 B.乙烷在光照下与氯气反应
C.甲烷在空气中燃烧 D.乙烯使酸性高锰酸钾溶液褪色
试卷第1页,共3页
参考答案:
1.C
【详解】A. 氯的核电荷数为17,37Cl-的结构示意图,A项错误;
B. 元素符号左上角的数字表示质量数,中子数为7的碳原子:,B项错误;
C. 氨分子含有三个共价键,C项正确;
D. 次氯酸的中心原子是氧原子,次氯酸的电子式,D项错误;
答案选C。
【点睛】化学用语是化学考试中的高频考点,其中元素符号的含义要牢记在心,其左上角为质量数(A)、左下角为质子数(Z),质子数(Z)=核电荷数=原子序数,质量数(A)=质子数(Z)+中子数(N)。
2.C
【详解】A.聚氯乙烯是有机合成高分子化合物,聚氯乙烯是混合物,故A错误;
B.烃的定义是只含碳氢两种元素的有机物,聚四氟乙烯材料的单体中含有氟元素,因此不属于烃,故B错误;
C.氮化硼陶瓷涂层具有耐高温、性质稳定的特性,它属于新型无机非金属材料,故C正确;
D.北斗卫星导航系统所用芯片的主要成分为Si,故D错误。
综上所述,答案为C。
3.C
【详解】A.二氧化碳是共价化合物,其电子式为:,A错误;
B.氮气的电子式应该为:,B错误;
C.氯化镁是离子化合物,故其电子式为:,C正确;
D.氯化氢是共价化合物,故其的形成过程:,D错误;
故答案为:C。
4.A
【详解】A.石头纸主要成分是碳酸钙和聚乙烯,难降解,故A错误;
B.石头纸主要成分是碳酸钙,所以可以减少对树木的依赖,故B正确;
C.石头纸主要成分是碳酸钙,碳酸钙不能燃烧,故C正确;
D.石头纸的主要成分是碳酸钙,难溶于水和油,故D正确。
故答案为:A。
5.C
【详解】1摩尔烃CxHy燃烧消耗的氧气为,根据计算,C3H4消耗O2的最多;
答案选C。
6.D
【详解】A.乙烯的结构简式为,A错误;
B.碳原子的半径比氯原子小,B错误;
C.氟化钙沉淀溶解平衡表达式为:,C错误;
D.溴化铵为离子化合物,铵根离子中氮原子与氢原子以共价键结合,其电子式为: ,D正确;
答案选D。
7.A
【详解】A.生石灰能够吸收水,可以用作食品干燥剂,选项A正确;
B.氢氧化钠有腐蚀性,不能用于治疗胃酸过多,选项B错误;
C.聚氯乙烯有毒,不能用于食品包装,选项C错误;
D.铁能与硫酸铜反应生成铜,使药效降低,不能用铁制容器盛放波尔多液,选项D错误;
答案选A。
8.A
【详解】A.该有机物相对分子质量较小,而高分子化合物的相对分子质量一般在10000以上,该有机物不是高分子化合物,A错误;
B.由结构简式可知靛蓝由碳、氢、氧、氮四种元素组成,B正确;
C.由结构简式可知分子式是C16H10N2O2,C正确;
D.由结构可知,该分子含有碳碳双键、苯环、碳氧双键等,属于不饱和的有机物,D正确;
答案选A。
9.D
【解析】设烃的化学式为CxHy,燃烧的化学方程式为CxHy+(x+)O2xCO2+H2O,等物质的量的烃完全燃烧耗氧量由x+值决定,x+的值越大,消耗氧气的量就越多。
【详解】A.CH4燃烧消耗的氧气的物质的量为(1+)mol=2mol;
B.C2H6燃烧消耗的氧气的物质的量为(2+)mol=3.5mol;
C.C3H8燃烧消耗的氧气的物质的量为(3+)mol=5mol;
D.C4H10燃烧消耗的氧气的物质的量为(4+)mol=6.5mol;
所以消耗氧气最多的是C4H10,故答案选D。
【点睛】有关有机物耗氧量的计算,注意利用分子式的变形较为直观,可以省去书写化学方程式的繁琐。
10.A
【详解】将CH2Br—CH2Br的分子式与乙烯的分子式C2H4相减,可得出差值为Br2,所以用乙烯为原料制取CH2Br—CH2Br时,加入的试剂是Br2,故选A。
11.B
【详解】A.聚乙烯纤维属于合成高分子材料,属于有机高分子化合物,A正确;
B.二氧化硅是构成光纤材料的成分,而不是硅,B错误;
C.钛是一种轻金属,钛合金密度小强度大,具有优良的金属特性,用于航天航空尖端领域,C正确;
D.氮化硅陶瓷是无机非金属材料,不是金属材料,D正确;
故合理选项是B。
12.B
【详解】A.中子数为18的氯原子,其质量数是18+17=35,可表示为:35Cl,A正确;
B.H2O是共价化合物,电子式为:,B错误;
C.HClO的结构式为:H-O-Cl,C正确;
D.S2﹣的核外电子数是18个,结构示意图为:,D正确;
答案选B。
13.D
【详解】A.氮化硼陶瓷材料能耐高温,属于新型无机非金属材料,A正确;
B.铷位于周期表第五周期第ⅠA族,属于碱金属,B正确;
C.芳纶属于合成纤维,是高分子材料,C正确;
D.可燃冰的主要成分是,作为能源燃烧时仍产生大量的不利于实现碳达峰、碳中和,故D错误。
故选D。
14.C
【详解】A.质量数=质子数+中子数,故中子数为18的氯原子的质量数为35,故表示为Cl,故A错误;
B.乙醇的结构简式为C2H5OH,结构式为,故B错误;
C.钠离子的核内有11个质子,核外有10个电子,故钠离子的结构示意图为,故C正确;
D.氯化铵是由铵根离子与氯离子通过离子键形成离子化合物,电子式,故D错误。
故选:C。
15.C
【详解】A.降冰片二烯与四环烷分子式相同,结构不同,因此二者互为同分异构体,A项正确;
B.降冰片二烯分子中含有碳碳双键,因此能使酸性高锰酸钾溶液褪色,B项正确;
C.四环烷含有三种化学环境不同的H原子,因此其一氯代物有三种,C项错误;
D.根据乙烯分子是平面分子,与碳碳双键连接的C原子在碳碳双键所在的平面上,可知降冰片二烯分子中位于同一平面的碳原子最多为4个,D项正确;
答案选C。
16.D
【详解】A.乙烯是聚乙烯的单体,它们的最简式相同,它们含C和H的质量分数分别相等,所以等质量的两者燃烧时生成CO2、H2O的量分别相等,故A正确。
B.PE、PVC都属于链状高分子化合物,能溶于氯仿,加热熔化、冷却后变成固体,可以反复进行,故B正确;
C.PVC加热产生氯化氢而PE不产生,根据是否有氯化氢产生即可鉴别,故C正确;
D.PVC单体为氯乙烯,应该由乙炔和HCl加成得到,故D错误。
故选D。
17.C
【分析】Y是构成物质种类最多的元素,则Y为C;Z的最外层电子数等于Y的核外电子数,X、Y、Z、R同周期,则Z为O;R形成一个共价键,则R为F;四种元素的最外层电子数之和为20,则X最外层电子数为20-4-6-7=3,由结构也可以X最外层电子数为3,则X为B,即X、Y、Z、R分别为B、C、O、F,据此解答。
【详解】A.Y、Z、R三种元素形成的简单氢化物分别为CH4、H2O、HF,H2O 常温呈液态,另外两种呈气态,则水的沸点最高,即X的氢化物沸点最高,A错误;
B.Y与Z形成的化合物即CO2、CO等,CO2无毒,B错误;
C.同周期从左往右原子半径减小,则原子半径X(B)>Y(C)>Z(O)>R(F),C正确;
D.F和B形成的化合物各原子最外层不一定满足8电子稳定结构,如BF,D错误;
答案选C。
18.B
【详解】A.氯化钠由钠离子和氯离子构成,不存在分子,A项错误;
B.次氯酸分子中氧原子共用2对电子,氯原子共用1对电子,其结构式为,B项正确;
C. 为甲烷的比例模型,C项错误;
D.为二氯甲烷的结构式,其结构简式为:,D项错误;
答案选B。
19.D
【详解】A.甲苯中甲基上的氢可以在光照条件下和氯气发生取代反应,A正确;
B.乙炔和乙烯与溴水都能发生加成反应,则褪色原理相同,B正确;
C.甲苯()和甘油()的含氢量相等,总质量一定的甲苯和甘油混合物中氢元素的质量一定,完全燃烧时生成水的质量一定,C正确;
D.对二氯苯仅一种结构,不能说明苯环结构中不存在单双键交替的结构,因为如果是单双键交替的结构,对二氯苯也是一种结构,故D错误;
故答案选D。
【点睛】邻二氯苯仅一种结构,才能说明苯环结构中不存在单双键交替的结构,因为如果是苯环结构中存在单双键交替的结构,邻二氯苯有2种结构。
20.A
【分析】从图中可以看出,C为单质,所含元素化合价为0价,A和B均为氢化物,M元素的化合价分别为-3和-2,所以M为氮元素,则A为NH3,B为N2H4,D为NO,E为NO2,F为HNO3,G为硝酸盐。
【详解】A.物质B为,其N元素之间只有1个共用电子对,故A说法错误;
B.依据题给价类二维图有两种氢化物且M的化合价为-3、-2价,综合分析可知M元素为氮元素,故B说法正确;
C.氢化物或均可在一定条件下与发生反应得到和,故C说法正确;
D.物质F为,其浓溶液具有强氧化性,可以使铁或铝在常温下发生钝化,因此可以用铁制或铝制容器盛放,故D说法正确;
综合答案选A。
21.D
【详解】A.无温度计,无法测量反应温度,若反应温度在140℃时,生成乙醚,170℃时生成乙烯,A错误;
B.实验室制备乙炔不能使用启普发生器及简易启普发生器,B错误;
C.温度计水银球的位置错误,应与蒸馏瓶支管下沿平齐,C错误;
D.强酸与弱酸的盐反应制弱酸,醋酸与碳酸钙贝壳反应制取二氧化碳,二氧化碳再与苯酚钠反应制取苯酚,D正确;
答案选D。
22.C
【详解】A.长城青砖的“青”是由于含铁的氧化物,如Fe3O4,故A正确;
B.云烟雾是胶体,能产生丁达尔效应,故B正确;
C.驼绒是化学成分是蛋白质、长绒棉的主体化学成分是纤维素,故C错误;
D.石墨烯可从石墨中剥离,根据石墨能导电,所以石墨烯具有导电性,故D正确;
选C;
23.C
【详解】A.PCl5中P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,P原子不满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,A错误;
B.H2O中O元素化合价为-2,O原子最外层电子数为6,所以2+6=8,O原子满足8电子结构;H元素化合价为+1,H原子最外层电子数为1,所以1+1=2,H原子不满足8电子结构,B错误;
C.CO2中C元素化合价为+4,C原子最外层电子数为4,所以4+4=8,C原子满足8电子结构;O元素化合价为-2,O原子最外层电子数为6,所以2+6=8,O原子满足8电子结构,C正确;
D.LiF是离子化合物,Li元素化合价为+1,Li满足2电子稳定结构。F元素化合价为-1,F原子最外层电子数为7,所以1+7=8,F原子满足8电子结构,D错误;
答案选C。
24.D
【详解】A.硝基苯中硝基-NO2中的N原子与苯环的C原子形成共价键,故其结构简式:,A正确;
B.Cl元素原子核内质子数为17,故Cl-的结构示意图:,B错误;
C.NH3分子中N原子上还有1对孤电子对,故NH3的电子式:,C错误;
D.乙炔分子中2个C原子形成共价三键,每个C原子再分别与H原子形成1个共价键,4个原子在同一条直线上,故乙炔分子的球棍模型:,D正确;
故合理选项是D。
25.C
【分析】由题给流程可知,煤干馏得到焦炭,焦炭在电炉中和氧化钙发生反应生成碳化钙,碳化钙与水反应生成乙炔,乙炔和氯化氢在催化剂的条件下发生加成反应生成氯乙烯,氯乙烯在一定的条件下发生加聚反应生成聚氯乙烯,既得PVC;由乙炔和人造羊毛的结构简式可知形成人造羊毛的单体为H2C═CH-OOCCH3和H2C═CH-CN,则乙炔和HCN发生加成反应生成CH2═CHCN,乙炔和乙酸加成反应生成H2C═CH-OOCCH3,一定条件下,CH2═CHCN和H2C═CH-OOCCH3发生加聚反应生成高分子化合物人造羊毛。
【详解】A.聚氯乙烯有毒,不能用于盛放食物,故A错误;
B.A生成C、D的反应为乙炔和HCN发生加成反应生成CH2═CHCN、乙炔和乙酸加成反应生成H2C═CH-OOCCH3,故B错误;
C.电石中混有硫化钙和磷化钙,与水反应生成的硫化氢和磷化氢能与硫酸铜溶液反应,则用硫酸铜溶液吸收硫化氢和磷化氢达到净化乙炔气体的目的,故C正确;
D.D的结构简式为H2C═CH-OOCCH3,与H2C═CH-OOCCH3互为同分异构体且可发生碱性水解的物质属于酯,符合条件的结构简式有CH2═CHCOOCH3、HCOOCH2CH═CH2、CH3COOCH═CH2、,共4种,故D错误;
故选C。
26. 无色 难 略小
【详解】乙烯是一种无色气体,难溶于水,密度比空气略小的气体,答案:无色;难;略小。
27. CH2=CH-CH=CH2和
【分析】(1)从信息中可以领会出,单体加聚就是将单体中的碳碳双键断裂一个键,将形成的链节连成长链。若为二烯烃,则中间可形成一个双键。
(2)由高聚物寻找单体,先判断是加聚产物还是缩聚产物,若为加聚产物,则先确定链节,然后采用断键成烯的方法确定单体。
【详解】(1)以为单体生成氯丁橡胶时,先断双键中的一个键形成链节,再形成高聚物,反应的化学方程式为。答案为:;
(2)丁腈橡胶的结构简式为,根据长链,丁腈橡胶是加聚产物,则其链节为,采用断键成烯法,可得该橡胶的单体为CH2=CH-CH=CH2和。答案为:CH2=CH-CH=CH2和。
【点睛】由加聚产物的链节确定单体时,若主链上没有碳碳双键,则以主链上每2个碳原子一组将链节上的碳碳键断开,从而形成碳碳双键;若链节上出现碳碳双键,则以双键左右各2个碳原子作为一组断裂碳碳键,从而形成二烯。
28.(1) CnH2n+2 14
(2) BD
(3) B A CD
【详解】(1)烷烃中,每个C形成4个共价单键,相邻的2个C原子间形成1对共用电子,相当于减少了2个H原子;若C为n个,则H为4n-2(n-1)=2n+2,所以通式是:CnH2n+2,烷烃分子中的碳原子数目每增加一个,氢原子就增加二个,则其相对分子质量增加14。答案为:CnH2n+2;14;
(2)乙烯的分子式为C2H4,结构式为,鉴别甲烷和乙烯时,可以使用溴水、溴的四氯化碳溶液、酸性高锰酸钾溶液,故试剂是BD。答案为:;BD;
(3)A.工业由乙烯与水反应制取乙醇,发生加成反应;
B.乙烷在光照下与氯气反应,生成氯代乙烷和氯化氢,发生取代反应;
C.甲烷在空气中燃烧,生成二氧化碳和水,发生氧化反应;
D.乙烯使酸性高锰酸钾溶液褪色,发生氧化反应;
则属于取代反应的是B,属于加成反应的是A,属于氧化反应的是CD。答案为:B;A;CD
一、单选题
1.下列有关化学用语的表述正确的是( )
A.37Cl-的结构示意图: B.中子数为7的碳原子:C
C.NH3的结构式: D.次氯酸的电子式:
2.建国以来我国的化学工业发展迅速,为提高我们的国际地位和改善人民群众的生产生活做出了突出贡献,下列说法正确的是
A.北京冬奥会吉祥物“冰墩墩”的材质中有聚氯乙烯,聚氯乙烯是纯净物
B.中国承建卡塔尔世界杯“大金碗”球场采用聚四氟乙烯材料的单体是不饱和烃
C.空间站天和核心舱的太阳电池翼的氮化硼陶瓷涂层属于新型无机非金属材料
D.北斗卫星导航系统由中国自主研发、独立运行,其所用芯片的主要成分为
3.下列化学用语表达正确的是
A.二氧化碳: B.氮气:
C.氯化镁: D.氯化氢的形成过程:
4.三层复合石头纸是一种新型纸张,其结构如图所示:上下两层为聚乙烯,中间层为碳酸钙。下列关于它的叙述错误的是
A.易生物降解 B.可替代木浆纸以减少树木砍伐
C.与普通纸相比难以燃烧 D.具有防水防油的特性
5.相同物质的量的下列各烃,完全燃烧消耗O2的量最大的是
A.CH4 B.C2H4
C.C3H4 D.C2H6
6.下列化学用语表达正确的是
A.乙烯的结构简式:
B.四氯化碳的比例模型:
C.氟化钙沉淀溶解平衡表达式:
D.溴化铵的电子式:
7.下列有关物质用途的说法,正确的是
A.生石灰可作为食品干燥剂 B.氢氧化钠可用来治疗胃酸过多
C.聚氯乙烯可用来包装食品 D.铁制容器可用来配制波尔多液
8.历史上最早应用的还原性染料是靛蓝,其结构简式如下,下列关于靛蓝的叙述中错误的是
A.该物质是高分子化合物
B.靛蓝由碳、氢、氧、氮四种元素组成
C.它的分子式是C16H10N2O2
D.它是不饱和的有机物
9.1mol下列物质完全燃烧,消耗氧气最多的是
A. B. C. D.
10.用乙烯为原料制取CH2Br—CH2Br,加入的试剂是
A.加Br2 B.加HBr C.加HCl D.Cl2
11.化学科学与技术在宇宙探索、改进生活、改善环境与促进发展方面均发挥着关键性的作用。下列说法不正确的是
A.港珠澳大桥采用超高分子量聚乙烯纤维吊绳,其商品名为“力纶”是有机高分子化合物
B.位于贵州省平塘县的中国天眼传输信息用的光纤材料是硅
C.3D打印钛合金材料用于航天航空尖端领域是利用了钛合金密度小强度大等特点
D.国产C919用到的氮化硅陶瓷是新型无机非金属材料
12.已知次氯酸具有强氧化性,可将S2﹣氧化,其反应为HClO+S2﹣+H+=Cl﹣+S↓+H2O。下列表示相关微粒的化学用语不正确的是
A.中子数为18的氯原子:35Cl B.H2O的电子式:H:O:H
C.HClO的结构式:H﹣O﹣Cl D.S2﹣的结构示意图:
13.近年我国在载人飞船、北斗卫星、5G技术、能源开发等领域取得了举世瞩目的成就,它们都与化学有着密切联系,下列判断错误的是
A.“天和”核心舱电推进系统中使用的氮化硼陶瓷材料属于新型无机非金属材料
B.北斗三号卫星搭载了精密计时的铷原子钟,铷(Rb)是碱金属元素
C.天问一号探测器着陆火星过程中使用了芳纶制作的降落伞,芳纶是高分子材料
D.大量开发可燃冰作为新能源有利于实现碳达峰、碳中和
14.下列有关微粒的化学用语正确的是
A.中子数为18的氯原子: B.乙醇的结构式:
C.的结构示意图: D.的电子式:
15.降冰片二烯在紫外线照射下可以发生下列转化。
下列说法错误的是
A.降冰片二烯与四环烷互为同分异构体
B.降冰片二烯能使酸性高锰酸钾溶液褪色
C.四环烷的一氯代物超过三种(不考虑立体异构)
D.降冰片二烯分子中位于同一平面的碳原子不超过4个
16.食品保鲜膜按材质分为聚乙烯(PE)、聚氯乙烯(PVC)、聚偏二氯乙烯(PVDC)等种类。PVC被广泛地用于食品、蔬菜外包装,它对人体有潜在危害。下列有关叙述不正确的是
A.等质量的聚乙烯和乙烯燃烧消耗的氧气相等
B.PVC保鲜膜属于链状聚合物,在加热时易熔化,能溶于氯仿
C.鉴别PE和PVC,可把其放入试管中加强热,在试管口放置一湿润的蓝色石蕊试纸,如果试纸变红,则是PVC;不变红,则为PE
D.PVC单体可由PE的单体与氯化氢加成制得
17.下图是锂离子电池的一种电解质电离出来的阴离子,该阴离子是由同周期元素X、Y、Z、R构成(如图所示),Y是构成物质种类最多的元素,Z的最外层电子数等于Y的核外电子数,四种元素的最外层电子数之和为20。下列说法正确的是
A.Y、Z、R三种元素形成的简单氢化物中,R的氢化物沸点最高
B.Y与Z形成的化合物均有毒
C.原子半径X>Y>Z>R
D.R分别与另外三种元素形成的二元化合物,各原子最外层均满足8电子稳定结构
18.下列表示物质结构的化学用语或模型正确的是
A.氯化钠的分子式: B.次氯酸的结构式:
C.甲烷的球棍模型: D.二氯甲烷的结构简式:
19.下列说法不正确的是( )
A.在光照条件下,甲苯能与Cl2发生取代反应
B.乙炔和乙烯都能使溴水褪色,其褪色原理相同
C.总质量一定的甲苯和甘油混合物完全燃烧时生成水的质量一定
D.对二氯苯只有一种结构,说明苯环结构中不存在单双建交替的结构
20.如图是M元素高中常见物质的价类二维图。其中A到D、D到E的转化都可加同一种物质实现,且E的相对分子质量比D的相对分子质量大16,则下列说法不正确的是
A.物质B可用作火箭燃料,其电子式为
B.依据题给价类二维图综合分析可知M元素为氮元素
C.氢化物A或B均可在一定条件下与氧气反应得到单质C
D.物质F的浓溶液具有强氧化性,可以用铁制或铝制容器盛放
21.下列装置或操作正确,能达到实验目的(必要的夹持装置及石棉网已省略)的是( )
A.实验室制乙烯
B.实验室制乙炔并验证乙炔能发生氧化反应
C.实验室中分馏石油
D.若甲为醋酸,乙为贝壳(粉状,主要成分碳酸钙),丙为苯酚钠溶液,验证醋酸、碳酸、苯酚酸性的强弱(不考虑醋酸的挥发)
22.2022年北京冬奥会制服装备公布设计密码:长城灰、霞光红、天霁蓝、瑞雪白。而中国运动员御寒服采用新疆长绒棉为面料,新疆驼绒为内胆,高科技纳米石墨烯为里布,诸多科技悉数亮相,助力“京彩”奥运。下面说法错误的是
A.长城青砖的“青”是由于含铁的氧化物
B.云蒸霞蔚中所说的霞光是胶体的丁达尔效应
C.驼绒与长绒棉主体化学成分相同,属于有机高分子
D.石墨烯可从石墨中剥离,具有导电性
23.下列分子中,所有原子都满足最外层8电子结构的是( )
A.PCl5 B.H2O C.CO2 D.LiF
24.下列表示正确的是
A.硝基苯的结构简式: B.Cl-的结构示意图:
C.NH3的电子式: D.乙炔分子的球棍模型:
25.人们发现生产人造羊毛和聚氯乙烯(PVC)可以用煤作为原料,合成路线如下。下列说法正确的是
A.PVC塑料制品可以直接用于盛放食物
B.A生成C、D的反应类型分别为加成反应、取代反应
C.实验室制备A的过程中,常用CuSO4溶液净化气体
D.与D互为同分异构体且可发生碱性水解的物质有5种(不包括环状化合物和D本身)
二、填空题
26.物理性质:乙烯是一种 ,稍有气味, 溶于水,密度比空气 的气体。
27.根据系统命名法,天然橡胶应称为聚2-甲基-1,3-丁二烯,其结构简式为,单体为2-甲基-1,3-丁二烯。该反应的化学方程式为。合成橡胶就是根据以上原理制成的。
(1)以为单体可生成氯丁橡胶,试写出该反应的化学方程式: 。
(2)丁腈橡胶的结构简式为,形成该橡胶的单体为 。
28.回答下列问题
(1)烷烃的通式是: ,烷烃分子中的碳原子数目每增加一个,其相对分子质量增加 。
(2)乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请问:乙烯的结构式 ,鉴别甲烷和乙烯的试剂是 (填序号)。
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列反应中,属于取代反应的是 ,属于加成反应的是 ,属于氧化反应的是 。(填序号
A.工业由乙烯制乙醇 B.乙烷在光照下与氯气反应
C.甲烷在空气中燃烧 D.乙烯使酸性高锰酸钾溶液褪色
试卷第1页,共3页
参考答案:
1.C
【详解】A. 氯的核电荷数为17,37Cl-的结构示意图,A项错误;
B. 元素符号左上角的数字表示质量数,中子数为7的碳原子:,B项错误;
C. 氨分子含有三个共价键,C项正确;
D. 次氯酸的中心原子是氧原子,次氯酸的电子式,D项错误;
答案选C。
【点睛】化学用语是化学考试中的高频考点,其中元素符号的含义要牢记在心,其左上角为质量数(A)、左下角为质子数(Z),质子数(Z)=核电荷数=原子序数,质量数(A)=质子数(Z)+中子数(N)。
2.C
【详解】A.聚氯乙烯是有机合成高分子化合物,聚氯乙烯是混合物,故A错误;
B.烃的定义是只含碳氢两种元素的有机物,聚四氟乙烯材料的单体中含有氟元素,因此不属于烃,故B错误;
C.氮化硼陶瓷涂层具有耐高温、性质稳定的特性,它属于新型无机非金属材料,故C正确;
D.北斗卫星导航系统所用芯片的主要成分为Si,故D错误。
综上所述,答案为C。
3.C
【详解】A.二氧化碳是共价化合物,其电子式为:,A错误;
B.氮气的电子式应该为:,B错误;
C.氯化镁是离子化合物,故其电子式为:,C正确;
D.氯化氢是共价化合物,故其的形成过程:,D错误;
故答案为:C。
4.A
【详解】A.石头纸主要成分是碳酸钙和聚乙烯,难降解,故A错误;
B.石头纸主要成分是碳酸钙,所以可以减少对树木的依赖,故B正确;
C.石头纸主要成分是碳酸钙,碳酸钙不能燃烧,故C正确;
D.石头纸的主要成分是碳酸钙,难溶于水和油,故D正确。
故答案为:A。
5.C
【详解】1摩尔烃CxHy燃烧消耗的氧气为,根据计算,C3H4消耗O2的最多;
答案选C。
6.D
【详解】A.乙烯的结构简式为,A错误;
B.碳原子的半径比氯原子小,B错误;
C.氟化钙沉淀溶解平衡表达式为:,C错误;
D.溴化铵为离子化合物,铵根离子中氮原子与氢原子以共价键结合,其电子式为: ,D正确;
答案选D。
7.A
【详解】A.生石灰能够吸收水,可以用作食品干燥剂,选项A正确;
B.氢氧化钠有腐蚀性,不能用于治疗胃酸过多,选项B错误;
C.聚氯乙烯有毒,不能用于食品包装,选项C错误;
D.铁能与硫酸铜反应生成铜,使药效降低,不能用铁制容器盛放波尔多液,选项D错误;
答案选A。
8.A
【详解】A.该有机物相对分子质量较小,而高分子化合物的相对分子质量一般在10000以上,该有机物不是高分子化合物,A错误;
B.由结构简式可知靛蓝由碳、氢、氧、氮四种元素组成,B正确;
C.由结构简式可知分子式是C16H10N2O2,C正确;
D.由结构可知,该分子含有碳碳双键、苯环、碳氧双键等,属于不饱和的有机物,D正确;
答案选A。
9.D
【解析】设烃的化学式为CxHy,燃烧的化学方程式为CxHy+(x+)O2xCO2+H2O,等物质的量的烃完全燃烧耗氧量由x+值决定,x+的值越大,消耗氧气的量就越多。
【详解】A.CH4燃烧消耗的氧气的物质的量为(1+)mol=2mol;
B.C2H6燃烧消耗的氧气的物质的量为(2+)mol=3.5mol;
C.C3H8燃烧消耗的氧气的物质的量为(3+)mol=5mol;
D.C4H10燃烧消耗的氧气的物质的量为(4+)mol=6.5mol;
所以消耗氧气最多的是C4H10,故答案选D。
【点睛】有关有机物耗氧量的计算,注意利用分子式的变形较为直观,可以省去书写化学方程式的繁琐。
10.A
【详解】将CH2Br—CH2Br的分子式与乙烯的分子式C2H4相减,可得出差值为Br2,所以用乙烯为原料制取CH2Br—CH2Br时,加入的试剂是Br2,故选A。
11.B
【详解】A.聚乙烯纤维属于合成高分子材料,属于有机高分子化合物,A正确;
B.二氧化硅是构成光纤材料的成分,而不是硅,B错误;
C.钛是一种轻金属,钛合金密度小强度大,具有优良的金属特性,用于航天航空尖端领域,C正确;
D.氮化硅陶瓷是无机非金属材料,不是金属材料,D正确;
故合理选项是B。
12.B
【详解】A.中子数为18的氯原子,其质量数是18+17=35,可表示为:35Cl,A正确;
B.H2O是共价化合物,电子式为:,B错误;
C.HClO的结构式为:H-O-Cl,C正确;
D.S2﹣的核外电子数是18个,结构示意图为:,D正确;
答案选B。
13.D
【详解】A.氮化硼陶瓷材料能耐高温,属于新型无机非金属材料,A正确;
B.铷位于周期表第五周期第ⅠA族,属于碱金属,B正确;
C.芳纶属于合成纤维,是高分子材料,C正确;
D.可燃冰的主要成分是,作为能源燃烧时仍产生大量的不利于实现碳达峰、碳中和,故D错误。
故选D。
14.C
【详解】A.质量数=质子数+中子数,故中子数为18的氯原子的质量数为35,故表示为Cl,故A错误;
B.乙醇的结构简式为C2H5OH,结构式为,故B错误;
C.钠离子的核内有11个质子,核外有10个电子,故钠离子的结构示意图为,故C正确;
D.氯化铵是由铵根离子与氯离子通过离子键形成离子化合物,电子式,故D错误。
故选:C。
15.C
【详解】A.降冰片二烯与四环烷分子式相同,结构不同,因此二者互为同分异构体,A项正确;
B.降冰片二烯分子中含有碳碳双键,因此能使酸性高锰酸钾溶液褪色,B项正确;
C.四环烷含有三种化学环境不同的H原子,因此其一氯代物有三种,C项错误;
D.根据乙烯分子是平面分子,与碳碳双键连接的C原子在碳碳双键所在的平面上,可知降冰片二烯分子中位于同一平面的碳原子最多为4个,D项正确;
答案选C。
16.D
【详解】A.乙烯是聚乙烯的单体,它们的最简式相同,它们含C和H的质量分数分别相等,所以等质量的两者燃烧时生成CO2、H2O的量分别相等,故A正确。
B.PE、PVC都属于链状高分子化合物,能溶于氯仿,加热熔化、冷却后变成固体,可以反复进行,故B正确;
C.PVC加热产生氯化氢而PE不产生,根据是否有氯化氢产生即可鉴别,故C正确;
D.PVC单体为氯乙烯,应该由乙炔和HCl加成得到,故D错误。
故选D。
17.C
【分析】Y是构成物质种类最多的元素,则Y为C;Z的最外层电子数等于Y的核外电子数,X、Y、Z、R同周期,则Z为O;R形成一个共价键,则R为F;四种元素的最外层电子数之和为20,则X最外层电子数为20-4-6-7=3,由结构也可以X最外层电子数为3,则X为B,即X、Y、Z、R分别为B、C、O、F,据此解答。
【详解】A.Y、Z、R三种元素形成的简单氢化物分别为CH4、H2O、HF,H2O 常温呈液态,另外两种呈气态,则水的沸点最高,即X的氢化物沸点最高,A错误;
B.Y与Z形成的化合物即CO2、CO等,CO2无毒,B错误;
C.同周期从左往右原子半径减小,则原子半径X(B)>Y(C)>Z(O)>R(F),C正确;
D.F和B形成的化合物各原子最外层不一定满足8电子稳定结构,如BF,D错误;
答案选C。
18.B
【详解】A.氯化钠由钠离子和氯离子构成,不存在分子,A项错误;
B.次氯酸分子中氧原子共用2对电子,氯原子共用1对电子,其结构式为,B项正确;
C. 为甲烷的比例模型,C项错误;
D.为二氯甲烷的结构式,其结构简式为:,D项错误;
答案选B。
19.D
【详解】A.甲苯中甲基上的氢可以在光照条件下和氯气发生取代反应,A正确;
B.乙炔和乙烯与溴水都能发生加成反应,则褪色原理相同,B正确;
C.甲苯()和甘油()的含氢量相等,总质量一定的甲苯和甘油混合物中氢元素的质量一定,完全燃烧时生成水的质量一定,C正确;
D.对二氯苯仅一种结构,不能说明苯环结构中不存在单双键交替的结构,因为如果是单双键交替的结构,对二氯苯也是一种结构,故D错误;
故答案选D。
【点睛】邻二氯苯仅一种结构,才能说明苯环结构中不存在单双键交替的结构,因为如果是苯环结构中存在单双键交替的结构,邻二氯苯有2种结构。
20.A
【分析】从图中可以看出,C为单质,所含元素化合价为0价,A和B均为氢化物,M元素的化合价分别为-3和-2,所以M为氮元素,则A为NH3,B为N2H4,D为NO,E为NO2,F为HNO3,G为硝酸盐。
【详解】A.物质B为,其N元素之间只有1个共用电子对,故A说法错误;
B.依据题给价类二维图有两种氢化物且M的化合价为-3、-2价,综合分析可知M元素为氮元素,故B说法正确;
C.氢化物或均可在一定条件下与发生反应得到和,故C说法正确;
D.物质F为,其浓溶液具有强氧化性,可以使铁或铝在常温下发生钝化,因此可以用铁制或铝制容器盛放,故D说法正确;
综合答案选A。
21.D
【详解】A.无温度计,无法测量反应温度,若反应温度在140℃时,生成乙醚,170℃时生成乙烯,A错误;
B.实验室制备乙炔不能使用启普发生器及简易启普发生器,B错误;
C.温度计水银球的位置错误,应与蒸馏瓶支管下沿平齐,C错误;
D.强酸与弱酸的盐反应制弱酸,醋酸与碳酸钙贝壳反应制取二氧化碳,二氧化碳再与苯酚钠反应制取苯酚,D正确;
答案选D。
22.C
【详解】A.长城青砖的“青”是由于含铁的氧化物,如Fe3O4,故A正确;
B.云烟雾是胶体,能产生丁达尔效应,故B正确;
C.驼绒是化学成分是蛋白质、长绒棉的主体化学成分是纤维素,故C错误;
D.石墨烯可从石墨中剥离,根据石墨能导电,所以石墨烯具有导电性,故D正确;
选C;
23.C
【详解】A.PCl5中P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,P原子不满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,A错误;
B.H2O中O元素化合价为-2,O原子最外层电子数为6,所以2+6=8,O原子满足8电子结构;H元素化合价为+1,H原子最外层电子数为1,所以1+1=2,H原子不满足8电子结构,B错误;
C.CO2中C元素化合价为+4,C原子最外层电子数为4,所以4+4=8,C原子满足8电子结构;O元素化合价为-2,O原子最外层电子数为6,所以2+6=8,O原子满足8电子结构,C正确;
D.LiF是离子化合物,Li元素化合价为+1,Li满足2电子稳定结构。F元素化合价为-1,F原子最外层电子数为7,所以1+7=8,F原子满足8电子结构,D错误;
答案选C。
24.D
【详解】A.硝基苯中硝基-NO2中的N原子与苯环的C原子形成共价键,故其结构简式:,A正确;
B.Cl元素原子核内质子数为17,故Cl-的结构示意图:,B错误;
C.NH3分子中N原子上还有1对孤电子对,故NH3的电子式:,C错误;
D.乙炔分子中2个C原子形成共价三键,每个C原子再分别与H原子形成1个共价键,4个原子在同一条直线上,故乙炔分子的球棍模型:,D正确;
故合理选项是D。
25.C
【分析】由题给流程可知,煤干馏得到焦炭,焦炭在电炉中和氧化钙发生反应生成碳化钙,碳化钙与水反应生成乙炔,乙炔和氯化氢在催化剂的条件下发生加成反应生成氯乙烯,氯乙烯在一定的条件下发生加聚反应生成聚氯乙烯,既得PVC;由乙炔和人造羊毛的结构简式可知形成人造羊毛的单体为H2C═CH-OOCCH3和H2C═CH-CN,则乙炔和HCN发生加成反应生成CH2═CHCN,乙炔和乙酸加成反应生成H2C═CH-OOCCH3,一定条件下,CH2═CHCN和H2C═CH-OOCCH3发生加聚反应生成高分子化合物人造羊毛。
【详解】A.聚氯乙烯有毒,不能用于盛放食物,故A错误;
B.A生成C、D的反应为乙炔和HCN发生加成反应生成CH2═CHCN、乙炔和乙酸加成反应生成H2C═CH-OOCCH3,故B错误;
C.电石中混有硫化钙和磷化钙,与水反应生成的硫化氢和磷化氢能与硫酸铜溶液反应,则用硫酸铜溶液吸收硫化氢和磷化氢达到净化乙炔气体的目的,故C正确;
D.D的结构简式为H2C═CH-OOCCH3,与H2C═CH-OOCCH3互为同分异构体且可发生碱性水解的物质属于酯,符合条件的结构简式有CH2═CHCOOCH3、HCOOCH2CH═CH2、CH3COOCH═CH2、,共4种,故D错误;
故选C。
26. 无色 难 略小
【详解】乙烯是一种无色气体,难溶于水,密度比空气略小的气体,答案:无色;难;略小。
27. CH2=CH-CH=CH2和
【分析】(1)从信息中可以领会出,单体加聚就是将单体中的碳碳双键断裂一个键,将形成的链节连成长链。若为二烯烃,则中间可形成一个双键。
(2)由高聚物寻找单体,先判断是加聚产物还是缩聚产物,若为加聚产物,则先确定链节,然后采用断键成烯的方法确定单体。
【详解】(1)以为单体生成氯丁橡胶时,先断双键中的一个键形成链节,再形成高聚物,反应的化学方程式为。答案为:;
(2)丁腈橡胶的结构简式为,根据长链,丁腈橡胶是加聚产物,则其链节为,采用断键成烯法,可得该橡胶的单体为CH2=CH-CH=CH2和。答案为:CH2=CH-CH=CH2和。
【点睛】由加聚产物的链节确定单体时,若主链上没有碳碳双键,则以主链上每2个碳原子一组将链节上的碳碳键断开,从而形成碳碳双键;若链节上出现碳碳双键,则以双键左右各2个碳原子作为一组断裂碳碳键,从而形成二烯。
28.(1) CnH2n+2 14
(2) BD
(3) B A CD
【详解】(1)烷烃中,每个C形成4个共价单键,相邻的2个C原子间形成1对共用电子,相当于减少了2个H原子;若C为n个,则H为4n-2(n-1)=2n+2,所以通式是:CnH2n+2,烷烃分子中的碳原子数目每增加一个,氢原子就增加二个,则其相对分子质量增加14。答案为:CnH2n+2;14;
(2)乙烯的分子式为C2H4,结构式为,鉴别甲烷和乙烯时,可以使用溴水、溴的四氯化碳溶液、酸性高锰酸钾溶液,故试剂是BD。答案为:;BD;
(3)A.工业由乙烯与水反应制取乙醇,发生加成反应;
B.乙烷在光照下与氯气反应,生成氯代乙烷和氯化氢,发生取代反应;
C.甲烷在空气中燃烧,生成二氧化碳和水,发生氧化反应;
D.乙烯使酸性高锰酸钾溶液褪色,发生氧化反应;
则属于取代反应的是B,属于加成反应的是A,属于氧化反应的是CD。答案为:B;A;CD
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
