广东省东莞市两校2023-2024学年高二上学期10月月考化学试题(含答案)
文档属性
| 名称 | 广东省东莞市两校2023-2024学年高二上学期10月月考化学试题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 455.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-19 19:43:30 | ||
图片预览


文档简介
东莞市两校2023-2024学年高二上学期10月月考
化学试题
一、单选题(16小题,共44分,前1-10每题2分,11-16每题4分)
1.下列诗句中包含吸热反应的是
A. 开窗尽见千山雪,雪未消时月正明 B. 千锤万凿出深山,烈火焚烧若等闲
C. 日照香炉生紫烟,遥看瀑布挂前川 D. 爆竹声中一岁除,春风送暖入屠苏
2.根据以下三个热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l) ΔH=-Q1 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(l) ΔH=-Q2 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(g) ΔH=-Q3 kJ·mol-1
判断Q1、Q2、Q3三者关系正确的是( )
A.Q1>Q2>Q3 B.Q1>Q3>Q2 C.Q3>Q2>Q1 D.Q2>Q1>Q3
3. 下列变化不能用勒夏特列原理释解的是
A. 工业生产硫酸的过程中使用过量的空气以提高二氧化硫的转化率
B. 反应达到平衡后,加压使混合气体颜色变深
C. 实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出
D. 实验室用饱和食盐水除去氯气中混有的少量氯化氢
4.当把晶体N2O4放入密闭容器中气化,并建立了N2O4(g) 2NO2(g)平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其 值 ( )
A. 不变 B. 变大 C.变小 D.无法确定
5.已知乙醇、石墨和氢气的燃烧热分别为、、均为正值,单位均为则反应石墨,的焓变为( )
A. B.
C. D.
6.下列有关化学反应速率的说法正确的是( )
A. 用铁片和稀硫酸反应制取氢气时,改用的浓硫酸可以加快产生氢气的速率
B. 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C. 恒温恒压的密闭容器中反应:,充入惰性气体,反应速率不变
D. 升高反应温度可增大活化分子百分数,使反应速率增大
7. 在密闭容器中发生如下反应:达到平衡后,保持温度不变,将容器体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.6倍.下列说法中正确的是
A. B. A的转化率降低 C. 平衡向正反应方向移动 D. C的体积分数增加
8.对于可逆反应,在不同条件下的化学反应速率如下,其中反应速率最快的是
A. B.
C. D.
9.反应经历两步:;。反应体系中、、的浓度随时间的变化曲线如图所示。下列说法不正确的是( )
A. 为随的变化曲线 B. 时,
C. 时,的消耗速率大于生成速率 D. 后,
10.在的密闭容器中,放入镍粉并充入一定量的气体,一定条件下发生反应:,已知该反应的平衡常数与温度的关系如下表所示:
温度
平衡常数
下列说法不正确的是( )
A. 上述生成的反应为放热反应
B. 时反应的平衡常数为
C. 在时,测得某时刻,、的浓度均为,则此时正逆
D. 达到平衡时,测得,则的平衡浓度为
11.反应N2O4(g)2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是( )
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.A、C两点气体的平均相对分子质量:A>C
D.由状态B到状态A,可以用加热的方法
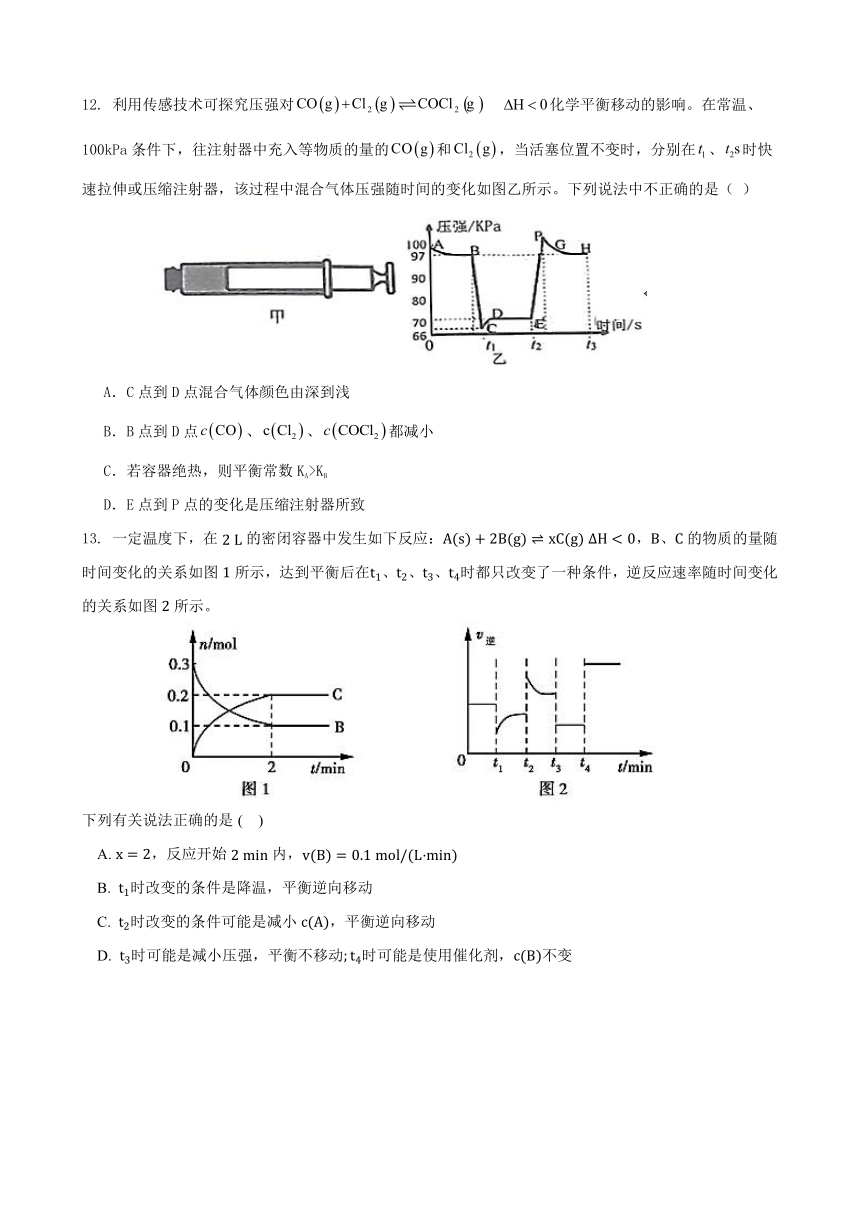
12. 利用传感技术可探究压强对 化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入等物质的量的和,当活塞位置不变时,分别在、时快速拉伸或压缩注射器,该过程中混合气体压强随时间的变化如图乙所示。下列说法中不正确的是( )
A.C点到D点混合气体颜色由深到浅
B.B点到D点、、都减小
C.若容器绝热,则平衡常数KA>KB
D.E点到P点的变化是压缩注射器所致
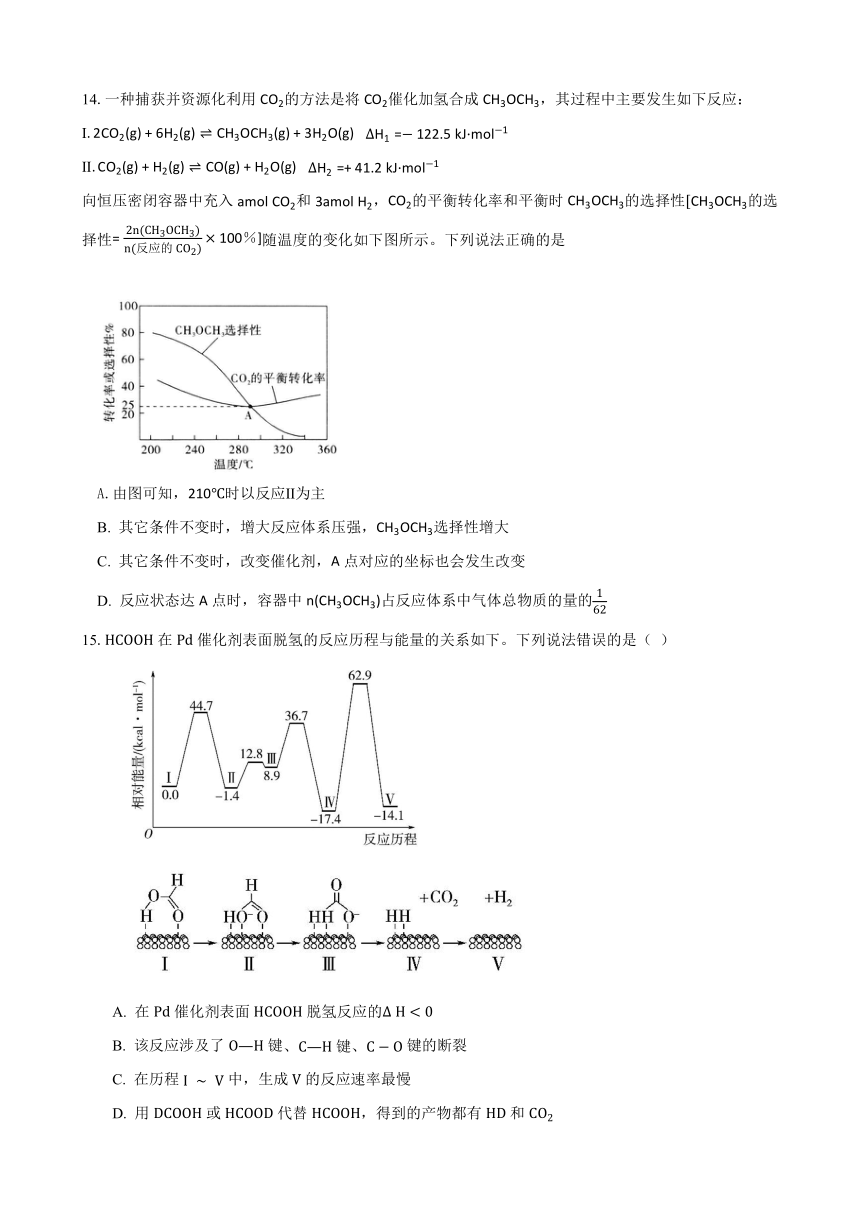
13. 一定温度下,在的密闭容器中发生如下反应: ,、的物质的量随时间变化的关系如图所示,达到平衡后在、、、时都只改变了一种条件,逆反应速率随时间变化的关系如图所示。
下列有关说法正确的是( )
A. ,反应开始内,
B. 时改变的条件是降温,平衡逆向移动
C. 时改变的条件可能是减小,平衡逆向移动
D. 时可能是减小压强,平衡不移动时可能是使用催化剂,不变
14.一种捕获并资源化利用的方法是将催化加氢合成,其过程中主要发生如下反应:
Ⅰ
Ⅱ
向恒压密闭容器中充入和,的平衡转化率和平衡时的选择性的选择性随温度的变化如下图所示。下列说法正确的是
A.由图可知,时以反应Ⅱ为主
B. 其它条件不变时,增大反应体系压强,选择性增大
C. 其它条件不变时,改变催化剂,点对应的坐标也会发生改变
D. 反应状态达点时,容器中占反应体系中气体总物质的量的
15.在催化剂表面脱氢的反应历程与能量的关系如下。下列说法错误的是( )
A. 在催化剂表面脱氢反应的
B. 该反应涉及了键键的断裂
C. 在历程中,生成的反应速率最慢
D. 用或代替,得到的产物都有和
16.已知的速率方程为,在下测定了不同初始浓度及正反应速率的关系,数据如下表,则下列说法中正确的是( )
实验
A. 降低温度,可能增大 B. 表中的为
C. 、的值分别为、 D. 若,则
二、解答题(共56分)
17.(14分)利用如图所示装置测定中和热的实验步骤如下:
用量筒量取盐酸倒入小烧杯中,测出盐酸温度;
用另一量筒量取溶液,并用同一温度计测出其温度;
将溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度.回答下列问题:
所用溶液要稍过量的原因是: 。
倒入溶液的正确操作是______。填字母,下同
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
使盐酸与溶液混合均匀的正确操作是______。填字母
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和的稀盐酸恰好完全反应,其反应热分别为、、,则、、的大小关系为 。
盐酸和氢氧化钠溶液的密度都是,又知中和反应后生成溶液的比热容为了计算中和热,某学生实验记录数据如下:
实验 序号 起始温度 终止温度
盐酸 氢氧化钠溶液 混合溶液
依据该学生的实验数据计算,该实验测得的中和热______。结果保留一位小数
______填“能”或“不能”用溶液和硫酸代替氢氧化钠溶液和盐酸,理由是
。
18.(14分)某化学兴趣小组依据反应,探究影响化学反应速率的因素并测定其化学反应速率。请回答下列问题:
Ⅰ该小组同学设计了组实验,探究影响化学反应速率的部分因素,具体情况如下表所示。
实验编号 加入溶液的体积 加入溶液的体积 加入水的体积 反应温度
表中_________,通过实验和实验可探究_________对化学反应速率的影响。
Ⅱ该小组同学依据实验的条件进行反应并测定其化学反应速率,所得数据如右图所示。
该反应在的化学反应速率为_________。
分析实验数据发现,反应过程中该反应的化学反应速率先增大后减小。
探究化学反应速率先增大的原因,具体情况如下表所示。
方案 假设 实验操作
该反应放热,使溶液温度升高,化学反应速率加快 向烧杯中加入溶液和溶液,
____________________________________ 取溶液加入烧杯中,向其中加入少量固体,再加入溶液。
补全方案中的实验操作 。
方案中的假设为 。
除方案、中的假设外,还可提出的假设是_ 。
反应后期化学反应速率减小的原因是 。
19.(18分)我国承诺2030年实现碳达峰,2060年实现碳中和,二氧化碳综合利用技术愈显重要。
Ⅰ.利用二氧化碳合成尿素
合成尿素的反应为 。向恒容密闭容器中按物质的量之比充入和,使反应进行,保持温度不变,测得的转化率随时间的变化情况如图所示。
若用的浓度变化表示反应速率,则点的逆反应速率__________点的正反应速率填“”“”或“”。
下列叙述中不能说明该反应达到平衡状态的是______________填选项字母。
A.体系压强不再变化 B.气体平均摩尔质量不再变化
C.的消耗速率和的消耗速率之比为
D.固体质量不再发生变化
工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有____________填选项字母。
A.升高温度 加入催化剂 C.将尿素及时分离出去 增大反应体系的压强
Ⅱ.二氧化碳催化加氢合成乙烯是综合利用的热点研究领域。回答下列问题:
催化加氢生成乙烯和水的反应中,产物的物质的量之比:____________。当反应达到平衡时,若增大压强,则______填“变大”“变小”或“不变”。
理论计算表明,原料初始组成::,在体系压强为,反应达到平衡时,四种组分的物质的量分数随温度的变化如下图所示。
图中,表示、变化的曲线分别是____________、____________。催化加氢合成反应的__________填“大于”或“小于”。
根据图中点,计算该温度时反应的平衡常数_______________列出计算式。以分压表示,分压总压物质的量分数。
20.(10分)年北京冬奥会首次使用氢能代替丙烷,体现了“绿色环保”办奥理念。丙烷脱氢制丙烯具有显著的经济价值和社会意义,丙烷无氧脱氢还可能生成甲烷、丙炔等副产物。回答下列问题:
已知:Ⅰ ;
Ⅱ 。
在一定催化剂下,丙烷无氧脱氢制丙烯的热化学方程式如下:
________。
时,将充入某恒容刚性密闭容器中,在催化剂作用下发生反应:。用压强传感器测出容器内体系压强随时间的变化关系如图所示:
内,用的分压变化表示上述脱氢反应的平均反应速率为________。
保持相同反应时间,在不同温度下,丙烯产率如图所示,丙烯产率在之前随温度升高而增大的原因可能是 或 。
之后,丙烯产率快速降低的主要原因可能是 任写一点。
东莞市两校2023-2024学年高二上学期10月月考
化学答案
一、选择题(44分)
1 2 3 4 5 6 7 8
B A B A B D B C
9 10 11 12 13 14 15 16
D C D A D B B C
二、解答题(56分)
17.(每空2分,共14分)
确保盐酸被完全中和 不能
与反应生成沉淀,沉淀的生成热会影响反应的反应热
(每空2分,共14分)
I. ;温度 .
.插入温度计 反应生成的使反应速率加快
反应生成的或使反应速率加快
. 反应物浓度降低使反应速率减小
(每空2分,共18分)
Ⅰ
Ⅱ: 变大
小于
(每空2分,共10分)
温度升高,反应速率加快 ;升高温度有利于反应向吸热方向进行 ;
催化剂失活,反应速率迅速减小或发生副反应,丙烷分解成其他产物
化学试题
一、单选题(16小题,共44分,前1-10每题2分,11-16每题4分)
1.下列诗句中包含吸热反应的是
A. 开窗尽见千山雪,雪未消时月正明 B. 千锤万凿出深山,烈火焚烧若等闲
C. 日照香炉生紫烟,遥看瀑布挂前川 D. 爆竹声中一岁除,春风送暖入屠苏
2.根据以下三个热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l) ΔH=-Q1 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(l) ΔH=-Q2 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(g) ΔH=-Q3 kJ·mol-1
判断Q1、Q2、Q3三者关系正确的是( )
A.Q1>Q2>Q3 B.Q1>Q3>Q2 C.Q3>Q2>Q1 D.Q2>Q1>Q3
3. 下列变化不能用勒夏特列原理释解的是
A. 工业生产硫酸的过程中使用过量的空气以提高二氧化硫的转化率
B. 反应达到平衡后,加压使混合气体颜色变深
C. 实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出
D. 实验室用饱和食盐水除去氯气中混有的少量氯化氢
4.当把晶体N2O4放入密闭容器中气化,并建立了N2O4(g) 2NO2(g)平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其 值 ( )
A. 不变 B. 变大 C.变小 D.无法确定
5.已知乙醇、石墨和氢气的燃烧热分别为、、均为正值,单位均为则反应石墨,的焓变为( )
A. B.
C. D.
6.下列有关化学反应速率的说法正确的是( )
A. 用铁片和稀硫酸反应制取氢气时,改用的浓硫酸可以加快产生氢气的速率
B. 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C. 恒温恒压的密闭容器中反应:,充入惰性气体,反应速率不变
D. 升高反应温度可增大活化分子百分数,使反应速率增大
7. 在密闭容器中发生如下反应:达到平衡后,保持温度不变,将容器体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.6倍.下列说法中正确的是
A. B. A的转化率降低 C. 平衡向正反应方向移动 D. C的体积分数增加
8.对于可逆反应,在不同条件下的化学反应速率如下,其中反应速率最快的是
A. B.
C. D.
9.反应经历两步:;。反应体系中、、的浓度随时间的变化曲线如图所示。下列说法不正确的是( )
A. 为随的变化曲线 B. 时,
C. 时,的消耗速率大于生成速率 D. 后,
10.在的密闭容器中,放入镍粉并充入一定量的气体,一定条件下发生反应:,已知该反应的平衡常数与温度的关系如下表所示:
温度
平衡常数
下列说法不正确的是( )
A. 上述生成的反应为放热反应
B. 时反应的平衡常数为
C. 在时,测得某时刻,、的浓度均为,则此时正逆
D. 达到平衡时,测得,则的平衡浓度为
11.反应N2O4(g)2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是( )
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.A、C两点气体的平均相对分子质量:A>C
D.由状态B到状态A,可以用加热的方法
12. 利用传感技术可探究压强对 化学平衡移动的影响。在常温、100kPa条件下,往注射器中充入等物质的量的和,当活塞位置不变时,分别在、时快速拉伸或压缩注射器,该过程中混合气体压强随时间的变化如图乙所示。下列说法中不正确的是( )
A.C点到D点混合气体颜色由深到浅
B.B点到D点、、都减小
C.若容器绝热,则平衡常数KA>KB
D.E点到P点的变化是压缩注射器所致
13. 一定温度下,在的密闭容器中发生如下反应: ,、的物质的量随时间变化的关系如图所示,达到平衡后在、、、时都只改变了一种条件,逆反应速率随时间变化的关系如图所示。
下列有关说法正确的是( )
A. ,反应开始内,
B. 时改变的条件是降温,平衡逆向移动
C. 时改变的条件可能是减小,平衡逆向移动
D. 时可能是减小压强,平衡不移动时可能是使用催化剂,不变
14.一种捕获并资源化利用的方法是将催化加氢合成,其过程中主要发生如下反应:
Ⅰ
Ⅱ
向恒压密闭容器中充入和,的平衡转化率和平衡时的选择性的选择性随温度的变化如下图所示。下列说法正确的是
A.由图可知,时以反应Ⅱ为主
B. 其它条件不变时,增大反应体系压强,选择性增大
C. 其它条件不变时,改变催化剂,点对应的坐标也会发生改变
D. 反应状态达点时,容器中占反应体系中气体总物质的量的
15.在催化剂表面脱氢的反应历程与能量的关系如下。下列说法错误的是( )
A. 在催化剂表面脱氢反应的
B. 该反应涉及了键键的断裂
C. 在历程中,生成的反应速率最慢
D. 用或代替,得到的产物都有和
16.已知的速率方程为,在下测定了不同初始浓度及正反应速率的关系,数据如下表,则下列说法中正确的是( )
实验
A. 降低温度,可能增大 B. 表中的为
C. 、的值分别为、 D. 若,则
二、解答题(共56分)
17.(14分)利用如图所示装置测定中和热的实验步骤如下:
用量筒量取盐酸倒入小烧杯中,测出盐酸温度;
用另一量筒量取溶液,并用同一温度计测出其温度;
将溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度.回答下列问题:
所用溶液要稍过量的原因是: 。
倒入溶液的正确操作是______。填字母,下同
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
使盐酸与溶液混合均匀的正确操作是______。填字母
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和的稀盐酸恰好完全反应,其反应热分别为、、,则、、的大小关系为 。
盐酸和氢氧化钠溶液的密度都是,又知中和反应后生成溶液的比热容为了计算中和热,某学生实验记录数据如下:
实验 序号 起始温度 终止温度
盐酸 氢氧化钠溶液 混合溶液
依据该学生的实验数据计算,该实验测得的中和热______。结果保留一位小数
______填“能”或“不能”用溶液和硫酸代替氢氧化钠溶液和盐酸,理由是
。
18.(14分)某化学兴趣小组依据反应,探究影响化学反应速率的因素并测定其化学反应速率。请回答下列问题:
Ⅰ该小组同学设计了组实验,探究影响化学反应速率的部分因素,具体情况如下表所示。
实验编号 加入溶液的体积 加入溶液的体积 加入水的体积 反应温度
表中_________,通过实验和实验可探究_________对化学反应速率的影响。
Ⅱ该小组同学依据实验的条件进行反应并测定其化学反应速率,所得数据如右图所示。
该反应在的化学反应速率为_________。
分析实验数据发现,反应过程中该反应的化学反应速率先增大后减小。
探究化学反应速率先增大的原因,具体情况如下表所示。
方案 假设 实验操作
该反应放热,使溶液温度升高,化学反应速率加快 向烧杯中加入溶液和溶液,
____________________________________ 取溶液加入烧杯中,向其中加入少量固体,再加入溶液。
补全方案中的实验操作 。
方案中的假设为 。
除方案、中的假设外,还可提出的假设是_ 。
反应后期化学反应速率减小的原因是 。
19.(18分)我国承诺2030年实现碳达峰,2060年实现碳中和,二氧化碳综合利用技术愈显重要。
Ⅰ.利用二氧化碳合成尿素
合成尿素的反应为 。向恒容密闭容器中按物质的量之比充入和,使反应进行,保持温度不变,测得的转化率随时间的变化情况如图所示。
若用的浓度变化表示反应速率,则点的逆反应速率__________点的正反应速率填“”“”或“”。
下列叙述中不能说明该反应达到平衡状态的是______________填选项字母。
A.体系压强不再变化 B.气体平均摩尔质量不再变化
C.的消耗速率和的消耗速率之比为
D.固体质量不再发生变化
工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有____________填选项字母。
A.升高温度 加入催化剂 C.将尿素及时分离出去 增大反应体系的压强
Ⅱ.二氧化碳催化加氢合成乙烯是综合利用的热点研究领域。回答下列问题:
催化加氢生成乙烯和水的反应中,产物的物质的量之比:____________。当反应达到平衡时,若增大压强,则______填“变大”“变小”或“不变”。
理论计算表明,原料初始组成::,在体系压强为,反应达到平衡时,四种组分的物质的量分数随温度的变化如下图所示。
图中,表示、变化的曲线分别是____________、____________。催化加氢合成反应的__________填“大于”或“小于”。
根据图中点,计算该温度时反应的平衡常数_______________列出计算式。以分压表示,分压总压物质的量分数。
20.(10分)年北京冬奥会首次使用氢能代替丙烷,体现了“绿色环保”办奥理念。丙烷脱氢制丙烯具有显著的经济价值和社会意义,丙烷无氧脱氢还可能生成甲烷、丙炔等副产物。回答下列问题:
已知:Ⅰ ;
Ⅱ 。
在一定催化剂下,丙烷无氧脱氢制丙烯的热化学方程式如下:
________。
时,将充入某恒容刚性密闭容器中,在催化剂作用下发生反应:。用压强传感器测出容器内体系压强随时间的变化关系如图所示:
内,用的分压变化表示上述脱氢反应的平均反应速率为________。
保持相同反应时间,在不同温度下,丙烯产率如图所示,丙烯产率在之前随温度升高而增大的原因可能是 或 。
之后,丙烯产率快速降低的主要原因可能是 任写一点。
东莞市两校2023-2024学年高二上学期10月月考
化学答案
一、选择题(44分)
1 2 3 4 5 6 7 8
B A B A B D B C
9 10 11 12 13 14 15 16
D C D A D B B C
二、解答题(56分)
17.(每空2分,共14分)
确保盐酸被完全中和 不能
与反应生成沉淀,沉淀的生成热会影响反应的反应热
(每空2分,共14分)
I. ;温度 .
.插入温度计 反应生成的使反应速率加快
反应生成的或使反应速率加快
. 反应物浓度降低使反应速率减小
(每空2分,共18分)
Ⅰ
Ⅱ: 变大
小于
(每空2分,共10分)
温度升高,反应速率加快 ;升高温度有利于反应向吸热方向进行 ;
催化剂失活,反应速率迅速减小或发生副反应,丙烷分解成其他产物
同课章节目录
