第1章原子结构与元素性质微项目及单元复习(共16张PPT)-2023-2024学年高二化学鲁科版选择性必修第二册课件
文档属性
| 名称 | 第1章原子结构与元素性质微项目及单元复习(共16张PPT)-2023-2024学年高二化学鲁科版选择性必修第二册课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-19 00:00:00 | ||
图片预览


文档简介
(共16张PPT)
第一章 原子结构与元素性质
微项目 甲醛的危害及去除
第三单元 复习
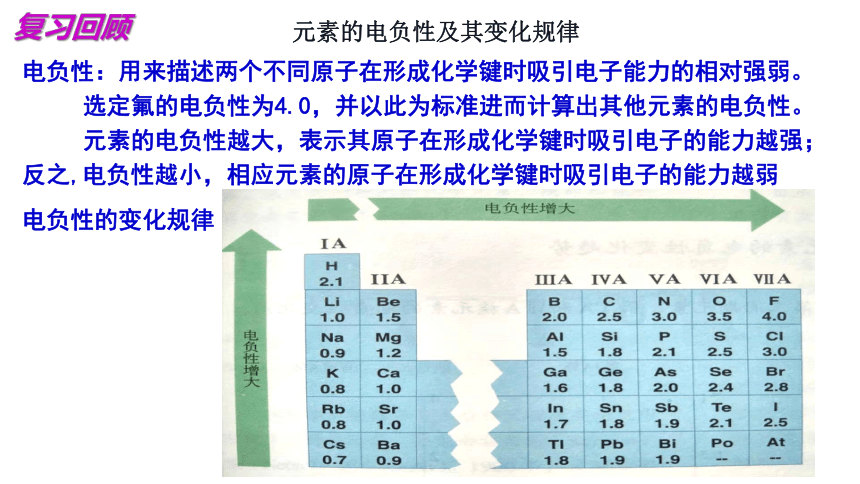
元素的电负性及其变化规律
电负性:用来描述两个不同原子在形成化学键时吸引电子能力的相对强弱。
选定氟的电负性为4.0,并以此为标准进而计算出其他元素的电负性。
元素的电负性越大,表示其原子在形成化学键时吸引电子的能力越强;反之,电负性越小,相应元素的原子在形成化学键时吸引电子的能力越弱
复习回顾
电负性的变化规律
(2)判断元素的化合价的正负。
①电负性数值小的元素在化合物中吸引电子的能力弱,元素的化合价为正值。
②电负性数值大的元素在化合物中吸收电子的能力强,元素的化合价为负值。
3.电负性的应用
(1)判断元素的金属性和非金属性及其强弱。
(3)判断化学键的类型。
一般地,如果两种成键元素的电负性差值较大(>1.7)时易形成离子键;如果两种成键元素的电负性差值较小(<1.7)时易形成共价键。
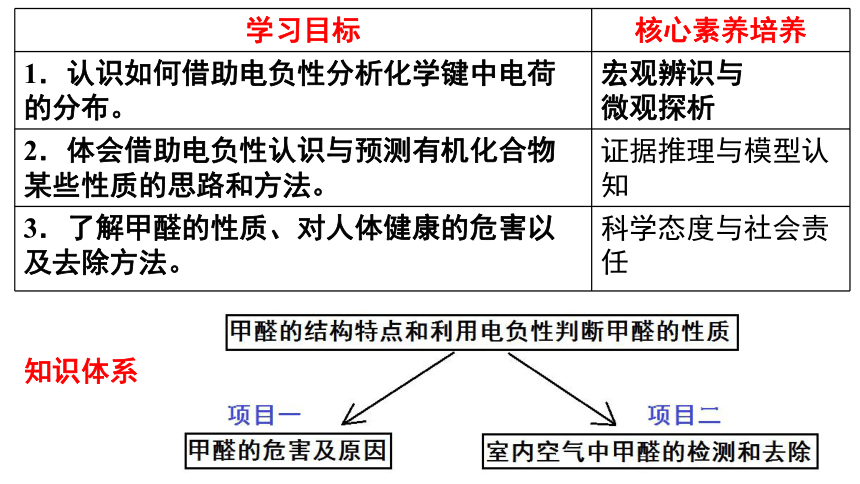
学习目标 核心素养培养
1.认识如何借助电负性分析化学键中电荷的分布。 宏观辨识与
微观探析
2.体会借助电负性认识与预测有机化合物某些性质的思路和方法。 证据推理与模型认知
3.了解甲醛的性质、对人体健康的危害以及去除方法。 科学态度与社会责任
知识体系
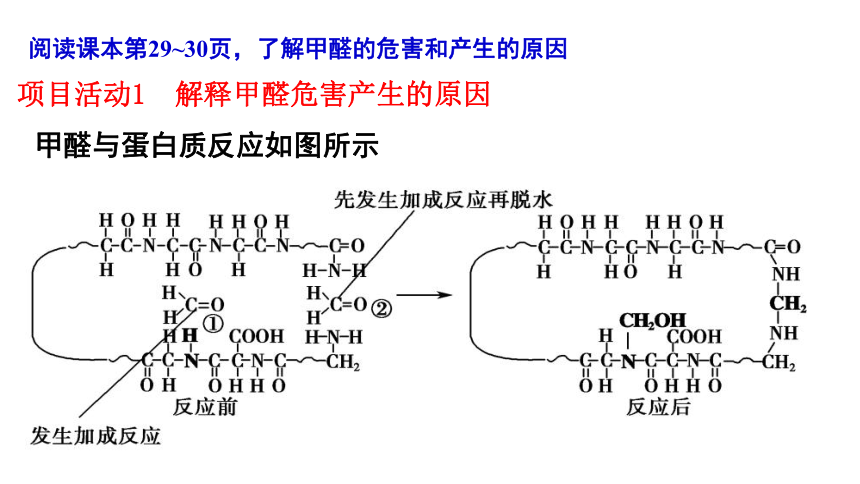
阅读课本第29~30页,了解甲醛的危害和产生的原因
甲醛与蛋白质反应如图所示
项目活动1 解释甲醛危害产生的原因
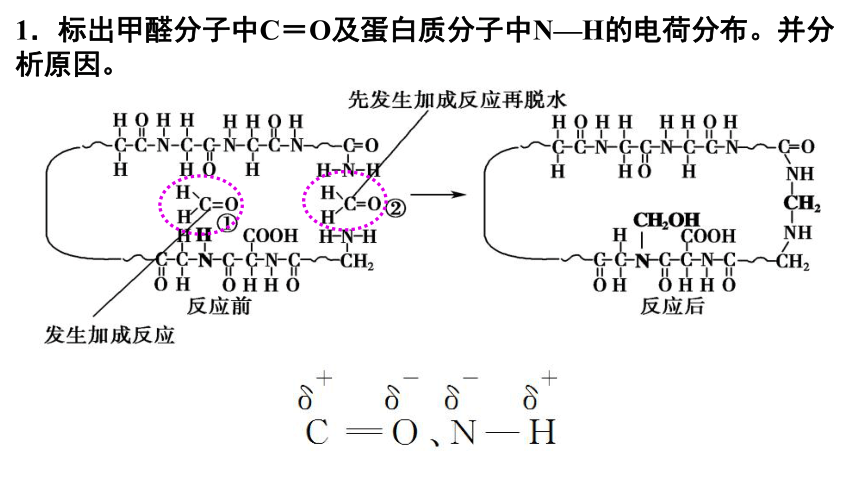
1.标出甲醛分子中C=O及蛋白质分子中N—H的电荷分布。并分析原因。
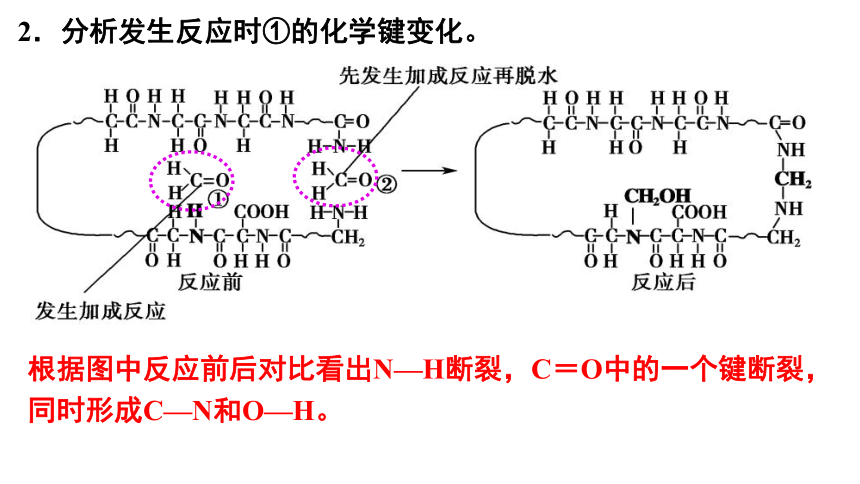
2.分析发生反应时①的化学键变化。
根据图中反应前后对比看出N—H断裂,C=O中的一个键断裂,同时形成C—N和O—H。
3.②处 先与一个—NH2发生加成反应,其产物又与另一个—NH2发生取代反应脱去一个H2O分子。试分析发生反应时②处的化学键变化。
发生加成反应时,断裂N—H和C=O中的一条键,形成C—N和O—H;加成产物继续反应时断裂C—O和N—H,同时形成C—N和H—O(生成了H2O)。
4.通过上述加成反应和取代反应分析,断键后的分子片断是如何重组的?
带部分正电荷的原子或基团,与带部分负电荷的原子或基团相连、重组。遵循“正找负”“负找正”的规律。如
探究总结
阅读课本第30~32页,了解甲醛的检测和去除的方法
项目活动2 室内空气中甲醛的检测与去除
检测室内空气中的甲醛含量时常用的检测试剂是3 甲基 2苯并噻唑啉酮腙盐酸盐水合物(MBTH)。该方法的原理是甲醛与MBTH反应生成物质A,A再参与一系列反应,最终生成蓝绿色化合物。
1、室内空气中甲醛的检测方法
2、室内空气中甲醛的去除方法
①氨、胺类、酚类物质均可与甲醛发生加成反应,继而发生消去反应,生成水和一种稳定的有机物,从而除去甲醛。
④某些植物可吸收甲醛如吊兰、芦荟、虎尾兰等。
②利用氧化剂将甲醛氧化除去如KMnO4、K2Cr2O7等。
③利用多孔材料通过物理吸附的方法除甲醛,如活性炭等。
本章知识网络
课本练习第34~35页
THANKS
第一章 原子结构与元素性质
微项目 甲醛的危害及去除
第三单元 复习
元素的电负性及其变化规律
电负性:用来描述两个不同原子在形成化学键时吸引电子能力的相对强弱。
选定氟的电负性为4.0,并以此为标准进而计算出其他元素的电负性。
元素的电负性越大,表示其原子在形成化学键时吸引电子的能力越强;反之,电负性越小,相应元素的原子在形成化学键时吸引电子的能力越弱
复习回顾
电负性的变化规律
(2)判断元素的化合价的正负。
①电负性数值小的元素在化合物中吸引电子的能力弱,元素的化合价为正值。
②电负性数值大的元素在化合物中吸收电子的能力强,元素的化合价为负值。
3.电负性的应用
(1)判断元素的金属性和非金属性及其强弱。
(3)判断化学键的类型。
一般地,如果两种成键元素的电负性差值较大(>1.7)时易形成离子键;如果两种成键元素的电负性差值较小(<1.7)时易形成共价键。
学习目标 核心素养培养
1.认识如何借助电负性分析化学键中电荷的分布。 宏观辨识与
微观探析
2.体会借助电负性认识与预测有机化合物某些性质的思路和方法。 证据推理与模型认知
3.了解甲醛的性质、对人体健康的危害以及去除方法。 科学态度与社会责任
知识体系
阅读课本第29~30页,了解甲醛的危害和产生的原因
甲醛与蛋白质反应如图所示
项目活动1 解释甲醛危害产生的原因
1.标出甲醛分子中C=O及蛋白质分子中N—H的电荷分布。并分析原因。
2.分析发生反应时①的化学键变化。
根据图中反应前后对比看出N—H断裂,C=O中的一个键断裂,同时形成C—N和O—H。
3.②处 先与一个—NH2发生加成反应,其产物又与另一个—NH2发生取代反应脱去一个H2O分子。试分析发生反应时②处的化学键变化。
发生加成反应时,断裂N—H和C=O中的一条键,形成C—N和O—H;加成产物继续反应时断裂C—O和N—H,同时形成C—N和H—O(生成了H2O)。
4.通过上述加成反应和取代反应分析,断键后的分子片断是如何重组的?
带部分正电荷的原子或基团,与带部分负电荷的原子或基团相连、重组。遵循“正找负”“负找正”的规律。如
探究总结
阅读课本第30~32页,了解甲醛的检测和去除的方法
项目活动2 室内空气中甲醛的检测与去除
检测室内空气中的甲醛含量时常用的检测试剂是3 甲基 2苯并噻唑啉酮腙盐酸盐水合物(MBTH)。该方法的原理是甲醛与MBTH反应生成物质A,A再参与一系列反应,最终生成蓝绿色化合物。
1、室内空气中甲醛的检测方法
2、室内空气中甲醛的去除方法
①氨、胺类、酚类物质均可与甲醛发生加成反应,继而发生消去反应,生成水和一种稳定的有机物,从而除去甲醛。
④某些植物可吸收甲醛如吊兰、芦荟、虎尾兰等。
②利用氧化剂将甲醛氧化除去如KMnO4、K2Cr2O7等。
③利用多孔材料通过物理吸附的方法除甲醛,如活性炭等。
本章知识网络
课本练习第34~35页
THANKS
