2.4元素课件---2023--2024学年九年级化学鲁教版上册
文档属性
| 名称 | 2.4元素课件---2023--2024学年九年级化学鲁教版上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 10.6MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-20 00:00:00 | ||
图片预览







文档简介
(共58张PPT)
2.4 元素
第二单元
复习旧知
PART
01
01
04
03
02
哪些物质是由分子构成的?
复习链接
哪些物质是由原子构成的?
哪些物质是由离子构成的?
它们之间有什么区别和联系?
02
01
03
问题答疑
H2O、H2、CO2……
C、Fe、S、Na……
由离子构成:
NaCl……
由分子构成:
由原子构成:
ADD RELATED TITLE WORDS
1.知道元素的含义,了解元素的分布;
2.知道物质与元素、分子、原子、离子的关系,将对物质的宏观组成与微观结构的认识统一起来。
学习目标
新知导入
一些广告常宣传“含人体必需的营养元素”,这里的“元素”是指什么呢?
知识点 元素
知识点 1
元素的概念
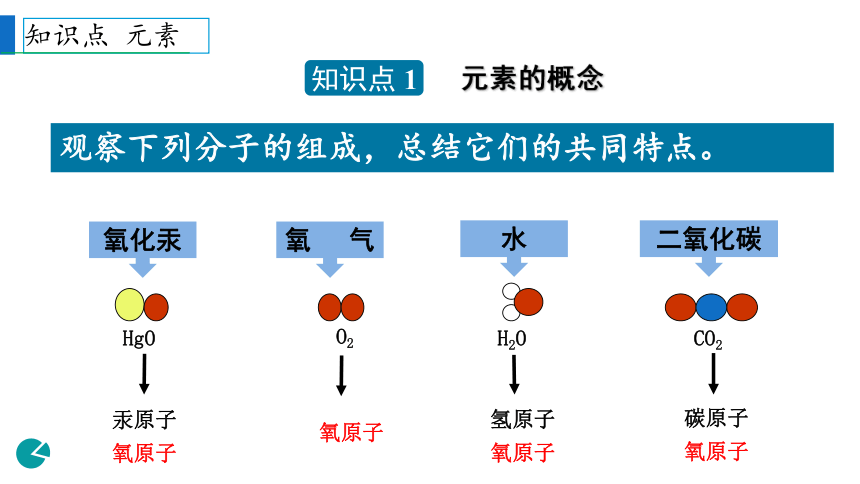
观察下列分子的组成,总结它们的共同特点。
HgO
汞原子
氧原子
H2O
氢原子
氧原子
CO2
碳原子
氧原子
O2
氧原子
氧化汞
氧气
水
二氧化碳
知识点 元素
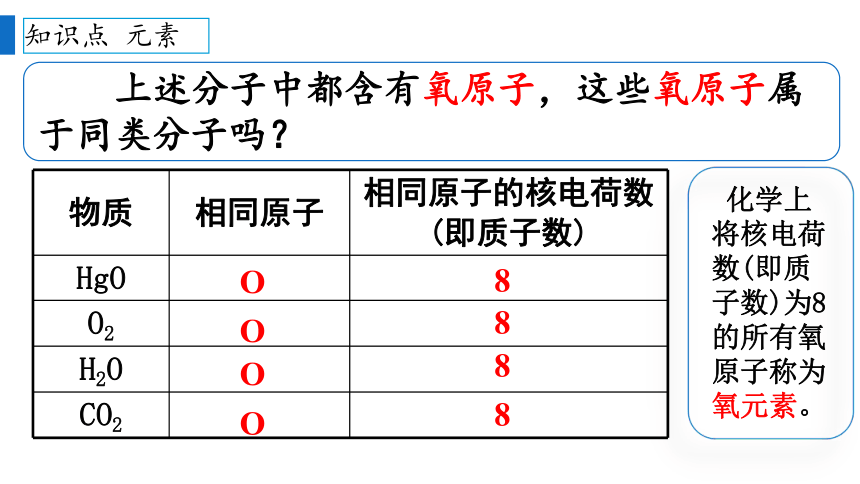
物质 相同原子 相同原子的核电荷数
(即质子数)
HgO
O2
H2O
CO2
8
O
上述分子中都含有氧原子,这些氧原子属于同类分子吗?
O
O
O
8
8
8
化学上将核电荷数(即质子数)为8的所有氧原子称为氧元素。
知识点 元素
钠原子(Na)
钠离子(Na+)
氯化钠(NaCl)
含有钠元素
知识点 元素
元素的定义
把质子数(即核电荷数)为8的氧原子统称为氧元素。
把质子数(即核电荷数)为1的氢原子统称为氢元素。
把质子数(即核电荷数)为6的碳原子统称为碳元素。
元素是质子数(即核电荷数)相同的一类原子的总称。
知识点 元素
2.4 元素
一、定义
质子数(即核电荷数)相同的一类原子的总称。
注:1.元素之间的本质区别是质子数(或核电荷数)不同。
2. “一类原子”指的是质子数相同而中子数并不一定相同的一类原子。
知识点 元素
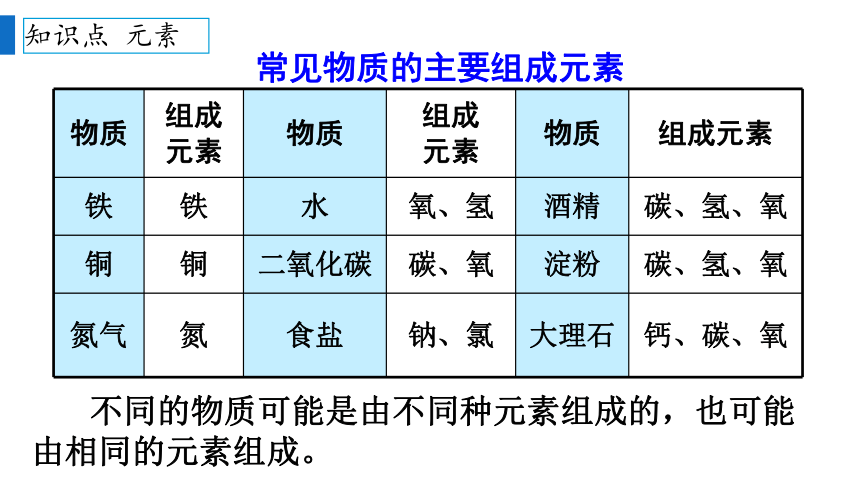
常见物质的主要组成元素
物质 组成 元素 物质 组成 元素 物质 组成元素
铁 铁 水 氧、氢 酒精 碳、氢、氧
铜 铜 二氧化碳 碳、氧 淀粉 碳、氢、氧
氮气 氮 食盐 钠、氯 大理石 钙、碳、氧
不同的物质可能是由不同种元素组成的,也可能由相同的元素组成。
知识点 元素
2.4 元素
二、分类
元素
金属元素:“钅”字旁(汞除外),如铁、铝等
非金属元素
固态非金属:“ 石”,如碘等
液态非金属:“ ”,如溴等
气态非金属:“气 ”,如氧等
知识点 元素
生物细胞(质量分数)
海水中
(质量分数)
地壳中
(质量分数)
空气中
(体积分数)
元素含量排行榜
氧>硅>铝>铁
氧>碳>氢>氮
氧>氢>氯>钠
氮>氧
知识点 元素
2.4 元素
三、含量
※地壳中(质量分数):氧、硅、铝、铁、钙(O、Si、Al、Fe、Ca)。
※人体中(质量分数):氧、碳、氢、氮、钙(O、C、H、N、Ca)。
海水中(质量分数):氧、氢、氯、钠、镁(O、H、Cl、Na、Mg)。
空气中(体积分数):氮、氧(N、O)。
知识点 元素
国际规定:用元素拉丁文名称的第一个字母大写来表示该元素。
元素符号的来历
如果几种元素拉丁文名称的第一个字母相同,就附加一个小写字母来区别。
知识点 元素
2.4 元素
四、元素符号
1.书写
元素符号的写法
① 由一个字母表示的元素符号要大写,
如:O、N
② 由两个字母表示的元素符号,
(只有第一个字母大写,第二个字母小写,“一大二小”)
如:Na、Cl
知识点 元素
钙 锰 氯 氢 铁 硅
CA mn cL h Fe SI
改正:Ca Mn Cl H Si
找一找,下列元素符号的书写有错误的吗,错在哪里?
知识点 元素
常见元素符号的书写
氢 氦 碳 氮 氧 氟 氖
钠 镁 铝 硅 磷 硫 氯
H He C N O F Ne
Na Mg Al Si P S Cl
知识点 元素
氩 钾 钙 锰 铁 铜 锌
银 钡 铂 金 汞 碘
Ar K Ca Mn Fe Cu Zn
Ag Ba Pt Au Hg I
知识点 元素
2.4 元素
意义
宏观
微观:
③表示这种元素的一个原子,如 Fe表示__________
①表示一种元素,如 Fe表示_________
②表示一种物质(仅限于由原子直接构成的物质)如 Fe表示____________
【注】当元素符号前面有数字时,只表示微观意义,如2Mg只能表示2个镁原子。
铁元素
铁这种物质
1个铁原子
2.意义(以Fe为例)
知识点 元素
请说出下列元素符号的意义?
①氢 H
②铜 Cu
③氧 O
④碳 C
知识点 元素
部分元素符号有三种意义
②表示钠这种物质
①表示钠元素
Na
③表示一个钠原子
具有三种意义的元素符号有:
Cu、Fe、Hg等金属元素、稀有气体元素以及C、P、S、Si等固态非金属元素。
②表示碳这种物质
①表示碳元素
C
③表示一个碳原子
知识点 元素
典例1 “中国芯”的主要材料是高纯度的单质硅,其结构类似于金刚石。下列有关硅的说法正确的是( )
D
A.属于金属元素
B.元素符号为SI
C.硅元素是地壳中含量最多的元素
D.单质硅由原子构成
硅是“石”字旁,属于非金属元素
Si
氧
知识点 元素
典例2 用符号表示或写出符号的意义。
(1)H:__________;______________。
(2)2H:____________。
(3)2个铜原子:________。
(4)铁元素:________。
氢元素
一个氢原子
两个氢原子
2Cu
Fe
知识点 元素
超市里的商品为什么摆放的那么整齐?
化学元素也可以分门别类整理吗?
知识点 元素
1869年2月,俄国化学家门捷列夫编制了他的第一张元素周期表。
知识点 3
元素周期表
门捷列夫与元素周期表
门捷列夫
门捷列夫第一张元素周期表
门捷列夫第二张元素周期表
知识点 元素
周期:每一横行叫一周期,共7个周期。
族:每一纵行叫一族(其中8、9、10三个纵行共同组成一个族),共16族。
元素周期表的起始:
原子序数=核电荷数=核内质子数=核外电子数
稀有气体元素
金属元素
非金属元素
知识点 元素
知识点2 元素周期表
新知探究
门捷列夫和元素周期表
知识点 元素
知识点 元素
五、元素周期表
1.发现者:门捷列夫
(1)编号:质子数递增的顺序
(2)横行(周期):共七周期,同一周期(行)电子层数相同,从左到右最外层电子数依次递增。
(3)纵行(族):共18纵行16个族,同一族(列)最外层电子数相同,从上到下电子层数依次递增。
2.结构
知识点 元素
※3.一格的信息
【注】主族元素:周期数=电子层数,族数=最外层电子数。
知识点 元素
典例4 下图是硫元素在元素周期表中的部分信息,请在框中填写出其各部分表示的意义。
16 S
硫
32.06
元素符号是S
元素名称是硫
硫的相对原子质量是32.06
硫的原子序数是16
知识点 元素
4.(2018 牡丹江)元素周期表是学习和研究化学的重要工具。如图是元素周期表的一部分,对相关信息表述正确的是( )
A.氟原子的核内中子数为9
B.氯原子的相对原子质量是35.45g
C.氟、硫、氯三种元素都属于非金属元素
D.氟元素和氯元素位于元素周期表的同一周期
C
基础巩固题
知识点 元素
能力提升题
1.(2018秋 江苏期末)元素周期表中锌元素的某些信息如图所示,下列有关锌的说法错误的是( )
A.锌原子核外有30个电子
B.锌的相对原子质量为65.38 g
C.锌是金属元素
D.锌离子核内质子数为30
B
知识点 元素
六、单质和化合物
1.定义:
单质:由一种元素组成的纯净物。
化合物:由两种或两种以上元素组成的纯净物。
注:(1)由同种元素组成的物质不一定是单质。如O2和O3(混合物)。
(2)由不同元素组成的物质不一定是化合物。如CO和CO2(混合物)。
课堂达标
1.“2O”表示的含义是( )
A
A.2个氧原子 B.1个氧分子
C.氧元素 D.氧气
O2
O
O2
知识点 元素
2.下列符号中,既有宏观意义,又有微观意义的是( )
A. Fe2+ B. Fe3+ C. Fe D. 2Fe
解析:Fe2+表示亚铁离子, Fe3+表示铁离子,2Fe表示2个铁原子,都只有微观意义;Fe表示铁元素、铁这种物质,同时又表示1个铁原子,既有宏观意义,又有微观意义。
C
知识点 元素
3.如图是镆元素的信息,下列有关说法错误的是( )
B
原子序数 115 汉语拼音 mò
符号 Mc 中文名称 镆
英文名称 Moscovium
A.镆属于金属元素
B.镆的原子序数115表示其核内有115个中子
C.“Mc” 表示镆这种物质、镆元素、1个镆原子
D.镆原子在化学反应中易失电子
解析:镆的原子序数是115,其原子核内质子数是115,但中子数不一定是115。
知识点 元素
4.中华文化,博大精深。利用元素名称或元素名称的谐音,仿照示例,用相应的元素符号补充成语。
示例:Fe石心肠 功高Ca世
______墙铁壁 火树 _____花 一诺千_____
十全十______ 汗流浃____ 大快人 _____
Cu
Ag
Au
Mg
Ba
Zn
知识点 元素
典例2 (2020 白银中考改编)C919大型客机部分机身采用了新型的铝锂合金。铝锂合金中铝(Al)元素与锂(Li)元素的本质区别是( )
A
A.质子数不同 B.核外电子数不同
C.中子数不同 D.最外层电子数不同
知识点 元素
知识点2 物质的组成、构成
新知探究
物质的组成可从宏观和微观两个方面进行描述,其中元素是从宏观上描述物质的组成,原子、分子是从微观上描述物质的构成。
物质的组成用元素描述,物质的构成用分子、原子或离子描述,分子的构成用原子描述。
知识点 元素
构成
得失电子
失得电子
元素
组成
氧气、氢气、水等
构成
分子
铁、汞、氦气等
硫酸铜、氯化钠等
构成
构成
原子
离子
分解
自然界中多种多样的物质
知识点 元素
物质
分子
原子
元素
组 成
构成
构成
构 成
分 解
得失电子
失得电子
宏观概念
只讲种类 不讲个数
离子
构成
微观概念
既讲种类 又讲个数
知识点 元素
典例3 二氧化碳(CO2)是植物进行光合作用的原料之一。下列关于二氧化碳的说法错误的是( )
C
A.二氧化碳由碳元素和氧元素组成
B.二氧化碳由二氧化碳分子构成
C.二氧化碳分子由碳元素和氧元素组成
D.一个二氧化碳分子由一个碳原子和两个氧原子构成
解析:元素只能用于描述物质的宏观组成。
知识点 元素
典例4 将正确答案填写在题中划线处。
1.氧气、氢气、氨等物质是由________构成的;
2.铁、汞、金刚石等物质是由________构成的;
3.氯化钠、硫酸铜等是由________构成的。
分子
原子
离子
知识点 元素
课堂达标
1.下列关于物质的组成与构成的说法正确的是( )
A.水是由氢原子和氧原子构成的
B.汞是由汞分子构成的
C.氧分子由氧元素组成
D.二氧化碳是由碳、氧两种元素组成的
D
水分子
原子
氧原子构成
知识点 元素
3.下列关于元素的叙述中正确的是( )
A.质子数相同的两种粒子属于同种元素
B.同种元素的原子结构和质量完全相同
C.元素的种类取决于该元素原子的核外电子数
D.不同种元素的根本区别是核内质子数不同
方法点拨:元素的种类是由质子数来决定的,质子数相同的原子或离子属于同种元素。
D
氢的质子数为1,中子数有0、1、2
知识点 元素
化学反应前后,分子种类发生变化,元素种类没有发生变化。
【分析讨论】
下述化学反应中:分子和元素的种类是否发生了
改变?
知识点 元素
元 素 原 子
定义
不 同 点 ①只讲 ,不讲______ ②是 观的概念 ③只能组成 ,不能构成____ ④化学变化中元素的 和____ 不变 ①既讲 ,又讲______
②是 观的概念
③可直接构成 ,也可构成_______
④化学变化中原子的 、
_____、 都不变
相互 关系 元素是 原子的总称,原子是 的个体,是 中的最小粒子 质子数(即核电荷数)相同的一类原子的总称
化学变化中的最小粒子
种类
种类
宏
微
物质
分子
物质
分子
质量
种类
质量
种类
质子数(即核电荷数)相同的一类
数目
化学变化
元素
个数
个数
元素和原子的比较
2.4 元素
第二单元
复习旧知
PART
01
01
04
03
02
哪些物质是由分子构成的?
复习链接
哪些物质是由原子构成的?
哪些物质是由离子构成的?
它们之间有什么区别和联系?
02
01
03
问题答疑
H2O、H2、CO2……
C、Fe、S、Na……
由离子构成:
NaCl……
由分子构成:
由原子构成:
ADD RELATED TITLE WORDS
1.知道元素的含义,了解元素的分布;
2.知道物质与元素、分子、原子、离子的关系,将对物质的宏观组成与微观结构的认识统一起来。
学习目标
新知导入
一些广告常宣传“含人体必需的营养元素”,这里的“元素”是指什么呢?
知识点 元素
知识点 1
元素的概念
观察下列分子的组成,总结它们的共同特点。
HgO
汞原子
氧原子
H2O
氢原子
氧原子
CO2
碳原子
氧原子
O2
氧原子
氧化汞
氧气
水
二氧化碳
知识点 元素
物质 相同原子 相同原子的核电荷数
(即质子数)
HgO
O2
H2O
CO2
8
O
上述分子中都含有氧原子,这些氧原子属于同类分子吗?
O
O
O
8
8
8
化学上将核电荷数(即质子数)为8的所有氧原子称为氧元素。
知识点 元素
钠原子(Na)
钠离子(Na+)
氯化钠(NaCl)
含有钠元素
知识点 元素
元素的定义
把质子数(即核电荷数)为8的氧原子统称为氧元素。
把质子数(即核电荷数)为1的氢原子统称为氢元素。
把质子数(即核电荷数)为6的碳原子统称为碳元素。
元素是质子数(即核电荷数)相同的一类原子的总称。
知识点 元素
2.4 元素
一、定义
质子数(即核电荷数)相同的一类原子的总称。
注:1.元素之间的本质区别是质子数(或核电荷数)不同。
2. “一类原子”指的是质子数相同而中子数并不一定相同的一类原子。
知识点 元素
常见物质的主要组成元素
物质 组成 元素 物质 组成 元素 物质 组成元素
铁 铁 水 氧、氢 酒精 碳、氢、氧
铜 铜 二氧化碳 碳、氧 淀粉 碳、氢、氧
氮气 氮 食盐 钠、氯 大理石 钙、碳、氧
不同的物质可能是由不同种元素组成的,也可能由相同的元素组成。
知识点 元素
2.4 元素
二、分类
元素
金属元素:“钅”字旁(汞除外),如铁、铝等
非金属元素
固态非金属:“ 石”,如碘等
液态非金属:“ ”,如溴等
气态非金属:“气 ”,如氧等
知识点 元素
生物细胞(质量分数)
海水中
(质量分数)
地壳中
(质量分数)
空气中
(体积分数)
元素含量排行榜
氧>硅>铝>铁
氧>碳>氢>氮
氧>氢>氯>钠
氮>氧
知识点 元素
2.4 元素
三、含量
※地壳中(质量分数):氧、硅、铝、铁、钙(O、Si、Al、Fe、Ca)。
※人体中(质量分数):氧、碳、氢、氮、钙(O、C、H、N、Ca)。
海水中(质量分数):氧、氢、氯、钠、镁(O、H、Cl、Na、Mg)。
空气中(体积分数):氮、氧(N、O)。
知识点 元素
国际规定:用元素拉丁文名称的第一个字母大写来表示该元素。
元素符号的来历
如果几种元素拉丁文名称的第一个字母相同,就附加一个小写字母来区别。
知识点 元素
2.4 元素
四、元素符号
1.书写
元素符号的写法
① 由一个字母表示的元素符号要大写,
如:O、N
② 由两个字母表示的元素符号,
(只有第一个字母大写,第二个字母小写,“一大二小”)
如:Na、Cl
知识点 元素
钙 锰 氯 氢 铁 硅
CA mn cL h Fe SI
改正:Ca Mn Cl H Si
找一找,下列元素符号的书写有错误的吗,错在哪里?
知识点 元素
常见元素符号的书写
氢 氦 碳 氮 氧 氟 氖
钠 镁 铝 硅 磷 硫 氯
H He C N O F Ne
Na Mg Al Si P S Cl
知识点 元素
氩 钾 钙 锰 铁 铜 锌
银 钡 铂 金 汞 碘
Ar K Ca Mn Fe Cu Zn
Ag Ba Pt Au Hg I
知识点 元素
2.4 元素
意义
宏观
微观:
③表示这种元素的一个原子,如 Fe表示__________
①表示一种元素,如 Fe表示_________
②表示一种物质(仅限于由原子直接构成的物质)如 Fe表示____________
【注】当元素符号前面有数字时,只表示微观意义,如2Mg只能表示2个镁原子。
铁元素
铁这种物质
1个铁原子
2.意义(以Fe为例)
知识点 元素
请说出下列元素符号的意义?
①氢 H
②铜 Cu
③氧 O
④碳 C
知识点 元素
部分元素符号有三种意义
②表示钠这种物质
①表示钠元素
Na
③表示一个钠原子
具有三种意义的元素符号有:
Cu、Fe、Hg等金属元素、稀有气体元素以及C、P、S、Si等固态非金属元素。
②表示碳这种物质
①表示碳元素
C
③表示一个碳原子
知识点 元素
典例1 “中国芯”的主要材料是高纯度的单质硅,其结构类似于金刚石。下列有关硅的说法正确的是( )
D
A.属于金属元素
B.元素符号为SI
C.硅元素是地壳中含量最多的元素
D.单质硅由原子构成
硅是“石”字旁,属于非金属元素
Si
氧
知识点 元素
典例2 用符号表示或写出符号的意义。
(1)H:__________;______________。
(2)2H:____________。
(3)2个铜原子:________。
(4)铁元素:________。
氢元素
一个氢原子
两个氢原子
2Cu
Fe
知识点 元素
超市里的商品为什么摆放的那么整齐?
化学元素也可以分门别类整理吗?
知识点 元素
1869年2月,俄国化学家门捷列夫编制了他的第一张元素周期表。
知识点 3
元素周期表
门捷列夫与元素周期表
门捷列夫
门捷列夫第一张元素周期表
门捷列夫第二张元素周期表
知识点 元素
周期:每一横行叫一周期,共7个周期。
族:每一纵行叫一族(其中8、9、10三个纵行共同组成一个族),共16族。
元素周期表的起始:
原子序数=核电荷数=核内质子数=核外电子数
稀有气体元素
金属元素
非金属元素
知识点 元素
知识点2 元素周期表
新知探究
门捷列夫和元素周期表
知识点 元素
知识点 元素
五、元素周期表
1.发现者:门捷列夫
(1)编号:质子数递增的顺序
(2)横行(周期):共七周期,同一周期(行)电子层数相同,从左到右最外层电子数依次递增。
(3)纵行(族):共18纵行16个族,同一族(列)最外层电子数相同,从上到下电子层数依次递增。
2.结构
知识点 元素
※3.一格的信息
【注】主族元素:周期数=电子层数,族数=最外层电子数。
知识点 元素
典例4 下图是硫元素在元素周期表中的部分信息,请在框中填写出其各部分表示的意义。
16 S
硫
32.06
元素符号是S
元素名称是硫
硫的相对原子质量是32.06
硫的原子序数是16
知识点 元素
4.(2018 牡丹江)元素周期表是学习和研究化学的重要工具。如图是元素周期表的一部分,对相关信息表述正确的是( )
A.氟原子的核内中子数为9
B.氯原子的相对原子质量是35.45g
C.氟、硫、氯三种元素都属于非金属元素
D.氟元素和氯元素位于元素周期表的同一周期
C
基础巩固题
知识点 元素
能力提升题
1.(2018秋 江苏期末)元素周期表中锌元素的某些信息如图所示,下列有关锌的说法错误的是( )
A.锌原子核外有30个电子
B.锌的相对原子质量为65.38 g
C.锌是金属元素
D.锌离子核内质子数为30
B
知识点 元素
六、单质和化合物
1.定义:
单质:由一种元素组成的纯净物。
化合物:由两种或两种以上元素组成的纯净物。
注:(1)由同种元素组成的物质不一定是单质。如O2和O3(混合物)。
(2)由不同元素组成的物质不一定是化合物。如CO和CO2(混合物)。
课堂达标
1.“2O”表示的含义是( )
A
A.2个氧原子 B.1个氧分子
C.氧元素 D.氧气
O2
O
O2
知识点 元素
2.下列符号中,既有宏观意义,又有微观意义的是( )
A. Fe2+ B. Fe3+ C. Fe D. 2Fe
解析:Fe2+表示亚铁离子, Fe3+表示铁离子,2Fe表示2个铁原子,都只有微观意义;Fe表示铁元素、铁这种物质,同时又表示1个铁原子,既有宏观意义,又有微观意义。
C
知识点 元素
3.如图是镆元素的信息,下列有关说法错误的是( )
B
原子序数 115 汉语拼音 mò
符号 Mc 中文名称 镆
英文名称 Moscovium
A.镆属于金属元素
B.镆的原子序数115表示其核内有115个中子
C.“Mc” 表示镆这种物质、镆元素、1个镆原子
D.镆原子在化学反应中易失电子
解析:镆的原子序数是115,其原子核内质子数是115,但中子数不一定是115。
知识点 元素
4.中华文化,博大精深。利用元素名称或元素名称的谐音,仿照示例,用相应的元素符号补充成语。
示例:Fe石心肠 功高Ca世
______墙铁壁 火树 _____花 一诺千_____
十全十______ 汗流浃____ 大快人 _____
Cu
Ag
Au
Mg
Ba
Zn
知识点 元素
典例2 (2020 白银中考改编)C919大型客机部分机身采用了新型的铝锂合金。铝锂合金中铝(Al)元素与锂(Li)元素的本质区别是( )
A
A.质子数不同 B.核外电子数不同
C.中子数不同 D.最外层电子数不同
知识点 元素
知识点2 物质的组成、构成
新知探究
物质的组成可从宏观和微观两个方面进行描述,其中元素是从宏观上描述物质的组成,原子、分子是从微观上描述物质的构成。
物质的组成用元素描述,物质的构成用分子、原子或离子描述,分子的构成用原子描述。
知识点 元素
构成
得失电子
失得电子
元素
组成
氧气、氢气、水等
构成
分子
铁、汞、氦气等
硫酸铜、氯化钠等
构成
构成
原子
离子
分解
自然界中多种多样的物质
知识点 元素
物质
分子
原子
元素
组 成
构成
构成
构 成
分 解
得失电子
失得电子
宏观概念
只讲种类 不讲个数
离子
构成
微观概念
既讲种类 又讲个数
知识点 元素
典例3 二氧化碳(CO2)是植物进行光合作用的原料之一。下列关于二氧化碳的说法错误的是( )
C
A.二氧化碳由碳元素和氧元素组成
B.二氧化碳由二氧化碳分子构成
C.二氧化碳分子由碳元素和氧元素组成
D.一个二氧化碳分子由一个碳原子和两个氧原子构成
解析:元素只能用于描述物质的宏观组成。
知识点 元素
典例4 将正确答案填写在题中划线处。
1.氧气、氢气、氨等物质是由________构成的;
2.铁、汞、金刚石等物质是由________构成的;
3.氯化钠、硫酸铜等是由________构成的。
分子
原子
离子
知识点 元素
课堂达标
1.下列关于物质的组成与构成的说法正确的是( )
A.水是由氢原子和氧原子构成的
B.汞是由汞分子构成的
C.氧分子由氧元素组成
D.二氧化碳是由碳、氧两种元素组成的
D
水分子
原子
氧原子构成
知识点 元素
3.下列关于元素的叙述中正确的是( )
A.质子数相同的两种粒子属于同种元素
B.同种元素的原子结构和质量完全相同
C.元素的种类取决于该元素原子的核外电子数
D.不同种元素的根本区别是核内质子数不同
方法点拨:元素的种类是由质子数来决定的,质子数相同的原子或离子属于同种元素。
D
氢的质子数为1,中子数有0、1、2
知识点 元素
化学反应前后,分子种类发生变化,元素种类没有发生变化。
【分析讨论】
下述化学反应中:分子和元素的种类是否发生了
改变?
知识点 元素
元 素 原 子
定义
不 同 点 ①只讲 ,不讲______ ②是 观的概念 ③只能组成 ,不能构成____ ④化学变化中元素的 和____ 不变 ①既讲 ,又讲______
②是 观的概念
③可直接构成 ,也可构成_______
④化学变化中原子的 、
_____、 都不变
相互 关系 元素是 原子的总称,原子是 的个体,是 中的最小粒子 质子数(即核电荷数)相同的一类原子的总称
化学变化中的最小粒子
种类
种类
宏
微
物质
分子
物质
分子
质量
种类
质量
种类
质子数(即核电荷数)相同的一类
数目
化学变化
元素
个数
个数
元素和原子的比较
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
