2024人教版高中化学选择性必修3同步练习题--第1课时 糖类的组成和分类 单糖(含解析)
文档属性
| 名称 | 2024人教版高中化学选择性必修3同步练习题--第1课时 糖类的组成和分类 单糖(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-20 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
2024人教版高中化学选择性必修3同步
第四章 生物大分子
第一节 糖类
第1课时 糖类的组成和分类 单糖
基础过关练
题组一 糖类的组成和分类
1.(2022江苏南通期中)下列对糖类的认识正确的是( )
A.糖类是有甜味的一类物质的总称
B.糖类都含有酮羰基,对氢氧化铜等弱氧化剂表现出还原性
C.糖类分为单糖、寡糖和多糖
D.葡萄糖是分子组成最简单的糖,与果糖互为同分异构体
2.(经典题)下列关于糖类的说法中正确的是( )
A.分子组成符合Cn(H2O)m通式的物质一定属于糖类
B.分子组成不符合Cn(H2O)m通式的物质一定不属于糖类
C.CH2OH(CHOH)4CHO、CH3CH(OH)CH2CHO都属于糖类
D.淀粉、纤维素的通式为Cn(H2O)m,都为天然高分子
题组二 单糖
3.下列有关葡萄糖与果糖的说法中,不正确的是( )
①二者互为同分异构体
②二者都易溶于水
③二者都能发生银镜反应,都能与新制Cu(OH)2反应生成砖红色沉淀
④葡萄糖能发生酯化反应,而果糖不能
⑤都能与H2发生加成反应生成六元醇
⑥果糖是最甜的糖,而葡萄糖无甜味
A.①②③ B.④⑤ C.④⑥ D.⑥
4.核糖与脱氧核糖分别是生物体遗传物质核糖核酸与脱氧核糖核酸的重要组成部分,其结构如图所示。下列关于核糖与脱氧核糖的说法正确的是( )
A.核糖与脱氧核糖均为非还原糖
B.核糖与脱氧核糖互为同分异构体
C.核糖与脱氧核糖、葡萄糖互为同系物
D.核糖与脱氧核糖均可以使酸性高锰酸钾溶液褪色
5.纯净的果糖是无色晶体,果糖比蔗糖的甜度高,在水果和蜂蜜中含量较高。果糖中含,在碱性条件下可发生异构化,如图所示:
下列说法正确的是( )
A.可用银氨溶液来鉴别葡萄糖和果糖
B.结构简式为CH2OH(CHOH)3CHO的有机物与葡萄糖互为同系物
C.果糖可发生加成反应、酯化反应、消去反应
D.果糖可以水解
能力提升练
题组一 新情境下单糖的结构与性质的考查
1.(经典题)葡萄糖可发生如图转化,设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.常温常压下,6.0 g葡萄糖和乳酸的混合物中O原子数为0.2NA
B.1 mol葡萄糖发生银镜反应能生成2 mol Ag
C.1 mol乳酸与足量的乙醇反应可生成NA个乳酸乙酯分子
D.相同条件下,相同物质的量的乳酸分别与足量的钠和碳酸氢钠溶液反应,产生的气体体积相同
2.(2023上海杨浦高级中学月考)葡萄糖在生物体内会发生分子内反应形成葡萄糖的半缩醛(如图所示),物质A和B分别为两种葡萄糖半缩醛,下列说法正确的是( )
A.形成半缩醛时发生了取代反应
B.葡萄糖半缩醛A和B的分子式均为C6H10O6
C.物质A分子不具有手性
D.半缩醛的形成可看作羟基与醛基发生了加成反应
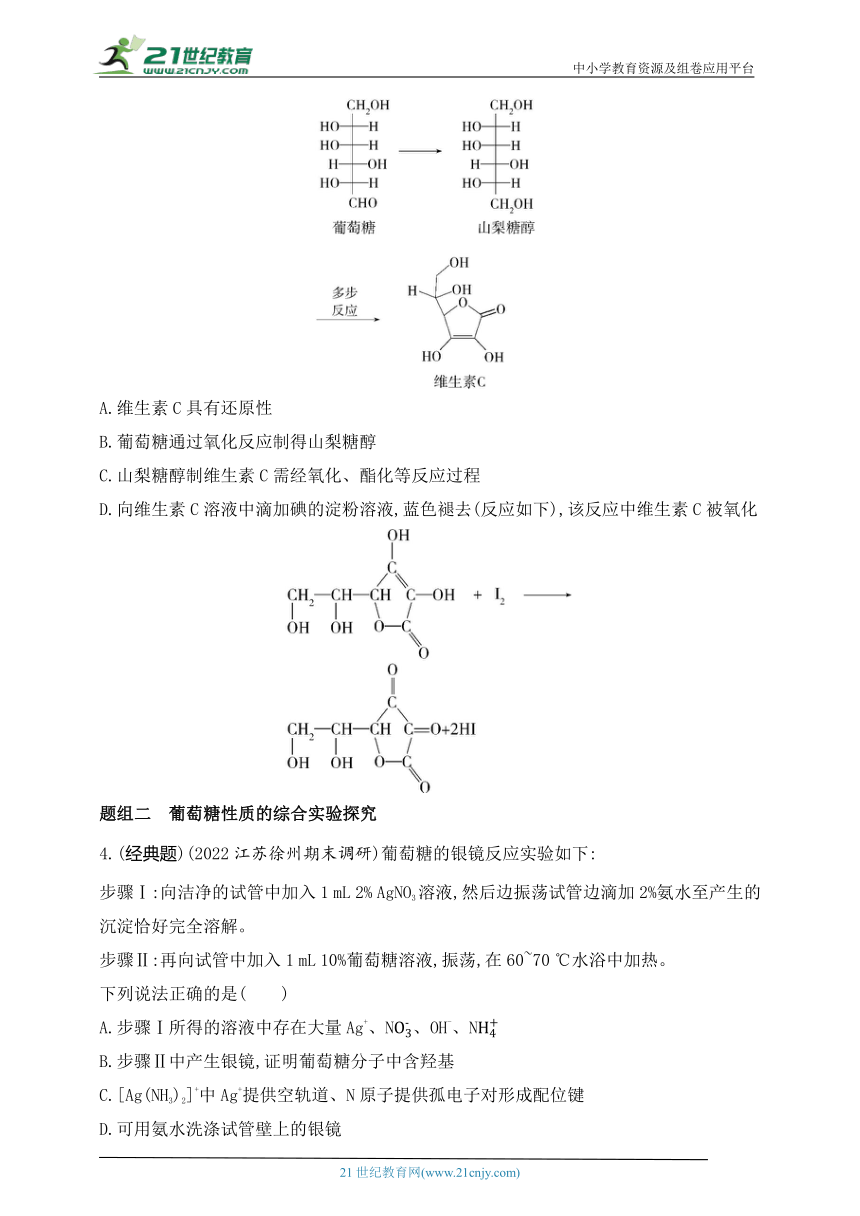
3.(经典题)(2022吉林一中月考)维生素C在人体中有抗氧化、延缓细胞衰老的作用。以葡萄糖为原料制取维生素C的过程如图所示,下列说法不正确的是( )
A.维生素C具有还原性
B.葡萄糖通过氧化反应制得山梨糖醇
C.山梨糖醇制维生素C需经氧化、酯化等反应过程
D.向维生素C溶液中滴加碘的淀粉溶液,蓝色褪去(反应如下),该反应中维生素C被氧化
题组二 葡萄糖性质的综合实验探究
4.(经典题)(2022江苏徐州期末调研)葡萄糖的银镜反应实验如下:
步骤Ⅰ:向洁净的试管中加入1 mL 2% AgNO3溶液,然后边振荡试管边滴加2%氨水至产生的沉淀恰好完全溶解。
步骤Ⅱ:再向试管中加入1 mL 10%葡萄糖溶液,振荡,在60~70 ℃水浴中加热。
下列说法正确的是( )
A.步骤Ⅰ所得的溶液中存在大量Ag+、N、OH-、N
B.步骤Ⅱ中产生银镜,证明葡萄糖分子中含羟基
C.[Ag(NH3)2]+中Ag+提供空轨道、N原子提供孤电子对形成配位键
D.可用氨水洗涤试管壁上的银镜
5.将下列四种液体各取2 mL分别加入四支盛有一定量新制Cu(OH)2的试管中,充分振荡。实验现象记录如下表:
葡萄糖 溶液 乙醇 甘油 (丙三醇) 水
氢氧化铜溶解,溶液呈绛蓝色 氢氧化铜不溶,混合物蓝色变浅 氢氧化铜溶解,溶液呈绛蓝色 氢氧化铜不溶,混合物蓝色变浅
根据上述实验及现象能够得出的正确结论是( )
A.葡萄糖分子中可能含有醛基
B.葡萄糖分子中可能含有多个羟基
C.葡萄糖的分子式为C6H12O6
D.葡萄糖分子碳链呈锯齿形
6.(2022内蒙古呼和浩特一模)葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下实验流程制得:
已知:a.CH2OH(CHOH)4CHO+Br2+H2O C6H12O7(葡萄糖酸)+2HBr;
b.2C6H12O7(葡萄糖酸)+CaCO3 Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑;
c.相关物质的溶解性见下表:
物质名称 葡萄糖酸钙 葡萄糖酸 溴化钙
在水中的溶解性 可溶于冷水, 易溶于热水 可溶 极易溶
在乙醇中的溶解性 微溶 微溶 可溶
回答下列问题:
(1)步骤Ⅰ中溴水氧化葡萄糖时,甲同学设计了如图所示装置。你认为缺少的仪器是 ,盛放NaOH溶液的烧杯中主要反应的离子方程式为 。
(2)步骤Ⅱ中加入过量CaCO3,除了能提高葡萄糖酸的转化率,还具有的主要作用是 。
(3)步骤Ⅲ的操作是将所得悬浊液煮沸,并趁热采用装置(如图所示)抽滤,过滤掉未反应的CaCO3,得到澄清透明的溶液。抽滤时自来水流的作用是使瓶内与大气形成压强差。与普通过滤操作相比,抽滤的优点是 ;抽滤过程需要趁热进行的原因是 。
(4)步骤Ⅴ洗涤操作所用的洗涤剂选用乙醇—水混合溶液,理由是 。
(5)该实验中葡萄糖酸钙的产率为 (保留3位有效数字)。
答案与分层梯度式解析
第四章 生物大分子
第一节 糖类
第1课时 糖类的组成和分类 单糖
基础过关练
1.C 2.D 3.C 4.D 5.C
1.C 糖类不一定有甜味,如纤维素,A项错误;糖类不一定都含有酮羰基,有一些含有醛基,含有醛基的糖能对氢氧化铜等弱氧化剂表现出还原性,B项错误;糖类可分为单糖、寡糖和多糖,C项正确;葡萄糖与果糖分子式相同,结构不同,互为同分异构体,但葡萄糖不是最简单的糖,D项错误。
易错分析 有甜味的不一定是糖,如木糖醇;没有甜味的也可能是糖,如淀粉、纤维素等。因此,糖类物质不等于甜味物质。
2.D 分子组成符合Cn(H2O)m通式的物质不一定为糖类化合物,如甲醛(CH2O)、乙酸(C2H4O2)等,A错误;分子组成不符合Cn(H2O)m通式的物质可能是糖类,如鼠李糖(C6H12O5),B错误;从分子结构上看,糖类是多羟基醛、多羟基酮和它们的脱水缩合物,CH2OH(CHOH)4CHO为葡萄糖,CH3CH(OH)CH2CHO不是多羟基醛,不属于糖类,C错误;淀粉、纤维素均为天然高分子,分子式均为(C6H10O5)n,分子组成符合通式Cn(H2O)m,D正确。
易错分析 糖类一般由C、H、O三种元素组成,大多数可用通式Cn(H2O)m表示,n与m可以相同,也可以是不同的正整数。但并非所有的糖都符合通式Cn(H2O)m,如鼠李糖的分子式为C6H12O5。
3.C 葡萄糖与果糖的分子式都是C6H12O6,二者结构不同,互为同分异构体,①正确;葡萄糖与果糖都易溶于水,②正确;果糖在碱性条件下可得到含醛基的物质,葡萄糖和果糖都能发生银镜反应,都能与新制Cu(OH)2反应,③正确;葡萄糖与果糖分子中都含羟基,一定条件下都能发生酯化反应,④错误;葡萄糖中的醛基、果糖中的酮羰基在一定条件下均能与H2发生加成反应,生成六元醇,⑤正确;果糖是最甜的糖,葡萄糖也有一定的甜味,⑥错误;故选C。
4.D 核糖与脱氧核糖分子中均含有醛基,属于还原糖,A错误;核糖的分子式为C5H10O5,脱氧核糖的分子式是C5H10O4,二者分子式不同,B错误;核糖与脱氧核糖、葡萄糖不互为同系物,C错误;核糖与脱氧核糖分子中的羟基与醛基均能被酸性高锰酸钾溶液氧化,故二者均可以使酸性高锰酸钾溶液褪色,D正确。
5.C 由题干可知,果糖在碱性条件下能发生异构化反应产生醛基,故葡萄糖和果糖都能发生银镜反应,不能用银氨溶液来鉴别二者,A错误;CH2OH(CHOH)3CHO与葡萄糖的分子组成相差一个“CH2O”,不互为同系物,B错误;果糖分子中含酮羰基,能发生加成反应,含羟基且与羟基相连的碳原子的邻位碳原子上有氢原子,能发生消去反应和酯化反应,C正确;果糖是单糖,不能水解,D错误。
能力提升练
1.C 2.D 3.B 4.C 5.B
C 葡萄糖与乳酸的最简式均为CH2O,所以6.0 g二者的混合物中O原子的物质的量为=0.2 mol,数目为0.2NA,A项正确;1个葡萄糖分子中含有1个醛基,1 mol葡萄糖发生银镜反应能生成2 mol Ag,B项正确;由于酯化反应为可逆反应,故1 mol乳酸与足量乙醇反应生成的乳酸乙酯的物质的量小于1 mol,C项错误;乳酸分子中的羟基和羧基均可与钠反应,所以与足量钠反应时,1 mol乳酸可产生
1 mol H2,1个乳酸分子中含有1个羧基,所以与足量碳酸氢钠溶液反应时,1 mol乳酸可产生1 mol CO2,D项正确。
2.D 形成半缩醛时,可以看成醇羟基与醛基发生了分子内的加成反应,葡萄糖、A和B的分子式均为C6H12O6,三者互为同分异构体,A、B错误,D正确;物质A的1个分子中含有5个手性碳原子,具有手性,C错误。
3.B 维生素C中含有碳碳双键和—CH2OH等,具有还原性,A正确;由葡萄糖转化为山梨糖醇的过程中,—CHO转化为—CH2OH,为还原反应,B错误;山梨糖醇制备维生素C的过程中,a位置处的—CH2OH被氧化为羧基,生成的羧基与b处C上的羟基发生酯化反应(如图:),再经反应引入碳碳双键,C正确;由反应方程式可知,该反应中维生素C被氧化,D正确。
4.C Ag+、OH-不能大量共存,A错误;银镜的产生证明葡萄糖分子中含醛基,B错误;[Ag(NH3)2]+中Ag+提供空轨道、氨分子中氮原子提供孤电子对形成配位键,C正确;银与氨水不反应,可用稀硝酸除去试管壁上的银镜,D错误。
5.B 本题一定要根据实验得出结论,四个选项的叙述均正确,但据题述实验及实验现象只能推断出B是正确的。
规律方法 利用官能团推测葡萄糖的性质
6.答案 (1)温度计 H++OH- H2O (2)除去反应体系中残余的HBr (3)过滤速率快 葡萄糖酸钙可溶于冷水,易溶于热水,防止葡萄糖酸钙因温度降低而析出,可减少葡萄糖酸钙的损失 (4)利用水可以将无机杂质溶解除去,同时利用葡萄糖酸钙在乙醇中微溶,减少葡萄糖酸钙的溶解损失 (5)76.3%
解析 【流程梳理】
实验目的:利用葡萄糖制备葡萄糖酸钙。
实验原理:CH2OH(CHOH)4CHO+Br2+H2O C6H12O7(葡萄糖酸)+2HBr,2C6H12O7(葡萄糖酸)+CaCO3 Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑。
步骤Ⅰ中溴水氧化葡萄糖时,反应温度为55 ℃,应用水浴加热,需用温度计测量水浴温度;NaOH溶液主要用于吸收HBr,反应的离子方程式为H++OH- H2O。(5)n(C6H12O6)==0.05 mol,根据已知信息a、b可知,n[Ca(C6H11O7)2]=n(C6H12O6)=0.025 mol,Ca(C6H11O7)2的理论产量为0.025 mol×430 g/mol=10.75 g,葡萄糖酸钙的产率=
×100%≈76.3%。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024人教版高中化学选择性必修3同步
第四章 生物大分子
第一节 糖类
第1课时 糖类的组成和分类 单糖
基础过关练
题组一 糖类的组成和分类
1.(2022江苏南通期中)下列对糖类的认识正确的是( )
A.糖类是有甜味的一类物质的总称
B.糖类都含有酮羰基,对氢氧化铜等弱氧化剂表现出还原性
C.糖类分为单糖、寡糖和多糖
D.葡萄糖是分子组成最简单的糖,与果糖互为同分异构体
2.(经典题)下列关于糖类的说法中正确的是( )
A.分子组成符合Cn(H2O)m通式的物质一定属于糖类
B.分子组成不符合Cn(H2O)m通式的物质一定不属于糖类
C.CH2OH(CHOH)4CHO、CH3CH(OH)CH2CHO都属于糖类
D.淀粉、纤维素的通式为Cn(H2O)m,都为天然高分子
题组二 单糖
3.下列有关葡萄糖与果糖的说法中,不正确的是( )
①二者互为同分异构体
②二者都易溶于水
③二者都能发生银镜反应,都能与新制Cu(OH)2反应生成砖红色沉淀
④葡萄糖能发生酯化反应,而果糖不能
⑤都能与H2发生加成反应生成六元醇
⑥果糖是最甜的糖,而葡萄糖无甜味
A.①②③ B.④⑤ C.④⑥ D.⑥
4.核糖与脱氧核糖分别是生物体遗传物质核糖核酸与脱氧核糖核酸的重要组成部分,其结构如图所示。下列关于核糖与脱氧核糖的说法正确的是( )
A.核糖与脱氧核糖均为非还原糖
B.核糖与脱氧核糖互为同分异构体
C.核糖与脱氧核糖、葡萄糖互为同系物
D.核糖与脱氧核糖均可以使酸性高锰酸钾溶液褪色
5.纯净的果糖是无色晶体,果糖比蔗糖的甜度高,在水果和蜂蜜中含量较高。果糖中含,在碱性条件下可发生异构化,如图所示:
下列说法正确的是( )
A.可用银氨溶液来鉴别葡萄糖和果糖
B.结构简式为CH2OH(CHOH)3CHO的有机物与葡萄糖互为同系物
C.果糖可发生加成反应、酯化反应、消去反应
D.果糖可以水解
能力提升练
题组一 新情境下单糖的结构与性质的考查
1.(经典题)葡萄糖可发生如图转化,设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.常温常压下,6.0 g葡萄糖和乳酸的混合物中O原子数为0.2NA
B.1 mol葡萄糖发生银镜反应能生成2 mol Ag
C.1 mol乳酸与足量的乙醇反应可生成NA个乳酸乙酯分子
D.相同条件下,相同物质的量的乳酸分别与足量的钠和碳酸氢钠溶液反应,产生的气体体积相同
2.(2023上海杨浦高级中学月考)葡萄糖在生物体内会发生分子内反应形成葡萄糖的半缩醛(如图所示),物质A和B分别为两种葡萄糖半缩醛,下列说法正确的是( )
A.形成半缩醛时发生了取代反应
B.葡萄糖半缩醛A和B的分子式均为C6H10O6
C.物质A分子不具有手性
D.半缩醛的形成可看作羟基与醛基发生了加成反应
3.(经典题)(2022吉林一中月考)维生素C在人体中有抗氧化、延缓细胞衰老的作用。以葡萄糖为原料制取维生素C的过程如图所示,下列说法不正确的是( )
A.维生素C具有还原性
B.葡萄糖通过氧化反应制得山梨糖醇
C.山梨糖醇制维生素C需经氧化、酯化等反应过程
D.向维生素C溶液中滴加碘的淀粉溶液,蓝色褪去(反应如下),该反应中维生素C被氧化
题组二 葡萄糖性质的综合实验探究
4.(经典题)(2022江苏徐州期末调研)葡萄糖的银镜反应实验如下:
步骤Ⅰ:向洁净的试管中加入1 mL 2% AgNO3溶液,然后边振荡试管边滴加2%氨水至产生的沉淀恰好完全溶解。
步骤Ⅱ:再向试管中加入1 mL 10%葡萄糖溶液,振荡,在60~70 ℃水浴中加热。
下列说法正确的是( )
A.步骤Ⅰ所得的溶液中存在大量Ag+、N、OH-、N
B.步骤Ⅱ中产生银镜,证明葡萄糖分子中含羟基
C.[Ag(NH3)2]+中Ag+提供空轨道、N原子提供孤电子对形成配位键
D.可用氨水洗涤试管壁上的银镜
5.将下列四种液体各取2 mL分别加入四支盛有一定量新制Cu(OH)2的试管中,充分振荡。实验现象记录如下表:
葡萄糖 溶液 乙醇 甘油 (丙三醇) 水
氢氧化铜溶解,溶液呈绛蓝色 氢氧化铜不溶,混合物蓝色变浅 氢氧化铜溶解,溶液呈绛蓝色 氢氧化铜不溶,混合物蓝色变浅
根据上述实验及现象能够得出的正确结论是( )
A.葡萄糖分子中可能含有醛基
B.葡萄糖分子中可能含有多个羟基
C.葡萄糖的分子式为C6H12O6
D.葡萄糖分子碳链呈锯齿形
6.(2022内蒙古呼和浩特一模)葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下实验流程制得:
已知:a.CH2OH(CHOH)4CHO+Br2+H2O C6H12O7(葡萄糖酸)+2HBr;
b.2C6H12O7(葡萄糖酸)+CaCO3 Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑;
c.相关物质的溶解性见下表:
物质名称 葡萄糖酸钙 葡萄糖酸 溴化钙
在水中的溶解性 可溶于冷水, 易溶于热水 可溶 极易溶
在乙醇中的溶解性 微溶 微溶 可溶
回答下列问题:
(1)步骤Ⅰ中溴水氧化葡萄糖时,甲同学设计了如图所示装置。你认为缺少的仪器是 ,盛放NaOH溶液的烧杯中主要反应的离子方程式为 。
(2)步骤Ⅱ中加入过量CaCO3,除了能提高葡萄糖酸的转化率,还具有的主要作用是 。
(3)步骤Ⅲ的操作是将所得悬浊液煮沸,并趁热采用装置(如图所示)抽滤,过滤掉未反应的CaCO3,得到澄清透明的溶液。抽滤时自来水流的作用是使瓶内与大气形成压强差。与普通过滤操作相比,抽滤的优点是 ;抽滤过程需要趁热进行的原因是 。
(4)步骤Ⅴ洗涤操作所用的洗涤剂选用乙醇—水混合溶液,理由是 。
(5)该实验中葡萄糖酸钙的产率为 (保留3位有效数字)。
答案与分层梯度式解析
第四章 生物大分子
第一节 糖类
第1课时 糖类的组成和分类 单糖
基础过关练
1.C 2.D 3.C 4.D 5.C
1.C 糖类不一定有甜味,如纤维素,A项错误;糖类不一定都含有酮羰基,有一些含有醛基,含有醛基的糖能对氢氧化铜等弱氧化剂表现出还原性,B项错误;糖类可分为单糖、寡糖和多糖,C项正确;葡萄糖与果糖分子式相同,结构不同,互为同分异构体,但葡萄糖不是最简单的糖,D项错误。
易错分析 有甜味的不一定是糖,如木糖醇;没有甜味的也可能是糖,如淀粉、纤维素等。因此,糖类物质不等于甜味物质。
2.D 分子组成符合Cn(H2O)m通式的物质不一定为糖类化合物,如甲醛(CH2O)、乙酸(C2H4O2)等,A错误;分子组成不符合Cn(H2O)m通式的物质可能是糖类,如鼠李糖(C6H12O5),B错误;从分子结构上看,糖类是多羟基醛、多羟基酮和它们的脱水缩合物,CH2OH(CHOH)4CHO为葡萄糖,CH3CH(OH)CH2CHO不是多羟基醛,不属于糖类,C错误;淀粉、纤维素均为天然高分子,分子式均为(C6H10O5)n,分子组成符合通式Cn(H2O)m,D正确。
易错分析 糖类一般由C、H、O三种元素组成,大多数可用通式Cn(H2O)m表示,n与m可以相同,也可以是不同的正整数。但并非所有的糖都符合通式Cn(H2O)m,如鼠李糖的分子式为C6H12O5。
3.C 葡萄糖与果糖的分子式都是C6H12O6,二者结构不同,互为同分异构体,①正确;葡萄糖与果糖都易溶于水,②正确;果糖在碱性条件下可得到含醛基的物质,葡萄糖和果糖都能发生银镜反应,都能与新制Cu(OH)2反应,③正确;葡萄糖与果糖分子中都含羟基,一定条件下都能发生酯化反应,④错误;葡萄糖中的醛基、果糖中的酮羰基在一定条件下均能与H2发生加成反应,生成六元醇,⑤正确;果糖是最甜的糖,葡萄糖也有一定的甜味,⑥错误;故选C。
4.D 核糖与脱氧核糖分子中均含有醛基,属于还原糖,A错误;核糖的分子式为C5H10O5,脱氧核糖的分子式是C5H10O4,二者分子式不同,B错误;核糖与脱氧核糖、葡萄糖不互为同系物,C错误;核糖与脱氧核糖分子中的羟基与醛基均能被酸性高锰酸钾溶液氧化,故二者均可以使酸性高锰酸钾溶液褪色,D正确。
5.C 由题干可知,果糖在碱性条件下能发生异构化反应产生醛基,故葡萄糖和果糖都能发生银镜反应,不能用银氨溶液来鉴别二者,A错误;CH2OH(CHOH)3CHO与葡萄糖的分子组成相差一个“CH2O”,不互为同系物,B错误;果糖分子中含酮羰基,能发生加成反应,含羟基且与羟基相连的碳原子的邻位碳原子上有氢原子,能发生消去反应和酯化反应,C正确;果糖是单糖,不能水解,D错误。
能力提升练
1.C 2.D 3.B 4.C 5.B
C 葡萄糖与乳酸的最简式均为CH2O,所以6.0 g二者的混合物中O原子的物质的量为=0.2 mol,数目为0.2NA,A项正确;1个葡萄糖分子中含有1个醛基,1 mol葡萄糖发生银镜反应能生成2 mol Ag,B项正确;由于酯化反应为可逆反应,故1 mol乳酸与足量乙醇反应生成的乳酸乙酯的物质的量小于1 mol,C项错误;乳酸分子中的羟基和羧基均可与钠反应,所以与足量钠反应时,1 mol乳酸可产生
1 mol H2,1个乳酸分子中含有1个羧基,所以与足量碳酸氢钠溶液反应时,1 mol乳酸可产生1 mol CO2,D项正确。
2.D 形成半缩醛时,可以看成醇羟基与醛基发生了分子内的加成反应,葡萄糖、A和B的分子式均为C6H12O6,三者互为同分异构体,A、B错误,D正确;物质A的1个分子中含有5个手性碳原子,具有手性,C错误。
3.B 维生素C中含有碳碳双键和—CH2OH等,具有还原性,A正确;由葡萄糖转化为山梨糖醇的过程中,—CHO转化为—CH2OH,为还原反应,B错误;山梨糖醇制备维生素C的过程中,a位置处的—CH2OH被氧化为羧基,生成的羧基与b处C上的羟基发生酯化反应(如图:),再经反应引入碳碳双键,C正确;由反应方程式可知,该反应中维生素C被氧化,D正确。
4.C Ag+、OH-不能大量共存,A错误;银镜的产生证明葡萄糖分子中含醛基,B错误;[Ag(NH3)2]+中Ag+提供空轨道、氨分子中氮原子提供孤电子对形成配位键,C正确;银与氨水不反应,可用稀硝酸除去试管壁上的银镜,D错误。
5.B 本题一定要根据实验得出结论,四个选项的叙述均正确,但据题述实验及实验现象只能推断出B是正确的。
规律方法 利用官能团推测葡萄糖的性质
6.答案 (1)温度计 H++OH- H2O (2)除去反应体系中残余的HBr (3)过滤速率快 葡萄糖酸钙可溶于冷水,易溶于热水,防止葡萄糖酸钙因温度降低而析出,可减少葡萄糖酸钙的损失 (4)利用水可以将无机杂质溶解除去,同时利用葡萄糖酸钙在乙醇中微溶,减少葡萄糖酸钙的溶解损失 (5)76.3%
解析 【流程梳理】
实验目的:利用葡萄糖制备葡萄糖酸钙。
实验原理:CH2OH(CHOH)4CHO+Br2+H2O C6H12O7(葡萄糖酸)+2HBr,2C6H12O7(葡萄糖酸)+CaCO3 Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑。
步骤Ⅰ中溴水氧化葡萄糖时,反应温度为55 ℃,应用水浴加热,需用温度计测量水浴温度;NaOH溶液主要用于吸收HBr,反应的离子方程式为H++OH- H2O。(5)n(C6H12O6)==0.05 mol,根据已知信息a、b可知,n[Ca(C6H11O7)2]=n(C6H12O6)=0.025 mol,Ca(C6H11O7)2的理论产量为0.025 mol×430 g/mol=10.75 g,葡萄糖酸钙的产率=
×100%≈76.3%。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
