2024人教版高中化学选择性必修3同步练习题--第1课时 有机化合物的分离、提纯(含解析)
文档属性
| 名称 | 2024人教版高中化学选择性必修3同步练习题--第1课时 有机化合物的分离、提纯(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-20 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
2024人教版高中化学选择性必修3同步
第二节 研究有机化合物的一般方法
第1课时 有机化合物的分离、提纯
基础过关练
题组一 蒸馏
1.(2023陕西西安航天城一中月考)在实验室用自来水制取蒸馏水的实验中,下列说法错误的是 ( )
A.蒸馏烧瓶中要放入碎瓷片以防止暴沸
B.通过蒸馏可以除去自来水中含有的Cl-等杂质
C.冷却水应该是下口进上口出,与水蒸气的流向相反
D.开始蒸馏时,应先加热再通冷却水;蒸馏完毕,应该先关冷却水再撤酒精灯
2.(经典题)(2022广东佛山顺德期中)现有一瓶A和B的混合液,已知A和B的某些性质如表:
物质 分子式 熔点/℃ 沸点/℃ 密度/ (g/cm3) 水溶性
A C3H6O2 -98 50.5 0.93 可溶
B C4H8O2 -93 80.8 0.9 可溶
由此推知分离A和B的最佳方法是( )
A.萃取 B.结晶 C.蒸馏 D.分液
3.(经典题)实验室可通过蒸馏石油得到多种沸点不同的馏分,装置如图所示。下列说法不正确的是( )
A.沸点较低的汽油比沸点较高的柴油先馏出
B.蒸馏烧瓶中放入碎瓷片,可防止蒸馏时发生暴沸
C.冷凝管中的冷却水应该从a口进b口出
D.温度计水银球位于蒸馏烧瓶支管口处
题组二 萃取、分液
4.(经典题)以下关于萃取、分液操作的叙述中,正确的是( )
A.把混合液体转移至分液漏斗,塞上玻璃塞,如图所示用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗上的小孔,再打开活塞
5.下列关于萃取操作的说法正确的是( )
A.从碘水中提取碘,可用酒精作萃取剂
B.萃取操作完成后,静置分层,上、下层液体依次从下口放出
C.萃取时所选溶剂应与原溶剂互不相溶,且与溶质不反应
D.用一种有机溶剂提取水溶液中的某物质,静置分层,“水层”应在上层
6.(2023辽宁沈阳阶段练习)下列每组中各有三对物质,它们都能用分液漏斗分离的是( )
A.乙酸乙酯和水,酒精和水,植物油和水
B.四氯化碳和水,溴苯和水,硝基苯和水
C.甘油和水,乙酸和水,乙酸和乙醇
D.汽油和水,苯和水,甲醇和水
7.(经典题)乙酸异戊酯的有关信息如下表所示:
相对分 子质量 密度/ (g·cm-3) 沸点/ ℃ 水溶性
乙酸 异戊酯 130 0.867 142 难溶
实验室制备乙酸异戊酯,在洗涤、分液操作中,应充分振荡,然后静置,待分层后操作正确的是 ( )
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
题组三 重结晶
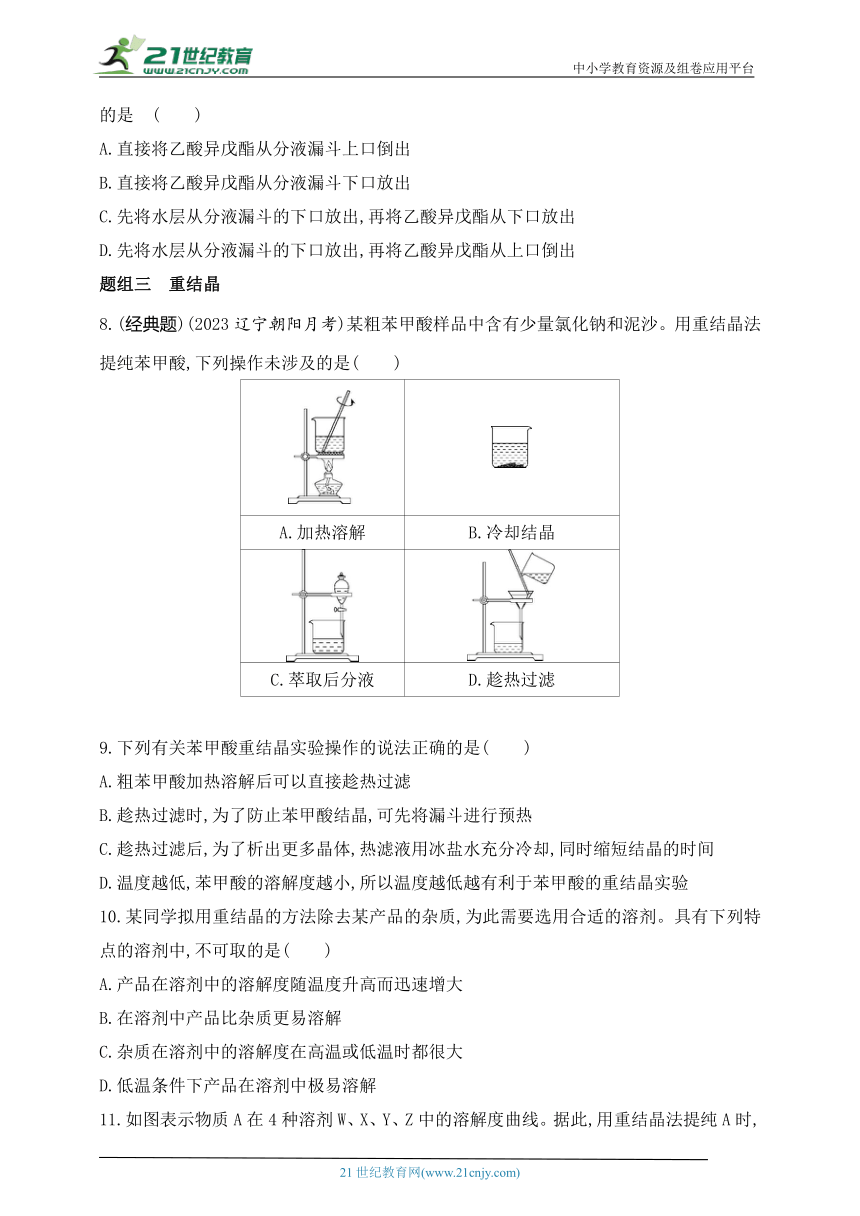
8.(经典题)(2023辽宁朝阳月考)某粗苯甲酸样品中含有少量氯化钠和泥沙。用重结晶法提纯苯甲酸,下列操作未涉及的是( )
A.加热溶解 B.冷却结晶
C.萃取后分液 D.趁热过滤
9.下列有关苯甲酸重结晶实验操作的说法正确的是( )
A.粗苯甲酸加热溶解后可以直接趁热过滤
B.趁热过滤时,为了防止苯甲酸结晶,可先将漏斗进行预热
C.趁热过滤后,为了析出更多晶体,热滤液用冰盐水充分冷却,同时缩短结晶的时间
D.温度越低,苯甲酸的溶解度越小,所以温度越低越有利于苯甲酸的重结晶实验
10.某同学拟用重结晶的方法除去某产品的杂质,为此需要选用合适的溶剂。具有下列特点的溶剂中,不可取的是( )
A.产品在溶剂中的溶解度随温度升高而迅速增大
B.在溶剂中产品比杂质更易溶解
C.杂质在溶剂中的溶解度在高温或低温时都很大
D.低温条件下产品在溶剂中极易溶解
11.如图表示物质A在4种溶剂W、X、Y、Z中的溶解度曲线。据此,用重结晶法提纯A时,最宜采用的溶剂是( )
A.W B.X
C.Y D.Z
12.乙酰苯胺是一种具有解热镇痛作用的白色晶体,某种乙酰苯胺样品中混入了少量氯化钠杂质。
已知:①20 ℃时乙酰苯胺在乙醇中的溶解度为36.9 g;
②氯化钠可分散在乙醇中形成胶体;
③乙酰苯胺在水中的溶解度如下表:
温度/℃ 25 50 80 100
溶解度/g 0.56 0.84 3.5 5.5
下列提纯乙酰苯胺使用的溶剂和操作方法都正确的是( )
A.水 分液
B.乙醇 过滤
C.水 重结晶
D.乙醇 重结晶
能力提升练
题组一 物质分离、提纯方法的选择
1.(2023广东广州三校期中联考,)下列实验中,所采取的分离方法或对应原理不正确的是( )
选项 目的 分离方法 原理
A 除去C2H6中的C2H4 洗气 C2H4能被酸性KMnO4溶液氧化,而C2H6不反应
B 分离苯和水 分液 苯和水不互溶
C 除去粗苯甲酸晶体中的沙子 重结晶 苯甲酸的溶解度受温度影响较大,沙子在水中的溶解度很小
D 分离苯和硝基苯 蒸馏 苯和硝基苯互溶,二者沸点相差较大
2.(经典题)(2022黑龙江大庆实验中学期中)青蒿素是治疗疟疾效果很好的药物,我国科学家屠呦呦因提取青蒿素用于治疗疟疾而获得诺贝尔奖,从中药中提取青蒿素的一种方法如图所示。
已知:①常温下,青蒿素是含有过氧基的倍半萜内酯的无色针状晶体,难溶于水,易溶于有机溶剂,熔点为156~157 ℃;
②乙醚的沸点为35 ℃,易燃;
③石油醚的沸点为30~80 ℃。
下列有关提取过程的叙述中不正确的是( )
A.“操作Ⅰ”需要用到的玻璃仪器只有分液漏斗、烧杯
B.若将乙醚用石油醚代替,也能达到实验目的
C.“操作Ⅲ”温度过高,会降低青蒿素的产率,其原因可能是青蒿素热稳定性差
D.“操作Ⅲ”包含了浓缩、结晶、过滤
题组二 有机化合物分离、提纯的综合应用
3.(2022湖北名校联盟联考)溴化苄是重要的有机合成工业原料,可由苯甲醇为原料合成,实验原理及装置(夹持、加热装置已略去)如图所示:
+HBr +H2O
相关物质的部分物理性质如表所示(常温常压下):
熔点/ ℃ 沸点/ ℃ 密度/ (g·cm-3) 溶解性
-15.3 205.7 1.04 微溶 于水
-3.0 199 1.44 不溶于水, 易溶于醇
下列有关说法不正确的是( )
A.先加热至反应温度,然后从冷凝管接口b处通水
B.该实验适宜水浴加热
C.浓硫酸作催化剂和吸水剂
D.反应液可按下列步骤分离、提纯:静置→分液→水洗→碱洗→水洗→干燥→减压蒸馏
4.(经典题)绿原酸具有抗病毒、降血压、抗氧化等作用。利用乙醚、95%乙醇浸泡杜仲干叶,得到提取液,进一步提取绿原酸的流程如下:
已知:常温下,绿原酸难溶于水,易溶于乙醚等有机溶剂。
下列说法错误的是( )
A.从“提取液”获取“有机层”的操作为萃取、分液
B.减压蒸馏时选用球形冷凝管
C.过滤时所需玻璃仪器有烧杯、漏斗、玻璃棒
D.绿原酸粗产品可通过重结晶的方法提纯
5.(2022江苏高邮期中统考)苯甲醇与苯甲酸都是常见化工原料,在化工生产中有广泛应用。工业上常在碱性条件下以苯甲醛作原料来制备苯甲醇和苯甲酸。某实验室模拟其生产过程,实验原理、实验步骤如下。
实验原理:
2+KOH +(该反应为放热反应)
相关资料:
①相关物质的物理性质如下表:
名称 相对分 子质量 熔点/℃ 沸点/℃ 溶解性
水 醇 醚
苯甲醛 106 -26 179.62 微溶 易溶 易溶
苯甲酸 122 122.13 249 微溶 易溶 易溶
苯甲醇 108 -15.3 205.7 微溶 易溶 易溶
乙醚 74 -116.3 34.6 微溶 易溶 —
②苯甲醛在空气中极易被氧化,生成白色苯甲酸。
实验步骤如下:
Ⅰ.向盛有足量KOH溶液的反应器中分批加入13.5 mL(14.0 g)苯甲醛,持续搅拌至反应混合物变成白色蜡糊状A,转移至锥形瓶中静置24小时以上。反应装置如图1所示。
图1
Ⅱ.步骤Ⅰ所得产物后续处理过程如图2所示。
图2
回答下列问题:
(1)仪器a的名称为 。
(2)步骤Ⅰ中苯甲醛需要分批加入且适时冷却,其原因是 。
(3)已知:苯甲醛可与饱和NaHSO3溶液反应。为获取产品1,将乙醚萃取液依次用饱和亚硫酸氢钠溶液、10%碳酸钠溶液和水进行洗涤并分液。乙醚萃取液的密度小于水,取分液后 (填“上”或“下”)层液体加入无水MgSO4,其作用为 ;操作①含多步操作,其中最后一步操作是对乙醚和产品1进行分离,其名称为 。
(4)水层中加入浓盐酸发生反应的离子方程式为 。
(5)操作②包含溶解、蒸发浓缩、冷却结晶、过滤、晾干等,下列仪器中在该操作中不需要用到的有 (填字母)。
A.分液漏斗 B.蒸发皿 C.研钵 D.玻璃棒
(6)①若产品2产率比预期值稍高,可能原因是 。
A.未彻底晾干
B.产品中混有其他杂质
C.过滤时滤液浑浊
D.部分苯甲醛被直接氧化为苯甲酸
②产品2经干燥后称量,质量为6.1 g,计算其产率为 (保留3位有效数字)。
答案与分层梯度式解析
第二节 研究有机化合物的一般方法
第1课时 有机化合物的分离、提纯
基础过关练
1.D 2.C 3.C 4.D 5.C 6.B 7.D 8.C
9.B 10.D 11.D 12.C
1.D 为防止液体暴沸,加热前应在蒸馏烧瓶中放入碎瓷片,A正确;蒸馏是利用沸点差异,实现物质的分离,自来水中的Cl-等杂质构成的物质沸点高,不会随水一起蒸出,B正确;水蒸气冷凝时冷凝管中水采用逆流方式,冷凝效果更好,则冷却水应该是下口进上口出,与水蒸气的流向相反,C正确;开始蒸馏时,应先通冷却水再加热,蒸馏完毕,应该先撤酒精灯再关冷却水,D错误。
2.C 根据题表中的信息可知,A和B的沸点相差较大,可利用蒸馏法分离A和B。
3.C 在蒸馏时,沸点较低的物质先馏出,所以沸点较低的汽油比沸点较高的柴油先馏出,A正确;碎瓷片具有防暴沸作用,所以蒸馏烧瓶中放入碎瓷片可防止蒸馏时发生暴沸,B正确;冷凝管中水采用逆流方式,冷凝效果更好,所以冷却水应该从b口进a口出,C错误;温度计用来测量馏分温度,则温度计水银球位于蒸馏烧瓶支管口处,D正确。
4.D 一只手压住玻璃塞,另一只手握住活塞,把分液漏斗倒转过来振荡,A错误;振荡几次后打开活塞放气,不需打开分液漏斗上口的玻璃塞放气,B错误;将分液漏斗放在铁架台上静置待液体分层,C错误;分液时将分液漏斗颈上的玻璃塞打开或使玻璃塞上的凹槽对准漏斗上的小孔,再打开活塞,待下层液体流尽时,关闭活塞,从上口倒出上层液体,D正确。
5.C 酒精与水互溶,从碘水中提取碘,不能用酒精作萃取剂,A错误;萃取操作完成后,静置分层,下层液体从下口放出,上层液体从上口倒出,B错误;题中未给出萃取剂和水的密度关系,萃取后“水层”可能在上层,也可能在下层,D错误。
6.B A项,酒精和水互溶,不能用分液漏斗分离,错误;B项,三组混合物均互不相溶,可用分液漏斗分离,正确;C项,三组混合物均互溶,不能用分液漏斗分离,错误;D项,甲醇和水互溶,不能用分液漏斗分离,错误。
7.D 乙酸异戊酯的密度比水小且难溶于水,分层后水层在下层,应先将水层从分液漏斗的下口放出,再将上层的乙酸异戊酯从上口倒出。
8.C 将粗苯甲酸加热溶解,可增大苯甲酸的溶解度,A不符合题意;趁热过滤后的滤液冷却后可析出苯甲酸晶体,B不符合题意;用重结晶法提纯苯甲酸的实验操作中不涉及萃取、分液,C符合题意;加热溶解后的固液混合物需要趁热过滤,以减少苯甲酸的损失,D不符合题意。
9.B 粗苯甲酸加热溶解后,考虑到过滤时溶液与环境的温差较大,易使苯甲酸晶体提前析出,滞留在过滤器中,故需在过滤前适当稀释,不能直接过滤,A项错误;趁热过滤后,用冰盐水冷却形成的结晶很小,表面积大,吸附的杂质多,C项错误;重结晶过程中温度太低,杂质的溶解度也会降低,部分杂质也会析出,D项错误。
10.D 根据重结晶的实验原理可知,如果低温条件下产品在溶剂中极易溶解,则该物质很难结晶析出。
规律方法 结晶的三种类型
(1)蒸发结晶:将溶剂蒸发获取晶体,此法适用于溶解度随温度变化不大的物质,如海水晒盐。
(2)降温结晶:将热的饱和溶液慢慢冷却后析出晶体,此法适用于溶解度随温度变化较大的物质,如从NaCl、KNO3的混合液中得KNO3晶体。
(3)重结晶:将待提纯固体混合物用蒸馏水溶解,经过滤、蒸发浓缩、冷却等步骤,再次析出晶体,得到更纯净的晶体的过程,如提纯粗苯甲酸。
11.D 通常重结晶要求被提纯的物质在溶剂中的溶解度受温度的影响较大,能够进行冷却结晶,故最宜采用Z作溶剂。
12.C 本题为情境信息题,主要考查选择合适的分离、提纯方法。解答基本思路:阅读题目,提取有用信息→结合被提纯物质与杂质性质的差异,确定合适的分离、提纯方法→结合选项解答问题。根据题表可知,乙酰苯胺在水中的溶解度随温度变化较大,而氯化钠在水中的溶解度随温度变化较小,故采用重结晶法提纯乙酰苯胺;根据已知信息①②可知,20 ℃时乙酰苯胺在乙醇中的溶解度大,NaCl可分散在乙醇中形成胶体,故不能选乙醇作溶剂通过重结晶法提纯乙酰苯胺。
能力提升练
1.A 2.A 3.A 4.B
1.A C2H4能被酸性KMnO4溶液氧化生成CO2,引入了新杂质,A错误;苯和水互不相溶,可用分液法分离苯和水,B正确;沙子难溶于水,苯甲酸的溶解度受温度影响较大,可用重结晶法除去粗苯甲酸晶体中的沙子,C正确;苯和硝基苯为互溶的两种液体,分离二者可利用沸点差异进行蒸馏,D正确。
方法技巧 有机化合物分离、提纯方法的选择
(1)首先要熟记各种分离、提纯方法的适用范围。常见的分离、提纯有机物的方法及适用范围如下表:
方法 适用范围
分液 互不相溶的两种液体
萃取 同温度下溶质在两种互不相溶的溶剂中的溶解度相差很大
蒸馏 互溶的液态有机物,沸点相差较大(一般大于30 ℃)且热稳定性强
重结晶 固体混合物,被提纯有机物在溶剂中的溶解度受温度影响较大,杂质在溶剂中的溶解度很大或很小
(2)根据给定混合物的状态、溶解性以及熔、沸点的差异等,选择合适的方法即可。
2.A 结合图示流程可知操作Ⅰ是过滤,需要用到的玻璃仪器有烧杯、漏斗、玻璃棒,A错误;乙醚的沸点为35 ℃,石油醚的沸点为30~80 ℃,青蒿素易溶于乙醚和石油醚,若将乙醚用石油醚代替,也能达到实验目的,B正确;青蒿素分子中含有过氧基,热稳定性差,“操作Ⅲ”温度过高,可能会使青蒿素分解,降低产率,C正确;“操作Ⅲ”包含了浓缩、结晶、过滤等操作,D正确。
3.A 为防止反应物受热挥发损失,应先从冷凝管接口b处通水,再加热至反应温度,A错误;该实验反应温度在100 ℃以下,适宜水浴加热,以便控制温度,B正确;由实验原理可知,浓硫酸作催化剂和吸水剂,产物中有水,浓硫酸吸水,促进反应进行更完全,C正确;反应结束后,反应液中含苯甲醇、浓硫酸、HBr、溴化苄、H2O等,经选项中的系列操作后可得较纯净的溴化苄,D正确。
归纳总结 当反应混合物需要加热,且加热温度不超过100 ℃时,可使用水浴加热。水浴加热的优点:便于控制温度,且可使反应物均匀受热。
4.B 由流程图可知,乙酸乙酯作萃取剂,从“提取液”得到“有机层”的实验操作为萃取、分液,A正确;减压蒸馏时若选用球形冷凝管,会有一部分馏分经冷凝后滞留在冷凝管中,而不能进入接收器中,B错误;过滤时所需玻璃仪器有烧杯、漏斗、玻璃棒,C正确;常温下绿原酸难溶于水,易溶于有机溶剂,可利用重结晶的方法进一步提纯,D正确。
5.答案 (1)球形冷凝管
(2)使反应不太剧烈,降低反应温度,避免苯甲醛、苯甲醇的挥发,减少副反应的发生,提高产率(答案合理即可)
(3)上 作干燥剂,除水 蒸馏
(4)+H+ ↓
(5)AC
(6)①ABD ②75.7%
解析 【流程梳理】结合实验流程图,可对本实验中物质A的分离、提纯过程进行如下梳理:
根据图示装置可知,仪器a的名称为球形冷凝管。(2)因为该反应是放热反应,温度过高,反应过于剧烈,会导致苯甲醛、苯甲醇挥发,同时也会使副反应产物增多,使产品的产率降低,所以在步骤Ⅰ中需分批加入苯甲醛且适时冷却,这样做既能减缓反应速率,又能提高产品产率。(3)由于乙醚萃取液的密度小于水,故苯甲醇的乙醚溶液在上层,取分液后上层液体,向其中加入无水MgSO4,进行干燥。产品1为苯甲醇,乙醚与苯甲醇互溶,二者沸点相差较大,故采用蒸馏法分离。(4)水层中含苯甲酸钾,加入浓盐酸,发生反应生成微溶于水的苯甲酸和易溶于水的KCl,反应的离子方程式为+H+ ↓。(5)操作②包含溶解、蒸发浓缩、冷却结晶、过滤、晾干等,不需要的仪器有分液漏斗和研钵,故选A、C。(6)①若过滤后未干燥完全,会导致苯甲酸产率偏高,A正确;若产品中混有其他杂质,测得苯甲酸的质量偏大,其产率偏高,B正确;若过滤时滤液浑浊,有部分苯甲酸滞留在滤液中,测得苯甲酸的质量偏小,其产率偏低,C错误;若部分苯甲醛被直接氧化为苯甲酸,测得苯甲酸的质量偏大,其产率偏高,D正确。②根据关系式:2C6H5CHO~C6H5COOH,参加反应的苯甲醛质量是14.0 g,则理论上生成m(苯甲酸)=××122 g·
mol-1≈8.06 g,实际产量是6.1 g,则苯甲酸的产率为×100%≈
75.7%。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024人教版高中化学选择性必修3同步
第二节 研究有机化合物的一般方法
第1课时 有机化合物的分离、提纯
基础过关练
题组一 蒸馏
1.(2023陕西西安航天城一中月考)在实验室用自来水制取蒸馏水的实验中,下列说法错误的是 ( )
A.蒸馏烧瓶中要放入碎瓷片以防止暴沸
B.通过蒸馏可以除去自来水中含有的Cl-等杂质
C.冷却水应该是下口进上口出,与水蒸气的流向相反
D.开始蒸馏时,应先加热再通冷却水;蒸馏完毕,应该先关冷却水再撤酒精灯
2.(经典题)(2022广东佛山顺德期中)现有一瓶A和B的混合液,已知A和B的某些性质如表:
物质 分子式 熔点/℃ 沸点/℃ 密度/ (g/cm3) 水溶性
A C3H6O2 -98 50.5 0.93 可溶
B C4H8O2 -93 80.8 0.9 可溶
由此推知分离A和B的最佳方法是( )
A.萃取 B.结晶 C.蒸馏 D.分液
3.(经典题)实验室可通过蒸馏石油得到多种沸点不同的馏分,装置如图所示。下列说法不正确的是( )
A.沸点较低的汽油比沸点较高的柴油先馏出
B.蒸馏烧瓶中放入碎瓷片,可防止蒸馏时发生暴沸
C.冷凝管中的冷却水应该从a口进b口出
D.温度计水银球位于蒸馏烧瓶支管口处
题组二 萃取、分液
4.(经典题)以下关于萃取、分液操作的叙述中,正确的是( )
A.把混合液体转移至分液漏斗,塞上玻璃塞,如图所示用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗上的小孔,再打开活塞
5.下列关于萃取操作的说法正确的是( )
A.从碘水中提取碘,可用酒精作萃取剂
B.萃取操作完成后,静置分层,上、下层液体依次从下口放出
C.萃取时所选溶剂应与原溶剂互不相溶,且与溶质不反应
D.用一种有机溶剂提取水溶液中的某物质,静置分层,“水层”应在上层
6.(2023辽宁沈阳阶段练习)下列每组中各有三对物质,它们都能用分液漏斗分离的是( )
A.乙酸乙酯和水,酒精和水,植物油和水
B.四氯化碳和水,溴苯和水,硝基苯和水
C.甘油和水,乙酸和水,乙酸和乙醇
D.汽油和水,苯和水,甲醇和水
7.(经典题)乙酸异戊酯的有关信息如下表所示:
相对分 子质量 密度/ (g·cm-3) 沸点/ ℃ 水溶性
乙酸 异戊酯 130 0.867 142 难溶
实验室制备乙酸异戊酯,在洗涤、分液操作中,应充分振荡,然后静置,待分层后操作正确的是 ( )
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
题组三 重结晶
8.(经典题)(2023辽宁朝阳月考)某粗苯甲酸样品中含有少量氯化钠和泥沙。用重结晶法提纯苯甲酸,下列操作未涉及的是( )
A.加热溶解 B.冷却结晶
C.萃取后分液 D.趁热过滤
9.下列有关苯甲酸重结晶实验操作的说法正确的是( )
A.粗苯甲酸加热溶解后可以直接趁热过滤
B.趁热过滤时,为了防止苯甲酸结晶,可先将漏斗进行预热
C.趁热过滤后,为了析出更多晶体,热滤液用冰盐水充分冷却,同时缩短结晶的时间
D.温度越低,苯甲酸的溶解度越小,所以温度越低越有利于苯甲酸的重结晶实验
10.某同学拟用重结晶的方法除去某产品的杂质,为此需要选用合适的溶剂。具有下列特点的溶剂中,不可取的是( )
A.产品在溶剂中的溶解度随温度升高而迅速增大
B.在溶剂中产品比杂质更易溶解
C.杂质在溶剂中的溶解度在高温或低温时都很大
D.低温条件下产品在溶剂中极易溶解
11.如图表示物质A在4种溶剂W、X、Y、Z中的溶解度曲线。据此,用重结晶法提纯A时,最宜采用的溶剂是( )
A.W B.X
C.Y D.Z
12.乙酰苯胺是一种具有解热镇痛作用的白色晶体,某种乙酰苯胺样品中混入了少量氯化钠杂质。
已知:①20 ℃时乙酰苯胺在乙醇中的溶解度为36.9 g;
②氯化钠可分散在乙醇中形成胶体;
③乙酰苯胺在水中的溶解度如下表:
温度/℃ 25 50 80 100
溶解度/g 0.56 0.84 3.5 5.5
下列提纯乙酰苯胺使用的溶剂和操作方法都正确的是( )
A.水 分液
B.乙醇 过滤
C.水 重结晶
D.乙醇 重结晶
能力提升练
题组一 物质分离、提纯方法的选择
1.(2023广东广州三校期中联考,)下列实验中,所采取的分离方法或对应原理不正确的是( )
选项 目的 分离方法 原理
A 除去C2H6中的C2H4 洗气 C2H4能被酸性KMnO4溶液氧化,而C2H6不反应
B 分离苯和水 分液 苯和水不互溶
C 除去粗苯甲酸晶体中的沙子 重结晶 苯甲酸的溶解度受温度影响较大,沙子在水中的溶解度很小
D 分离苯和硝基苯 蒸馏 苯和硝基苯互溶,二者沸点相差较大
2.(经典题)(2022黑龙江大庆实验中学期中)青蒿素是治疗疟疾效果很好的药物,我国科学家屠呦呦因提取青蒿素用于治疗疟疾而获得诺贝尔奖,从中药中提取青蒿素的一种方法如图所示。
已知:①常温下,青蒿素是含有过氧基的倍半萜内酯的无色针状晶体,难溶于水,易溶于有机溶剂,熔点为156~157 ℃;
②乙醚的沸点为35 ℃,易燃;
③石油醚的沸点为30~80 ℃。
下列有关提取过程的叙述中不正确的是( )
A.“操作Ⅰ”需要用到的玻璃仪器只有分液漏斗、烧杯
B.若将乙醚用石油醚代替,也能达到实验目的
C.“操作Ⅲ”温度过高,会降低青蒿素的产率,其原因可能是青蒿素热稳定性差
D.“操作Ⅲ”包含了浓缩、结晶、过滤
题组二 有机化合物分离、提纯的综合应用
3.(2022湖北名校联盟联考)溴化苄是重要的有机合成工业原料,可由苯甲醇为原料合成,实验原理及装置(夹持、加热装置已略去)如图所示:
+HBr +H2O
相关物质的部分物理性质如表所示(常温常压下):
熔点/ ℃ 沸点/ ℃ 密度/ (g·cm-3) 溶解性
-15.3 205.7 1.04 微溶 于水
-3.0 199 1.44 不溶于水, 易溶于醇
下列有关说法不正确的是( )
A.先加热至反应温度,然后从冷凝管接口b处通水
B.该实验适宜水浴加热
C.浓硫酸作催化剂和吸水剂
D.反应液可按下列步骤分离、提纯:静置→分液→水洗→碱洗→水洗→干燥→减压蒸馏
4.(经典题)绿原酸具有抗病毒、降血压、抗氧化等作用。利用乙醚、95%乙醇浸泡杜仲干叶,得到提取液,进一步提取绿原酸的流程如下:
已知:常温下,绿原酸难溶于水,易溶于乙醚等有机溶剂。
下列说法错误的是( )
A.从“提取液”获取“有机层”的操作为萃取、分液
B.减压蒸馏时选用球形冷凝管
C.过滤时所需玻璃仪器有烧杯、漏斗、玻璃棒
D.绿原酸粗产品可通过重结晶的方法提纯
5.(2022江苏高邮期中统考)苯甲醇与苯甲酸都是常见化工原料,在化工生产中有广泛应用。工业上常在碱性条件下以苯甲醛作原料来制备苯甲醇和苯甲酸。某实验室模拟其生产过程,实验原理、实验步骤如下。
实验原理:
2+KOH +(该反应为放热反应)
相关资料:
①相关物质的物理性质如下表:
名称 相对分 子质量 熔点/℃ 沸点/℃ 溶解性
水 醇 醚
苯甲醛 106 -26 179.62 微溶 易溶 易溶
苯甲酸 122 122.13 249 微溶 易溶 易溶
苯甲醇 108 -15.3 205.7 微溶 易溶 易溶
乙醚 74 -116.3 34.6 微溶 易溶 —
②苯甲醛在空气中极易被氧化,生成白色苯甲酸。
实验步骤如下:
Ⅰ.向盛有足量KOH溶液的反应器中分批加入13.5 mL(14.0 g)苯甲醛,持续搅拌至反应混合物变成白色蜡糊状A,转移至锥形瓶中静置24小时以上。反应装置如图1所示。
图1
Ⅱ.步骤Ⅰ所得产物后续处理过程如图2所示。
图2
回答下列问题:
(1)仪器a的名称为 。
(2)步骤Ⅰ中苯甲醛需要分批加入且适时冷却,其原因是 。
(3)已知:苯甲醛可与饱和NaHSO3溶液反应。为获取产品1,将乙醚萃取液依次用饱和亚硫酸氢钠溶液、10%碳酸钠溶液和水进行洗涤并分液。乙醚萃取液的密度小于水,取分液后 (填“上”或“下”)层液体加入无水MgSO4,其作用为 ;操作①含多步操作,其中最后一步操作是对乙醚和产品1进行分离,其名称为 。
(4)水层中加入浓盐酸发生反应的离子方程式为 。
(5)操作②包含溶解、蒸发浓缩、冷却结晶、过滤、晾干等,下列仪器中在该操作中不需要用到的有 (填字母)。
A.分液漏斗 B.蒸发皿 C.研钵 D.玻璃棒
(6)①若产品2产率比预期值稍高,可能原因是 。
A.未彻底晾干
B.产品中混有其他杂质
C.过滤时滤液浑浊
D.部分苯甲醛被直接氧化为苯甲酸
②产品2经干燥后称量,质量为6.1 g,计算其产率为 (保留3位有效数字)。
答案与分层梯度式解析
第二节 研究有机化合物的一般方法
第1课时 有机化合物的分离、提纯
基础过关练
1.D 2.C 3.C 4.D 5.C 6.B 7.D 8.C
9.B 10.D 11.D 12.C
1.D 为防止液体暴沸,加热前应在蒸馏烧瓶中放入碎瓷片,A正确;蒸馏是利用沸点差异,实现物质的分离,自来水中的Cl-等杂质构成的物质沸点高,不会随水一起蒸出,B正确;水蒸气冷凝时冷凝管中水采用逆流方式,冷凝效果更好,则冷却水应该是下口进上口出,与水蒸气的流向相反,C正确;开始蒸馏时,应先通冷却水再加热,蒸馏完毕,应该先撤酒精灯再关冷却水,D错误。
2.C 根据题表中的信息可知,A和B的沸点相差较大,可利用蒸馏法分离A和B。
3.C 在蒸馏时,沸点较低的物质先馏出,所以沸点较低的汽油比沸点较高的柴油先馏出,A正确;碎瓷片具有防暴沸作用,所以蒸馏烧瓶中放入碎瓷片可防止蒸馏时发生暴沸,B正确;冷凝管中水采用逆流方式,冷凝效果更好,所以冷却水应该从b口进a口出,C错误;温度计用来测量馏分温度,则温度计水银球位于蒸馏烧瓶支管口处,D正确。
4.D 一只手压住玻璃塞,另一只手握住活塞,把分液漏斗倒转过来振荡,A错误;振荡几次后打开活塞放气,不需打开分液漏斗上口的玻璃塞放气,B错误;将分液漏斗放在铁架台上静置待液体分层,C错误;分液时将分液漏斗颈上的玻璃塞打开或使玻璃塞上的凹槽对准漏斗上的小孔,再打开活塞,待下层液体流尽时,关闭活塞,从上口倒出上层液体,D正确。
5.C 酒精与水互溶,从碘水中提取碘,不能用酒精作萃取剂,A错误;萃取操作完成后,静置分层,下层液体从下口放出,上层液体从上口倒出,B错误;题中未给出萃取剂和水的密度关系,萃取后“水层”可能在上层,也可能在下层,D错误。
6.B A项,酒精和水互溶,不能用分液漏斗分离,错误;B项,三组混合物均互不相溶,可用分液漏斗分离,正确;C项,三组混合物均互溶,不能用分液漏斗分离,错误;D项,甲醇和水互溶,不能用分液漏斗分离,错误。
7.D 乙酸异戊酯的密度比水小且难溶于水,分层后水层在下层,应先将水层从分液漏斗的下口放出,再将上层的乙酸异戊酯从上口倒出。
8.C 将粗苯甲酸加热溶解,可增大苯甲酸的溶解度,A不符合题意;趁热过滤后的滤液冷却后可析出苯甲酸晶体,B不符合题意;用重结晶法提纯苯甲酸的实验操作中不涉及萃取、分液,C符合题意;加热溶解后的固液混合物需要趁热过滤,以减少苯甲酸的损失,D不符合题意。
9.B 粗苯甲酸加热溶解后,考虑到过滤时溶液与环境的温差较大,易使苯甲酸晶体提前析出,滞留在过滤器中,故需在过滤前适当稀释,不能直接过滤,A项错误;趁热过滤后,用冰盐水冷却形成的结晶很小,表面积大,吸附的杂质多,C项错误;重结晶过程中温度太低,杂质的溶解度也会降低,部分杂质也会析出,D项错误。
10.D 根据重结晶的实验原理可知,如果低温条件下产品在溶剂中极易溶解,则该物质很难结晶析出。
规律方法 结晶的三种类型
(1)蒸发结晶:将溶剂蒸发获取晶体,此法适用于溶解度随温度变化不大的物质,如海水晒盐。
(2)降温结晶:将热的饱和溶液慢慢冷却后析出晶体,此法适用于溶解度随温度变化较大的物质,如从NaCl、KNO3的混合液中得KNO3晶体。
(3)重结晶:将待提纯固体混合物用蒸馏水溶解,经过滤、蒸发浓缩、冷却等步骤,再次析出晶体,得到更纯净的晶体的过程,如提纯粗苯甲酸。
11.D 通常重结晶要求被提纯的物质在溶剂中的溶解度受温度的影响较大,能够进行冷却结晶,故最宜采用Z作溶剂。
12.C 本题为情境信息题,主要考查选择合适的分离、提纯方法。解答基本思路:阅读题目,提取有用信息→结合被提纯物质与杂质性质的差异,确定合适的分离、提纯方法→结合选项解答问题。根据题表可知,乙酰苯胺在水中的溶解度随温度变化较大,而氯化钠在水中的溶解度随温度变化较小,故采用重结晶法提纯乙酰苯胺;根据已知信息①②可知,20 ℃时乙酰苯胺在乙醇中的溶解度大,NaCl可分散在乙醇中形成胶体,故不能选乙醇作溶剂通过重结晶法提纯乙酰苯胺。
能力提升练
1.A 2.A 3.A 4.B
1.A C2H4能被酸性KMnO4溶液氧化生成CO2,引入了新杂质,A错误;苯和水互不相溶,可用分液法分离苯和水,B正确;沙子难溶于水,苯甲酸的溶解度受温度影响较大,可用重结晶法除去粗苯甲酸晶体中的沙子,C正确;苯和硝基苯为互溶的两种液体,分离二者可利用沸点差异进行蒸馏,D正确。
方法技巧 有机化合物分离、提纯方法的选择
(1)首先要熟记各种分离、提纯方法的适用范围。常见的分离、提纯有机物的方法及适用范围如下表:
方法 适用范围
分液 互不相溶的两种液体
萃取 同温度下溶质在两种互不相溶的溶剂中的溶解度相差很大
蒸馏 互溶的液态有机物,沸点相差较大(一般大于30 ℃)且热稳定性强
重结晶 固体混合物,被提纯有机物在溶剂中的溶解度受温度影响较大,杂质在溶剂中的溶解度很大或很小
(2)根据给定混合物的状态、溶解性以及熔、沸点的差异等,选择合适的方法即可。
2.A 结合图示流程可知操作Ⅰ是过滤,需要用到的玻璃仪器有烧杯、漏斗、玻璃棒,A错误;乙醚的沸点为35 ℃,石油醚的沸点为30~80 ℃,青蒿素易溶于乙醚和石油醚,若将乙醚用石油醚代替,也能达到实验目的,B正确;青蒿素分子中含有过氧基,热稳定性差,“操作Ⅲ”温度过高,可能会使青蒿素分解,降低产率,C正确;“操作Ⅲ”包含了浓缩、结晶、过滤等操作,D正确。
3.A 为防止反应物受热挥发损失,应先从冷凝管接口b处通水,再加热至反应温度,A错误;该实验反应温度在100 ℃以下,适宜水浴加热,以便控制温度,B正确;由实验原理可知,浓硫酸作催化剂和吸水剂,产物中有水,浓硫酸吸水,促进反应进行更完全,C正确;反应结束后,反应液中含苯甲醇、浓硫酸、HBr、溴化苄、H2O等,经选项中的系列操作后可得较纯净的溴化苄,D正确。
归纳总结 当反应混合物需要加热,且加热温度不超过100 ℃时,可使用水浴加热。水浴加热的优点:便于控制温度,且可使反应物均匀受热。
4.B 由流程图可知,乙酸乙酯作萃取剂,从“提取液”得到“有机层”的实验操作为萃取、分液,A正确;减压蒸馏时若选用球形冷凝管,会有一部分馏分经冷凝后滞留在冷凝管中,而不能进入接收器中,B错误;过滤时所需玻璃仪器有烧杯、漏斗、玻璃棒,C正确;常温下绿原酸难溶于水,易溶于有机溶剂,可利用重结晶的方法进一步提纯,D正确。
5.答案 (1)球形冷凝管
(2)使反应不太剧烈,降低反应温度,避免苯甲醛、苯甲醇的挥发,减少副反应的发生,提高产率(答案合理即可)
(3)上 作干燥剂,除水 蒸馏
(4)+H+ ↓
(5)AC
(6)①ABD ②75.7%
解析 【流程梳理】结合实验流程图,可对本实验中物质A的分离、提纯过程进行如下梳理:
根据图示装置可知,仪器a的名称为球形冷凝管。(2)因为该反应是放热反应,温度过高,反应过于剧烈,会导致苯甲醛、苯甲醇挥发,同时也会使副反应产物增多,使产品的产率降低,所以在步骤Ⅰ中需分批加入苯甲醛且适时冷却,这样做既能减缓反应速率,又能提高产品产率。(3)由于乙醚萃取液的密度小于水,故苯甲醇的乙醚溶液在上层,取分液后上层液体,向其中加入无水MgSO4,进行干燥。产品1为苯甲醇,乙醚与苯甲醇互溶,二者沸点相差较大,故采用蒸馏法分离。(4)水层中含苯甲酸钾,加入浓盐酸,发生反应生成微溶于水的苯甲酸和易溶于水的KCl,反应的离子方程式为+H+ ↓。(5)操作②包含溶解、蒸发浓缩、冷却结晶、过滤、晾干等,不需要的仪器有分液漏斗和研钵,故选A、C。(6)①若过滤后未干燥完全,会导致苯甲酸产率偏高,A正确;若产品中混有其他杂质,测得苯甲酸的质量偏大,其产率偏高,B正确;若过滤时滤液浑浊,有部分苯甲酸滞留在滤液中,测得苯甲酸的质量偏小,其产率偏低,C错误;若部分苯甲醛被直接氧化为苯甲酸,测得苯甲酸的质量偏大,其产率偏高,D正确。②根据关系式:2C6H5CHO~C6H5COOH,参加反应的苯甲醛质量是14.0 g,则理论上生成m(苯甲酸)=××122 g·
mol-1≈8.06 g,实际产量是6.1 g,则苯甲酸的产率为×100%≈
75.7%。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
