2024人教版高中化学选择性必修3同步练习题--第2课时 有机化合物中的共价键(含解析)
文档属性
| 名称 | 2024人教版高中化学选择性必修3同步练习题--第2课时 有机化合物中的共价键(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-20 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2024人教版高中化学选择性必修3同步
第2课时 有机化合物中的共价键
基础过关练
题组一 共价键的类型
1.烷烃分子中的碳原子与其他原子的结合方式是 ( )
A.每个碳原子形成4对共用电子对
B.通过非极性键
C.通过两个共价键
D.通过离子键和共价键
2.(经典题)(2023河北武安月考)下列说法错误的是 ( )
A.有机化合物都含有极性键和非极性键
B.有机化合物一定含有σ键,不一定含有π键
C.1个碳原子可以与其他原子形成4个共价键
D.乙烯和乙炔都含有π键,都能发生加成反应
3.(2022黑龙江佳木斯四校期末联考)关于有机化合物中碳原子的成键特点,下列叙述不正确的是 ( )
A.碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键
B.常温下碳原子性质活泼,可以跟多种元素原子形成共价键
C.碳原子之间既可以形成单键,又可以形成双键或三键
D.多个碳原子之间可以结合成碳链(可以带有支链),也可以结合成碳环,构成有机物链状或环状的碳骨架
4.乙烯的空间填充模型如图所示,乙烯分子中有5个σ键和1个π键。下列有关乙烯分子的叙述正确的是( )
A.碳原子的sp2杂化轨道形成σ键,未杂化的2p轨道形成π键
B.碳原子的sp2杂化轨道形成π键,未杂化的2p轨道形成σ键
C.两个碳原子的杂化方式为sp
D.碳原子之间的σ键是由碳原子的sp2杂化轨道形成的,碳原子与氢原子之间的π键是未参加杂化的2p轨道形成的
5.(2022山西大同名校联考)下列物质的分子所含原子中,既有sp3杂化,又有sp杂化的是( )
A.乙酸
B.甲酸甲酯()
C.丙烯腈()
D.丙炔()
6.(经典题)(2022辽宁大连开学考)碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如图所示。下列有关该物质的说法不正确的是 ( )
A.分子式为C3H4O3
B.分子中σ键与π键个数之比为10∶1
C.分子中既有极性键也有非极性键
D.分子中碳原子的杂化方式全部为sp2
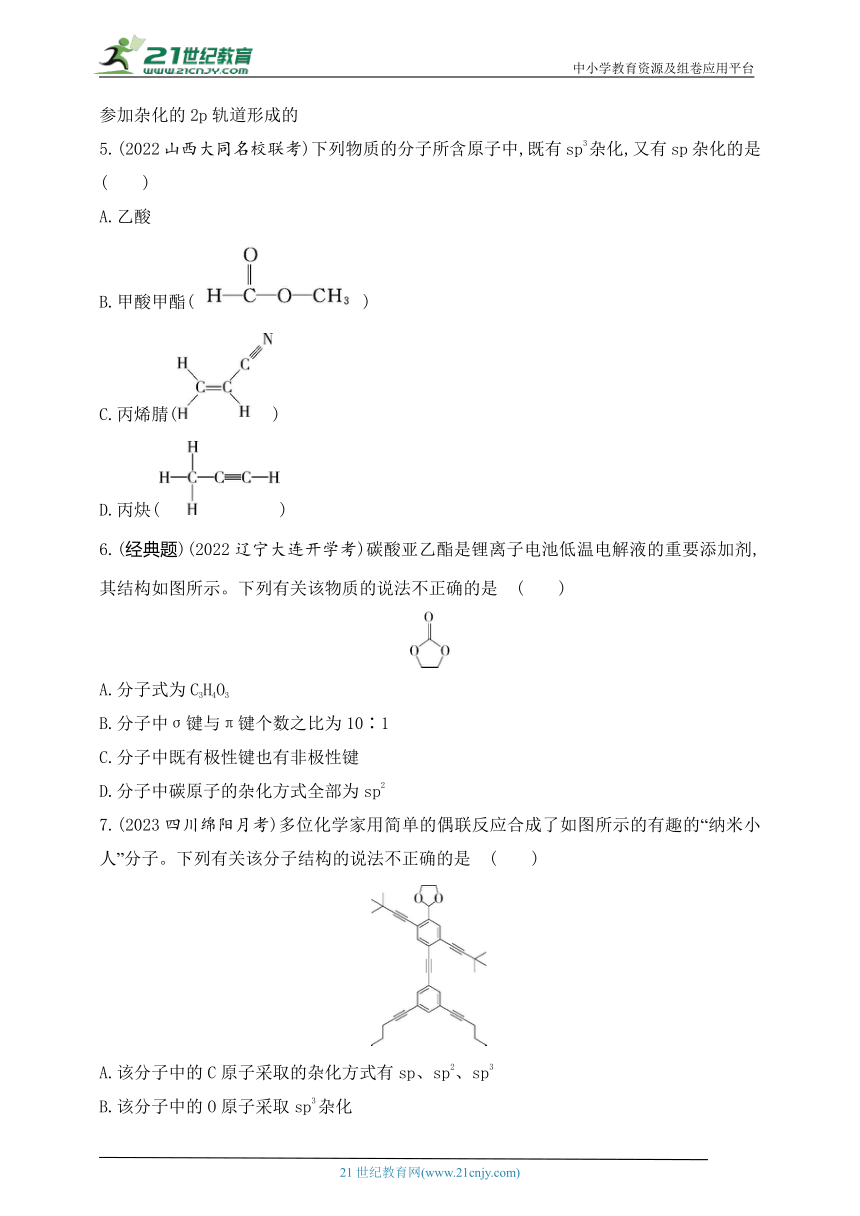
7.(2023四川绵阳月考)多位化学家用简单的偶联反应合成了如图所示的有趣的“纳米小人”分子。下列有关该分子结构的说法不正确的是 ( )
A.该分子中的C原子采取的杂化方式有sp、sp2、sp3
B.该分子中的O原子采取sp3杂化
C.“纳米小人”头部的所有原子在同一平面内
D.该分子中既含σ键,又含π键
8.有下列物质:
①CH3CH3 ②CH3—CHCH—CH3
③ ④CH3CH2OH
(1)上述4种有机物分子中只含有σ键的有 (填序号)。
(2)②分子中σ键与π键的个数比为 。
(3)②③分子中碳原子的杂化类型有 。
题组二 共价键的极性与有机反应
9.(2022浙江杭州九中月考)下列说法错误的是( )
A.一般仅含σ键的烃易发生取代反应,含有π键的烃易发生加成反应
B.一般共价键极性越强,在反应中越容易发生断裂
C.有机化合物分子中基团之间的相互影响不会影响官能团和物质的性质
D.乙醇分子和水分子中的氢氧键极性不同,所以乙醇和水分别与钠反应的剧烈程度不同
10.下列说法不正确的是( )
A.有机物分子中共价键的极性越强,越稳定
B.有机物分子中碳原子间可以形成单键、双键或三键,但每个碳原子成键总数相同
C.共用电子偏向吸电子能力强的一方,形成的共价键是极性键
D.共价键是否具有极性及极性强弱对有机化合物的性质有重要影响
11.(经典题)(2022吉林长春期末)乙酸、水和乙醇的分子结构如表所示,三者结构的相同点是都含有羟基。下列说法错误的是( )
物质 结构
乙酸
水
乙醇 CH3—CH2—OH
A.羟基的极性:乙酸>水>乙醇
B.与金属钠反应的剧烈程度:水>乙醇
C.羟基连接不同的基团可影响羟基的活性
D.羟基极性不同的原因是羟基中的共价键类型不同
12.有机化合物的结构和性质有着密切的关系。如果已知某种有机化合物的结构,我们就可以根据结构预测其性质。
(1)乙烯分子的碳碳双键中,π键容易发生断裂。乙炔分子()中有两个π键,将乙炔分别通入酸性高锰酸钾溶液和溴的四氯化碳溶液中,现象分别是 、 。
(2)乙酸与乙醇发生酯化反应的化学方程式为 ,根据乙酸与乙醇发生酯化反应的原理,说明乙酸分子结构中极性较大的共价键是 。
(3)苯酚()俗称石炭酸,是一种一元弱酸,电离方程式为 +H+,苯酚分子中O—H键的极性 水分子中O—H键的极性。(填“>”“<”或“=”)
答案与分层梯度式解析
第2课时 有机化合物中的共价键
基础过关练
1.A 2.A 3.B 4.A 5.D 6.D 7.C 9.C
10.A 11.D
1.A 碳原子最外层有4个电子,烷烃分子中每个碳原子形成4个共价键,即形成4对共用电子对,A正确;烷烃分子中碳原子间可形成非极性共价键,碳、氢原子间形成极性键,B、C、D均错误。
2.A 甲烷、甲醇等物质中均只含极性键,不含非极性键,A错误;有机化合物一定含σ键,不一定含π键,B正确;1个碳原子最多能和其他原子形成4个共价键,C正确;乙烯、乙炔中分别含碳碳双键、碳碳三键,都含π键,都能发生加成反应,D正确。
3.B 碳原子最外层有4个电子,碳原子与碳原子、其他原子(如氢原子)形成4个共价键,达到稳定结构,故A正确;常温下碳原子性质不活泼,故B错误;碳原子最外层有4个电子,碳原子之间可以形成单键,也可以形成双键或三键,不仅可以形成碳链,还可以形成碳环,故C、D正确。
4.A 乙烯分子中每个碳原子均采取sp2杂化,其中杂化轨道形成σ键,未杂化的2p轨道形成π键。
5.D CH3COOH中甲基、羧基中的碳原子分别采取sp3、sp2杂化,A错误;中酯基、甲基中的碳原子分别采取sp2、sp3杂化,B错误;丙烯腈中双键碳原子采取sp2杂化,另一碳原子采取sp杂化,C错误;丙炔中甲基中的碳原子采取sp3杂化,碳碳三键中的碳原子采取sp杂化,D正确。
6.D 根据该物质的结构可知分子式为C3H4O3,故A正确。共价单键为σ键,共价双键中含有1个σ键、1个π键,则1个该分子中含有10个σ键、1个π键,分子中σ键与π键个数之比为10∶1,故B正确。该分子中存在C—C非极性键、C—O极性键、C—H极性键,故C正确。该分子中C—C键中C原子的杂化方式为sp3,CO键中C原子的杂化方式为sp2,故D错误。
7.C 该分子中碳碳三键中的碳原子采取sp杂化,苯环中的碳原子采取sp2杂化,其他碳原子采取sp3杂化,A正确;该分子中每个氧原子形成2个σ键,还有2对孤电子对,故氧原子采取sp3杂化,B正确;“纳米小人”头部的碳原子均为sp3杂化,故头部的所有原子不可能在同一平面内,C错误;该分子中所有单键都是σ键,含有碳碳三键,故含有π键,D正确。
8.答案 (1)①④ (2)11∶1 (3)sp3、sp2、sp
解析 (1)单键都是σ键,双键中有1个σ键和1个π键。(2)1个CH3—CHCH—CH3分子中有11个σ键,1个π键。(3)单键碳原子为sp3杂化,双键碳原子为sp2杂化,三键碳原子为sp杂化。
9.C 仅含σ键的烃中只含单键,易发生取代反应,含π键的烃中含碳碳双键或碳碳三键等不饱和键,一般易发生加成反应,A正确;一般共价键极性越强,在反应中越容易断裂,B正确;有机物分子中基团间的相互影响使官能团中化学键的极性发生变化,从而影响官能团和物质的性质,C错误;乙醇分子中氢氧键的极性比水分子中氢氧键的极性弱,水分子中O—H键更容易断裂,故乙醇和水分别与钠反应的剧烈程度不同,D正确。
10.A 有机物中共价键的极性越强,越活泼,A错误;碳原子最外层电子数为4,有机物分子中碳原子间可形成单键、双键或三键,但每个碳原子均形成4对共用电子对,即成键总数相同,B正确;共用电子对将偏向吸引电子能力强的一方,形成的共价键是极性键,C正确;共价键是否具有极性及极性强弱对有机化合物的性质有重要影响,如CH3CH2OH中存在C—O、O—H极性键,其化学性质主要体现在这两个极性键上,D正确。
11.D 与Na反应越剧烈,羟基氢原子的活泼性越强,对应羟基的极性越强,与Na反应的剧烈程度:乙酸>水>乙醇,则羟基的极性:乙酸>水>乙醇,A、B正确;有机物分子中基团间相互影响,则羟基连接不同的基团可影响羟基的活性,C正确;羟基中的共价键类型相同,羟基极性不同的原因是羟基连接的基团不同,D错误。
12.答案 (1)酸性高锰酸钾溶液褪色 溴的四氯化碳溶液褪色
(2)CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O C—O键
(3)>
解析 (1)的性质与乙烯相似,乙炔分子中有两个π键,不稳定,容易发生断裂,所以乙炔能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色。(2)乙酸与乙醇发生酯化反应时“酸脱羟基、醇脱氢”,说明乙酸分子中的C—O键的极性较大,容易发生断裂。(3)苯酚分子中O—H键比水分子中O—H键易断裂,苯酚分子中O—H键的极性较大。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024人教版高中化学选择性必修3同步
第2课时 有机化合物中的共价键
基础过关练
题组一 共价键的类型
1.烷烃分子中的碳原子与其他原子的结合方式是 ( )
A.每个碳原子形成4对共用电子对
B.通过非极性键
C.通过两个共价键
D.通过离子键和共价键
2.(经典题)(2023河北武安月考)下列说法错误的是 ( )
A.有机化合物都含有极性键和非极性键
B.有机化合物一定含有σ键,不一定含有π键
C.1个碳原子可以与其他原子形成4个共价键
D.乙烯和乙炔都含有π键,都能发生加成反应
3.(2022黑龙江佳木斯四校期末联考)关于有机化合物中碳原子的成键特点,下列叙述不正确的是 ( )
A.碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键
B.常温下碳原子性质活泼,可以跟多种元素原子形成共价键
C.碳原子之间既可以形成单键,又可以形成双键或三键
D.多个碳原子之间可以结合成碳链(可以带有支链),也可以结合成碳环,构成有机物链状或环状的碳骨架
4.乙烯的空间填充模型如图所示,乙烯分子中有5个σ键和1个π键。下列有关乙烯分子的叙述正确的是( )
A.碳原子的sp2杂化轨道形成σ键,未杂化的2p轨道形成π键
B.碳原子的sp2杂化轨道形成π键,未杂化的2p轨道形成σ键
C.两个碳原子的杂化方式为sp
D.碳原子之间的σ键是由碳原子的sp2杂化轨道形成的,碳原子与氢原子之间的π键是未参加杂化的2p轨道形成的
5.(2022山西大同名校联考)下列物质的分子所含原子中,既有sp3杂化,又有sp杂化的是( )
A.乙酸
B.甲酸甲酯()
C.丙烯腈()
D.丙炔()
6.(经典题)(2022辽宁大连开学考)碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如图所示。下列有关该物质的说法不正确的是 ( )
A.分子式为C3H4O3
B.分子中σ键与π键个数之比为10∶1
C.分子中既有极性键也有非极性键
D.分子中碳原子的杂化方式全部为sp2
7.(2023四川绵阳月考)多位化学家用简单的偶联反应合成了如图所示的有趣的“纳米小人”分子。下列有关该分子结构的说法不正确的是 ( )
A.该分子中的C原子采取的杂化方式有sp、sp2、sp3
B.该分子中的O原子采取sp3杂化
C.“纳米小人”头部的所有原子在同一平面内
D.该分子中既含σ键,又含π键
8.有下列物质:
①CH3CH3 ②CH3—CHCH—CH3
③ ④CH3CH2OH
(1)上述4种有机物分子中只含有σ键的有 (填序号)。
(2)②分子中σ键与π键的个数比为 。
(3)②③分子中碳原子的杂化类型有 。
题组二 共价键的极性与有机反应
9.(2022浙江杭州九中月考)下列说法错误的是( )
A.一般仅含σ键的烃易发生取代反应,含有π键的烃易发生加成反应
B.一般共价键极性越强,在反应中越容易发生断裂
C.有机化合物分子中基团之间的相互影响不会影响官能团和物质的性质
D.乙醇分子和水分子中的氢氧键极性不同,所以乙醇和水分别与钠反应的剧烈程度不同
10.下列说法不正确的是( )
A.有机物分子中共价键的极性越强,越稳定
B.有机物分子中碳原子间可以形成单键、双键或三键,但每个碳原子成键总数相同
C.共用电子偏向吸电子能力强的一方,形成的共价键是极性键
D.共价键是否具有极性及极性强弱对有机化合物的性质有重要影响
11.(经典题)(2022吉林长春期末)乙酸、水和乙醇的分子结构如表所示,三者结构的相同点是都含有羟基。下列说法错误的是( )
物质 结构
乙酸
水
乙醇 CH3—CH2—OH
A.羟基的极性:乙酸>水>乙醇
B.与金属钠反应的剧烈程度:水>乙醇
C.羟基连接不同的基团可影响羟基的活性
D.羟基极性不同的原因是羟基中的共价键类型不同
12.有机化合物的结构和性质有着密切的关系。如果已知某种有机化合物的结构,我们就可以根据结构预测其性质。
(1)乙烯分子的碳碳双键中,π键容易发生断裂。乙炔分子()中有两个π键,将乙炔分别通入酸性高锰酸钾溶液和溴的四氯化碳溶液中,现象分别是 、 。
(2)乙酸与乙醇发生酯化反应的化学方程式为 ,根据乙酸与乙醇发生酯化反应的原理,说明乙酸分子结构中极性较大的共价键是 。
(3)苯酚()俗称石炭酸,是一种一元弱酸,电离方程式为 +H+,苯酚分子中O—H键的极性 水分子中O—H键的极性。(填“>”“<”或“=”)
答案与分层梯度式解析
第2课时 有机化合物中的共价键
基础过关练
1.A 2.A 3.B 4.A 5.D 6.D 7.C 9.C
10.A 11.D
1.A 碳原子最外层有4个电子,烷烃分子中每个碳原子形成4个共价键,即形成4对共用电子对,A正确;烷烃分子中碳原子间可形成非极性共价键,碳、氢原子间形成极性键,B、C、D均错误。
2.A 甲烷、甲醇等物质中均只含极性键,不含非极性键,A错误;有机化合物一定含σ键,不一定含π键,B正确;1个碳原子最多能和其他原子形成4个共价键,C正确;乙烯、乙炔中分别含碳碳双键、碳碳三键,都含π键,都能发生加成反应,D正确。
3.B 碳原子最外层有4个电子,碳原子与碳原子、其他原子(如氢原子)形成4个共价键,达到稳定结构,故A正确;常温下碳原子性质不活泼,故B错误;碳原子最外层有4个电子,碳原子之间可以形成单键,也可以形成双键或三键,不仅可以形成碳链,还可以形成碳环,故C、D正确。
4.A 乙烯分子中每个碳原子均采取sp2杂化,其中杂化轨道形成σ键,未杂化的2p轨道形成π键。
5.D CH3COOH中甲基、羧基中的碳原子分别采取sp3、sp2杂化,A错误;中酯基、甲基中的碳原子分别采取sp2、sp3杂化,B错误;丙烯腈中双键碳原子采取sp2杂化,另一碳原子采取sp杂化,C错误;丙炔中甲基中的碳原子采取sp3杂化,碳碳三键中的碳原子采取sp杂化,D正确。
6.D 根据该物质的结构可知分子式为C3H4O3,故A正确。共价单键为σ键,共价双键中含有1个σ键、1个π键,则1个该分子中含有10个σ键、1个π键,分子中σ键与π键个数之比为10∶1,故B正确。该分子中存在C—C非极性键、C—O极性键、C—H极性键,故C正确。该分子中C—C键中C原子的杂化方式为sp3,CO键中C原子的杂化方式为sp2,故D错误。
7.C 该分子中碳碳三键中的碳原子采取sp杂化,苯环中的碳原子采取sp2杂化,其他碳原子采取sp3杂化,A正确;该分子中每个氧原子形成2个σ键,还有2对孤电子对,故氧原子采取sp3杂化,B正确;“纳米小人”头部的碳原子均为sp3杂化,故头部的所有原子不可能在同一平面内,C错误;该分子中所有单键都是σ键,含有碳碳三键,故含有π键,D正确。
8.答案 (1)①④ (2)11∶1 (3)sp3、sp2、sp
解析 (1)单键都是σ键,双键中有1个σ键和1个π键。(2)1个CH3—CHCH—CH3分子中有11个σ键,1个π键。(3)单键碳原子为sp3杂化,双键碳原子为sp2杂化,三键碳原子为sp杂化。
9.C 仅含σ键的烃中只含单键,易发生取代反应,含π键的烃中含碳碳双键或碳碳三键等不饱和键,一般易发生加成反应,A正确;一般共价键极性越强,在反应中越容易断裂,B正确;有机物分子中基团间的相互影响使官能团中化学键的极性发生变化,从而影响官能团和物质的性质,C错误;乙醇分子中氢氧键的极性比水分子中氢氧键的极性弱,水分子中O—H键更容易断裂,故乙醇和水分别与钠反应的剧烈程度不同,D正确。
10.A 有机物中共价键的极性越强,越活泼,A错误;碳原子最外层电子数为4,有机物分子中碳原子间可形成单键、双键或三键,但每个碳原子均形成4对共用电子对,即成键总数相同,B正确;共用电子对将偏向吸引电子能力强的一方,形成的共价键是极性键,C正确;共价键是否具有极性及极性强弱对有机化合物的性质有重要影响,如CH3CH2OH中存在C—O、O—H极性键,其化学性质主要体现在这两个极性键上,D正确。
11.D 与Na反应越剧烈,羟基氢原子的活泼性越强,对应羟基的极性越强,与Na反应的剧烈程度:乙酸>水>乙醇,则羟基的极性:乙酸>水>乙醇,A、B正确;有机物分子中基团间相互影响,则羟基连接不同的基团可影响羟基的活性,C正确;羟基中的共价键类型相同,羟基极性不同的原因是羟基连接的基团不同,D错误。
12.答案 (1)酸性高锰酸钾溶液褪色 溴的四氯化碳溶液褪色
(2)CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O C—O键
(3)>
解析 (1)的性质与乙烯相似,乙炔分子中有两个π键,不稳定,容易发生断裂,所以乙炔能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色。(2)乙酸与乙醇发生酯化反应时“酸脱羟基、醇脱氢”,说明乙酸分子中的C—O键的极性较大,容易发生断裂。(3)苯酚分子中O—H键比水分子中O—H键易断裂,苯酚分子中O—H键的极性较大。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
