2023—2024学年鲁教版化学九年级上册第四单元 我们周围的空气 跟踪选题(含答案)
文档属性
| 名称 | 2023—2024学年鲁教版化学九年级上册第四单元 我们周围的空气 跟踪选题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 232.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-20 00:00:00 | ||
图片预览



文档简介
2023—2024学年鲁教版化学九年级上册第四单元 我们周围的空气 跟踪选题含答案
鲁教版第四单元 我们周围的空气
一、选择题。(16题)
1、每年的6月5日世界环境日,环境保护是我国的一项基本国策,空气的净化日益受到人们的关注.下列气体组中的各种气体都属于空气污染物的是( )
A.二氧化硫 一氧化碳 二氧化氮
B.二氧化碳 一氧化碳 二氧化硫
C.一氧化碳 二氧化碳 氮气
D.氮气 二氧化氮 一氧化碳
2、高铁酸钠(Na2FeO4)中,铁元素的化合价是( )
A.+2 B.+3 C.+6 D.+7
3、下列关于氧气的说法正确的是( )
A.分离液态空气获得氧气是化学变化
B.植物的光合作用会消耗氧气
C.氧气的化学性质不活泼
D.液态氧可用作火箭助燃剂
4、下列有关氧气的说法错误的是 ( )
A.能燃烧 B.无色 C.无味 D.能供给呼吸
5、根据化学式C6H2Cl4,判断下列说法正确的是( )
A.该物质属于化合物
B.该物质的相对分子质量为216g
C.该物质的一个分子中含有一个氢分子
D.该分子中碳元素质量分数大于氯元素
6、实验室用燃烧法测定空气中氧气的含量,最适宜选用的物质是( )
A.木炭 B.红磷 C.硫磺 D.铁丝
7、虾青素(C40H52O4)是一种具有极强的抗肿瘤、抗氧化性能的物质,可增强动物免疫力.下列有关它的说法正确的是( )
A.虾青素是一种氧化物
B.虾青素中碳、氢、氧元素的质量比为10:13:1
C.虾青素的相对分子质量是596
D.虾青素是由96个原子构成
8、下列关于物质的变化说法不正确的是( )
A.葡萄酿酒是化学变化
B.红磷燃烧是化学变化
C.工业制氧气和实验室制取氧气都是化学变化
D.干冰升华是物理变化
9、实验室制取气体选择收集方法时,下列气体性质不需考虑的是 ( )
A.密度 B.可燃性 C.溶解性 D.能否与水反应
10、下列说法正确的是( )
A.有氧气参加的反应都是化合反应
B.化合反应一定是氧化反应
C.化合反应不一定是氧化反应,氧化反应也不一定是化合反应
D.分解反应的特点是两种物质反应生成两种或两种以上的物质
11、下列气体在洁净空气中不应该含有的是( )
A.氧气 B.氮气 C.稀有气体 D.二氧化硫
12、已知一种碳﹣12原子的质量为mg,另一种原子的质量为ng,则该原子的相对原子质量为( )
A. B. C.n D.
13、下列物质属于氧化物的是( )
A.O3 B.SO3 C.NaOH D.K2SO4
14、下列物质在空气或氧气中燃烧时的现象描述正确的是 ( )
A.红磷在空气中燃烧,产生大量白烟,放出热量,生成白色气体
B.铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成四氧化三铁
C.木炭在氧气中燃烧,发出红光,放出热量,产生能使石灰水变浑浊的气体
D.镁带在空气中燃烧,发出白光,放热,生成白色固体
15、婴儿“尿不湿”最关键的材料是聚丙烯酸钠,它是由丙烯酸(C3H4O2)与氢氧化钠经过一系列的复杂反应而制得。下列有关丙烯酸(C3H4O2)的说法正确的是( )
A.丙烯酸中氢元素的质量分数最大
B.丙烯酸是由碳、氢、氧三种元素组成
C.丙烯酸中碳、氢、氧元素的质量比是3:4:2
D.丙烯酸是由3个碳原子4个氢原子和2个氧原子构成
16、利用如图装置验证了空气中氧气的含量。下列叙述不正确的是( )
A.实验前需检查装置气密性
B.白磷的作用是消耗试管中的氧气
C.白磷熄火、试管冷却后再打开止水夹
D.最终量筒中液面约降至40mL刻度线处
二、填空题。
17、实验是学习化学的一条重要途径,正确的实验操作是实验成功的关键。造成下列实验后果的原因可能是:
(1)加热固体时试管炸裂_______ ;(任答一条原因即可,下同)
(2)用量筒量取一定量体积的水时,实际量得的体积偏大_______ ;
(3)在用红磷燃烧测定空气里氧气含量的实验中,结果偏低_______ 。
18、食醋中含有醋酸,醋酸的化学式为CH3COOH,则醋酸是由 元素组成的。一个醋酸分子中共含有 个原子,醋酸的式量为 ,元素百分含量最低的是 (填元素符号)
19、化学实验技能是学习和进行化学探究活动的基础和保证。请回答下列问题:
(1)在实验室里给烧杯中的液体加热时,应将烧杯放置在______上,使之受热均匀,加热完成后,必须用______盖灭酒精灯。
(2)铁丝在氧气中燃烧的实验,将细铁丝盘成螺旋状的目的是______。
(3)用10%的硝酸钾溶液配制50g的硝酸钾溶液,实验步骤包括:计算、量取、______、装入细口瓶并贴标签,若量取水的体积时俯视读数,则所配制的硝酸钾溶液的溶质质量分数______(填“偏大”、“偏小”或“不受影响 ”)。
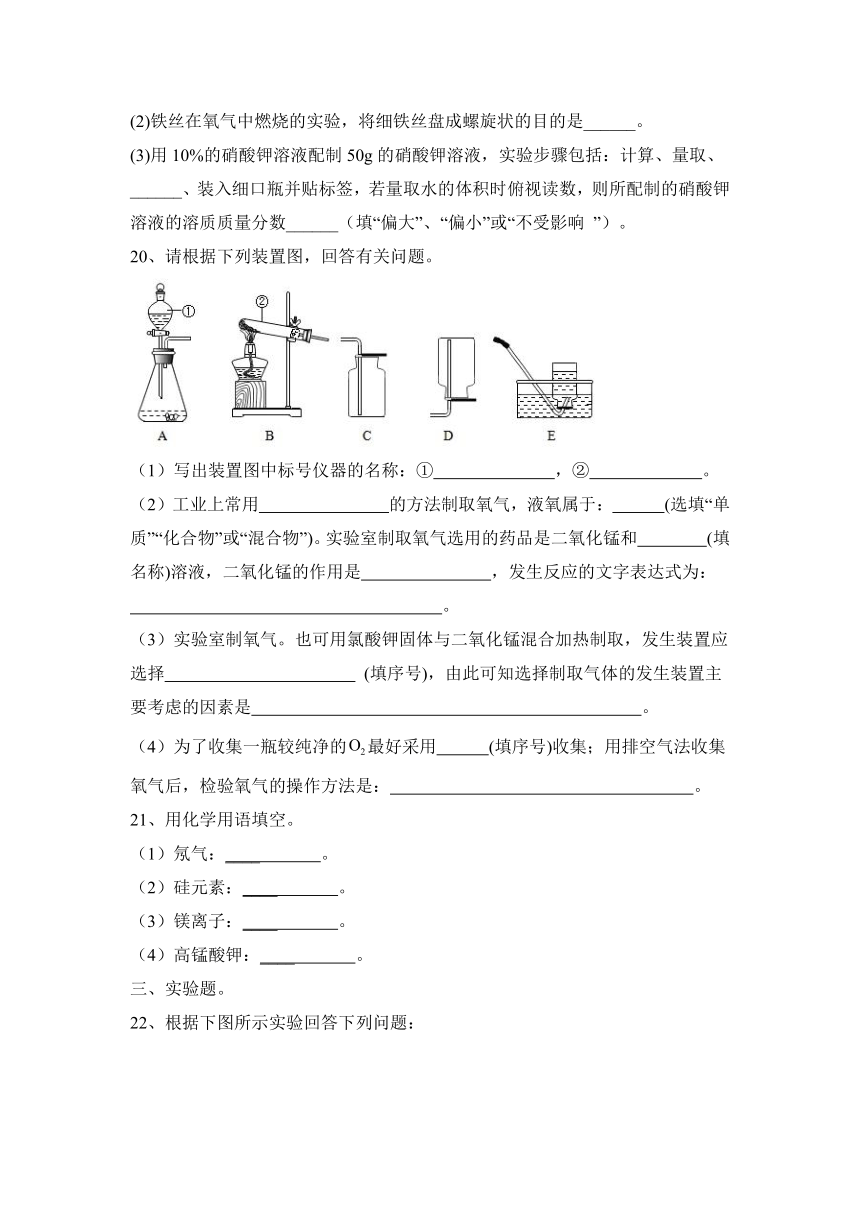
20、请根据下列装置图,回答有关问题。
(1)写出装置图中标号仪器的名称:① ,② 。
(2)工业上常用 的方法制取氧气,液氧属于: (选填“单质”“化合物”或“混合物”)。实验室制取氧气选用的药品是二氧化锰和 (填名称)溶液,二氧化锰的作用是 ,发生反应的文字表达式为:
。
(3)实验室制氧气。也可用氯酸钾固体与二氧化锰混合加热制取,发生装置应选择 (填序号),由此可知选择制取气体的发生装置主要考虑的因素是 。
(4)为了收集一瓶较纯净的最好采用 (填序号)收集;用排空气法收集氧气后,检验氧气的操作方法是: 。
21、用化学用语填空。
(1)氖气:____ 。
(2)硅元素:____ 。
(3)镁离子:____ 。
(4)高锰酸钾:____ 。
三、实验题。
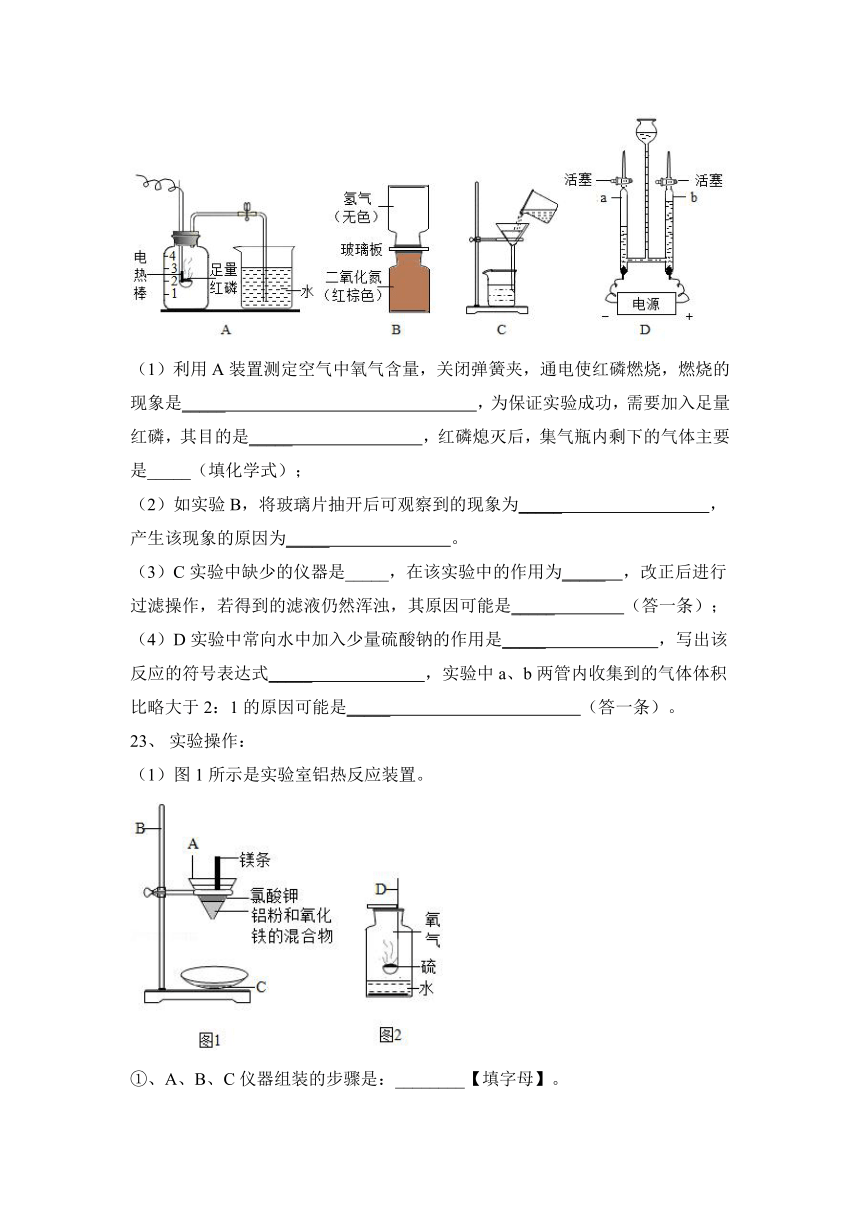
22、根据下图所示实验回答下列问题:
(1)利用A装置测定空气中氧气含量,关闭弹簧夹,通电使红磷燃烧,燃烧的现象是_____ ,为保证实验成功,需要加入足量红磷,其目的是_____ ,红磷熄灭后,集气瓶内剩下的气体主要是_____(填化学式);
(2)如实验B,将玻璃片抽开后可观察到的现象为_____ ,产生该现象的原因为_____ 。
(3)C实验中缺少的仪器是_____,在该实验中的作用为_____ ,改正后进行过滤操作,若得到的滤液仍然浑浊,其原因可能是_____ (答一条);
(4)D实验中常向水中加入少量硫酸钠的作用是_____ ,写出该反应的符号表达式_____ ,实验中a、b两管内收集到的气体体积比略大于2:1的原因可能是_____ (答一条)。
23、 实验操作:
(1)图1所示是实验室铝热反应装置。
①、A、B、C仪器组装的步骤是:________【填字母】。
②仪器组装完毕,引燃镁条,反应剧烈进行,放出大量的热,并发出耀眼的白光。纸漏斗A的下部被烧穿,有高温熔融物落入C仪器中。回答下列问题:
承接生成物的C中铺上适量_______,一是防止____________________________,二是防止高温熔融物溅出伤人:氯酸钾的作用是___ ,使深入混合物内部的镁条继续燃烧。
(2)图2是硫在氧气中燃烧的反应,仪器D的名称是___________,实验现象是:剧烈燃烧,_________ ,产生刺激性气味,放出大量的热。图中水的作用是________ 。
五、计算类题。
24、计算下列物质的相对分子质量。
①O2 ②HCl ③Ca(OH)2
④KMnO4 ⑤CaCO3 ⑥C2H5OH
2023—2024学年鲁教版化学九年级上册第四单元 我们周围的空气 跟踪选题含答案
鲁教版第四单元 我们周围的空气
一、选择题。(16题)
1、每年的6月5日世界环境日,环境保护是我国的一项基本国策,空气的净化日益受到人们的关注.下列气体组中的各种气体都属于空气污染物的是( )
A.二氧化硫 一氧化碳 二氧化氮
B.二氧化碳 一氧化碳 二氧化硫
C.一氧化碳 二氧化碳 氮气
D.氮气 二氧化氮 一氧化碳
【答案】A。
2、高铁酸钠(Na2FeO4)中,铁元素的化合价是( )
A.+2 B.+3 C.+6 D.+7
【答案】C
3、下列关于氧气的说法正确的是( )
A.分离液态空气获得氧气是化学变化
B.植物的光合作用会消耗氧气
C.氧气的化学性质不活泼
D.液态氧可用作火箭助燃剂
【答案】D
4、下列有关氧气的说法错误的是 ( )
A.能燃烧 B.无色 C.无味 D.能供给呼吸
【答案】A
5、根据化学式C6H2Cl4,判断下列说法正确的是( )
A.该物质属于化合物
B.该物质的相对分子质量为216g
C.该物质的一个分子中含有一个氢分子
D.该分子中碳元素质量分数大于氯元素
【答案】A
6、实验室用燃烧法测定空气中氧气的含量,最适宜选用的物质是( )
A.木炭 B.红磷 C.硫磺 D.铁丝
【答案】B。
7、虾青素(C40H52O4)是一种具有极强的抗肿瘤、抗氧化性能的物质,可增强动物免疫力.下列有关它的说法正确的是( )
A.虾青素是一种氧化物
B.虾青素中碳、氢、氧元素的质量比为10:13:1
C.虾青素的相对分子质量是596
D.虾青素是由96个原子构成
【答案】C
8、下列关于物质的变化说法不正确的是( )
A.葡萄酿酒是化学变化
B.红磷燃烧是化学变化
C.工业制氧气和实验室制取氧气都是化学变化
D.干冰升华是物理变化
【答案】C
9、实验室制取气体选择收集方法时,下列气体性质不需考虑的是 ( )
A.密度 B.可燃性 C.溶解性 D.能否与水反应
【答案】B
10、下列说法正确的是( )
A.有氧气参加的反应都是化合反应
B.化合反应一定是氧化反应
C.化合反应不一定是氧化反应,氧化反应也不一定是化合反应
D.分解反应的特点是两种物质反应生成两种或两种以上的物质
【答案】C
11、下列气体在洁净空气中不应该含有的是( )
A.氧气 B.氮气 C.稀有气体 D.二氧化硫
【答案】D。
12、已知一种碳﹣12原子的质量为mg,另一种原子的质量为ng,则该原子的相对原子质量为( )
A. B. C.n D.
【答案】A
13、下列物质属于氧化物的是( )
A.O3 B.SO3 C.NaOH D.K2SO4
【答案】B
14、下列物质在空气或氧气中燃烧时的现象描述正确的是 ( )
A.红磷在空气中燃烧,产生大量白烟,放出热量,生成白色气体
B.铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成四氧化三铁
C.木炭在氧气中燃烧,发出红光,放出热量,产生能使石灰水变浑浊的气体
D.镁带在空气中燃烧,发出白光,放热,生成白色固体
【答案】D
15、婴儿“尿不湿”最关键的材料是聚丙烯酸钠,它是由丙烯酸(C3H4O2)与氢氧化钠经过一系列的复杂反应而制得。下列有关丙烯酸(C3H4O2)的说法正确的是( )
A.丙烯酸中氢元素的质量分数最大
B.丙烯酸是由碳、氢、氧三种元素组成
C.丙烯酸中碳、氢、氧元素的质量比是3:4:2
D.丙烯酸是由3个碳原子4个氢原子和2个氧原子构成
【答案】B
16、利用如图装置验证了空气中氧气的含量。下列叙述不正确的是( )
A.实验前需检查装置气密性
B.白磷的作用是消耗试管中的氧气
C.白磷熄火、试管冷却后再打开止水夹
D.最终量筒中液面约降至40mL刻度线处
【答案】D
二、填空题。
17、实验是学习化学的一条重要途径,正确的实验操作是实验成功的关键。造成下列实验后果的原因可能是:
(1)加热固体时试管炸裂_______ ;(任答一条原因即可,下同)
(2)用量筒量取一定量体积的水时,实际量得的体积偏大_______ ;
(3)在用红磷燃烧测定空气里氧气含量的实验中,结果偏低_______ 。
【答案】试管口没有略向下倾斜(答案合理即可)
(2)仰视读数
(3)红磷的量不足(答案合理即可)
18、食醋中含有醋酸,醋酸的化学式为CH3COOH,则醋酸是由 元素组成的。一个醋酸分子中共含有 个原子,醋酸的式量为 ,元素百分含量最低的是 (填元素符号)
【答案】碳、氢、氧; 8; 60;氢。
19、化学实验技能是学习和进行化学探究活动的基础和保证。请回答下列问题:
(1)在实验室里给烧杯中的液体加热时,应将烧杯放置在______上,使之受热均匀,加热完成后,必须用______盖灭酒精灯。
(2)铁丝在氧气中燃烧的实验,将细铁丝盘成螺旋状的目的是______。
(3)用10%的硝酸钾溶液配制50g的硝酸钾溶液,实验步骤包括:计算、量取、______、装入细口瓶并贴标签,若量取水的体积时俯视读数,则所配制的硝酸钾溶液的溶质质量分数______(填“偏大”、“偏小”或“不受影响 ”)。
【答案】(1) 陶土网 灯帽
(2)增大铁丝与氧气的接触面积##增大铁丝的受热面积
(3) 混匀 偏大
20、请根据下列装置图,回答有关问题。
(1)写出装置图中标号仪器的名称:① ,② 。
(2)工业上常用 的方法制取氧气,液氧属于: (选填“单质”“化合物”或“混合物”)。实验室制取氧气选用的药品是二氧化锰和 (填名称)溶液,二氧化锰的作用是 ,发生反应的文字表达式为:
。
(3)实验室制氧气。也可用氯酸钾固体与二氧化锰混合加热制取,发生装置应选择 (填序号),由此可知选择制取气体的发生装置主要考虑的因素是 。
(4)为了收集一瓶较纯净的最好采用 (填序号)收集;用排空气法收集氧气后,检验氧气的操作方法是: 。
【答案】(1)分液漏斗 试管
(2)分离液态空气 单质 过氧化氢
催化作用 过氧化氢水+氧气
(3)B 反应物的状态和反应条件
(4)E 将带火星的木条伸入集气瓶内,木条复燃,证明是氧气
21、用化学用语填空。
(1)氖气:____ 。
(2)硅元素:____ 。
(3)镁离子:____ 。
(4)高锰酸钾:____ 。
【答案】(1) Ne (2)Si (3) Mg2+ (4)KMnO4
三、实验题。
22、根据下图所示实验回答下列问题:
(1)利用A装置测定空气中氧气含量,关闭弹簧夹,通电使红磷燃烧,燃烧的现象是_____ ,为保证实验成功,需要加入足量红磷,其目的是_____ ,红磷熄灭后,集气瓶内剩下的气体主要是_____(填化学式);
(2)如实验B,将玻璃片抽开后可观察到的现象为_____ ,产生该现象的原因为_____ 。
(3)C实验中缺少的仪器是_____,在该实验中的作用为_____ ,改正后进行过滤操作,若得到的滤液仍然浑浊,其原因可能是_____ (答一条);
(4)D实验中常向水中加入少量硫酸钠的作用是_____ ,写出该反应的符号表达式_____ ,实验中a、b两管内收集到的气体体积比略大于2:1的原因可能是_____ (答一条)。
【答案】(1)红磷燃烧,产生大量白烟,放出热量
将装置内氧气完全耗尽 N2
(2)过一段时间,两瓶中颜色相同 分子在不断运动
(3)玻璃棒 引流 滤纸破碎
(4)增强水的导电性 相同条件下,氧气的溶解性大
23、 实验操作:
(1)图1所示是实验室铝热反应装置。
①、A、B、C仪器组装的步骤是:________【填字母】。
②仪器组装完毕,引燃镁条,反应剧烈进行,放出大量的热,并发出耀眼的白光。纸漏斗A的下部被烧穿,有高温熔融物落入C仪器中。回答下列问题:
承接生成物的C中铺上适量_______,一是防止____________________________,二是防止高温熔融物溅出伤人:氯酸钾的作用是___ ,使深入混合物内部的镁条继续燃烧。
(2)图2是硫在氧气中燃烧的反应,仪器D的名称是___________,实验现象是:剧烈燃烧,_________ ,产生刺激性气味,放出大量的热。图中水的作用是________ 。
【答案】(1)根据仪器的组装顺序可知,先放好铁架台,然后放置C,最后放置A;细沙;高温熔融物溅落炸裂仪器C;分解产生氧气。
(2)燃烧匙;产生明亮的蓝紫色火焰;
吸收生成的二氧化硫,防止造成空气污染。
五、计算类题。
24、计算下列物质的相对分子质量。
①O2 ②HCl ③Ca(OH)2
④KMnO4 ⑤CaCO3 ⑥C2H5OH
【答案】①O2的相对分子质量为:16×2=32;
②HCl的相对分子质量为:1+35.5=36.5;
③Ca(OH)2的相对分子质量为:40+(16+1)×2=74;
④KMnO4的相对分子质量为:39+55+16×4=158;
⑤CaCO3的相对分子质量为:40+12+16×3=100;
⑥C2H5OH的相对分子质量为:12×2+1×6+16=46。
鲁教版第四单元 我们周围的空气
一、选择题。(16题)
1、每年的6月5日世界环境日,环境保护是我国的一项基本国策,空气的净化日益受到人们的关注.下列气体组中的各种气体都属于空气污染物的是( )
A.二氧化硫 一氧化碳 二氧化氮
B.二氧化碳 一氧化碳 二氧化硫
C.一氧化碳 二氧化碳 氮气
D.氮气 二氧化氮 一氧化碳
2、高铁酸钠(Na2FeO4)中,铁元素的化合价是( )
A.+2 B.+3 C.+6 D.+7
3、下列关于氧气的说法正确的是( )
A.分离液态空气获得氧气是化学变化
B.植物的光合作用会消耗氧气
C.氧气的化学性质不活泼
D.液态氧可用作火箭助燃剂
4、下列有关氧气的说法错误的是 ( )
A.能燃烧 B.无色 C.无味 D.能供给呼吸
5、根据化学式C6H2Cl4,判断下列说法正确的是( )
A.该物质属于化合物
B.该物质的相对分子质量为216g
C.该物质的一个分子中含有一个氢分子
D.该分子中碳元素质量分数大于氯元素
6、实验室用燃烧法测定空气中氧气的含量,最适宜选用的物质是( )
A.木炭 B.红磷 C.硫磺 D.铁丝
7、虾青素(C40H52O4)是一种具有极强的抗肿瘤、抗氧化性能的物质,可增强动物免疫力.下列有关它的说法正确的是( )
A.虾青素是一种氧化物
B.虾青素中碳、氢、氧元素的质量比为10:13:1
C.虾青素的相对分子质量是596
D.虾青素是由96个原子构成
8、下列关于物质的变化说法不正确的是( )
A.葡萄酿酒是化学变化
B.红磷燃烧是化学变化
C.工业制氧气和实验室制取氧气都是化学变化
D.干冰升华是物理变化
9、实验室制取气体选择收集方法时,下列气体性质不需考虑的是 ( )
A.密度 B.可燃性 C.溶解性 D.能否与水反应
10、下列说法正确的是( )
A.有氧气参加的反应都是化合反应
B.化合反应一定是氧化反应
C.化合反应不一定是氧化反应,氧化反应也不一定是化合反应
D.分解反应的特点是两种物质反应生成两种或两种以上的物质
11、下列气体在洁净空气中不应该含有的是( )
A.氧气 B.氮气 C.稀有气体 D.二氧化硫
12、已知一种碳﹣12原子的质量为mg,另一种原子的质量为ng,则该原子的相对原子质量为( )
A. B. C.n D.
13、下列物质属于氧化物的是( )
A.O3 B.SO3 C.NaOH D.K2SO4
14、下列物质在空气或氧气中燃烧时的现象描述正确的是 ( )
A.红磷在空气中燃烧,产生大量白烟,放出热量,生成白色气体
B.铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成四氧化三铁
C.木炭在氧气中燃烧,发出红光,放出热量,产生能使石灰水变浑浊的气体
D.镁带在空气中燃烧,发出白光,放热,生成白色固体
15、婴儿“尿不湿”最关键的材料是聚丙烯酸钠,它是由丙烯酸(C3H4O2)与氢氧化钠经过一系列的复杂反应而制得。下列有关丙烯酸(C3H4O2)的说法正确的是( )
A.丙烯酸中氢元素的质量分数最大
B.丙烯酸是由碳、氢、氧三种元素组成
C.丙烯酸中碳、氢、氧元素的质量比是3:4:2
D.丙烯酸是由3个碳原子4个氢原子和2个氧原子构成
16、利用如图装置验证了空气中氧气的含量。下列叙述不正确的是( )
A.实验前需检查装置气密性
B.白磷的作用是消耗试管中的氧气
C.白磷熄火、试管冷却后再打开止水夹
D.最终量筒中液面约降至40mL刻度线处
二、填空题。
17、实验是学习化学的一条重要途径,正确的实验操作是实验成功的关键。造成下列实验后果的原因可能是:
(1)加热固体时试管炸裂_______ ;(任答一条原因即可,下同)
(2)用量筒量取一定量体积的水时,实际量得的体积偏大_______ ;
(3)在用红磷燃烧测定空气里氧气含量的实验中,结果偏低_______ 。
18、食醋中含有醋酸,醋酸的化学式为CH3COOH,则醋酸是由 元素组成的。一个醋酸分子中共含有 个原子,醋酸的式量为 ,元素百分含量最低的是 (填元素符号)
19、化学实验技能是学习和进行化学探究活动的基础和保证。请回答下列问题:
(1)在实验室里给烧杯中的液体加热时,应将烧杯放置在______上,使之受热均匀,加热完成后,必须用______盖灭酒精灯。
(2)铁丝在氧气中燃烧的实验,将细铁丝盘成螺旋状的目的是______。
(3)用10%的硝酸钾溶液配制50g的硝酸钾溶液,实验步骤包括:计算、量取、______、装入细口瓶并贴标签,若量取水的体积时俯视读数,则所配制的硝酸钾溶液的溶质质量分数______(填“偏大”、“偏小”或“不受影响 ”)。
20、请根据下列装置图,回答有关问题。
(1)写出装置图中标号仪器的名称:① ,② 。
(2)工业上常用 的方法制取氧气,液氧属于: (选填“单质”“化合物”或“混合物”)。实验室制取氧气选用的药品是二氧化锰和 (填名称)溶液,二氧化锰的作用是 ,发生反应的文字表达式为:
。
(3)实验室制氧气。也可用氯酸钾固体与二氧化锰混合加热制取,发生装置应选择 (填序号),由此可知选择制取气体的发生装置主要考虑的因素是 。
(4)为了收集一瓶较纯净的最好采用 (填序号)收集;用排空气法收集氧气后,检验氧气的操作方法是: 。
21、用化学用语填空。
(1)氖气:____ 。
(2)硅元素:____ 。
(3)镁离子:____ 。
(4)高锰酸钾:____ 。
三、实验题。
22、根据下图所示实验回答下列问题:
(1)利用A装置测定空气中氧气含量,关闭弹簧夹,通电使红磷燃烧,燃烧的现象是_____ ,为保证实验成功,需要加入足量红磷,其目的是_____ ,红磷熄灭后,集气瓶内剩下的气体主要是_____(填化学式);
(2)如实验B,将玻璃片抽开后可观察到的现象为_____ ,产生该现象的原因为_____ 。
(3)C实验中缺少的仪器是_____,在该实验中的作用为_____ ,改正后进行过滤操作,若得到的滤液仍然浑浊,其原因可能是_____ (答一条);
(4)D实验中常向水中加入少量硫酸钠的作用是_____ ,写出该反应的符号表达式_____ ,实验中a、b两管内收集到的气体体积比略大于2:1的原因可能是_____ (答一条)。
23、 实验操作:
(1)图1所示是实验室铝热反应装置。
①、A、B、C仪器组装的步骤是:________【填字母】。
②仪器组装完毕,引燃镁条,反应剧烈进行,放出大量的热,并发出耀眼的白光。纸漏斗A的下部被烧穿,有高温熔融物落入C仪器中。回答下列问题:
承接生成物的C中铺上适量_______,一是防止____________________________,二是防止高温熔融物溅出伤人:氯酸钾的作用是___ ,使深入混合物内部的镁条继续燃烧。
(2)图2是硫在氧气中燃烧的反应,仪器D的名称是___________,实验现象是:剧烈燃烧,_________ ,产生刺激性气味,放出大量的热。图中水的作用是________ 。
五、计算类题。
24、计算下列物质的相对分子质量。
①O2 ②HCl ③Ca(OH)2
④KMnO4 ⑤CaCO3 ⑥C2H5OH
2023—2024学年鲁教版化学九年级上册第四单元 我们周围的空气 跟踪选题含答案
鲁教版第四单元 我们周围的空气
一、选择题。(16题)
1、每年的6月5日世界环境日,环境保护是我国的一项基本国策,空气的净化日益受到人们的关注.下列气体组中的各种气体都属于空气污染物的是( )
A.二氧化硫 一氧化碳 二氧化氮
B.二氧化碳 一氧化碳 二氧化硫
C.一氧化碳 二氧化碳 氮气
D.氮气 二氧化氮 一氧化碳
【答案】A。
2、高铁酸钠(Na2FeO4)中,铁元素的化合价是( )
A.+2 B.+3 C.+6 D.+7
【答案】C
3、下列关于氧气的说法正确的是( )
A.分离液态空气获得氧气是化学变化
B.植物的光合作用会消耗氧气
C.氧气的化学性质不活泼
D.液态氧可用作火箭助燃剂
【答案】D
4、下列有关氧气的说法错误的是 ( )
A.能燃烧 B.无色 C.无味 D.能供给呼吸
【答案】A
5、根据化学式C6H2Cl4,判断下列说法正确的是( )
A.该物质属于化合物
B.该物质的相对分子质量为216g
C.该物质的一个分子中含有一个氢分子
D.该分子中碳元素质量分数大于氯元素
【答案】A
6、实验室用燃烧法测定空气中氧气的含量,最适宜选用的物质是( )
A.木炭 B.红磷 C.硫磺 D.铁丝
【答案】B。
7、虾青素(C40H52O4)是一种具有极强的抗肿瘤、抗氧化性能的物质,可增强动物免疫力.下列有关它的说法正确的是( )
A.虾青素是一种氧化物
B.虾青素中碳、氢、氧元素的质量比为10:13:1
C.虾青素的相对分子质量是596
D.虾青素是由96个原子构成
【答案】C
8、下列关于物质的变化说法不正确的是( )
A.葡萄酿酒是化学变化
B.红磷燃烧是化学变化
C.工业制氧气和实验室制取氧气都是化学变化
D.干冰升华是物理变化
【答案】C
9、实验室制取气体选择收集方法时,下列气体性质不需考虑的是 ( )
A.密度 B.可燃性 C.溶解性 D.能否与水反应
【答案】B
10、下列说法正确的是( )
A.有氧气参加的反应都是化合反应
B.化合反应一定是氧化反应
C.化合反应不一定是氧化反应,氧化反应也不一定是化合反应
D.分解反应的特点是两种物质反应生成两种或两种以上的物质
【答案】C
11、下列气体在洁净空气中不应该含有的是( )
A.氧气 B.氮气 C.稀有气体 D.二氧化硫
【答案】D。
12、已知一种碳﹣12原子的质量为mg,另一种原子的质量为ng,则该原子的相对原子质量为( )
A. B. C.n D.
【答案】A
13、下列物质属于氧化物的是( )
A.O3 B.SO3 C.NaOH D.K2SO4
【答案】B
14、下列物质在空气或氧气中燃烧时的现象描述正确的是 ( )
A.红磷在空气中燃烧,产生大量白烟,放出热量,生成白色气体
B.铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成四氧化三铁
C.木炭在氧气中燃烧,发出红光,放出热量,产生能使石灰水变浑浊的气体
D.镁带在空气中燃烧,发出白光,放热,生成白色固体
【答案】D
15、婴儿“尿不湿”最关键的材料是聚丙烯酸钠,它是由丙烯酸(C3H4O2)与氢氧化钠经过一系列的复杂反应而制得。下列有关丙烯酸(C3H4O2)的说法正确的是( )
A.丙烯酸中氢元素的质量分数最大
B.丙烯酸是由碳、氢、氧三种元素组成
C.丙烯酸中碳、氢、氧元素的质量比是3:4:2
D.丙烯酸是由3个碳原子4个氢原子和2个氧原子构成
【答案】B
16、利用如图装置验证了空气中氧气的含量。下列叙述不正确的是( )
A.实验前需检查装置气密性
B.白磷的作用是消耗试管中的氧气
C.白磷熄火、试管冷却后再打开止水夹
D.最终量筒中液面约降至40mL刻度线处
【答案】D
二、填空题。
17、实验是学习化学的一条重要途径,正确的实验操作是实验成功的关键。造成下列实验后果的原因可能是:
(1)加热固体时试管炸裂_______ ;(任答一条原因即可,下同)
(2)用量筒量取一定量体积的水时,实际量得的体积偏大_______ ;
(3)在用红磷燃烧测定空气里氧气含量的实验中,结果偏低_______ 。
【答案】试管口没有略向下倾斜(答案合理即可)
(2)仰视读数
(3)红磷的量不足(答案合理即可)
18、食醋中含有醋酸,醋酸的化学式为CH3COOH,则醋酸是由 元素组成的。一个醋酸分子中共含有 个原子,醋酸的式量为 ,元素百分含量最低的是 (填元素符号)
【答案】碳、氢、氧; 8; 60;氢。
19、化学实验技能是学习和进行化学探究活动的基础和保证。请回答下列问题:
(1)在实验室里给烧杯中的液体加热时,应将烧杯放置在______上,使之受热均匀,加热完成后,必须用______盖灭酒精灯。
(2)铁丝在氧气中燃烧的实验,将细铁丝盘成螺旋状的目的是______。
(3)用10%的硝酸钾溶液配制50g的硝酸钾溶液,实验步骤包括:计算、量取、______、装入细口瓶并贴标签,若量取水的体积时俯视读数,则所配制的硝酸钾溶液的溶质质量分数______(填“偏大”、“偏小”或“不受影响 ”)。
【答案】(1) 陶土网 灯帽
(2)增大铁丝与氧气的接触面积##增大铁丝的受热面积
(3) 混匀 偏大
20、请根据下列装置图,回答有关问题。
(1)写出装置图中标号仪器的名称:① ,② 。
(2)工业上常用 的方法制取氧气,液氧属于: (选填“单质”“化合物”或“混合物”)。实验室制取氧气选用的药品是二氧化锰和 (填名称)溶液,二氧化锰的作用是 ,发生反应的文字表达式为:
。
(3)实验室制氧气。也可用氯酸钾固体与二氧化锰混合加热制取,发生装置应选择 (填序号),由此可知选择制取气体的发生装置主要考虑的因素是 。
(4)为了收集一瓶较纯净的最好采用 (填序号)收集;用排空气法收集氧气后,检验氧气的操作方法是: 。
【答案】(1)分液漏斗 试管
(2)分离液态空气 单质 过氧化氢
催化作用 过氧化氢水+氧气
(3)B 反应物的状态和反应条件
(4)E 将带火星的木条伸入集气瓶内,木条复燃,证明是氧气
21、用化学用语填空。
(1)氖气:____ 。
(2)硅元素:____ 。
(3)镁离子:____ 。
(4)高锰酸钾:____ 。
【答案】(1) Ne (2)Si (3) Mg2+ (4)KMnO4
三、实验题。
22、根据下图所示实验回答下列问题:
(1)利用A装置测定空气中氧气含量,关闭弹簧夹,通电使红磷燃烧,燃烧的现象是_____ ,为保证实验成功,需要加入足量红磷,其目的是_____ ,红磷熄灭后,集气瓶内剩下的气体主要是_____(填化学式);
(2)如实验B,将玻璃片抽开后可观察到的现象为_____ ,产生该现象的原因为_____ 。
(3)C实验中缺少的仪器是_____,在该实验中的作用为_____ ,改正后进行过滤操作,若得到的滤液仍然浑浊,其原因可能是_____ (答一条);
(4)D实验中常向水中加入少量硫酸钠的作用是_____ ,写出该反应的符号表达式_____ ,实验中a、b两管内收集到的气体体积比略大于2:1的原因可能是_____ (答一条)。
【答案】(1)红磷燃烧,产生大量白烟,放出热量
将装置内氧气完全耗尽 N2
(2)过一段时间,两瓶中颜色相同 分子在不断运动
(3)玻璃棒 引流 滤纸破碎
(4)增强水的导电性 相同条件下,氧气的溶解性大
23、 实验操作:
(1)图1所示是实验室铝热反应装置。
①、A、B、C仪器组装的步骤是:________【填字母】。
②仪器组装完毕,引燃镁条,反应剧烈进行,放出大量的热,并发出耀眼的白光。纸漏斗A的下部被烧穿,有高温熔融物落入C仪器中。回答下列问题:
承接生成物的C中铺上适量_______,一是防止____________________________,二是防止高温熔融物溅出伤人:氯酸钾的作用是___ ,使深入混合物内部的镁条继续燃烧。
(2)图2是硫在氧气中燃烧的反应,仪器D的名称是___________,实验现象是:剧烈燃烧,_________ ,产生刺激性气味,放出大量的热。图中水的作用是________ 。
【答案】(1)根据仪器的组装顺序可知,先放好铁架台,然后放置C,最后放置A;细沙;高温熔融物溅落炸裂仪器C;分解产生氧气。
(2)燃烧匙;产生明亮的蓝紫色火焰;
吸收生成的二氧化硫,防止造成空气污染。
五、计算类题。
24、计算下列物质的相对分子质量。
①O2 ②HCl ③Ca(OH)2
④KMnO4 ⑤CaCO3 ⑥C2H5OH
【答案】①O2的相对分子质量为:16×2=32;
②HCl的相对分子质量为:1+35.5=36.5;
③Ca(OH)2的相对分子质量为:40+(16+1)×2=74;
④KMnO4的相对分子质量为:39+55+16×4=158;
⑤CaCO3的相对分子质量为:40+12+16×3=100;
⑥C2H5OH的相对分子质量为:12×2+1×6+16=46。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
