1.1.反应热(含解析) 测试题 023-2024学年高二上学期化学人教版(2019)选择性必修1
文档属性
| 名称 | 1.1.反应热(含解析) 测试题 023-2024学年高二上学期化学人教版(2019)选择性必修1 |

|
|
| 格式 | docx | ||
| 文件大小 | 959.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-20 00:00:00 | ||
图片预览




文档简介
1.1.反应热测试题-2023-2024学年高二上学期化学人教版(2019)选修第一册
一、单选题
1.下列有关化学反应与能量变化的叙述正确的是
A.晶体与晶体的反应,为放热反应
B.石墨转化为金刚石需要吸收热量,据此可判断金刚石比石墨稳定
C.放热反应不需要条件即可发生,而吸热反应必须加热才能实现
D.化学反应中的能量变化主要是由化学键变化引起的
2.下列关于中和热、燃烧热的说法中正确的是( )
A.已知下列热化学方程式:2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol,则氢气的燃烧热为242 kJ/mol
B.中和热包括物质溶解、电离、水合等过程中的热效应
C.燃烧热是指在1.01×105 Pa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量
D.燃烧热随化学方程式前的化学计量数的改变而改变
3.下列反应属于吸热反应的是
A.能量变化如图所示的反应 B.盐酸与NaOH反应
C.CaCO3高温分解 D.CO不完全燃烧
4.下列能正确地表示燃烧热的热化学方程式是
A.
B.
C.
D.
5.下列生产活动或生活中涉及的化学反应不属于放热反应的是
A.燃放爆竹 B.石灰石分解 C.利用铝热反应焊接钢轨 D.牛奶变质
A.A B.B C.C D.D
6.下列叙述错误的是
A.世界是物质的,物质是在不断变化的,而物质的变化总是伴随着能量的变化
B.人类日常利用的煤、天然气、石油等的能量,归根到底是由太阳能转变来的
C.反应热是指反应过程中以热能的形式释放或吸收的反应物和生成物中具有的总能量的差值
D.天然气是二级能源
7.H2在O2中的燃烧是放热反应,下列说法正确的是( )
A.该过程中热能转化为化学能 B.该过程中化学能转化为热能
C.生成物的总能量等于反应物的总能量 D.该反应放热是因为成键过程放出能量
8.环戊二烯广泛用于农药、橡胶、塑料等工业合成,是一种重要的有机化工原料。其相关键能和能量循环图如下所示,下列说法不正确的是
共价键 键能/(kJ/mol)
H-H 436
H-I 299
I-I 151
A.在相同条件下,反应:,则
B.表中三种物质,H-H键能最大,故相同条件下,最稳定
C.
D.将和混合加热,充分反应后测得的反应热与相同
9.下列说法正确的是
A.物质发生化学反应都伴随着能量变化
B.干冰汽化需吸收大量的热,这个变化是吸热反应
C.在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量
D.放热反应的发生无需任何条件
10.已知:25 ℃、101 kPa下,强酸的稀溶液与强碱的稀溶液发生中和反应生成1 mol H2O时,放出57.3 kJ热量,下列有关热化学方程式正确的是
A.H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6 kJ·mol-1
B.H2SO4(aq)+2NH3·H2O (aq)=(NH4)2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
C.2HCl(aq)+Ba(OH)2(aq)=BaCl2(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
D.HCl(aq)+NH3·H2O(aq)=NH4Cl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
11.下列反应中,属于吸热反应同时又是氧化还原反应的是( )
A.Ba(OH)2·8H2O与NH4Cl反应
B.铝热反应
C.灼热的炭与水蒸气生成一氧化碳和氢气的反应
D.氢氧化钠与稀盐酸
12.红热的炭和水蒸气反应生成2 mol H2和2 mol CO气体,吸收262.6 kJ热量,能表示该反应热化学方程式的是
A.
B.
C.
D.
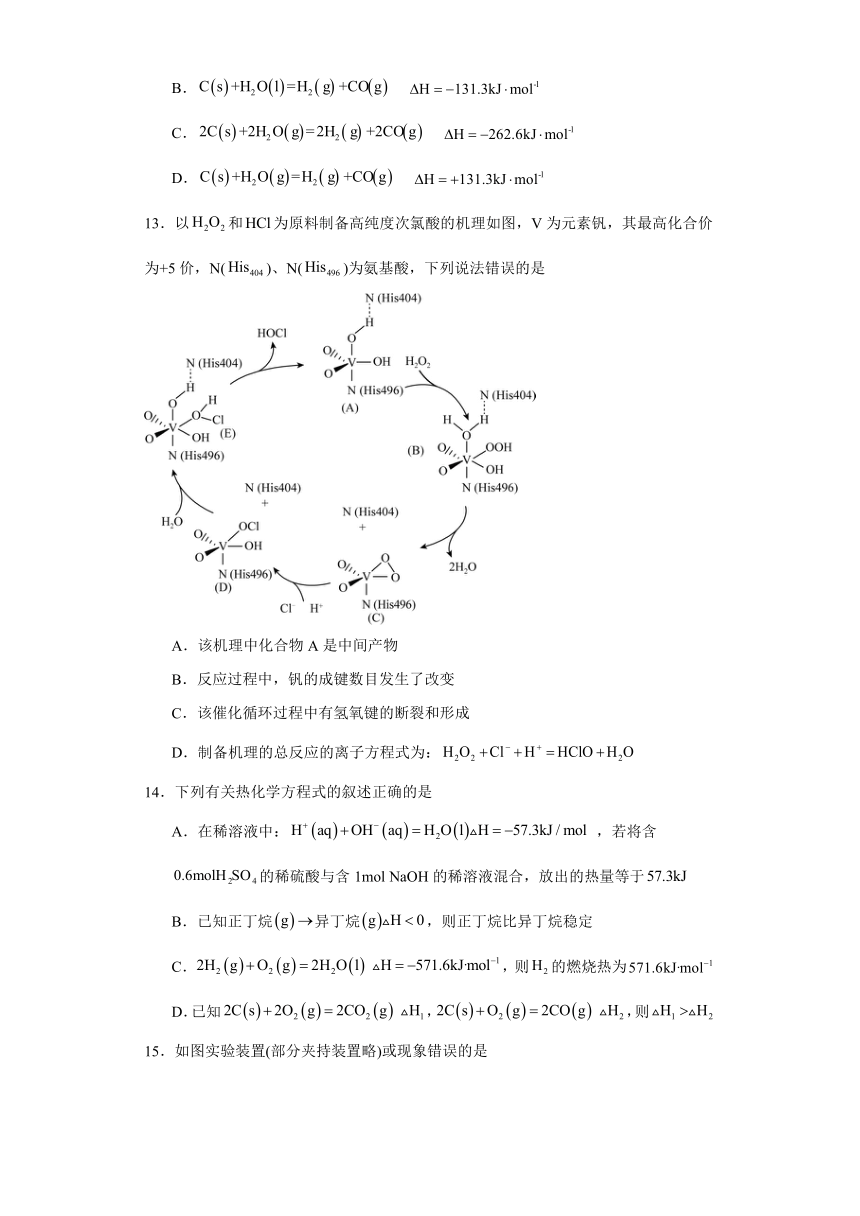
13.以和为原料制备高纯度次氯酸的机理如图,V为元素钒,其最高化合价为+5价,N()、N()为氨基酸,下列说法错误的是
A.该机理中化合物A是中间产物
B.反应过程中,钒的成键数目发生了改变
C.该催化循环过程中有氢氧键的断裂和形成
D.制备机理的总反应的离子方程式为:
14.下列有关热化学方程式的叙述正确的是
A.在稀溶液中: ,若将含的稀硫酸与含1mol NaOH的稀溶液混合,放出的热量等于
B.已知正丁烷异丁烷,则正丁烷比异丁烷稳定
C.,则的燃烧热为
D.已知,,则
15.如图实验装置(部分夹持装置略)或现象错误的是
A.图1表示钠的燃烧
B.图2表示测量盐酸和NaOH溶液反应前后的温度
C.图3表示滴入酚酞溶液
D.图4表示制备并收集乙酸乙酯
16.用“循环电沉积”法处理制备锂电池,其中和C在的催化作用下发生电极反应,其反应历程中的能量变化如下图。下列说法不正确的是
A.反应历程中存在极性键和非极性键的断裂和形成
B.反应历程中涉及电子转移的变化均吸收能量
C.催化剂通过降低电极反应的活化能使反应速率加快
D.电极上失去时,生成的体积为2.24L(标况下)
17.已知相同条件下,12gC(石墨)和12gC(金刚石)发生下列反应的能量变化:
C(石墨) 放热393.5kJ
C(金刚石) 放热395.4kJ
下列判断不正确的是
A.金刚石比石墨稳定
B.金刚石转变成石墨是化学变化
C.12g石墨所具有的能量比12g金刚石低
D.同素异形体具有的能量不同的原因可能是其中的化学键不同
18.含1molBa(OH)2的稀溶液与足量稀盐酸反应,放出热量114.6kJ。下列热化学方程式中,正确的是
A.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l) ΔH=+114.6kJ/mol
B.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(aq) ΔH=-114.6kJ/mol
C.1/2Ba(OH)2(aq)+HCl(aq)=1/2BaCl2(aq)+H2O(l) ΔH=-57.3kJ/mol
D.1/2Ba(OH)2(aq)+HCl(aq)=1/2BaCl2(aq)+H2O(l) ΔH=+57.3kJ/mol
19.已知(石墨) = (金刚石),在该反应进程中其能量变化如图所示,有关该反应的描述正确的是
A.该反应为放热反应
B.金刚石比石墨稳定
C.该反应为氧化还原反应
D.石墨比金刚石稳定
20.下列方程式书写正确的是
A.一氧化碳燃烧热化学方程式为CO+O2=CO2 △H=-283kJ mol-1
B.拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为N2(g)+3H2(g) 2NH3(g) △H=-92kJ mol-1
C.碳酸电离的方程式H2CO32H++CO
D.将SO2气体通入NaClO溶液中:SO2+2ClO-+H2O=SO+2HClO
21.中和热测定实验中,用盐酸和溶液进行实验,下列说法不正确的是
A.用量筒量取盐酸时仰视取液,测得的中和热偏小
B.装置中的大小烧杯之闻填满碎泡沫塑料的作用是保温隔热减少热量损失
C.酸碱混合时,量筒中溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌
D.改用盐酸跟溶液进行反应,求出的中和热和原来相同
22.下列热化学方程式中,正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1
B.由N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·mol-1可知,当反应中转移6 mol电子时,反应放出的热量小于92.4 kJ
C.甲烷的燃烧热ΔH为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
D.在101 kPa时,4 g H2完全燃烧生成液态水,放出571.6 kJ热量,氢气燃烧热的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
23.《中国诗词大会》节目不仅继承和发扬中华优秀传统文化,还蕴含许多化学知识。下列诗句中的化学知识分析不正确的是
A.李商隐诗句“春蚕到死丝方尽,蜡炬成灰泪始干”,蚕丝的主要成分是高分子化合物
B.李白诗句“炉火照天地,红星乱紫烟”,“紫烟”是指碘升华的现象
C.王安石诗句“爆竹声中一岁除,春风送暖人屠苏”,爆竹的燃放涉及氧化还原反应
D.曹植诗句“煮豆燃互萁,豆在釜中泣”,其中的能量变化主要是化学能转化为热能
24.最近有科学家发现正丁烷()脱氢或不完全氧化也可制得1,3-丁二烯(),已知热化学方程式如下:( )
①=
②=
③=
下列说法正确的是( )
A.由②可知,正丁烷()的燃烧热为
B.由①和②可推知:=
C.=
D.由①和②可知,同质量的正丁烷()转变为1,3-丁二烯()所需要的能量相同
25.中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图。下列说法不正确的是
A.该过程将太阳能转化成为化学能
B.该过程中,只涉及非极性键的断裂与生成
C.氧化剂与还原剂的物质的量之比为1∶3
D.原料气N2可通过分离液态空气获得
二、填空题
26.燃煤发电是目前我国主要的火力发电形式,思考并回答下列问题:
(1)写出碳完全燃烧的化学方程式并用双线桥标出上述反应中电子转移的方向和数目: 。
(2)上述燃烧反应中发生氧化反应的是 ,氧化剂是 。
(3)碳燃烧过程中化学能主要转变为 能和 能。
(4)试从资源、能效、对环境的影响等方面,阐述火力发电的弊端有哪些? 。
27.(1) S2O可以与Fe2+反应制备Fe2O3纳米颗粒。
①若S2O与Fe2+的物质的量之比为1:2,配平该反应的离子方程式:
Fe2++ S2O + H2O2+ OH- = Fe2O3+ S2O+ H2O
②下列关于该反应的说法中正确的是 (填序号)。
A 该反应中S2O表现了氧化性
B 已知生成的Fe2O3纳米颗粒直径为10纳米,则Fe2O3纳米颗粒为胶体
C 该反应中H2O2作氧化剂
(2)人们可利用Fe2(SO4)3作强氧化剂溶解铜矿石(Cu2S),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:
Cu2S+ Fe3++ H2O Cu2++ Fe2++ ( )+ SO
(3)书写下列反应的热化学方程式: 1 molN2(g)与适量O2(g)反应生成NO (g),需吸收68 kJ的热量; 。
28.化学反应过程中发生物质变化的同时,常常伴有能量的变化。这种能量的变化常以热量的形式表现出来,叫做反应热。由于反应的情况不同,反应热可分为许多种,如标准燃烧热和中和反应反应热等。
(1)下列ΔH表示物质标准燃烧热的是 ;表示中和反应反应热的是 。(填“ΔH1”、“ΔH2”、“ΔH3”等)
A.2H2(g)+O2(g)=2H2O(l) ΔH1
B.C(s)+O2(g)=CO(g) ΔH2=-Q1kJ·mol-1
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH3
D.C(s)+O2(g)=CO2(g) ΔH4=-Q2kJ·mol-1
E.Ba(OH) 2(aq)+H2SO4(aq)= BaSO4(aq)+2H2O(l) ΔH5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH6
(2)1 g C2H2气体完全燃烧生成液态水和CO2气体,放出50 kJ的热量,写出该反应的热化学方程式: 。
(3)根据题(1)中B、D判断1 molCO(g)完全燃烧的ΔH= 。
(4)反应F的ΔH6可以用如图所示的装置进行测量。
从实验装置上看,图中有两种错误,分别是 ; ;大烧杯上如不塞碎塑料泡沫,求得的中和反应的反应热的数值 (填“偏大”“偏小”或“无影响”)。
试卷第1页,共3页
参考答案:
1.D
【详解】A.晶体与晶体反应生成氯化钡、氨气和水,该反应是吸热反应,A错误;
B.石墨转化为金刚石需要吸收热量,说明在相同条件下,石墨的能量较低,能量越低越稳定,故据此可判断石墨比金刚石稳定,B错误;
C.有些放热反应需要加热或高温的条件才能引发,而有些吸热反应不用加热也能实现,一个反应是放热反应还是吸热反应,与反应条件无关,C错误;
D.在化学反应中,破坏反应物中的化学要吸收能量,而形成生成物中的化学要放出能量,因此,化学反应中的能量变化主要是由化学键变化引起的,D正确;
故选D。
2.C
【详解】燃烧热是指1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,水为液态水;中和热是指在稀溶液中,酸跟碱发生中和反应生成1 mol液态水时的反应热,据此分析解题:
A.已知下列热化学方程式:2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol,水必须为液态水,故无法得出氢气的燃烧热,A错误;
B.中和热就是反应过程中的热效应,不包括物质溶解、电离、水合等过程中的热效应,B错误;
C.在1.01×105 Pa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量就是该物质的燃烧热,C正确;
D.根据燃烧热定义可知,燃烧热不随化学方程式前的化学计量数的改变而改变,D错误;
故答案为:C。
3.C
【详解】A.反应物能量总和大于生成物能量总和,当反应发生时,剩余能量以热能形式释放出来,所以是放热反应,不符题意;
B.酸碱中和反应是放热反应,不符题意;
C.碳酸钙受热分解属于吸热反应,符合题意;
D.所有燃烧均是放热反应,不符题意;
综上,本题选C。
4.A
【详解】燃烧热是指1mol可燃物完全燃烧生成稳定化合物放出的热量,的燃烧热为,则完全燃烧生成1mol二氧化碳和2mol液态水放出的热量,所以燃烧的热化学方程式为: ,故A正确。
5.B
【详解】A.燃烧爆炸属于放热反应,A错误;
B.石灰石分解属于吸热反应,B正确;
C.铝热反应属于放热反应,C错误;
D.牛奶变质,缓慢的氧化反应属于放热反应,D错误;
故选B。
6.D
【详解】A.世界是物质的,物质是在不断变化的,而物质的变化总是伴随着能量的变化,正确;
B.人类日常利用的煤、天然气、石油等的能量,归根到底是由古代的动物、植物等经过漫长的历史时期形成的,因此是由太阳能转变而来的,正确;
C.反应热是指反应过程中以热能的形式释放或吸收的反应物和生成物中具有的总能量的差值,正确;
D.天然气是直接开采出来就使用的能源,是一级能源,错误;
故选D。
7.B
【详解】
A.H2在O2中燃烧生成水时会放出热能,是由于化学能转化为热能,故A错误;
B.H2在O2中燃烧生成水时会放出热能,是由于化学能转化为热能,故B正确;
C.放热反应中反应物的总能量高于生成物的总能量,故C错误;
D.该反应放热是因为新化学键形成时所释放的总能量大于旧化学键断裂时所吸收的总能量,故D错误;
答案选B。
8.D
【详解】A.比更活泼,说明自身具有的能量大于具有的能量,所以和反应生成,放出的能量大于与反应生成放出的能量,,A项正确;
B.键能越大越稳定,H-H键能最大,故相同条件下, 最稳定,B项正确;
C.根据盖斯定律:,,C项正确;
D.反应热与 不相同,D项错误;
答案选D。
9.A
【详解】A.化学反应的特征是:一是生成新物质,二是伴随着能量的变化,A项正确;
B.吸热反应属于化学变化,干冰汽化需吸收大量的热,该过程是物理变化,不是吸热反应,B项错误;
C.在一个确定的化学反应关系中,反应物的总能量不等于生成物的总能量,若反应物的总能量总是高于生成物的总能量,该反应为放热反应,若反应物的总能量总是低于生成物的总能量,该反应为吸热反应,C项错误;
D.有的放热反应也需要条件,如铝热反应,需要高温加热,D项错误;
答案选A。
10.C
【详解】A.生成硫酸钡放热,由中和热及物质的量与热量成正比可知H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)△H<-114.6 kJ mol-1,故A错误;
B.NH3·H2O是弱碱,电离过程吸热,热化学方程式为H2SO4(aq)+2NH3·H2O (aq)=(NH4)2SO4(aq)+2H2O(l) ΔH>-114.6 kJ·mol-1,故B错误;
C.发生中和反应生成1 mol H2O时,放出57.3 kJ热量,则生成2 mol H2O时,放出114.6 kJ热量,热化学方程式为2HCl(aq)+Ba(OH)2(aq)=BaCl2(aq)+2H2O(l)ΔH=-114.6 kJ·mol-1,故C正确;
D.NH3·H2O是弱碱,电离过程吸热,热化学方程式为HCl(aq)+NH3·H2O(aq)=NH4Cl(aq)+H2O(l)ΔH>-57.3 kJ·mol-1,故D错误;
故选:C。
11.B
【详解】A. Ba(OH)2·8H2O与NH4Cl反应为吸热反应,但该反应中各元素的化合价没有发生变化,不属于氧化还原反应,故A不选;
B. 铝热反应属于放热反应,也是氧化还原反应,故B选;
C. 灼热的炭与水蒸气反应为吸热反应,故C不选;
D. 氢氧化钠与稀盐酸为放热反应,但该反应中各元素的化合价没有发生变化,不属于氧化还原反应,故D不选。
故答案选:B。
12.D
【分析】红热的炭和水蒸气反应生成2mol H2和2molCO气体,吸收262.6kJ热量;红热的炭和水蒸气反应生成1mol氢气和1mol一氧化碳气体,吸收131.3kJ热量,“+”表示放热,“-”表示吸热,由此分析。
【详解】A.热化学方程式需要标注各物质的状态,故A不符合题意;
B.根据分析,红热的炭和水蒸气反应生成1mol氢气和1mol一氧化碳气体,吸收131.3kJ热量,“+”表示吸热,热化学方程式为:C(s)+H2O(g)=H2(g)+CO(g) +131.3kJ,故B不符合题意;
C.红热的炭和水蒸气反应生成2mol氢气和2mol一氧化碳气体,吸收262.6kJ热量,该反应热化学方程式为 ,故C不符合题意;
D.由分析可知,红热的炭和水蒸气反应生成1mol氢气和1mol一氧化碳气体,吸收131.3kJ热量,则该反应热化学方程式为C(s)+H2O(g)=H2(g)+CO(g) ,故D符合题意;
答案为D。
13.A
【详解】A.化合物A先和反应,经过一系列反应又生成了A,因此该机理中化合物A作催化剂,故A错误;
B.反应过程中,A到B、B到C,D到E,钒的成键数改变了,故B正确;
C.A到B的反应过程中有氢氧键的断裂和形成,故C正确;
D.根据图中的转化关系得到制备机理的总反应的方程式为:,故D正确。
综上所述,答案为A。
14.A
【详解】A.将含的稀硫酸即是,与含1molNaOH即是1mol的溶液混合,生成1mol水放出的热量等于 kJ,故A正确;
B.已知,反应放热,正丁烷能量比异丁烷高,据能量越低,越稳定,则异丁烷比正丁烷稳定,故B错误;
C.燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,则的燃烧热为 ,故C错误;
D.已知;,碳完全燃烧比不完全燃烧放热多,则,故D错误。
故选A。
15.A
【详解】A.钠的燃烧反应需要在坩埚中进行,不能在表面皿中加热,故A错误;
B.中和热测量实验中,主要是在量热器中测定反应前后的温度,该装置可以测量中和热,故B正确;
C.Na2CO3、NaHCO3溶液都呈碱性,碳酸钠碱性较强,酚酞遇碱溶液呈红色,所以向相同浓度的Na2CO3、NaHCO3溶液中滴加几滴酚酞,前者呈红色、后者为浅红色,故C正确;
D.乙酸、乙醇在浓硫酸催化下发生酯化反应,饱和碳酸钠溶液可以溶解乙醇、吸收乙酸、分离乙酸乙酯,该装置正确,故D正确;
故选:A。
16.D
【分析】从图中可以看出,起始到第一个台阶C与碳酸根反应生成CO和CO2,失去电子,吸收能量;第二个台阶到第三个台阶,CO和碳酸根生成草酸根,吸收能量,过程中有CO2放出;第三个台阶到第四个台阶,草酸根失去电子生成CO2,吸收过量;第四个台阶到终态CO2释放出来,放出能量。
【详解】A.整个过程中有碳酸根中C-O键断裂,CO中C-O键生成,含极性键的断裂和生成;有草酸根中C-C键的生成的断裂,故有非极性键的生成和断裂,A正确;
B.图示中可以看出,涉及电子转移的变化均吸收能量,B正确;
C.催化剂可以降低反应的活化能,故MoS2 催化剂也是通过降低电极反应的活化能使反应速率加快,C正确;
D.从图中可看出,整个电极总反应为,电极上失去0.2mole 时,生成CO2的体积为3.36L(标况下),D错误;
故选D。
17.A
【分析】由题中所给两个方程式可知:C(石墨)=C(金刚石),吸热1.9kJ。
【详解】A.能量越高越不稳定,故石墨比金刚石稳定,A错误;
B.金刚石和石墨中的化学键和结构不同,转化过程中旧键断裂新键形成,发生的是化学变化,B正确;
C.根据分析,石墨转化为金刚石吸热,说明相同质量的情况下石墨的能量低,C正确;
D.石墨和金刚石的结构不同,故同素异形体具有的能量不同的原因可能是其中的化学键不同,D正确;
故选A。
18.C
【详解】A.放热反应,焓变为负值,故A错误;
B.产物水的状态为液态,故B错误;
C.含1molBa(OH)2的稀溶液与足量稀盐酸反应,放出热量114.6kJ,则生成1mol液态水放热57.3kJ,1/2Ba(OH)2(aq)+HCl(aq)=1/2BaCl2(aq)+H2O(l) ΔH=-57.3kJ/mol,故C正确;
D.放热反应,焓变为负值,故D错误;
选C。
19.D
【详解】根据图象可知石墨的能量低于金刚石的能量,所以该反应是吸热反应。由于能量越低,物质越稳定,所以石墨比金刚石稳定。反应中并没有电子的转移,不属于氧化还原反应。答案选D。
20.B
【详解】A.没有标明物质的状态,A错误;
B.拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,化学方程式为N2(g)+3H2(g) 2NH3(g),依据化学方程式计算反应热为,故其热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-92kJ mol-1,B正确;
C.碳酸的二元弱酸,其电离是分步进行的,电离方程式为:H2CO3 H++HCO,C错误;
D.次氯酸钠有强氧化性,可以把+4价硫氧化为+6价硫,则将SO2气体通入NaClO溶液中的方程式为:,D错误;
故选B。
21.C
【详解】A.量取盐酸溶液的体积时仰视取液,会导致所量的盐酸体积偏大,放出的热量偏高,测得的中和热△H偏小,故A不选;
B. 大小烧杯之间填满碎泡沫塑料的作用是:保温、隔热、减少实验过程中的热量散失,故B不选;
C. 酸碱混合时,量筒中的NaOH溶液应快速倒入盛有盐酸的小烧杯中,以减少热量散失,故C选;
D. 中和热均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以改用盐酸跟溶液进行反应,测得中和热数值相等,故D不选;
故选:C。
22.C
【详解】A.中和热是强酸、强碱的稀溶液发生中和反应产生1 mol液态水和可溶性盐时放出的热量,与反应产生的水的多少无关。HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1, H2SO4和Ca(OH)2反应产生CaSO4和水的中和热ΔH=-57.3 kJ·mol-1,A错误;
B.由N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·mol-1可知:该反应是可逆反应,每1 mol N2发生反应,转移6 mol电子,反应放出热量92.4 kJ。若反应中转移6 mol电子时,反应的N2的物质的量是1 mol,反应放出的热量为92.4 kJ,B错误;
C.燃烧热是1 mol可燃物完全燃烧产生稳定的氧化物时放出是热量,水的稳定状态是液态,所以由甲烷的燃烧热ΔH为-890.3 kJ·mol-1,可知表示甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1,C正确;
D.4 g H2的物质的量是2 mol,2 mol H2完全燃烧生成液态水,放出571.6 kJ热量,1 mol H2完全燃烧生成液态水,放出285.8 kJ。燃烧热是1 mol可燃物完全燃烧产生稳定的氧化物时放出是热量,水的稳定状态是液态,所以表示H2燃烧热的热化学方程式表示为:H2(g)+O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1,D错误;
故合理选项是C。
23.B
【详解】A.李商隐诗句“春蚕到死丝方尽,蜡炬成灰泪始干”,蚕丝为蛋白质,主要成分是高分子化合物,A分析正确;
B.李白诗句“炉火照天地,红星乱紫烟”,紫烟:高温条件下冶炼金属铁、铜,炉火照天地,与碘升华无关,B分析错误;
C.王安石诗句“爆竹声中一岁除,春风送暖人屠苏”,爆竹的燃放,有C、S等元素化合价的改变,为氧化还原反应,C分析正确;
D.曹植诗句“煮豆燃互萁,豆在釜中泣”,可燃物的燃烧,能量变化主要是化学能转化为热能,D分析正确;
答案为B。
24.B
【详解】A. 燃烧热的定义是1mol纯物质完全燃烧生成稳定的氧化物时放出的热量,正丁烷()的燃烧热指的是生成二氧化碳和液态水,故A错误;
B. 根据盖斯定律,由②减①得,=,故B正确;
C.中和热指的是稀的强酸和强碱反应生成1mol液态水时放出的热量,=中除了生成液态水时,还生成了硫酸钡,生成硫酸钡沉淀是要放出热量,故C错误;
D. 由①和②可知,同质量的正丁烷(C4H10)转变为1,3-丁二烯(C4H6)所需要的能量不相同,故D错误;
答案选B。
25.B
【详解】A. 该过程将太阳能转化成为化学能,A正确;B. 该过程中,既有极性键(N-H、O-H)的断裂与生成,也有非极性键(NN、O=O)的断裂与生成,B不正确;C. 该反应的化学方程式为2N2+6H2O=4NH3+3O2,氮气是氧化剂、水是还原剂,氧化剂与还原剂的物质的量之比为1∶3,C正确;D. 原料气N2可通过分离液态空气获得,D正确。本题选B。
26.(1)
(2) 碳 氧气
(3) 光 热
(4)①化石燃料属于不可再生能源,用化石燃料发电会造成资源的浪费;②火力发电的过程中,能量经过多次转化,利用率低,能量损失大;③化石燃料燃烧会产生大量的有害物质(如SO2、CO、NO2、粉尘等),污染环境
【解析】略
27. 2 1 4 4 1 1 6 C 1 10 4 2 10 8 H+ 1 N2(g)+ O2(g)= 2NO(g) △H = +68 kJ/mol
【详解】(1)①反应中Fe、S元素元素的化合价升高,H2O2中O元素的化合价降低,若S2O与Fe2+的物质的量之比为1:2,该反应中Fe2+、S2O都是还原剂,H2O2是氧化剂;1mol S2O和2molFe2+共失去电子[2×(5-2)+2×1]mol=8mol,1molH2O2得到电子2mol,根据电子守恒有4molH2O2反应,最后观察配平H、O原子,该离子反应配平后为:2Fe2++ S2O+4H2O2+4OH ═Fe2O3+ S2O+6H2O;
②A.根据①中分析,S2O→S2O,S的化合价升高,S2O被氧化,该反应中S2O表现了还原性,故A错误;
B.胶体是混合物,Fe2O3纳米颗粒是纯净物,不是混合物,则不是胶体,故B错误;
C.根据①中分析,该反应中H2O2作氧化剂,故C正确;
答案选C。
(2)根据原子守恒可知,另一种生成物是氢离子,Cu 2S中Cu、S元素化合价升高,Fe元素化合价降低,1molCu 2S失去10mol电子,所以需要氧化剂Fe3+ 是10mol,根据得失电子守恒和物料守恒,该过程中发生的离子反应方程为:Cu2S+10Fe3++4H2O2Cu2++10Fe2++8H++SO;
(3)已知1 molN2(g)与适量O2(g)反应生成NO (g),需吸收68 kJ的热量;则热化学反应方程式为:N2(g)+ O2(g)=2NO(g)△H=+68 kJ/mol。
28. △H4 △H6 C2H2(g)+O2(g)=2CO2(g)+H2O(l) △H=-1300KJ/mol (Q1-Q2)KJ/mol 缺少环形玻璃搅拌棒 大小烧杯未齐平 偏小
【分析】(1)燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的能量;中和热是稀强酸、稀强碱反应生成1mol水放出的能量;
(2)1 g C2H2气体完全燃烧生成液态水和CO2气体,放出50 kJ的热量,则1mol乙炔气体完全燃烧生成液态水和CO2气体,放出1300KJ热量;
(3)根据题(1)中B、D,利用盖斯定律计算1 molCO(g)完全燃烧的ΔH;
(4)根据量热计的构造分析装置错误;
【详解】(1) 燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的能量,ΔH表示物质标准燃烧热的是C(s)+O2(g)=CO2(g) ΔH4=-Q2kJ·mol-1;中和热是稀强酸、稀强碱反应生成1mol水放出的能量,表示中和反应反应热的是NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH6;
(2)1 g C2H2气体完全燃烧生成液态水和CO2气体,放出50 kJ的热量,则1mol乙炔气体完全燃烧生成液态水和CO2气体,放出1300KJ热量,该反应的热化学方程式C2H2(g)+O2(g)=2CO2(g)+H2O(l) △H=-1300KJ/mol;
(3) B. C(s)+O2(g)=CO(g) ΔH2=-Q1kJ·mol-1
D. C(s)+O2(g)=CO2(g) ΔH4=-Q2kJ·mol-1
根据盖斯定律D-B得CO(g)+O2(g)= CO2(g) ΔH=(Q1-Q2)KJ/mol;
(4) 根据量热计的构造,实验装置图中的错误是缺少环形玻璃搅拌棒、大小烧杯未齐平;大烧杯上如不塞碎塑料泡沫,热量损失较多,求得的中和反应的反应热的数值偏小。
【点睛】本题考查化学反应的热效应,明确燃烧热、中和热的概念是解题关键,注意量热计的构造,中和热测定实验成败的关键是减少热量损失,会根据盖斯定律计算反应热
一、单选题
1.下列有关化学反应与能量变化的叙述正确的是
A.晶体与晶体的反应,为放热反应
B.石墨转化为金刚石需要吸收热量,据此可判断金刚石比石墨稳定
C.放热反应不需要条件即可发生,而吸热反应必须加热才能实现
D.化学反应中的能量变化主要是由化学键变化引起的
2.下列关于中和热、燃烧热的说法中正确的是( )
A.已知下列热化学方程式:2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol,则氢气的燃烧热为242 kJ/mol
B.中和热包括物质溶解、电离、水合等过程中的热效应
C.燃烧热是指在1.01×105 Pa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量
D.燃烧热随化学方程式前的化学计量数的改变而改变
3.下列反应属于吸热反应的是
A.能量变化如图所示的反应 B.盐酸与NaOH反应
C.CaCO3高温分解 D.CO不完全燃烧
4.下列能正确地表示燃烧热的热化学方程式是
A.
B.
C.
D.
5.下列生产活动或生活中涉及的化学反应不属于放热反应的是
A.燃放爆竹 B.石灰石分解 C.利用铝热反应焊接钢轨 D.牛奶变质
A.A B.B C.C D.D
6.下列叙述错误的是
A.世界是物质的,物质是在不断变化的,而物质的变化总是伴随着能量的变化
B.人类日常利用的煤、天然气、石油等的能量,归根到底是由太阳能转变来的
C.反应热是指反应过程中以热能的形式释放或吸收的反应物和生成物中具有的总能量的差值
D.天然气是二级能源
7.H2在O2中的燃烧是放热反应,下列说法正确的是( )
A.该过程中热能转化为化学能 B.该过程中化学能转化为热能
C.生成物的总能量等于反应物的总能量 D.该反应放热是因为成键过程放出能量
8.环戊二烯广泛用于农药、橡胶、塑料等工业合成,是一种重要的有机化工原料。其相关键能和能量循环图如下所示,下列说法不正确的是
共价键 键能/(kJ/mol)
H-H 436
H-I 299
I-I 151
A.在相同条件下,反应:,则
B.表中三种物质,H-H键能最大,故相同条件下,最稳定
C.
D.将和混合加热,充分反应后测得的反应热与相同
9.下列说法正确的是
A.物质发生化学反应都伴随着能量变化
B.干冰汽化需吸收大量的热,这个变化是吸热反应
C.在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量
D.放热反应的发生无需任何条件
10.已知:25 ℃、101 kPa下,强酸的稀溶液与强碱的稀溶液发生中和反应生成1 mol H2O时,放出57.3 kJ热量,下列有关热化学方程式正确的是
A.H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) ΔH=-114.6 kJ·mol-1
B.H2SO4(aq)+2NH3·H2O (aq)=(NH4)2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
C.2HCl(aq)+Ba(OH)2(aq)=BaCl2(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
D.HCl(aq)+NH3·H2O(aq)=NH4Cl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
11.下列反应中,属于吸热反应同时又是氧化还原反应的是( )
A.Ba(OH)2·8H2O与NH4Cl反应
B.铝热反应
C.灼热的炭与水蒸气生成一氧化碳和氢气的反应
D.氢氧化钠与稀盐酸
12.红热的炭和水蒸气反应生成2 mol H2和2 mol CO气体,吸收262.6 kJ热量,能表示该反应热化学方程式的是
A.
B.
C.
D.
13.以和为原料制备高纯度次氯酸的机理如图,V为元素钒,其最高化合价为+5价,N()、N()为氨基酸,下列说法错误的是
A.该机理中化合物A是中间产物
B.反应过程中,钒的成键数目发生了改变
C.该催化循环过程中有氢氧键的断裂和形成
D.制备机理的总反应的离子方程式为:
14.下列有关热化学方程式的叙述正确的是
A.在稀溶液中: ,若将含的稀硫酸与含1mol NaOH的稀溶液混合,放出的热量等于
B.已知正丁烷异丁烷,则正丁烷比异丁烷稳定
C.,则的燃烧热为
D.已知,,则
15.如图实验装置(部分夹持装置略)或现象错误的是
A.图1表示钠的燃烧
B.图2表示测量盐酸和NaOH溶液反应前后的温度
C.图3表示滴入酚酞溶液
D.图4表示制备并收集乙酸乙酯
16.用“循环电沉积”法处理制备锂电池,其中和C在的催化作用下发生电极反应,其反应历程中的能量变化如下图。下列说法不正确的是
A.反应历程中存在极性键和非极性键的断裂和形成
B.反应历程中涉及电子转移的变化均吸收能量
C.催化剂通过降低电极反应的活化能使反应速率加快
D.电极上失去时,生成的体积为2.24L(标况下)
17.已知相同条件下,12gC(石墨)和12gC(金刚石)发生下列反应的能量变化:
C(石墨) 放热393.5kJ
C(金刚石) 放热395.4kJ
下列判断不正确的是
A.金刚石比石墨稳定
B.金刚石转变成石墨是化学变化
C.12g石墨所具有的能量比12g金刚石低
D.同素异形体具有的能量不同的原因可能是其中的化学键不同
18.含1molBa(OH)2的稀溶液与足量稀盐酸反应,放出热量114.6kJ。下列热化学方程式中,正确的是
A.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(l) ΔH=+114.6kJ/mol
B.Ba(OH)2(aq)+2HCl(aq)=BaCl2(aq)+2H2O(aq) ΔH=-114.6kJ/mol
C.1/2Ba(OH)2(aq)+HCl(aq)=1/2BaCl2(aq)+H2O(l) ΔH=-57.3kJ/mol
D.1/2Ba(OH)2(aq)+HCl(aq)=1/2BaCl2(aq)+H2O(l) ΔH=+57.3kJ/mol
19.已知(石墨) = (金刚石),在该反应进程中其能量变化如图所示,有关该反应的描述正确的是
A.该反应为放热反应
B.金刚石比石墨稳定
C.该反应为氧化还原反应
D.石墨比金刚石稳定
20.下列方程式书写正确的是
A.一氧化碳燃烧热化学方程式为CO+O2=CO2 △H=-283kJ mol-1
B.拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为N2(g)+3H2(g) 2NH3(g) △H=-92kJ mol-1
C.碳酸电离的方程式H2CO32H++CO
D.将SO2气体通入NaClO溶液中:SO2+2ClO-+H2O=SO+2HClO
21.中和热测定实验中,用盐酸和溶液进行实验,下列说法不正确的是
A.用量筒量取盐酸时仰视取液,测得的中和热偏小
B.装置中的大小烧杯之闻填满碎泡沫塑料的作用是保温隔热减少热量损失
C.酸碱混合时,量筒中溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌
D.改用盐酸跟溶液进行反应,求出的中和热和原来相同
22.下列热化学方程式中,正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1
B.由N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·mol-1可知,当反应中转移6 mol电子时,反应放出的热量小于92.4 kJ
C.甲烷的燃烧热ΔH为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
D.在101 kPa时,4 g H2完全燃烧生成液态水,放出571.6 kJ热量,氢气燃烧热的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
23.《中国诗词大会》节目不仅继承和发扬中华优秀传统文化,还蕴含许多化学知识。下列诗句中的化学知识分析不正确的是
A.李商隐诗句“春蚕到死丝方尽,蜡炬成灰泪始干”,蚕丝的主要成分是高分子化合物
B.李白诗句“炉火照天地,红星乱紫烟”,“紫烟”是指碘升华的现象
C.王安石诗句“爆竹声中一岁除,春风送暖人屠苏”,爆竹的燃放涉及氧化还原反应
D.曹植诗句“煮豆燃互萁,豆在釜中泣”,其中的能量变化主要是化学能转化为热能
24.最近有科学家发现正丁烷()脱氢或不完全氧化也可制得1,3-丁二烯(),已知热化学方程式如下:( )
①=
②=
③=
下列说法正确的是( )
A.由②可知,正丁烷()的燃烧热为
B.由①和②可推知:=
C.=
D.由①和②可知,同质量的正丁烷()转变为1,3-丁二烯()所需要的能量相同
25.中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图。下列说法不正确的是
A.该过程将太阳能转化成为化学能
B.该过程中,只涉及非极性键的断裂与生成
C.氧化剂与还原剂的物质的量之比为1∶3
D.原料气N2可通过分离液态空气获得
二、填空题
26.燃煤发电是目前我国主要的火力发电形式,思考并回答下列问题:
(1)写出碳完全燃烧的化学方程式并用双线桥标出上述反应中电子转移的方向和数目: 。
(2)上述燃烧反应中发生氧化反应的是 ,氧化剂是 。
(3)碳燃烧过程中化学能主要转变为 能和 能。
(4)试从资源、能效、对环境的影响等方面,阐述火力发电的弊端有哪些? 。
27.(1) S2O可以与Fe2+反应制备Fe2O3纳米颗粒。
①若S2O与Fe2+的物质的量之比为1:2,配平该反应的离子方程式:
Fe2++ S2O + H2O2+ OH- = Fe2O3+ S2O+ H2O
②下列关于该反应的说法中正确的是 (填序号)。
A 该反应中S2O表现了氧化性
B 已知生成的Fe2O3纳米颗粒直径为10纳米,则Fe2O3纳米颗粒为胶体
C 该反应中H2O2作氧化剂
(2)人们可利用Fe2(SO4)3作强氧化剂溶解铜矿石(Cu2S),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:
Cu2S+ Fe3++ H2O Cu2++ Fe2++ ( )+ SO
(3)书写下列反应的热化学方程式: 1 molN2(g)与适量O2(g)反应生成NO (g),需吸收68 kJ的热量; 。
28.化学反应过程中发生物质变化的同时,常常伴有能量的变化。这种能量的变化常以热量的形式表现出来,叫做反应热。由于反应的情况不同,反应热可分为许多种,如标准燃烧热和中和反应反应热等。
(1)下列ΔH表示物质标准燃烧热的是 ;表示中和反应反应热的是 。(填“ΔH1”、“ΔH2”、“ΔH3”等)
A.2H2(g)+O2(g)=2H2O(l) ΔH1
B.C(s)+O2(g)=CO(g) ΔH2=-Q1kJ·mol-1
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH3
D.C(s)+O2(g)=CO2(g) ΔH4=-Q2kJ·mol-1
E.Ba(OH) 2(aq)+H2SO4(aq)= BaSO4(aq)+2H2O(l) ΔH5
F.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH6
(2)1 g C2H2气体完全燃烧生成液态水和CO2气体,放出50 kJ的热量,写出该反应的热化学方程式: 。
(3)根据题(1)中B、D判断1 molCO(g)完全燃烧的ΔH= 。
(4)反应F的ΔH6可以用如图所示的装置进行测量。
从实验装置上看,图中有两种错误,分别是 ; ;大烧杯上如不塞碎塑料泡沫,求得的中和反应的反应热的数值 (填“偏大”“偏小”或“无影响”)。
试卷第1页,共3页
参考答案:
1.D
【详解】A.晶体与晶体反应生成氯化钡、氨气和水,该反应是吸热反应,A错误;
B.石墨转化为金刚石需要吸收热量,说明在相同条件下,石墨的能量较低,能量越低越稳定,故据此可判断石墨比金刚石稳定,B错误;
C.有些放热反应需要加热或高温的条件才能引发,而有些吸热反应不用加热也能实现,一个反应是放热反应还是吸热反应,与反应条件无关,C错误;
D.在化学反应中,破坏反应物中的化学要吸收能量,而形成生成物中的化学要放出能量,因此,化学反应中的能量变化主要是由化学键变化引起的,D正确;
故选D。
2.C
【详解】燃烧热是指1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,水为液态水;中和热是指在稀溶液中,酸跟碱发生中和反应生成1 mol液态水时的反应热,据此分析解题:
A.已知下列热化学方程式:2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol,水必须为液态水,故无法得出氢气的燃烧热,A错误;
B.中和热就是反应过程中的热效应,不包括物质溶解、电离、水合等过程中的热效应,B错误;
C.在1.01×105 Pa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量就是该物质的燃烧热,C正确;
D.根据燃烧热定义可知,燃烧热不随化学方程式前的化学计量数的改变而改变,D错误;
故答案为:C。
3.C
【详解】A.反应物能量总和大于生成物能量总和,当反应发生时,剩余能量以热能形式释放出来,所以是放热反应,不符题意;
B.酸碱中和反应是放热反应,不符题意;
C.碳酸钙受热分解属于吸热反应,符合题意;
D.所有燃烧均是放热反应,不符题意;
综上,本题选C。
4.A
【详解】燃烧热是指1mol可燃物完全燃烧生成稳定化合物放出的热量,的燃烧热为,则完全燃烧生成1mol二氧化碳和2mol液态水放出的热量,所以燃烧的热化学方程式为: ,故A正确。
5.B
【详解】A.燃烧爆炸属于放热反应,A错误;
B.石灰石分解属于吸热反应,B正确;
C.铝热反应属于放热反应,C错误;
D.牛奶变质,缓慢的氧化反应属于放热反应,D错误;
故选B。
6.D
【详解】A.世界是物质的,物质是在不断变化的,而物质的变化总是伴随着能量的变化,正确;
B.人类日常利用的煤、天然气、石油等的能量,归根到底是由古代的动物、植物等经过漫长的历史时期形成的,因此是由太阳能转变而来的,正确;
C.反应热是指反应过程中以热能的形式释放或吸收的反应物和生成物中具有的总能量的差值,正确;
D.天然气是直接开采出来就使用的能源,是一级能源,错误;
故选D。
7.B
【详解】
A.H2在O2中燃烧生成水时会放出热能,是由于化学能转化为热能,故A错误;
B.H2在O2中燃烧生成水时会放出热能,是由于化学能转化为热能,故B正确;
C.放热反应中反应物的总能量高于生成物的总能量,故C错误;
D.该反应放热是因为新化学键形成时所释放的总能量大于旧化学键断裂时所吸收的总能量,故D错误;
答案选B。
8.D
【详解】A.比更活泼,说明自身具有的能量大于具有的能量,所以和反应生成,放出的能量大于与反应生成放出的能量,,A项正确;
B.键能越大越稳定,H-H键能最大,故相同条件下, 最稳定,B项正确;
C.根据盖斯定律:,,C项正确;
D.反应热与 不相同,D项错误;
答案选D。
9.A
【详解】A.化学反应的特征是:一是生成新物质,二是伴随着能量的变化,A项正确;
B.吸热反应属于化学变化,干冰汽化需吸收大量的热,该过程是物理变化,不是吸热反应,B项错误;
C.在一个确定的化学反应关系中,反应物的总能量不等于生成物的总能量,若反应物的总能量总是高于生成物的总能量,该反应为放热反应,若反应物的总能量总是低于生成物的总能量,该反应为吸热反应,C项错误;
D.有的放热反应也需要条件,如铝热反应,需要高温加热,D项错误;
答案选A。
10.C
【详解】A.生成硫酸钡放热,由中和热及物质的量与热量成正比可知H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)△H<-114.6 kJ mol-1,故A错误;
B.NH3·H2O是弱碱,电离过程吸热,热化学方程式为H2SO4(aq)+2NH3·H2O (aq)=(NH4)2SO4(aq)+2H2O(l) ΔH>-114.6 kJ·mol-1,故B错误;
C.发生中和反应生成1 mol H2O时,放出57.3 kJ热量,则生成2 mol H2O时,放出114.6 kJ热量,热化学方程式为2HCl(aq)+Ba(OH)2(aq)=BaCl2(aq)+2H2O(l)ΔH=-114.6 kJ·mol-1,故C正确;
D.NH3·H2O是弱碱,电离过程吸热,热化学方程式为HCl(aq)+NH3·H2O(aq)=NH4Cl(aq)+H2O(l)ΔH>-57.3 kJ·mol-1,故D错误;
故选:C。
11.B
【详解】A. Ba(OH)2·8H2O与NH4Cl反应为吸热反应,但该反应中各元素的化合价没有发生变化,不属于氧化还原反应,故A不选;
B. 铝热反应属于放热反应,也是氧化还原反应,故B选;
C. 灼热的炭与水蒸气反应为吸热反应,故C不选;
D. 氢氧化钠与稀盐酸为放热反应,但该反应中各元素的化合价没有发生变化,不属于氧化还原反应,故D不选。
故答案选:B。
12.D
【分析】红热的炭和水蒸气反应生成2mol H2和2molCO气体,吸收262.6kJ热量;红热的炭和水蒸气反应生成1mol氢气和1mol一氧化碳气体,吸收131.3kJ热量,“+”表示放热,“-”表示吸热,由此分析。
【详解】A.热化学方程式需要标注各物质的状态,故A不符合题意;
B.根据分析,红热的炭和水蒸气反应生成1mol氢气和1mol一氧化碳气体,吸收131.3kJ热量,“+”表示吸热,热化学方程式为:C(s)+H2O(g)=H2(g)+CO(g) +131.3kJ,故B不符合题意;
C.红热的炭和水蒸气反应生成2mol氢气和2mol一氧化碳气体,吸收262.6kJ热量,该反应热化学方程式为 ,故C不符合题意;
D.由分析可知,红热的炭和水蒸气反应生成1mol氢气和1mol一氧化碳气体,吸收131.3kJ热量,则该反应热化学方程式为C(s)+H2O(g)=H2(g)+CO(g) ,故D符合题意;
答案为D。
13.A
【详解】A.化合物A先和反应,经过一系列反应又生成了A,因此该机理中化合物A作催化剂,故A错误;
B.反应过程中,A到B、B到C,D到E,钒的成键数改变了,故B正确;
C.A到B的反应过程中有氢氧键的断裂和形成,故C正确;
D.根据图中的转化关系得到制备机理的总反应的方程式为:,故D正确。
综上所述,答案为A。
14.A
【详解】A.将含的稀硫酸即是,与含1molNaOH即是1mol的溶液混合,生成1mol水放出的热量等于 kJ,故A正确;
B.已知,反应放热,正丁烷能量比异丁烷高,据能量越低,越稳定,则异丁烷比正丁烷稳定,故B错误;
C.燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,则的燃烧热为 ,故C错误;
D.已知;,碳完全燃烧比不完全燃烧放热多,则,故D错误。
故选A。
15.A
【详解】A.钠的燃烧反应需要在坩埚中进行,不能在表面皿中加热,故A错误;
B.中和热测量实验中,主要是在量热器中测定反应前后的温度,该装置可以测量中和热,故B正确;
C.Na2CO3、NaHCO3溶液都呈碱性,碳酸钠碱性较强,酚酞遇碱溶液呈红色,所以向相同浓度的Na2CO3、NaHCO3溶液中滴加几滴酚酞,前者呈红色、后者为浅红色,故C正确;
D.乙酸、乙醇在浓硫酸催化下发生酯化反应,饱和碳酸钠溶液可以溶解乙醇、吸收乙酸、分离乙酸乙酯,该装置正确,故D正确;
故选:A。
16.D
【分析】从图中可以看出,起始到第一个台阶C与碳酸根反应生成CO和CO2,失去电子,吸收能量;第二个台阶到第三个台阶,CO和碳酸根生成草酸根,吸收能量,过程中有CO2放出;第三个台阶到第四个台阶,草酸根失去电子生成CO2,吸收过量;第四个台阶到终态CO2释放出来,放出能量。
【详解】A.整个过程中有碳酸根中C-O键断裂,CO中C-O键生成,含极性键的断裂和生成;有草酸根中C-C键的生成的断裂,故有非极性键的生成和断裂,A正确;
B.图示中可以看出,涉及电子转移的变化均吸收能量,B正确;
C.催化剂可以降低反应的活化能,故MoS2 催化剂也是通过降低电极反应的活化能使反应速率加快,C正确;
D.从图中可看出,整个电极总反应为,电极上失去0.2mole 时,生成CO2的体积为3.36L(标况下),D错误;
故选D。
17.A
【分析】由题中所给两个方程式可知:C(石墨)=C(金刚石),吸热1.9kJ。
【详解】A.能量越高越不稳定,故石墨比金刚石稳定,A错误;
B.金刚石和石墨中的化学键和结构不同,转化过程中旧键断裂新键形成,发生的是化学变化,B正确;
C.根据分析,石墨转化为金刚石吸热,说明相同质量的情况下石墨的能量低,C正确;
D.石墨和金刚石的结构不同,故同素异形体具有的能量不同的原因可能是其中的化学键不同,D正确;
故选A。
18.C
【详解】A.放热反应,焓变为负值,故A错误;
B.产物水的状态为液态,故B错误;
C.含1molBa(OH)2的稀溶液与足量稀盐酸反应,放出热量114.6kJ,则生成1mol液态水放热57.3kJ,1/2Ba(OH)2(aq)+HCl(aq)=1/2BaCl2(aq)+H2O(l) ΔH=-57.3kJ/mol,故C正确;
D.放热反应,焓变为负值,故D错误;
选C。
19.D
【详解】根据图象可知石墨的能量低于金刚石的能量,所以该反应是吸热反应。由于能量越低,物质越稳定,所以石墨比金刚石稳定。反应中并没有电子的转移,不属于氧化还原反应。答案选D。
20.B
【详解】A.没有标明物质的状态,A错误;
B.拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,化学方程式为N2(g)+3H2(g) 2NH3(g),依据化学方程式计算反应热为,故其热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-92kJ mol-1,B正确;
C.碳酸的二元弱酸,其电离是分步进行的,电离方程式为:H2CO3 H++HCO,C错误;
D.次氯酸钠有强氧化性,可以把+4价硫氧化为+6价硫,则将SO2气体通入NaClO溶液中的方程式为:,D错误;
故选B。
21.C
【详解】A.量取盐酸溶液的体积时仰视取液,会导致所量的盐酸体积偏大,放出的热量偏高,测得的中和热△H偏小,故A不选;
B. 大小烧杯之间填满碎泡沫塑料的作用是:保温、隔热、减少实验过程中的热量散失,故B不选;
C. 酸碱混合时,量筒中的NaOH溶液应快速倒入盛有盐酸的小烧杯中,以减少热量散失,故C选;
D. 中和热均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以改用盐酸跟溶液进行反应,测得中和热数值相等,故D不选;
故选:C。
22.C
【详解】A.中和热是强酸、强碱的稀溶液发生中和反应产生1 mol液态水和可溶性盐时放出的热量,与反应产生的水的多少无关。HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1, H2SO4和Ca(OH)2反应产生CaSO4和水的中和热ΔH=-57.3 kJ·mol-1,A错误;
B.由N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·mol-1可知:该反应是可逆反应,每1 mol N2发生反应,转移6 mol电子,反应放出热量92.4 kJ。若反应中转移6 mol电子时,反应的N2的物质的量是1 mol,反应放出的热量为92.4 kJ,B错误;
C.燃烧热是1 mol可燃物完全燃烧产生稳定的氧化物时放出是热量,水的稳定状态是液态,所以由甲烷的燃烧热ΔH为-890.3 kJ·mol-1,可知表示甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1,C正确;
D.4 g H2的物质的量是2 mol,2 mol H2完全燃烧生成液态水,放出571.6 kJ热量,1 mol H2完全燃烧生成液态水,放出285.8 kJ。燃烧热是1 mol可燃物完全燃烧产生稳定的氧化物时放出是热量,水的稳定状态是液态,所以表示H2燃烧热的热化学方程式表示为:H2(g)+O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1,D错误;
故合理选项是C。
23.B
【详解】A.李商隐诗句“春蚕到死丝方尽,蜡炬成灰泪始干”,蚕丝为蛋白质,主要成分是高分子化合物,A分析正确;
B.李白诗句“炉火照天地,红星乱紫烟”,紫烟:高温条件下冶炼金属铁、铜,炉火照天地,与碘升华无关,B分析错误;
C.王安石诗句“爆竹声中一岁除,春风送暖人屠苏”,爆竹的燃放,有C、S等元素化合价的改变,为氧化还原反应,C分析正确;
D.曹植诗句“煮豆燃互萁,豆在釜中泣”,可燃物的燃烧,能量变化主要是化学能转化为热能,D分析正确;
答案为B。
24.B
【详解】A. 燃烧热的定义是1mol纯物质完全燃烧生成稳定的氧化物时放出的热量,正丁烷()的燃烧热指的是生成二氧化碳和液态水,故A错误;
B. 根据盖斯定律,由②减①得,=,故B正确;
C.中和热指的是稀的强酸和强碱反应生成1mol液态水时放出的热量,=中除了生成液态水时,还生成了硫酸钡,生成硫酸钡沉淀是要放出热量,故C错误;
D. 由①和②可知,同质量的正丁烷(C4H10)转变为1,3-丁二烯(C4H6)所需要的能量不相同,故D错误;
答案选B。
25.B
【详解】A. 该过程将太阳能转化成为化学能,A正确;B. 该过程中,既有极性键(N-H、O-H)的断裂与生成,也有非极性键(NN、O=O)的断裂与生成,B不正确;C. 该反应的化学方程式为2N2+6H2O=4NH3+3O2,氮气是氧化剂、水是还原剂,氧化剂与还原剂的物质的量之比为1∶3,C正确;D. 原料气N2可通过分离液态空气获得,D正确。本题选B。
26.(1)
(2) 碳 氧气
(3) 光 热
(4)①化石燃料属于不可再生能源,用化石燃料发电会造成资源的浪费;②火力发电的过程中,能量经过多次转化,利用率低,能量损失大;③化石燃料燃烧会产生大量的有害物质(如SO2、CO、NO2、粉尘等),污染环境
【解析】略
27. 2 1 4 4 1 1 6 C 1 10 4 2 10 8 H+ 1 N2(g)+ O2(g)= 2NO(g) △H = +68 kJ/mol
【详解】(1)①反应中Fe、S元素元素的化合价升高,H2O2中O元素的化合价降低,若S2O与Fe2+的物质的量之比为1:2,该反应中Fe2+、S2O都是还原剂,H2O2是氧化剂;1mol S2O和2molFe2+共失去电子[2×(5-2)+2×1]mol=8mol,1molH2O2得到电子2mol,根据电子守恒有4molH2O2反应,最后观察配平H、O原子,该离子反应配平后为:2Fe2++ S2O+4H2O2+4OH ═Fe2O3+ S2O+6H2O;
②A.根据①中分析,S2O→S2O,S的化合价升高,S2O被氧化,该反应中S2O表现了还原性,故A错误;
B.胶体是混合物,Fe2O3纳米颗粒是纯净物,不是混合物,则不是胶体,故B错误;
C.根据①中分析,该反应中H2O2作氧化剂,故C正确;
答案选C。
(2)根据原子守恒可知,另一种生成物是氢离子,Cu 2S中Cu、S元素化合价升高,Fe元素化合价降低,1molCu 2S失去10mol电子,所以需要氧化剂Fe3+ 是10mol,根据得失电子守恒和物料守恒,该过程中发生的离子反应方程为:Cu2S+10Fe3++4H2O2Cu2++10Fe2++8H++SO;
(3)已知1 molN2(g)与适量O2(g)反应生成NO (g),需吸收68 kJ的热量;则热化学反应方程式为:N2(g)+ O2(g)=2NO(g)△H=+68 kJ/mol。
28. △H4 △H6 C2H2(g)+O2(g)=2CO2(g)+H2O(l) △H=-1300KJ/mol (Q1-Q2)KJ/mol 缺少环形玻璃搅拌棒 大小烧杯未齐平 偏小
【分析】(1)燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的能量;中和热是稀强酸、稀强碱反应生成1mol水放出的能量;
(2)1 g C2H2气体完全燃烧生成液态水和CO2气体,放出50 kJ的热量,则1mol乙炔气体完全燃烧生成液态水和CO2气体,放出1300KJ热量;
(3)根据题(1)中B、D,利用盖斯定律计算1 molCO(g)完全燃烧的ΔH;
(4)根据量热计的构造分析装置错误;
【详解】(1) 燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的能量,ΔH表示物质标准燃烧热的是C(s)+O2(g)=CO2(g) ΔH4=-Q2kJ·mol-1;中和热是稀强酸、稀强碱反应生成1mol水放出的能量,表示中和反应反应热的是NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH6;
(2)1 g C2H2气体完全燃烧生成液态水和CO2气体,放出50 kJ的热量,则1mol乙炔气体完全燃烧生成液态水和CO2气体,放出1300KJ热量,该反应的热化学方程式C2H2(g)+O2(g)=2CO2(g)+H2O(l) △H=-1300KJ/mol;
(3) B. C(s)+O2(g)=CO(g) ΔH2=-Q1kJ·mol-1
D. C(s)+O2(g)=CO2(g) ΔH4=-Q2kJ·mol-1
根据盖斯定律D-B得CO(g)+O2(g)= CO2(g) ΔH=(Q1-Q2)KJ/mol;
(4) 根据量热计的构造,实验装置图中的错误是缺少环形玻璃搅拌棒、大小烧杯未齐平;大烧杯上如不塞碎塑料泡沫,热量损失较多,求得的中和反应的反应热的数值偏小。
【点睛】本题考查化学反应的热效应,明确燃烧热、中和热的概念是解题关键,注意量热计的构造,中和热测定实验成败的关键是减少热量损失,会根据盖斯定律计算反应热
