2.3.1 常见的醛、酮 醛、酮的化学性质(共24张PPT)-2023-2024学年高二化学鲁科版选择性必修第三册课件
文档属性
| 名称 | 2.3.1 常见的醛、酮 醛、酮的化学性质(共24张PPT)-2023-2024学年高二化学鲁科版选择性必修第三册课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-20 00:00:00 | ||
图片预览






文档简介
(共24张PPT)
第三节 醛和酮 糖类和核酸
第1课时 常见的醛、酮 醛、酮的化学性质
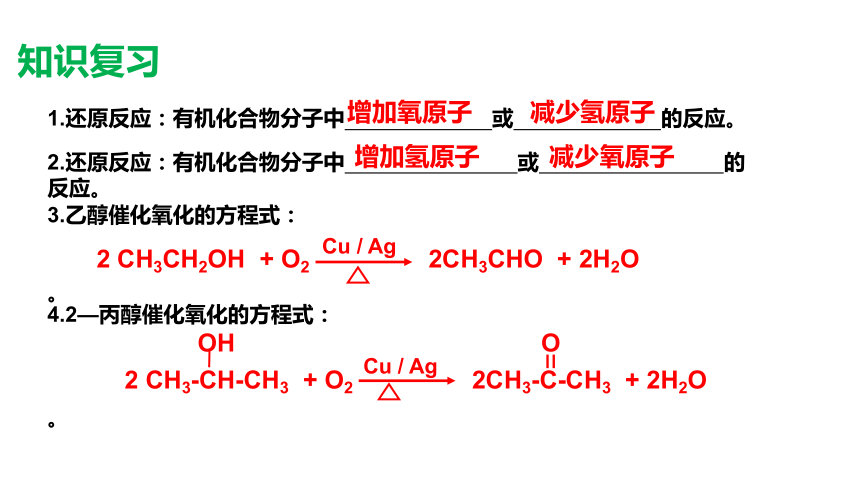
知识复习
2.还原反应:有机化合物分子中 或 的反应。
1.还原反应:有机化合物分子中 或 的反应。
3.乙醇催化氧化的方程式:
。
4.2—丙醇催化氧化的方程式:
。
2 CH3CH2OH + O2 2CH3CHO + 2H2O
Cu / Ag
2 CH3-CH-CH3 + O2 2CH3-C-CH3 + 2H2O
OH
Cu / Ag
O
=
增加氢原子
减少氧原子
增加氧原子
减少氢原子
联想·质疑
福尔马林是 35%~ 45%的甲醛水溶液,某些动物标本通常被保存在稀释的福尔马林中。
酮是一种重要的有机溶剂,它在化学实验和工业生产中都有着广泛的应用。例如,工业上常以丙酮为原料制造塑料和涂料。
葡萄糖是供给人体能量的物质之一。高浓度的葡萄糖溶液(葡萄糖的质量分数在50%以上)配以相关的药物输入患者体内可以治疗肠道感染、静脉炎等多种疾病。
甲醛和丙酮分别属于哪类有机化合物?它们的结构和性质是怎样的?葡萄糖是一种组成较简单的糖类物质,它与甲醛和丙酮有什么联系吗?
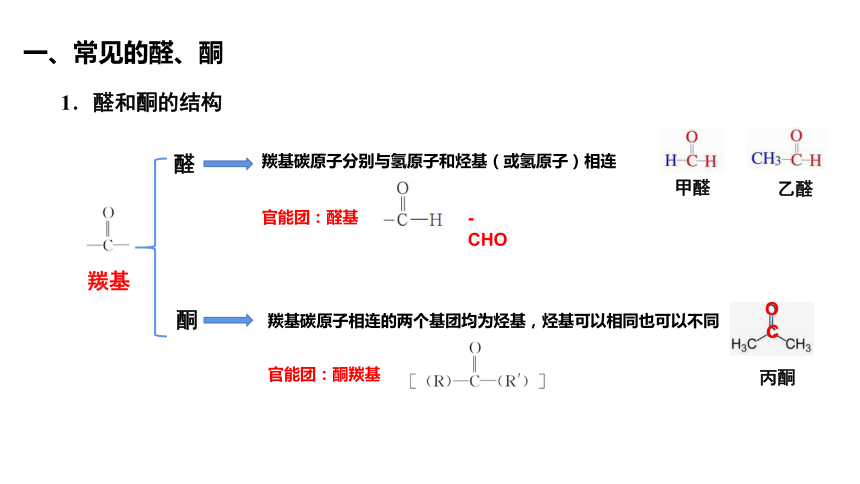
一、常见的醛、酮
1.醛和酮的结构
羰基
醛
羰基碳原子分别与氢原子和烃基(或氢原子)相连
官能团:醛基
-CHO
酮
羰基碳原子相连的两个基团均为烃基,烃基可以相同也可以不同
官能团:酮羰基
甲醛
乙醛
O
C
丙酮
2.醛和酮的命名
醛、酮的命名和醇的命名相似。
2 - 甲基丙醛
2 - 戊酮
1. 选择分子中连有醛基(或羰基)的碳原子在内的最长碳链做主链,按主链所含碳原子数称为某醛(或酮)。
2. 对主链碳原子的编号由接近醛基(或羰基)的一端开始。
3. 命名时,醛基碳为1号碳,不用注明位置;羰基的位次号写在“某酮”的前面,其他取代基的名称和位次号写在母体名称的前面。
3.饱和一元醛和饱和一元酮
通式:
CnH2nO
分子中碳原子数相同的饱和一元醛和饱和一元酮互为同分异构体。
1.丙醛(CH3CH2CHO)与丙酮(CH3COCH3)有何联系?
2.分子式为C2H4O和C3H6O的有机物一定是同系物吗?
思考:
两者互为同分异构体。
不一定,C2H4O是乙醛,分子式为C3H6O的有机物可能是丙醛,也可能是丙酮,还可能是环丙醇或烯丙醇。
交流·研讨
下表列出了分子式为 C5H10O 的醛和酮的部分同分异构体的结构简式,请写出属于醛、酮的其他同分异构体的结构简式,并举例说明这些异构体异构关系的类型。
异构体的结构简式
异构类型 (每种各举几例即可) 碳骨架异构 如:①和②
官能团类型异构 如:①和③
官能团位置异构 如:③和④
CH3CHCH2CHO
|
CH3
CH3CCHO
|
CH3
|
CH3
⑤
⑥
CH3CH—C—CH3
|
CH3
|
|
O
⑦
②和⑤
②和⑥
①和⑤
②和④
⑤和⑦
⑥和⑦
⑤和③
②和⑦
①和④
①和⑦
②和③
⑤和④
⑥和③
⑥和④
①和⑥
⑤和⑥
④和⑦
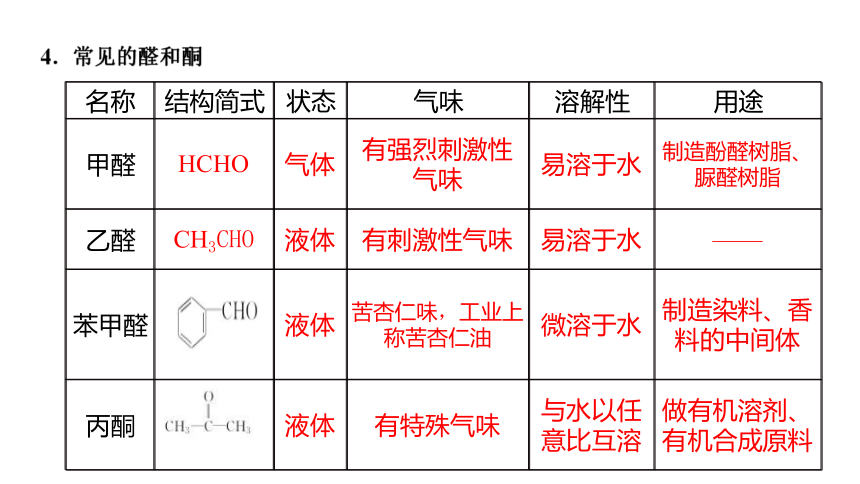
4.常见的醛和酮
名称 结构简式 状态 气味 溶解性 用途
甲醛
乙醛
苯甲醛
丙酮
HCHO 气体 有强烈刺激性气味 易溶于水 制造酚醛树脂、脲醛树脂
CH3CHO 液体 有刺激性气味 易溶于水 ——
液体 苦杏仁味,工业上称苦杏仁油 微溶于水 制造染料、香料的中间体
液体 有特殊气味 与水以任意比互溶 做有机溶剂、有机合成原料
福尔马林浸泡的动物尸体
身边的化学
视黄醛 人体内缺乏维生素 A 会导致眼角膜硬化,表现为在光线昏暗环境下或夜晚视物不清,即夜盲症。这是因为维生素 A 在人体内很容易被氧化成视黄醛,而视黄醛的缺乏是引起视觉障碍的主要原因。
常见的醛、酮举例
2- 庚酮 蜜蜂传递警戒信息的激素含有的 2- 庚酮( ),是昆虫之间进行化学通信的高活性微量化学信息物质之一。
交流·研讨
与其他有机化合物相比,醛、酮的化学性质较活泼,这与它们官能团的结构密切相关。
1. 请分析醛的结构特点,利用你所掌握的有机化合物结构与性质间关系的知识,推测醛可能具有的化学性质,完成下表。
分析结构 预测性质
断键部位 反应类型 反应试剂和条件 反应产物
官能团: 是否含不饱和键: 键的极性: 基团之间的相互影响:
2. 思考酮的化学性质与醛的化学性质有哪些相同点和不同点。
二、醛、酮的化学性质
1. 羰基的加成反应
羰基上的C=O键在一定条件下可与H2、HX、HCN、NH3、氨的衍生物、醇等发生加成反应。
醛或酮与氢氰酸加成,反应产物的分子比原来的醛分子或酮分子多了一个碳原子。这类加成反应在有机合成中可以用于增长碳链。
现代科学研究表明,甲醛对人体健康有很大危害。当室内空气中甲醛含量为 0.1 mg·m-3时,就会有异味并引起人的不适感;食用含有甲醛的食品,也会使人中毒。
甲醛为什么有毒?它在人体内发生了什么变化?
醛、酮能与氨的衍生物发生加成反应,反应的产物还会发生分子内脱水反应。从总的结果来看,这类反应相当于在醛、酮和氨的衍生物的分子之间脱掉了水分子。甲醛参与的相关反应可表示为:
身边的化学
甲醛为什么有毒
人体中重要的生物大分子如核酸、蛋白质均含有氨基(-NH2),当甲醛进入人体后,其分子中的羰基会与这些氨基发生类似醛与氨的衍生物的反应,使得核酸或蛋白质大分子的结构发生改变;轻者导致人体出现病变,重者可造成一些重要基因突变而导致癌症发生。
活动探究
通过化学必修课程的学习,你已经知道葡萄糖能与新制氢氧化铜悬浊液反应产生砖红色的氧化亚铜(Cu2O)沉淀,这其实就是葡萄糖分子中醛基发生的氧化反应。请设计实验验证醛基的还原性。
醛的氧化反应
乙醛, 0.5% 酸性 KMnO4 溶液,银氨溶液,10% NaOH 溶液,2% CuSO4 溶液;
试管,烧杯,胶头滴管,酒精灯,三脚架,石棉网,试管夹等。
实验用品
银氨溶液的配制和使用
在一支洁净的试管中,加入 1 mL 2% AgNO3 溶液,边振荡边滴加 2% 氨水,直至最初产生的沉淀恰好消失,便得到银氨溶液,其主要成分的化学式为[Ag(NH3)2]OH。银氨溶液与醛的反应需要在 60 ~70 ℃的水浴中进行。
实验内容 实验操作 实验现象 化学方程式
1.乙醛与酸性高锰酸钾溶液反应 取适量乙醛溶液与试管,加入酸性高锰酸钾溶液,振荡,观察现象。 酸性高锰酸钾溶液褪色
2.乙醛与银氨溶液的反应 取适量乙醛溶液与干净洁净的试管,加入配置好的银氨溶液,水浴加热 洁净的试管内壁形成光亮的银镜 CH3CHO+2[Ag(NH3)2]OH CH3COONH4+2Ag↓+3NH3+H2O
3.乙醛与新制氢氧化铜悬浊液反应 向10%的氢氧化钠溶液中加入5—6滴2%硫酸铜溶液,然后再加入乙醛溶液,用酒精等加热,观察实验现象 有砖红色沉淀生成 CH3CHO+2Cu(OH)2+NaOH
CH3COONa+Cu2O↓+3H2O
实验方案设计及实施
你所得到的实验现象和其他同学的相同吗?如不同,请分析原因。
思考:
(1)银镜反应的注意事项①试管必须洁净。②银氨溶液必须现用现配,不能久置;且氨水不能过量,否则,都容易产生易爆炸物质。③用水浴加热,不能直接加热,加热时不能振荡或摇动试管。④生成银镜的试管用稀硝酸溶解洗净。
(2)与新制氢氧化铜悬浊液反应的注意事项①氢氧化铜悬浊液要现用现配。②NaOH必须过量。③直接加热至沸腾。
2. 氧化反应和还原反应
(1) 氧化反应
醛和酮具有还原性,可被KMnO4(H+)溶液、溴水等较强的氧化剂氧化。
KMnO4(H+)溶液
加入乙醛溶液
醛的还原性较强比酮容易发生氧化反应,可被KMnO4(H+)溶液、溴水等较强的氧化剂氧化,也可被较弱的氧化剂银氨溶液、新制Cu(OH)2悬浊液氧化,而酮一般需很强的氧化剂才能被氧化。
CH3CHO+2[Ag(NH3)2]OH CH3COONH4+2Ag↓+3NH3+H2O
CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
△
△
银氨溶液和新制Cu(OH)2悬浊液常用于鉴别有机化合物分子中是否含有醛基。
(2) 还原反应
醛、酮中都含羰基,都能发生还原反应,还原产物一般是醇,化学反应的通式分别为
归纳总结
类别 醛 酮
区别 官能团
官能团位置
简写形式
性质
联系 通式
同分异构现象
性质
醛、酮的区别与联系
归纳总结
类别 醛 酮
区别 官能团
官能团位置 碳链末端 碳链中间
简写形式
性质 能被弱氧化剂氧化,发生银镜反应等 不能被弱氧化剂氧化
联系 通式 饱和一元醛:CnH2nO 饱和一元酮:CnH2nO
同分异构现象 碳原子数相同的饱和一元醛和饱和一元酮互为同分异构体
性质 可与H2、HX、HCN、NH3、氨的衍生物、醇等发生加成反应 均可加氢还原成醇 均可被强氧化剂氧化,都能使酸性高锰酸钾钾溶液褪色
醛、酮的区别与联系
课堂小结
醛、酮
共性
结构
官能团
饱和一元醛、酮的通式
醛
酮
醛基
羰基
CnH2nO
羰基的加成反应
氧化反应
燃烧
使酸性高锰酸钾、溴水褪色
醛的银镜反应
还原反应
与氢气加成反应,生成醇
新制氢氧化铜悬浊液反应
第三节 醛和酮 糖类和核酸
第1课时 常见的醛、酮 醛、酮的化学性质
知识复习
2.还原反应:有机化合物分子中 或 的反应。
1.还原反应:有机化合物分子中 或 的反应。
3.乙醇催化氧化的方程式:
。
4.2—丙醇催化氧化的方程式:
。
2 CH3CH2OH + O2 2CH3CHO + 2H2O
Cu / Ag
2 CH3-CH-CH3 + O2 2CH3-C-CH3 + 2H2O
OH
Cu / Ag
O
=
增加氢原子
减少氧原子
增加氧原子
减少氢原子
联想·质疑
福尔马林是 35%~ 45%的甲醛水溶液,某些动物标本通常被保存在稀释的福尔马林中。
酮是一种重要的有机溶剂,它在化学实验和工业生产中都有着广泛的应用。例如,工业上常以丙酮为原料制造塑料和涂料。
葡萄糖是供给人体能量的物质之一。高浓度的葡萄糖溶液(葡萄糖的质量分数在50%以上)配以相关的药物输入患者体内可以治疗肠道感染、静脉炎等多种疾病。
甲醛和丙酮分别属于哪类有机化合物?它们的结构和性质是怎样的?葡萄糖是一种组成较简单的糖类物质,它与甲醛和丙酮有什么联系吗?
一、常见的醛、酮
1.醛和酮的结构
羰基
醛
羰基碳原子分别与氢原子和烃基(或氢原子)相连
官能团:醛基
-CHO
酮
羰基碳原子相连的两个基团均为烃基,烃基可以相同也可以不同
官能团:酮羰基
甲醛
乙醛
O
C
丙酮
2.醛和酮的命名
醛、酮的命名和醇的命名相似。
2 - 甲基丙醛
2 - 戊酮
1. 选择分子中连有醛基(或羰基)的碳原子在内的最长碳链做主链,按主链所含碳原子数称为某醛(或酮)。
2. 对主链碳原子的编号由接近醛基(或羰基)的一端开始。
3. 命名时,醛基碳为1号碳,不用注明位置;羰基的位次号写在“某酮”的前面,其他取代基的名称和位次号写在母体名称的前面。
3.饱和一元醛和饱和一元酮
通式:
CnH2nO
分子中碳原子数相同的饱和一元醛和饱和一元酮互为同分异构体。
1.丙醛(CH3CH2CHO)与丙酮(CH3COCH3)有何联系?
2.分子式为C2H4O和C3H6O的有机物一定是同系物吗?
思考:
两者互为同分异构体。
不一定,C2H4O是乙醛,分子式为C3H6O的有机物可能是丙醛,也可能是丙酮,还可能是环丙醇或烯丙醇。
交流·研讨
下表列出了分子式为 C5H10O 的醛和酮的部分同分异构体的结构简式,请写出属于醛、酮的其他同分异构体的结构简式,并举例说明这些异构体异构关系的类型。
异构体的结构简式
异构类型 (每种各举几例即可) 碳骨架异构 如:①和②
官能团类型异构 如:①和③
官能团位置异构 如:③和④
CH3CHCH2CHO
|
CH3
CH3CCHO
|
CH3
|
CH3
⑤
⑥
CH3CH—C—CH3
|
CH3
|
|
O
⑦
②和⑤
②和⑥
①和⑤
②和④
⑤和⑦
⑥和⑦
⑤和③
②和⑦
①和④
①和⑦
②和③
⑤和④
⑥和③
⑥和④
①和⑥
⑤和⑥
④和⑦
4.常见的醛和酮
名称 结构简式 状态 气味 溶解性 用途
甲醛
乙醛
苯甲醛
丙酮
HCHO 气体 有强烈刺激性气味 易溶于水 制造酚醛树脂、脲醛树脂
CH3CHO 液体 有刺激性气味 易溶于水 ——
液体 苦杏仁味,工业上称苦杏仁油 微溶于水 制造染料、香料的中间体
液体 有特殊气味 与水以任意比互溶 做有机溶剂、有机合成原料
福尔马林浸泡的动物尸体
身边的化学
视黄醛 人体内缺乏维生素 A 会导致眼角膜硬化,表现为在光线昏暗环境下或夜晚视物不清,即夜盲症。这是因为维生素 A 在人体内很容易被氧化成视黄醛,而视黄醛的缺乏是引起视觉障碍的主要原因。
常见的醛、酮举例
2- 庚酮 蜜蜂传递警戒信息的激素含有的 2- 庚酮( ),是昆虫之间进行化学通信的高活性微量化学信息物质之一。
交流·研讨
与其他有机化合物相比,醛、酮的化学性质较活泼,这与它们官能团的结构密切相关。
1. 请分析醛的结构特点,利用你所掌握的有机化合物结构与性质间关系的知识,推测醛可能具有的化学性质,完成下表。
分析结构 预测性质
断键部位 反应类型 反应试剂和条件 反应产物
官能团: 是否含不饱和键: 键的极性: 基团之间的相互影响:
2. 思考酮的化学性质与醛的化学性质有哪些相同点和不同点。
二、醛、酮的化学性质
1. 羰基的加成反应
羰基上的C=O键在一定条件下可与H2、HX、HCN、NH3、氨的衍生物、醇等发生加成反应。
醛或酮与氢氰酸加成,反应产物的分子比原来的醛分子或酮分子多了一个碳原子。这类加成反应在有机合成中可以用于增长碳链。
现代科学研究表明,甲醛对人体健康有很大危害。当室内空气中甲醛含量为 0.1 mg·m-3时,就会有异味并引起人的不适感;食用含有甲醛的食品,也会使人中毒。
甲醛为什么有毒?它在人体内发生了什么变化?
醛、酮能与氨的衍生物发生加成反应,反应的产物还会发生分子内脱水反应。从总的结果来看,这类反应相当于在醛、酮和氨的衍生物的分子之间脱掉了水分子。甲醛参与的相关反应可表示为:
身边的化学
甲醛为什么有毒
人体中重要的生物大分子如核酸、蛋白质均含有氨基(-NH2),当甲醛进入人体后,其分子中的羰基会与这些氨基发生类似醛与氨的衍生物的反应,使得核酸或蛋白质大分子的结构发生改变;轻者导致人体出现病变,重者可造成一些重要基因突变而导致癌症发生。
活动探究
通过化学必修课程的学习,你已经知道葡萄糖能与新制氢氧化铜悬浊液反应产生砖红色的氧化亚铜(Cu2O)沉淀,这其实就是葡萄糖分子中醛基发生的氧化反应。请设计实验验证醛基的还原性。
醛的氧化反应
乙醛, 0.5% 酸性 KMnO4 溶液,银氨溶液,10% NaOH 溶液,2% CuSO4 溶液;
试管,烧杯,胶头滴管,酒精灯,三脚架,石棉网,试管夹等。
实验用品
银氨溶液的配制和使用
在一支洁净的试管中,加入 1 mL 2% AgNO3 溶液,边振荡边滴加 2% 氨水,直至最初产生的沉淀恰好消失,便得到银氨溶液,其主要成分的化学式为[Ag(NH3)2]OH。银氨溶液与醛的反应需要在 60 ~70 ℃的水浴中进行。
实验内容 实验操作 实验现象 化学方程式
1.乙醛与酸性高锰酸钾溶液反应 取适量乙醛溶液与试管,加入酸性高锰酸钾溶液,振荡,观察现象。 酸性高锰酸钾溶液褪色
2.乙醛与银氨溶液的反应 取适量乙醛溶液与干净洁净的试管,加入配置好的银氨溶液,水浴加热 洁净的试管内壁形成光亮的银镜 CH3CHO+2[Ag(NH3)2]OH CH3COONH4+2Ag↓+3NH3+H2O
3.乙醛与新制氢氧化铜悬浊液反应 向10%的氢氧化钠溶液中加入5—6滴2%硫酸铜溶液,然后再加入乙醛溶液,用酒精等加热,观察实验现象 有砖红色沉淀生成 CH3CHO+2Cu(OH)2+NaOH
CH3COONa+Cu2O↓+3H2O
实验方案设计及实施
你所得到的实验现象和其他同学的相同吗?如不同,请分析原因。
思考:
(1)银镜反应的注意事项①试管必须洁净。②银氨溶液必须现用现配,不能久置;且氨水不能过量,否则,都容易产生易爆炸物质。③用水浴加热,不能直接加热,加热时不能振荡或摇动试管。④生成银镜的试管用稀硝酸溶解洗净。
(2)与新制氢氧化铜悬浊液反应的注意事项①氢氧化铜悬浊液要现用现配。②NaOH必须过量。③直接加热至沸腾。
2. 氧化反应和还原反应
(1) 氧化反应
醛和酮具有还原性,可被KMnO4(H+)溶液、溴水等较强的氧化剂氧化。
KMnO4(H+)溶液
加入乙醛溶液
醛的还原性较强比酮容易发生氧化反应,可被KMnO4(H+)溶液、溴水等较强的氧化剂氧化,也可被较弱的氧化剂银氨溶液、新制Cu(OH)2悬浊液氧化,而酮一般需很强的氧化剂才能被氧化。
CH3CHO+2[Ag(NH3)2]OH CH3COONH4+2Ag↓+3NH3+H2O
CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
△
△
银氨溶液和新制Cu(OH)2悬浊液常用于鉴别有机化合物分子中是否含有醛基。
(2) 还原反应
醛、酮中都含羰基,都能发生还原反应,还原产物一般是醇,化学反应的通式分别为
归纳总结
类别 醛 酮
区别 官能团
官能团位置
简写形式
性质
联系 通式
同分异构现象
性质
醛、酮的区别与联系
归纳总结
类别 醛 酮
区别 官能团
官能团位置 碳链末端 碳链中间
简写形式
性质 能被弱氧化剂氧化,发生银镜反应等 不能被弱氧化剂氧化
联系 通式 饱和一元醛:CnH2nO 饱和一元酮:CnH2nO
同分异构现象 碳原子数相同的饱和一元醛和饱和一元酮互为同分异构体
性质 可与H2、HX、HCN、NH3、氨的衍生物、醇等发生加成反应 均可加氢还原成醇 均可被强氧化剂氧化,都能使酸性高锰酸钾钾溶液褪色
醛、酮的区别与联系
课堂小结
醛、酮
共性
结构
官能团
饱和一元醛、酮的通式
醛
酮
醛基
羰基
CnH2nO
羰基的加成反应
氧化反应
燃烧
使酸性高锰酸钾、溴水褪色
醛的银镜反应
还原反应
与氢气加成反应,生成醇
新制氢氧化铜悬浊液反应
