沪教版九年级上册 第3章 物质构成的奥秘 2023年单元测试卷(含解析)
文档属性
| 名称 | 沪教版九年级上册 第3章 物质构成的奥秘 2023年单元测试卷(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 254.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-21 00:00:00 | ||
图片预览




文档简介
沪教版九年级上册《第3章 物质构成的奥秘》2023年单元测试卷
一、选择题
1.我们在商场的货架上经常会看到标有“补钙”“补铁”“补锌”“补碘”等字样的食品和保健品,这里的“钙、铁、锌、碘”指的是( )
A.分子 B.原子 C.元素 D.单质
2.地壳中含量最多的元素是( )
A.Fe B.Al C.Si D.O
3.下列人体必需的元素中,幼儿及青少年缺乏会患佝偻病和发育不良的是( )
A.铁 B.锌 C.碘 D.钙
4.下列物质是化合物的是( )
A.铁粉 B.牛奶 C.石油 D.氯酸钾
5.下列各组物质中,都由原子构成的一组是( )
A.铁、汞 B.氨、干冰
C.水、金刚石 D.硫酸铜、氯化钠
6.下列关于分子、原子、离子的说法中,正确的是( )
A.原子是最小的粒子,不可再分
B.温度升高,分子间的间隔增大
C.分子是保持物质性质的一种粒子
D.铝原子与铝离子的化学性质相同
7.下列化学用语中,关于数字“2”表示的意义叙述正确的是( )
A.2H:表示两个氢元素
B.Mg2+:表示镁元素的化合价为+2
C.NO2:表示二氧化氮中含有两个氧原子
D.2NH3:表示两个氨分子
8.原子的构成示意图如图,下列叙述正确的是( )
A.原子是实心球体
B.质子、中子、电子均匀分布在原子中
C.质子与电子质量相等
D.整个原子的质量主要集中在原子核上
9.如图为锶(Sr)和溴(Br)的原子结构示意图,下列推断正确的是( )
A.Sr原子在化学反应中易失去2个电子
B.Br原子在化学反应中易失去7个电子
C.Sr和Br可形成化合物SrBr
D.Sr和Br可形成化合物Sr2Br
10.有NH3、N2、NO、X、HNO3五种物质,均含氮元素,且氮元素的化合价按一定的顺序排列,则物质X是( )
A.NO2 B.N2O C.N2O5 D.NaNO3
11.芒果中含有芒果苷(化学式为C19H18O11),芒果苷具有使中枢神经系统兴奋的作用,并具有抗糖尿病、抗病毒等活性。下列关于芒果苷的说法错误的是( )
A.含有氧元素,属于氧化物
B.相对分子质量为422
C.质量分数最大的是碳元素
D.该分子中氢、氧原子个数比为18:11
12.如图是四种微粒的结构示意图。下列有关说法错误的是( )
A.当X的数值为10时,①表示一种原子
B.②属于阳离子
C.②③属于同种元素
D.④在化学反应中易得电子
二、填空题
13.用适当的化学用语填空:
(1)磷元素: ;
(2)四个氢分子: ;
(3)三个亚铁离子: ;
(4)标出氢氧化铝中铝元素的化合价: 。
14.元素周期表是学习化学的重要工具。如图是元素周期表的一部分,请回答下列问题:
(1)原子序数为11的元素属于 (填“金属”或“非金属”)元素。
(2)原子序数为9的元素的原子结构示意图为 。
(3)地壳中含量最多的元素是 (填元素符号)。
(4)含有原子序数为1、7、17三种元素的化合物的化学式为 。
(5)化学符号2OH﹣表示的意义为 。
15.初中化学学习中,我们初步认识了物质的微观结构。
(1)氯化钠、金刚石、干冰三种物质中,由离子构成的物质是 。
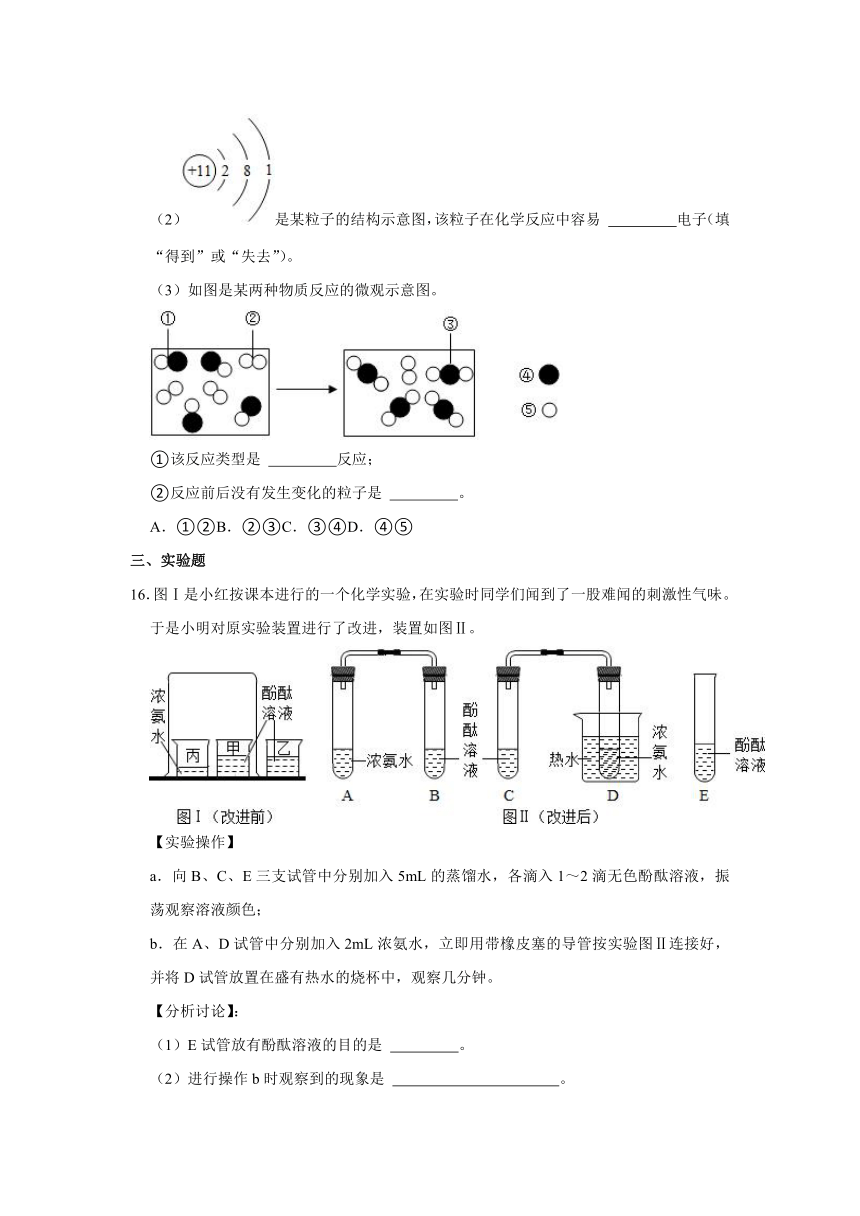
(2)是某粒子的结构示意图,该粒子在化学反应中容易 电子(填“得到”或“失去”)。
(3)如图是某两种物质反应的微观示意图。
①该反应类型是 反应;
②反应前后没有发生变化的粒子是 。
A.①②B.②③C.③④D.④⑤
三、实验题
16.图Ⅰ是小红按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。于是小明对原实验装置进行了改进,装置如图Ⅱ。
【实验操作】
a.向B、C、E三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡观察溶液颜色;
b.在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
【分析讨论】:
(1)E试管放有酚酞溶液的目的是 。
(2)进行操作b时观察到的现象是 。
(3)由此可以得到的实验结论是① ,② 。
(4)对比改进前的实验,改进后实验的优点是 ;由此推知我们在改进实验时需要考虑的因素包括 (答一点即可)。
四、推断题
17.用微粒的观点解释下列事实.
(1)碘固体(I2)和碘蒸气都能使淀粉变蓝 ;
(2)等质量的碘固体和碘蒸气比较,碘蒸气的体积远大于碘固体 ;
(3)空气是一种混合物 ;
(4)取一个透明的玻璃杯,先倒入半杯水,再放入一大块冰糖,立即在玻璃杯外壁液面位置做上记号,冰糖完全溶解后液面低于记号 .
五、解答题
18.空气又称大气,是生命、燃烧和工业等所需氧的主要来源。
(1)空气中,氧气的体积分数约为 ;构成氧气的粒子是 (写化学式)。
(2)氧原子结构示意图为 ,在化学变化中易 (填“得到”或“失去”)电子。
(3)在低温、加压条件下,将空气液化,然后将温度升高至﹣196℃~﹣183℃,使液态氮先蒸发,剩余液态氧储存于钢瓶中。从微观视角分析,空气液化过程中,主要改变的是 。
19.食品安全与人体健康密切相关。
(1)据报道,某包子铺违规使用含铝的泡打粉发面用来做包子,“铝包子”就是添加了硫酸铝钾或硫酸铝铵[NH4Al(SO4)2 12H2O]而制作出来的包子。在硫酸铝铵中,所含非金属元素共有 种。
(2)露天烧烤不仅污染环境,导致周边空气中PM2.5严重超标,在烧烤的肉类食物中还含有强致癌物质——苯并(α)芘,化学式为C20H12。在苯并(α)芘中,碳元素与氢元素的原子个数之比为 。
(3)据报道,在104国道某段,一辆载有20吨浓硫酸槽罐车不慎侧翻,造成大量硫酸(H2SO4)泄漏。硫酸中硫元素的化合价为 。
(4)世界卫生组织将5月31日定为“世界无烟日”,我国采取了公共场所禁止吸烟等控烟措施。烟雾中主要含有一氧化碳、尼古丁(C10H14N2)和焦油,这三种物质被称为香烟的三大杀手。下列有关说法中正确的是 (填字母)。
①尼古丁由3种元素组成
②尼古丁中含10个碳原子
③吸烟对他人无害
④一氧化碳和二氧化碳都属于氧化物
⑤尼古丁中碳元素的含量最高
A.①④⑤ B.①②③ C.①②④ D.②③⑤
20.钠摄入过量或钾摄入不足都是导致高血压的风险因素。日常生活中选择食用低钠盐能实现减钠补钾。如图为某品牌低钠盐的标签,请你根据标签回答以下问题:
(1)氯化钾的相对分子质量为 。
(2)人体每天摄入钠元素的质量不宜超过2.3g。如果人体所需的钠元素全部来自该品牌食盐,那么一个人每天摄入该品牌低钠盐的质量不宜超过多少克?(结果保留一位小数)
沪教版九年级上册《第3章 物质构成的奥秘》2023年单元测试卷
参考答案与试题解析
一、选择题
1.我们在商场的货架上经常会看到标有“补钙”“补铁”“补锌”“补碘”等字样的食品和保健品,这里的“钙、铁、锌、碘”指的是( )
A.分子 B.原子 C.元素 D.单质
【解答】解:“补钙”、“补铁”、“补锌”、“补碘”等字样的食品和保健品,这里的“钙、铁、锌、碘”不是以单质、分子、原子等形式存在,这里所指的“钙、铁、锌、碘”是强调存在的元素,与具体形态无关。
故选:C。
2.地壳中含量最多的元素是( )
A.Fe B.Al C.Si D.O
【解答】解:根据记忆可知在地壳中元素含量排在前四位的元素是:氧、硅、铝、铁;
故选:D。
3.下列人体必需的元素中,幼儿及青少年缺乏会患佝偻病和发育不良的是( )
A.铁 B.锌 C.碘 D.钙
【解答】解:A、人体缺铁易患缺铁性贫血,不合题意;
B、人体缺锌会引起食欲不振、生长迟缓,造成思维迟钝,不合题意;
C、人体缺碘易患甲状腺肿大,不合题意;
D、幼儿及青少年缺钙会患佝偻病和发育不良;老年人缺钙易患骨质疏松症,符合题意。
故选:D。
4.下列物质是化合物的是( )
A.铁粉 B.牛奶 C.石油 D.氯酸钾
【解答】解:A、铁粉属于单质,故A错误;
B、牛奶属于混合物,故B错误;
C、石油属于混合物,故C错误;
D、氯酸钾是由钾、氯、氧元素组成的纯净物,属于化合物,故D正确。
故选:D。
5.下列各组物质中,都由原子构成的一组是( )
A.铁、汞 B.氨、干冰
C.水、金刚石 D.硫酸铜、氯化钠
【解答】解:A、铁、汞均属于金属单质,分别是由铁原子、汞原子直接构成的,故选项正确。
B、氨、干冰是由非金属元素组成的化合物,分别是由氨分子、二氧化碳分子构成的,故选项错误。
C、水是由非金属元素组成的化合物,是由水分子构成;金刚石属于固态非金属单质,是由碳原子直接构成的,故选项错误。
D、硫酸铜、氯化钠均是含有金属元素和非金属元素的化合物,硫酸铜是由铜离子和硫酸根离子构成的,氯化钠是由钠离子和氯离子构成的,故选项错误。
故选:A。
6.下列关于分子、原子、离子的说法中,正确的是( )
A.原子是最小的粒子,不可再分
B.温度升高,分子间的间隔增大
C.分子是保持物质性质的一种粒子
D.铝原子与铝离子的化学性质相同
【解答】解:A、原子并不是最小的粒子,原子是由原子核和核外电子构成,还可以再分。原子在化学变化中是不能再分的,故A错误;
B、分子间存在着间隔,温室升高,分子间的间隔变大,故B正确;
C、分子是保持物质化学性质的一种微粒,不能保持物质的物理性质,故C错误;
D、微粒的化学性质取决于最外层电子数,铝原子的最外层有3个电子,易失去电子;铝离子的最外层有8个电子,属于稳定结构,化学性质不同,故D错误。
故选:B。
7.下列化学用语中,关于数字“2”表示的意义叙述正确的是( )
A.2H:表示两个氢元素
B.Mg2+:表示镁元素的化合价为+2
C.NO2:表示二氧化氮中含有两个氧原子
D.2NH3:表示两个氨分子
【解答】解:A、元素符号之前数字表示原子个数,2H中2表示2个氢原子,故A错误。
B、元素符号右上角数字表示一个离子带的电荷数,Mg2+表示1个镁离子带2个单位正电荷,故B错误。
C、化学式元素右下角的数字表示一个分子中含有的该元素原子的个数,NO2中数字“2”表示1个二氧化氮分子中含有2个氧原子,故C错误。
D、化学式前数字表示分子个数,2NH3中数字“2”表示两个氨分子,故D正确。
故选:D。
8.原子的构成示意图如图,下列叙述正确的是( )
A.原子是实心球体
B.质子、中子、电子均匀分布在原子中
C.质子与电子质量相等
D.整个原子的质量主要集中在原子核上
【解答】解:A、原子由带正电的原子核和核外带负电的电子构成,原子核又是由带正电的质子和不带电的中子构成,原子不是不可分割的实心球体,故A错误;
B、质子、中子、电子不是均匀分布在原子中,故B错误;
C、质子与电子质量不相等,故C错误;
D、原子质量主要集中在原子核上,故D正确。
故选:D。
9.如图为锶(Sr)和溴(Br)的原子结构示意图,下列推断正确的是( )
A.Sr原子在化学反应中易失去2个电子
B.Br原子在化学反应中易失去7个电子
C.Sr和Br可形成化合物SrBr
D.Sr和Br可形成化合物Sr2Br
【解答】解:A.Sr最外层电子数是2,反应中容易失去2个电子形成带2个单位正电荷的离子,故A正确。
B.溴元素最外层电子数是7,反应中容易得到1个电子形成带1个单位负电荷的离子,故B错误。
C.Sr最外层电子数是2,反应中容易失去2个电子形成带2个单位正电荷的离子,在化合物中化合价是+2,溴元素最外层电子数是7,反应中容易得到1个电子形成带1个单位负电荷的离子,在化合物中化合价是﹣1,根据化合物中元素化合价代数和为零可知,Sr和Br可形成化合物化学式是SrBr2,故C错误。D.Sr最外层电子数是2,反应中容易失去2个电子形成带2个单位正电荷的离子,在化合物中化合价是+2,溴元素最外层电子数是7,反应中容易得到1个电子形成带1个单位负电荷的离子,在化合物中化合价是﹣1,根据化合物中元素化合价代数和为零可知,Sr和Br可形成化合物化学式是SrBr2,故D错误。
故选:A。
10.有NH3、N2、NO、X、HNO3五种物质,均含氮元素,且氮元素的化合价按一定的顺序排列,则物质X是( )
A.NO2 B.N2O C.N2O5 D.NaNO3
【解答】解:已知氢元素的化合价为+1价,氧元素的化合价为﹣2价,根据化合价的原则(在化合物中正、负化合价的代数和为零),则:NH3中氮元素的化合价为:﹣3价;N2中氮元素的化合价为0;NO中氮元素的化合价为+2价;HNO3中氮元素的化合价为+5价,则X中氮元素的化合价为+3或+4。
A、NO2中氮元素的化合价为:+4价,故A符合题意;
B、N2O中氮元素的化合价为:+1价,故B不符合题意;
C、N2O5中氮元素的化合价为:+5价,故C不符合题意;
D、NaNO3中氮元素的化合价为:+5价,故D不符合题意。
故选:A。
11.芒果中含有芒果苷(化学式为C19H18O11),芒果苷具有使中枢神经系统兴奋的作用,并具有抗糖尿病、抗病毒等活性。下列关于芒果苷的说法错误的是( )
A.含有氧元素,属于氧化物
B.相对分子质量为422
C.质量分数最大的是碳元素
D.该分子中氢、氧原子个数比为18:11
【解答】解:A、芒果苷是由碳、氢、氧三种元素组成的化合物,不属于氧化物,故选项说法错误。
B、芒果苷的相对分子质量为12×19+1×18+16×11=422,故选项说法正确。
C、碳、氢、氧元素的质量比为(12×19):(1×18):(16×11)=114:9:88,则质量分数最大的是碳元素,故选项说法正确。
D、1个芒果苷分子中含有18个氢原子、11个氧原子,则该分子中氢、氧原子个数比为18:11,故选项说法正确。
故选:A。
12.如图是四种微粒的结构示意图。下列有关说法错误的是( )
A.当X的数值为10时,①表示一种原子
B.②属于阳离子
C.②③属于同种元素
D.④在化学反应中易得电子
【解答】解:A、当X的数值为10时,该粒子的质子数=核外电子数,因此①表示一种原子,故A正确;
B、②中质子数大于电子数,带正电荷,属于阳离子,故B正确;
C、②③的质子数不同,不属于同种元素,故C错误;
D、④的最外层有6个电子,多于4个,在化学反应中易得电子,故D正确。
故选:C。
二、填空题
13.用适当的化学用语填空:
(1)磷元素: P ;
(2)四个氢分子: 4H2 ;
(3)三个亚铁离子: 3Fe2+ ;
(4)标出氢氧化铝中铝元素的化合价: (OH)3 。
【解答】解:(1)书写元素符号注意“一大二小”,磷的元素符号是P。
(2)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则四个氢分子可表示为4H2。
(3)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,故三个亚铁离子可表示为3Fe2+。
(4)由化合价的表示方法,在该元素符号的上方用正负号和数字表示,正负号在前,数字在后,故氢氧化铝中铝元素的化合价为正三价可表示为:(OH)3。
故答案为:
(1)P;
(2)4H2;
(3)3Fe2+;
(4)(OH)3。
14.元素周期表是学习化学的重要工具。如图是元素周期表的一部分,请回答下列问题:
(1)原子序数为11的元素属于 金属 (填“金属”或“非金属”)元素。
(2)原子序数为9的元素的原子结构示意图为 。
(3)地壳中含量最多的元素是 O (填元素符号)。
(4)含有原子序数为1、7、17三种元素的化合物的化学式为 NH4Cl 。
(5)化学符号2OH﹣表示的意义为 2个氢氧根离子 。
【解答】解:(1)原子序数为11的元素是钠元素,带“钅”字旁,属于金属元素。
(2)原子序数为9的元素为氟元素,氟原子核内有9个质子,核外有2个电子层,第一层上有2个电子、最外层上有7个电子,其原子结构示意图为。
(3)地壳中含量最多的元素是氧元素,其元素符号为O。
(4)原子序数为1、7、17三种元素分别氢、氮、氯,可组成氯化铵这一化合物,其化学式为NH4Cl。
(5)由离子的表示方法,在表示该离子的元素符号或原子团的右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个单位电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字。2OH﹣表示的意义是2个氢氧根离子。
故答案为:
(1)金属;
(2);
(3)O;
(4)NH4Cl;
(5)2个氢氧根离子。
15.初中化学学习中,我们初步认识了物质的微观结构。
(1)氯化钠、金刚石、干冰三种物质中,由离子构成的物质是 氯化钠 。
(2)是某粒子的结构示意图,该粒子在化学反应中容易 失去 电子(填“得到”或“失去”)。
(3)如图是某两种物质反应的微观示意图。
①该反应类型是 化合 反应;
②反应前后没有发生变化的粒子是 ④⑤ 。
A.①②B.②③C.③④D.④⑤
【解答】解:(1)氯化钠是由离子构成的物质,金刚石是由碳原子直接构成的物质,干冰是由二氧化碳分子构成的物质;
(2)该原子的最外层电子数是1,最外层电子数小于4,在化学反应中易失去最外层的电子;
(3)①根据图示可知:该反应是CO与O2反应,生成二氧化碳,生成物的化学式为CO2;符合多变一,属于化合反应;
②化学反应前后分子的种类改变,故①②③改变;化学反应前后原子的种类不变,故④⑤不变。
故答案为:(1)氯化钠;(2)失去;(3)化合;④⑤。
三、实验题
16.图Ⅰ是小红按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。于是小明对原实验装置进行了改进,装置如图Ⅱ。
【实验操作】
a.向B、C、E三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡观察溶液颜色;
b.在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
【分析讨论】:
(1)E试管放有酚酞溶液的目的是 对比 。
(2)进行操作b时观察到的现象是 C中酚酞变红的快,B中酚酞变红的慢 。
(3)由此可以得到的实验结论是① 分子在不断地运动 ,② 温度越高分子运动的越快 。
(4)对比改进前的实验,改进后实验的优点是 有利于环境保护,且能说明影响分子的运动快慢的因素 ;由此推知我们在改进实验时需要考虑的因素包括 是否有利于环境保护 (答一点即可)。
【解答】解:(1)E试管盛有酚酞溶液的目的是做对照试验,故填:对比;
(2)在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,在热水中分子的运动速度快,故可以观察到C中变红的快,B中变红的慢,故填:C中酚酞变红的快,B中酚酞变红的慢;
(3)根据实验可以看出,分子在不断地运动;分子的运动与温度有关,温度越高分子运动的越快,故填:分子在不断地运动,温度越高分子运动的越快;
(4)对比改进前的实验,改进后实验在密闭容器中进行,有利于环境保护,且同一温度下不能说明影响分子的运动快慢的因素,而改进后的装置则解决了这个问题,故填:有利于环境保护,且能说明影响分子的运动快慢的因素;是否有利于环境保护。
四、推断题
17.用微粒的观点解释下列事实.
(1)碘固体(I2)和碘蒸气都能使淀粉变蓝 碘固体和碘蒸气都是由碘分子构成的,同种物质的分子化学性质相同 ;
(2)等质量的碘固体和碘蒸气比较,碘蒸气的体积远大于碘固体 等质量的碘固体和碘蒸气,含有的碘分子个数相等,碘蒸气中碘分子之间的间隔远远大于碘固体中碘分子之间的间隔,所以质量相等时,碘蒸气的体积远大于碘固体 ;
(3)空气是一种混合物 空气中含有氮气、氧气、二氧化碳等多种物质的分子 ;
(4)取一个透明的玻璃杯,先倒入半杯水,再放入一大块冰糖,立即在玻璃杯外壁液面位置做上记号,冰糖完全溶解后液面低于记号 分子之间有间隔,分子在不断运动,糖分子和水分子运动到彼此的间隔中去了,使液面下降 .
【解答】解:(1)碘固体(I2)和碘蒸气都能使淀粉变蓝,是由于碘固体和碘蒸气都是由碘分子构成的,同种物质的分子化学性质相同;
(2)等质量的碘固体和碘蒸气比较,碘蒸气的体积远大于碘固体,原因是:等质量的碘固体和碘蒸气,含有的碘分子个数相等,碘蒸气中碘分子之间的间隔远远大于碘固体中碘分子之间的间隔,所以质量相等时,碘蒸气的体积远大于碘固体;
(3)空气是一种混合物,原因是空气中含有氮气、氧气、二氧化碳等多种物质的分子;
(4)取一个透明的玻璃杯,先倒入半杯水,再放入一大块冰糖,立即在玻璃杯外壁液面位置做上记号,冰糖完全溶解后液面低于记号,是由于分子之间有间隔,分子在不断运动,糖分子和水分子运动到彼此的间隔中去了,使液面下.
故答案为:(1)碘固体和碘蒸气都是由碘分子构成的,同种物质的分子化学性质相同;
(2)等质量的碘固体和碘蒸气,含有的碘分子个数相等,碘蒸气中碘分子之间的间隔远远大于碘固体中碘分子之间的间隔,所以质量相等时,碘蒸气的体积远大于碘固体;
(3)空气中含有氮气、氧气、二氧化碳等多种物质的分子;
(4)分子之间有间隔,分子在不断运动,糖分子和水分子运动到彼此的间隔中去了,使液面下降.
五、解答题
18.空气又称大气,是生命、燃烧和工业等所需氧的主要来源。
(1)空气中,氧气的体积分数约为 21% ;构成氧气的粒子是 O2 (写化学式)。
(2)氧原子结构示意图为 ,在化学变化中易 得到 (填“得到”或“失去”)电子。
(3)在低温、加压条件下,将空气液化,然后将温度升高至﹣196℃~﹣183℃,使液态氮先蒸发,剩余液态氧储存于钢瓶中。从微观视角分析,空气液化过程中,主要改变的是 分子间隔 。
【解答】解:(1)空气中,氧气的体积分数约为21%;氧气是由氧分子构成的,氧分子符号为O2;故答案为:21%;O2;
(2)氧原子的质子数为8,核外有8个电子,第一层上有2个,第二层上有6个,即氧原子结构示意图为:,氧原子的最外层有6个电子,多于4个,在化学反应中易得到电子;故答案为:;得到;
(3)从微观视角分析,空气液化过程中,主要改变的是分子间隔;故答案为:分子间隔。
19.食品安全与人体健康密切相关。
(1)据报道,某包子铺违规使用含铝的泡打粉发面用来做包子,“铝包子”就是添加了硫酸铝钾或硫酸铝铵[NH4Al(SO4)2 12H2O]而制作出来的包子。在硫酸铝铵中,所含非金属元素共有 4 种。
(2)露天烧烤不仅污染环境,导致周边空气中PM2.5严重超标,在烧烤的肉类食物中还含有强致癌物质——苯并(α)芘,化学式为C20H12。在苯并(α)芘中,碳元素与氢元素的原子个数之比为 5:3 。
(3)据报道,在104国道某段,一辆载有20吨浓硫酸槽罐车不慎侧翻,造成大量硫酸(H2SO4)泄漏。硫酸中硫元素的化合价为 +6 。
(4)世界卫生组织将5月31日定为“世界无烟日”,我国采取了公共场所禁止吸烟等控烟措施。烟雾中主要含有一氧化碳、尼古丁(C10H14N2)和焦油,这三种物质被称为香烟的三大杀手。下列有关说法中正确的是 A (填字母)。
①尼古丁由3种元素组成
②尼古丁中含10个碳原子
③吸烟对他人无害
④一氧化碳和二氧化碳都属于氧化物
⑤尼古丁中碳元素的含量最高
A.①④⑤ B.①②③ C.①②④ D.②③⑤
【解答】解:(1)硫酸铝铵是由氮元素、氢元素、铝元素、硫元素、氧元素组成的,其中氮、氢、硫、氧4种元素属于非金属元素;
(2)由苯并(a)芘的化学式C20H12可知,在苯并(a)芘中,碳元素与氢元素的原子个数之比为:20:12=5:3;
(3)设硫酸中硫元素的化合价为x,硫酸中氢元素化合价是+1,氧元素化合价是﹣2,根据化合物中元素的化合价代数和为零:(+1)×2+x+(﹣2)×4=0,x=+6;
(4)①尼古丁由碳、氢、氮3种元素组成,正确;
②尼古丁是由尼古丁分子构成的,1个尼古丁分子中含10个碳原子,错误;
③吸烟对他人也有害,错误;
④氧化物是由两种元素组成的化合物,且一种元素为氧元素,一氧化碳和二氧化碳都属于氧化物,正确;
⑤根据尼古丁(C10H14N2)化学式可知,尼古丁中碳元素、氢元素和氧元素的质量比=(10×12):(1×14):(14×2)=60:7:14,在尼古丁中碳元素的含量最高,正确。
故答案为:(1)4;
(2)5:3;
(3)+6;
(4)A。
20.钠摄入过量或钾摄入不足都是导致高血压的风险因素。日常生活中选择食用低钠盐能实现减钠补钾。如图为某品牌低钠盐的标签,请你根据标签回答以下问题:
(1)氯化钾的相对分子质量为 74.5 。
(2)人体每天摄入钠元素的质量不宜超过2.3g。如果人体所需的钠元素全部来自该品牌食盐,那么一个人每天摄入该品牌低钠盐的质量不宜超过多少克?(结果保留一位小数)
【解答】解:(1)KCl的相对分子质量为:39+35.5=74.5;故填:74.5;
(2)一个人每天摄入该品牌低钠盐的质量不宜超过:2.3g÷÷70%=8.4g
故填:8.4g.
一、选择题
1.我们在商场的货架上经常会看到标有“补钙”“补铁”“补锌”“补碘”等字样的食品和保健品,这里的“钙、铁、锌、碘”指的是( )
A.分子 B.原子 C.元素 D.单质
2.地壳中含量最多的元素是( )
A.Fe B.Al C.Si D.O
3.下列人体必需的元素中,幼儿及青少年缺乏会患佝偻病和发育不良的是( )
A.铁 B.锌 C.碘 D.钙
4.下列物质是化合物的是( )
A.铁粉 B.牛奶 C.石油 D.氯酸钾
5.下列各组物质中,都由原子构成的一组是( )
A.铁、汞 B.氨、干冰
C.水、金刚石 D.硫酸铜、氯化钠
6.下列关于分子、原子、离子的说法中,正确的是( )
A.原子是最小的粒子,不可再分
B.温度升高,分子间的间隔增大
C.分子是保持物质性质的一种粒子
D.铝原子与铝离子的化学性质相同
7.下列化学用语中,关于数字“2”表示的意义叙述正确的是( )
A.2H:表示两个氢元素
B.Mg2+:表示镁元素的化合价为+2
C.NO2:表示二氧化氮中含有两个氧原子
D.2NH3:表示两个氨分子
8.原子的构成示意图如图,下列叙述正确的是( )
A.原子是实心球体
B.质子、中子、电子均匀分布在原子中
C.质子与电子质量相等
D.整个原子的质量主要集中在原子核上
9.如图为锶(Sr)和溴(Br)的原子结构示意图,下列推断正确的是( )
A.Sr原子在化学反应中易失去2个电子
B.Br原子在化学反应中易失去7个电子
C.Sr和Br可形成化合物SrBr
D.Sr和Br可形成化合物Sr2Br
10.有NH3、N2、NO、X、HNO3五种物质,均含氮元素,且氮元素的化合价按一定的顺序排列,则物质X是( )
A.NO2 B.N2O C.N2O5 D.NaNO3
11.芒果中含有芒果苷(化学式为C19H18O11),芒果苷具有使中枢神经系统兴奋的作用,并具有抗糖尿病、抗病毒等活性。下列关于芒果苷的说法错误的是( )
A.含有氧元素,属于氧化物
B.相对分子质量为422
C.质量分数最大的是碳元素
D.该分子中氢、氧原子个数比为18:11
12.如图是四种微粒的结构示意图。下列有关说法错误的是( )
A.当X的数值为10时,①表示一种原子
B.②属于阳离子
C.②③属于同种元素
D.④在化学反应中易得电子
二、填空题
13.用适当的化学用语填空:
(1)磷元素: ;
(2)四个氢分子: ;
(3)三个亚铁离子: ;
(4)标出氢氧化铝中铝元素的化合价: 。
14.元素周期表是学习化学的重要工具。如图是元素周期表的一部分,请回答下列问题:
(1)原子序数为11的元素属于 (填“金属”或“非金属”)元素。
(2)原子序数为9的元素的原子结构示意图为 。
(3)地壳中含量最多的元素是 (填元素符号)。
(4)含有原子序数为1、7、17三种元素的化合物的化学式为 。
(5)化学符号2OH﹣表示的意义为 。
15.初中化学学习中,我们初步认识了物质的微观结构。
(1)氯化钠、金刚石、干冰三种物质中,由离子构成的物质是 。
(2)是某粒子的结构示意图,该粒子在化学反应中容易 电子(填“得到”或“失去”)。
(3)如图是某两种物质反应的微观示意图。
①该反应类型是 反应;
②反应前后没有发生变化的粒子是 。
A.①②B.②③C.③④D.④⑤
三、实验题
16.图Ⅰ是小红按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。于是小明对原实验装置进行了改进,装置如图Ⅱ。
【实验操作】
a.向B、C、E三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡观察溶液颜色;
b.在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
【分析讨论】:
(1)E试管放有酚酞溶液的目的是 。
(2)进行操作b时观察到的现象是 。
(3)由此可以得到的实验结论是① ,② 。
(4)对比改进前的实验,改进后实验的优点是 ;由此推知我们在改进实验时需要考虑的因素包括 (答一点即可)。
四、推断题
17.用微粒的观点解释下列事实.
(1)碘固体(I2)和碘蒸气都能使淀粉变蓝 ;
(2)等质量的碘固体和碘蒸气比较,碘蒸气的体积远大于碘固体 ;
(3)空气是一种混合物 ;
(4)取一个透明的玻璃杯,先倒入半杯水,再放入一大块冰糖,立即在玻璃杯外壁液面位置做上记号,冰糖完全溶解后液面低于记号 .
五、解答题
18.空气又称大气,是生命、燃烧和工业等所需氧的主要来源。
(1)空气中,氧气的体积分数约为 ;构成氧气的粒子是 (写化学式)。
(2)氧原子结构示意图为 ,在化学变化中易 (填“得到”或“失去”)电子。
(3)在低温、加压条件下,将空气液化,然后将温度升高至﹣196℃~﹣183℃,使液态氮先蒸发,剩余液态氧储存于钢瓶中。从微观视角分析,空气液化过程中,主要改变的是 。
19.食品安全与人体健康密切相关。
(1)据报道,某包子铺违规使用含铝的泡打粉发面用来做包子,“铝包子”就是添加了硫酸铝钾或硫酸铝铵[NH4Al(SO4)2 12H2O]而制作出来的包子。在硫酸铝铵中,所含非金属元素共有 种。
(2)露天烧烤不仅污染环境,导致周边空气中PM2.5严重超标,在烧烤的肉类食物中还含有强致癌物质——苯并(α)芘,化学式为C20H12。在苯并(α)芘中,碳元素与氢元素的原子个数之比为 。
(3)据报道,在104国道某段,一辆载有20吨浓硫酸槽罐车不慎侧翻,造成大量硫酸(H2SO4)泄漏。硫酸中硫元素的化合价为 。
(4)世界卫生组织将5月31日定为“世界无烟日”,我国采取了公共场所禁止吸烟等控烟措施。烟雾中主要含有一氧化碳、尼古丁(C10H14N2)和焦油,这三种物质被称为香烟的三大杀手。下列有关说法中正确的是 (填字母)。
①尼古丁由3种元素组成
②尼古丁中含10个碳原子
③吸烟对他人无害
④一氧化碳和二氧化碳都属于氧化物
⑤尼古丁中碳元素的含量最高
A.①④⑤ B.①②③ C.①②④ D.②③⑤
20.钠摄入过量或钾摄入不足都是导致高血压的风险因素。日常生活中选择食用低钠盐能实现减钠补钾。如图为某品牌低钠盐的标签,请你根据标签回答以下问题:
(1)氯化钾的相对分子质量为 。
(2)人体每天摄入钠元素的质量不宜超过2.3g。如果人体所需的钠元素全部来自该品牌食盐,那么一个人每天摄入该品牌低钠盐的质量不宜超过多少克?(结果保留一位小数)
沪教版九年级上册《第3章 物质构成的奥秘》2023年单元测试卷
参考答案与试题解析
一、选择题
1.我们在商场的货架上经常会看到标有“补钙”“补铁”“补锌”“补碘”等字样的食品和保健品,这里的“钙、铁、锌、碘”指的是( )
A.分子 B.原子 C.元素 D.单质
【解答】解:“补钙”、“补铁”、“补锌”、“补碘”等字样的食品和保健品,这里的“钙、铁、锌、碘”不是以单质、分子、原子等形式存在,这里所指的“钙、铁、锌、碘”是强调存在的元素,与具体形态无关。
故选:C。
2.地壳中含量最多的元素是( )
A.Fe B.Al C.Si D.O
【解答】解:根据记忆可知在地壳中元素含量排在前四位的元素是:氧、硅、铝、铁;
故选:D。
3.下列人体必需的元素中,幼儿及青少年缺乏会患佝偻病和发育不良的是( )
A.铁 B.锌 C.碘 D.钙
【解答】解:A、人体缺铁易患缺铁性贫血,不合题意;
B、人体缺锌会引起食欲不振、生长迟缓,造成思维迟钝,不合题意;
C、人体缺碘易患甲状腺肿大,不合题意;
D、幼儿及青少年缺钙会患佝偻病和发育不良;老年人缺钙易患骨质疏松症,符合题意。
故选:D。
4.下列物质是化合物的是( )
A.铁粉 B.牛奶 C.石油 D.氯酸钾
【解答】解:A、铁粉属于单质,故A错误;
B、牛奶属于混合物,故B错误;
C、石油属于混合物,故C错误;
D、氯酸钾是由钾、氯、氧元素组成的纯净物,属于化合物,故D正确。
故选:D。
5.下列各组物质中,都由原子构成的一组是( )
A.铁、汞 B.氨、干冰
C.水、金刚石 D.硫酸铜、氯化钠
【解答】解:A、铁、汞均属于金属单质,分别是由铁原子、汞原子直接构成的,故选项正确。
B、氨、干冰是由非金属元素组成的化合物,分别是由氨分子、二氧化碳分子构成的,故选项错误。
C、水是由非金属元素组成的化合物,是由水分子构成;金刚石属于固态非金属单质,是由碳原子直接构成的,故选项错误。
D、硫酸铜、氯化钠均是含有金属元素和非金属元素的化合物,硫酸铜是由铜离子和硫酸根离子构成的,氯化钠是由钠离子和氯离子构成的,故选项错误。
故选:A。
6.下列关于分子、原子、离子的说法中,正确的是( )
A.原子是最小的粒子,不可再分
B.温度升高,分子间的间隔增大
C.分子是保持物质性质的一种粒子
D.铝原子与铝离子的化学性质相同
【解答】解:A、原子并不是最小的粒子,原子是由原子核和核外电子构成,还可以再分。原子在化学变化中是不能再分的,故A错误;
B、分子间存在着间隔,温室升高,分子间的间隔变大,故B正确;
C、分子是保持物质化学性质的一种微粒,不能保持物质的物理性质,故C错误;
D、微粒的化学性质取决于最外层电子数,铝原子的最外层有3个电子,易失去电子;铝离子的最外层有8个电子,属于稳定结构,化学性质不同,故D错误。
故选:B。
7.下列化学用语中,关于数字“2”表示的意义叙述正确的是( )
A.2H:表示两个氢元素
B.Mg2+:表示镁元素的化合价为+2
C.NO2:表示二氧化氮中含有两个氧原子
D.2NH3:表示两个氨分子
【解答】解:A、元素符号之前数字表示原子个数,2H中2表示2个氢原子,故A错误。
B、元素符号右上角数字表示一个离子带的电荷数,Mg2+表示1个镁离子带2个单位正电荷,故B错误。
C、化学式元素右下角的数字表示一个分子中含有的该元素原子的个数,NO2中数字“2”表示1个二氧化氮分子中含有2个氧原子,故C错误。
D、化学式前数字表示分子个数,2NH3中数字“2”表示两个氨分子,故D正确。
故选:D。
8.原子的构成示意图如图,下列叙述正确的是( )
A.原子是实心球体
B.质子、中子、电子均匀分布在原子中
C.质子与电子质量相等
D.整个原子的质量主要集中在原子核上
【解答】解:A、原子由带正电的原子核和核外带负电的电子构成,原子核又是由带正电的质子和不带电的中子构成,原子不是不可分割的实心球体,故A错误;
B、质子、中子、电子不是均匀分布在原子中,故B错误;
C、质子与电子质量不相等,故C错误;
D、原子质量主要集中在原子核上,故D正确。
故选:D。
9.如图为锶(Sr)和溴(Br)的原子结构示意图,下列推断正确的是( )
A.Sr原子在化学反应中易失去2个电子
B.Br原子在化学反应中易失去7个电子
C.Sr和Br可形成化合物SrBr
D.Sr和Br可形成化合物Sr2Br
【解答】解:A.Sr最外层电子数是2,反应中容易失去2个电子形成带2个单位正电荷的离子,故A正确。
B.溴元素最外层电子数是7,反应中容易得到1个电子形成带1个单位负电荷的离子,故B错误。
C.Sr最外层电子数是2,反应中容易失去2个电子形成带2个单位正电荷的离子,在化合物中化合价是+2,溴元素最外层电子数是7,反应中容易得到1个电子形成带1个单位负电荷的离子,在化合物中化合价是﹣1,根据化合物中元素化合价代数和为零可知,Sr和Br可形成化合物化学式是SrBr2,故C错误。D.Sr最外层电子数是2,反应中容易失去2个电子形成带2个单位正电荷的离子,在化合物中化合价是+2,溴元素最外层电子数是7,反应中容易得到1个电子形成带1个单位负电荷的离子,在化合物中化合价是﹣1,根据化合物中元素化合价代数和为零可知,Sr和Br可形成化合物化学式是SrBr2,故D错误。
故选:A。
10.有NH3、N2、NO、X、HNO3五种物质,均含氮元素,且氮元素的化合价按一定的顺序排列,则物质X是( )
A.NO2 B.N2O C.N2O5 D.NaNO3
【解答】解:已知氢元素的化合价为+1价,氧元素的化合价为﹣2价,根据化合价的原则(在化合物中正、负化合价的代数和为零),则:NH3中氮元素的化合价为:﹣3价;N2中氮元素的化合价为0;NO中氮元素的化合价为+2价;HNO3中氮元素的化合价为+5价,则X中氮元素的化合价为+3或+4。
A、NO2中氮元素的化合价为:+4价,故A符合题意;
B、N2O中氮元素的化合价为:+1价,故B不符合题意;
C、N2O5中氮元素的化合价为:+5价,故C不符合题意;
D、NaNO3中氮元素的化合价为:+5价,故D不符合题意。
故选:A。
11.芒果中含有芒果苷(化学式为C19H18O11),芒果苷具有使中枢神经系统兴奋的作用,并具有抗糖尿病、抗病毒等活性。下列关于芒果苷的说法错误的是( )
A.含有氧元素,属于氧化物
B.相对分子质量为422
C.质量分数最大的是碳元素
D.该分子中氢、氧原子个数比为18:11
【解答】解:A、芒果苷是由碳、氢、氧三种元素组成的化合物,不属于氧化物,故选项说法错误。
B、芒果苷的相对分子质量为12×19+1×18+16×11=422,故选项说法正确。
C、碳、氢、氧元素的质量比为(12×19):(1×18):(16×11)=114:9:88,则质量分数最大的是碳元素,故选项说法正确。
D、1个芒果苷分子中含有18个氢原子、11个氧原子,则该分子中氢、氧原子个数比为18:11,故选项说法正确。
故选:A。
12.如图是四种微粒的结构示意图。下列有关说法错误的是( )
A.当X的数值为10时,①表示一种原子
B.②属于阳离子
C.②③属于同种元素
D.④在化学反应中易得电子
【解答】解:A、当X的数值为10时,该粒子的质子数=核外电子数,因此①表示一种原子,故A正确;
B、②中质子数大于电子数,带正电荷,属于阳离子,故B正确;
C、②③的质子数不同,不属于同种元素,故C错误;
D、④的最外层有6个电子,多于4个,在化学反应中易得电子,故D正确。
故选:C。
二、填空题
13.用适当的化学用语填空:
(1)磷元素: P ;
(2)四个氢分子: 4H2 ;
(3)三个亚铁离子: 3Fe2+ ;
(4)标出氢氧化铝中铝元素的化合价: (OH)3 。
【解答】解:(1)书写元素符号注意“一大二小”,磷的元素符号是P。
(2)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则四个氢分子可表示为4H2。
(3)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,故三个亚铁离子可表示为3Fe2+。
(4)由化合价的表示方法,在该元素符号的上方用正负号和数字表示,正负号在前,数字在后,故氢氧化铝中铝元素的化合价为正三价可表示为:(OH)3。
故答案为:
(1)P;
(2)4H2;
(3)3Fe2+;
(4)(OH)3。
14.元素周期表是学习化学的重要工具。如图是元素周期表的一部分,请回答下列问题:
(1)原子序数为11的元素属于 金属 (填“金属”或“非金属”)元素。
(2)原子序数为9的元素的原子结构示意图为 。
(3)地壳中含量最多的元素是 O (填元素符号)。
(4)含有原子序数为1、7、17三种元素的化合物的化学式为 NH4Cl 。
(5)化学符号2OH﹣表示的意义为 2个氢氧根离子 。
【解答】解:(1)原子序数为11的元素是钠元素,带“钅”字旁,属于金属元素。
(2)原子序数为9的元素为氟元素,氟原子核内有9个质子,核外有2个电子层,第一层上有2个电子、最外层上有7个电子,其原子结构示意图为。
(3)地壳中含量最多的元素是氧元素,其元素符号为O。
(4)原子序数为1、7、17三种元素分别氢、氮、氯,可组成氯化铵这一化合物,其化学式为NH4Cl。
(5)由离子的表示方法,在表示该离子的元素符号或原子团的右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个单位电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字。2OH﹣表示的意义是2个氢氧根离子。
故答案为:
(1)金属;
(2);
(3)O;
(4)NH4Cl;
(5)2个氢氧根离子。
15.初中化学学习中,我们初步认识了物质的微观结构。
(1)氯化钠、金刚石、干冰三种物质中,由离子构成的物质是 氯化钠 。
(2)是某粒子的结构示意图,该粒子在化学反应中容易 失去 电子(填“得到”或“失去”)。
(3)如图是某两种物质反应的微观示意图。
①该反应类型是 化合 反应;
②反应前后没有发生变化的粒子是 ④⑤ 。
A.①②B.②③C.③④D.④⑤
【解答】解:(1)氯化钠是由离子构成的物质,金刚石是由碳原子直接构成的物质,干冰是由二氧化碳分子构成的物质;
(2)该原子的最外层电子数是1,最外层电子数小于4,在化学反应中易失去最外层的电子;
(3)①根据图示可知:该反应是CO与O2反应,生成二氧化碳,生成物的化学式为CO2;符合多变一,属于化合反应;
②化学反应前后分子的种类改变,故①②③改变;化学反应前后原子的种类不变,故④⑤不变。
故答案为:(1)氯化钠;(2)失去;(3)化合;④⑤。
三、实验题
16.图Ⅰ是小红按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。于是小明对原实验装置进行了改进,装置如图Ⅱ。
【实验操作】
a.向B、C、E三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡观察溶液颜色;
b.在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
【分析讨论】:
(1)E试管放有酚酞溶液的目的是 对比 。
(2)进行操作b时观察到的现象是 C中酚酞变红的快,B中酚酞变红的慢 。
(3)由此可以得到的实验结论是① 分子在不断地运动 ,② 温度越高分子运动的越快 。
(4)对比改进前的实验,改进后实验的优点是 有利于环境保护,且能说明影响分子的运动快慢的因素 ;由此推知我们在改进实验时需要考虑的因素包括 是否有利于环境保护 (答一点即可)。
【解答】解:(1)E试管盛有酚酞溶液的目的是做对照试验,故填:对比;
(2)在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,在热水中分子的运动速度快,故可以观察到C中变红的快,B中变红的慢,故填:C中酚酞变红的快,B中酚酞变红的慢;
(3)根据实验可以看出,分子在不断地运动;分子的运动与温度有关,温度越高分子运动的越快,故填:分子在不断地运动,温度越高分子运动的越快;
(4)对比改进前的实验,改进后实验在密闭容器中进行,有利于环境保护,且同一温度下不能说明影响分子的运动快慢的因素,而改进后的装置则解决了这个问题,故填:有利于环境保护,且能说明影响分子的运动快慢的因素;是否有利于环境保护。
四、推断题
17.用微粒的观点解释下列事实.
(1)碘固体(I2)和碘蒸气都能使淀粉变蓝 碘固体和碘蒸气都是由碘分子构成的,同种物质的分子化学性质相同 ;
(2)等质量的碘固体和碘蒸气比较,碘蒸气的体积远大于碘固体 等质量的碘固体和碘蒸气,含有的碘分子个数相等,碘蒸气中碘分子之间的间隔远远大于碘固体中碘分子之间的间隔,所以质量相等时,碘蒸气的体积远大于碘固体 ;
(3)空气是一种混合物 空气中含有氮气、氧气、二氧化碳等多种物质的分子 ;
(4)取一个透明的玻璃杯,先倒入半杯水,再放入一大块冰糖,立即在玻璃杯外壁液面位置做上记号,冰糖完全溶解后液面低于记号 分子之间有间隔,分子在不断运动,糖分子和水分子运动到彼此的间隔中去了,使液面下降 .
【解答】解:(1)碘固体(I2)和碘蒸气都能使淀粉变蓝,是由于碘固体和碘蒸气都是由碘分子构成的,同种物质的分子化学性质相同;
(2)等质量的碘固体和碘蒸气比较,碘蒸气的体积远大于碘固体,原因是:等质量的碘固体和碘蒸气,含有的碘分子个数相等,碘蒸气中碘分子之间的间隔远远大于碘固体中碘分子之间的间隔,所以质量相等时,碘蒸气的体积远大于碘固体;
(3)空气是一种混合物,原因是空气中含有氮气、氧气、二氧化碳等多种物质的分子;
(4)取一个透明的玻璃杯,先倒入半杯水,再放入一大块冰糖,立即在玻璃杯外壁液面位置做上记号,冰糖完全溶解后液面低于记号,是由于分子之间有间隔,分子在不断运动,糖分子和水分子运动到彼此的间隔中去了,使液面下.
故答案为:(1)碘固体和碘蒸气都是由碘分子构成的,同种物质的分子化学性质相同;
(2)等质量的碘固体和碘蒸气,含有的碘分子个数相等,碘蒸气中碘分子之间的间隔远远大于碘固体中碘分子之间的间隔,所以质量相等时,碘蒸气的体积远大于碘固体;
(3)空气中含有氮气、氧气、二氧化碳等多种物质的分子;
(4)分子之间有间隔,分子在不断运动,糖分子和水分子运动到彼此的间隔中去了,使液面下降.
五、解答题
18.空气又称大气,是生命、燃烧和工业等所需氧的主要来源。
(1)空气中,氧气的体积分数约为 21% ;构成氧气的粒子是 O2 (写化学式)。
(2)氧原子结构示意图为 ,在化学变化中易 得到 (填“得到”或“失去”)电子。
(3)在低温、加压条件下,将空气液化,然后将温度升高至﹣196℃~﹣183℃,使液态氮先蒸发,剩余液态氧储存于钢瓶中。从微观视角分析,空气液化过程中,主要改变的是 分子间隔 。
【解答】解:(1)空气中,氧气的体积分数约为21%;氧气是由氧分子构成的,氧分子符号为O2;故答案为:21%;O2;
(2)氧原子的质子数为8,核外有8个电子,第一层上有2个,第二层上有6个,即氧原子结构示意图为:,氧原子的最外层有6个电子,多于4个,在化学反应中易得到电子;故答案为:;得到;
(3)从微观视角分析,空气液化过程中,主要改变的是分子间隔;故答案为:分子间隔。
19.食品安全与人体健康密切相关。
(1)据报道,某包子铺违规使用含铝的泡打粉发面用来做包子,“铝包子”就是添加了硫酸铝钾或硫酸铝铵[NH4Al(SO4)2 12H2O]而制作出来的包子。在硫酸铝铵中,所含非金属元素共有 4 种。
(2)露天烧烤不仅污染环境,导致周边空气中PM2.5严重超标,在烧烤的肉类食物中还含有强致癌物质——苯并(α)芘,化学式为C20H12。在苯并(α)芘中,碳元素与氢元素的原子个数之比为 5:3 。
(3)据报道,在104国道某段,一辆载有20吨浓硫酸槽罐车不慎侧翻,造成大量硫酸(H2SO4)泄漏。硫酸中硫元素的化合价为 +6 。
(4)世界卫生组织将5月31日定为“世界无烟日”,我国采取了公共场所禁止吸烟等控烟措施。烟雾中主要含有一氧化碳、尼古丁(C10H14N2)和焦油,这三种物质被称为香烟的三大杀手。下列有关说法中正确的是 A (填字母)。
①尼古丁由3种元素组成
②尼古丁中含10个碳原子
③吸烟对他人无害
④一氧化碳和二氧化碳都属于氧化物
⑤尼古丁中碳元素的含量最高
A.①④⑤ B.①②③ C.①②④ D.②③⑤
【解答】解:(1)硫酸铝铵是由氮元素、氢元素、铝元素、硫元素、氧元素组成的,其中氮、氢、硫、氧4种元素属于非金属元素;
(2)由苯并(a)芘的化学式C20H12可知,在苯并(a)芘中,碳元素与氢元素的原子个数之比为:20:12=5:3;
(3)设硫酸中硫元素的化合价为x,硫酸中氢元素化合价是+1,氧元素化合价是﹣2,根据化合物中元素的化合价代数和为零:(+1)×2+x+(﹣2)×4=0,x=+6;
(4)①尼古丁由碳、氢、氮3种元素组成,正确;
②尼古丁是由尼古丁分子构成的,1个尼古丁分子中含10个碳原子,错误;
③吸烟对他人也有害,错误;
④氧化物是由两种元素组成的化合物,且一种元素为氧元素,一氧化碳和二氧化碳都属于氧化物,正确;
⑤根据尼古丁(C10H14N2)化学式可知,尼古丁中碳元素、氢元素和氧元素的质量比=(10×12):(1×14):(14×2)=60:7:14,在尼古丁中碳元素的含量最高,正确。
故答案为:(1)4;
(2)5:3;
(3)+6;
(4)A。
20.钠摄入过量或钾摄入不足都是导致高血压的风险因素。日常生活中选择食用低钠盐能实现减钠补钾。如图为某品牌低钠盐的标签,请你根据标签回答以下问题:
(1)氯化钾的相对分子质量为 74.5 。
(2)人体每天摄入钠元素的质量不宜超过2.3g。如果人体所需的钠元素全部来自该品牌食盐,那么一个人每天摄入该品牌低钠盐的质量不宜超过多少克?(结果保留一位小数)
【解答】解:(1)KCl的相对分子质量为:39+35.5=74.5;故填:74.5;
(2)一个人每天摄入该品牌低钠盐的质量不宜超过:2.3g÷÷70%=8.4g
故填:8.4g.
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
