化学人教版九年级第六单元 碳和碳的氧化物课题2 二氧化碳制取的研究课件(共17张PPT)
文档属性
| 名称 | 化学人教版九年级第六单元 碳和碳的氧化物课题2 二氧化碳制取的研究课件(共17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-21 00:00:00 | ||
图片预览


文档简介
(共17张PPT)
二氧化碳制取的研究(第2课时)
实验室制取二氧化碳 药品
化学方程式
实验装置 发生装置器材:
收集装置器材:
检验
验满
锥形瓶、双孔橡胶塞、长颈漏斗、
玻璃导管、胶皮管
集气瓶、玻璃片、玻璃导管
将产生的气体通入澄清石灰水中
将燃着的木条置于集气瓶口
块状大理石、稀盐酸
制取二氧化碳气体
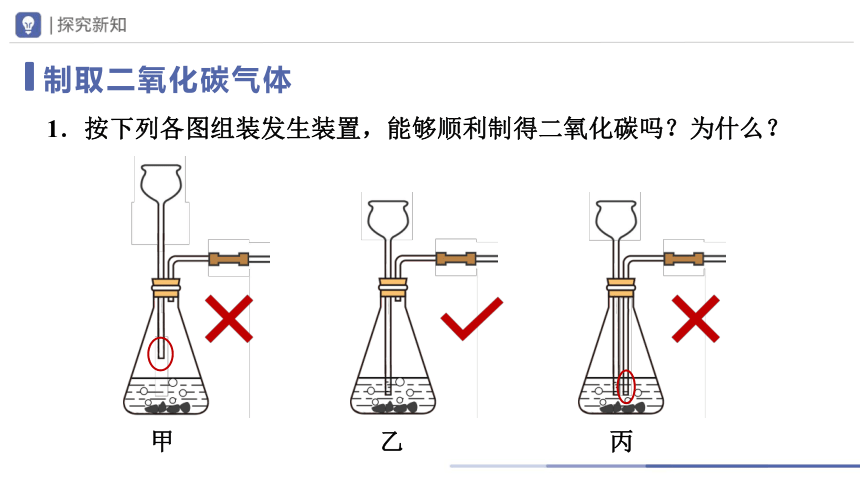
1.按下列各图组装发生装置,能够顺利制得二氧化碳吗?为什么?
甲
乙
丙
制取二氧化碳气体
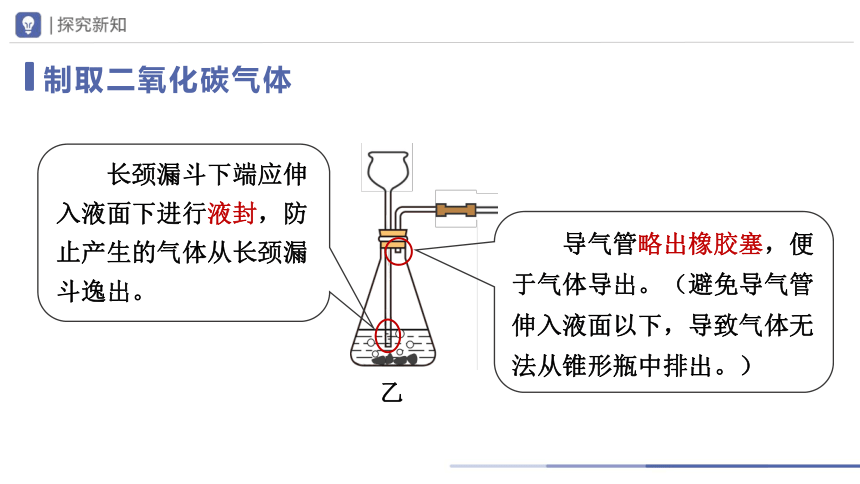
乙
导气管略出橡胶塞,便于气体导出。(避免导气管伸入液面以下,导致气体无法从锥形瓶中排出。)
长颈漏斗下端应伸入液面下进行液封,防止产生的气体从长颈漏斗逸出。
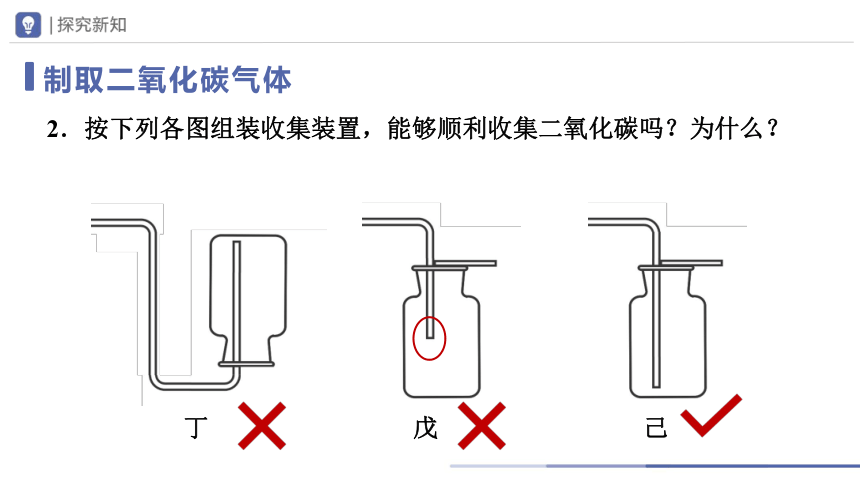
2.按下列各图组装收集装置,能够顺利收集二氧化碳吗?为什么?
制取二氧化碳气体
丁
戊
己
制取二氧化碳气体
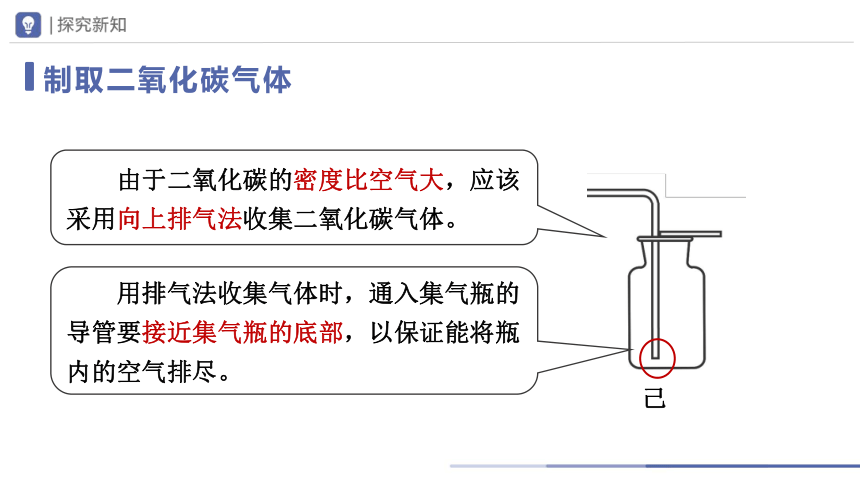
己
由于二氧化碳的密度比空气大,应该采用向上排气法收集二氧化碳气体。
用排气法收集气体时,通入集气瓶的导管要接近集气瓶的底部,以保证能将瓶内的空气排尽。
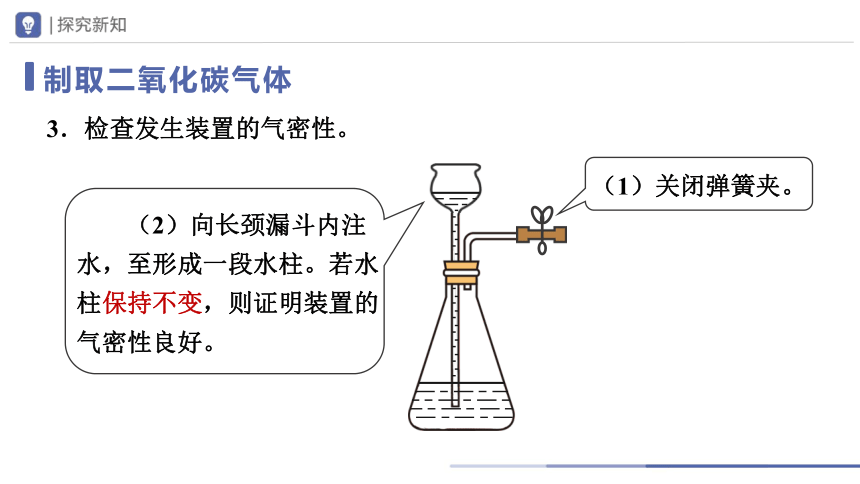
3.检查发生装置的气密性。
制取二氧化碳气体
(1)关闭弹簧夹。
(2)向长颈漏斗内注水,至形成一段水柱。若水柱保持不变,则证明装置的
气密性良好。
把锥形瓶横放,用镊子夹取大理石放入锥形瓶的瓶口,之后把锥形瓶慢慢地竖起来,使大理石缓缓地滑到瓶底,以免打破容器。
(2)倾倒稀盐酸时,细口瓶贴标签的一面要___________,细口瓶的瓶塞要___放在桌面上。倒完液体后,立刻盖紧瓶塞,放回原处。
(1)怎样向锥形瓶中装入块状大理石?
朝向手心处
倒
制取二氧化碳气体
4.装入药品。
40+12+3×16
制取二氧化碳气体
5.要制取 0.88 g 的 CO2 ,至少需要多少克的碳酸钙和足量的稀盐酸?
【解】设:需要碳酸钙的质量为 x 。
x
12+2×16
0.88 g
答:需要 2 g 的碳酸钙。
实验室制取气体的一般思路和方法
确定制取气体的化学反应原理
确定如何验证
气体是所需气体
确定采用的
实验装置
原料廉价易得
反应条件易实现
生成的气体单一纯净
反应速率适中等
选择什么药品
实验室制取气体的一般思路和方法
确定制取气体的化学反应原理
确定如何验证
气体是所需气体
确定采用的
实验装置
原料廉价易得
反应条件易实现
生成的气体单一纯净
反应速率适中等
实验室中易实现的反应条件:
常温、加热、加催化剂等
实验室制取气体的一般思路和方法
确定制取气体的化学反应原理
确定如何验证
气体是所需气体
确定采用的
实验装置
原料廉价易得
反应条件易实现
生成的气体单一纯净
反应速率适中等
选择什么反应制取这种气体
确定制取气体的化学反应原理
确定如何验证
气体是所需气体
实验室制取气体的一般思路和方法
确定采用的
实验装置
发生装置:
收集装置
不易溶于水,不与水反应——排水法
气体密度比空气的大——向上排气法
气体密度比空气的小——向下排气法
密度差别越大,气体越纯净
反应物的状态、反应条件(是否加热等)
(气体更纯净)
确定制取气体的化学反应原理
确定如何验证
气体是所需气体
实验室制取气体的一般思路和方法
确定采用的
实验装置
根据所需气体区别于其他气体的某种特性或特征进行验证,
如二氧化碳使澄清石灰水变浑浊、氧气的助燃性等。
注意区分验证与验满:验满只需根据气体区别于空气的一种
特性,采用简单的方法进行,如二氧化碳不支持燃烧。
1.实验室中制取氢气,收集装置可以采用哪种方法?
氢气不溶于水、不与水反应,可以采用排水法收集;
氢气的密度比空气的密度小且不与空气中的成分反应,可以采用向下排空气法收集。
2.氨气(NH3)极易溶于水,加热氯化铵固体和氢氧化钙固体的混合物可制得氨气。简单画出制取氨气的实验装置图。
14+3×1=17<29
氨气密度比空气小
组装实验装置,检查气密性
制取二氧化碳的操作步骤
装药品
检验和验满
收集气体
实验室制取气体的一般思路
确定化学反应原理
确定实验装置
验证气体
二氧化碳制取的研究(第2课时)
实验室制取二氧化碳 药品
化学方程式
实验装置 发生装置器材:
收集装置器材:
检验
验满
锥形瓶、双孔橡胶塞、长颈漏斗、
玻璃导管、胶皮管
集气瓶、玻璃片、玻璃导管
将产生的气体通入澄清石灰水中
将燃着的木条置于集气瓶口
块状大理石、稀盐酸
制取二氧化碳气体
1.按下列各图组装发生装置,能够顺利制得二氧化碳吗?为什么?
甲
乙
丙
制取二氧化碳气体
乙
导气管略出橡胶塞,便于气体导出。(避免导气管伸入液面以下,导致气体无法从锥形瓶中排出。)
长颈漏斗下端应伸入液面下进行液封,防止产生的气体从长颈漏斗逸出。
2.按下列各图组装收集装置,能够顺利收集二氧化碳吗?为什么?
制取二氧化碳气体
丁
戊
己
制取二氧化碳气体
己
由于二氧化碳的密度比空气大,应该采用向上排气法收集二氧化碳气体。
用排气法收集气体时,通入集气瓶的导管要接近集气瓶的底部,以保证能将瓶内的空气排尽。
3.检查发生装置的气密性。
制取二氧化碳气体
(1)关闭弹簧夹。
(2)向长颈漏斗内注水,至形成一段水柱。若水柱保持不变,则证明装置的
气密性良好。
把锥形瓶横放,用镊子夹取大理石放入锥形瓶的瓶口,之后把锥形瓶慢慢地竖起来,使大理石缓缓地滑到瓶底,以免打破容器。
(2)倾倒稀盐酸时,细口瓶贴标签的一面要___________,细口瓶的瓶塞要___放在桌面上。倒完液体后,立刻盖紧瓶塞,放回原处。
(1)怎样向锥形瓶中装入块状大理石?
朝向手心处
倒
制取二氧化碳气体
4.装入药品。
40+12+3×16
制取二氧化碳气体
5.要制取 0.88 g 的 CO2 ,至少需要多少克的碳酸钙和足量的稀盐酸?
【解】设:需要碳酸钙的质量为 x 。
x
12+2×16
0.88 g
答:需要 2 g 的碳酸钙。
实验室制取气体的一般思路和方法
确定制取气体的化学反应原理
确定如何验证
气体是所需气体
确定采用的
实验装置
原料廉价易得
反应条件易实现
生成的气体单一纯净
反应速率适中等
选择什么药品
实验室制取气体的一般思路和方法
确定制取气体的化学反应原理
确定如何验证
气体是所需气体
确定采用的
实验装置
原料廉价易得
反应条件易实现
生成的气体单一纯净
反应速率适中等
实验室中易实现的反应条件:
常温、加热、加催化剂等
实验室制取气体的一般思路和方法
确定制取气体的化学反应原理
确定如何验证
气体是所需气体
确定采用的
实验装置
原料廉价易得
反应条件易实现
生成的气体单一纯净
反应速率适中等
选择什么反应制取这种气体
确定制取气体的化学反应原理
确定如何验证
气体是所需气体
实验室制取气体的一般思路和方法
确定采用的
实验装置
发生装置:
收集装置
不易溶于水,不与水反应——排水法
气体密度比空气的大——向上排气法
气体密度比空气的小——向下排气法
密度差别越大,气体越纯净
反应物的状态、反应条件(是否加热等)
(气体更纯净)
确定制取气体的化学反应原理
确定如何验证
气体是所需气体
实验室制取气体的一般思路和方法
确定采用的
实验装置
根据所需气体区别于其他气体的某种特性或特征进行验证,
如二氧化碳使澄清石灰水变浑浊、氧气的助燃性等。
注意区分验证与验满:验满只需根据气体区别于空气的一种
特性,采用简单的方法进行,如二氧化碳不支持燃烧。
1.实验室中制取氢气,收集装置可以采用哪种方法?
氢气不溶于水、不与水反应,可以采用排水法收集;
氢气的密度比空气的密度小且不与空气中的成分反应,可以采用向下排空气法收集。
2.氨气(NH3)极易溶于水,加热氯化铵固体和氢氧化钙固体的混合物可制得氨气。简单画出制取氨气的实验装置图。
14+3×1=17<29
氨气密度比空气小
组装实验装置,检查气密性
制取二氧化碳的操作步骤
装药品
检验和验满
收集气体
实验室制取气体的一般思路
确定化学反应原理
确定实验装置
验证气体
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
