2.4元素课件(共28张PPT)---2023--2024学年九年级化学鲁教版上册
文档属性
| 名称 | 2.4元素课件(共28张PPT)---2023--2024学年九年级化学鲁教版上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 752.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-21 00:00:00 | ||
图片预览








文档简介
(共28张PPT)
第四节 元素
课时1 元素与元素符号
1.认识物质是由元素组成的,知道质子数相同的一类原子属于同种元素。
2.初步形成基于元素和分子、原子认识物质及其变化的视角,建立认识物质的宏观和微观视角之间的关联,知道物质的性质与组成、结构有关。
一、元素与元素符号
1.元素:把具有 的原子归为一类,每一类原子称为一种元素。
2.元素符号:国际上规定每种元素都采用 的符号来表示,这种符号叫作元素符号。
二、单质和化合物
1.单质:只由 种元素组成的 。
2.化合物:由 元素组成的 。
相同质子数
统一
一
纯净物
两种或两种以上
纯净物
技巧点拨
(1)分子、原子、元素、物质之间的关系
(2)元素符号前面添加数字时只具有微观意义,即只表示 n个原子。
(3)元素只讲种类,不讲个数。
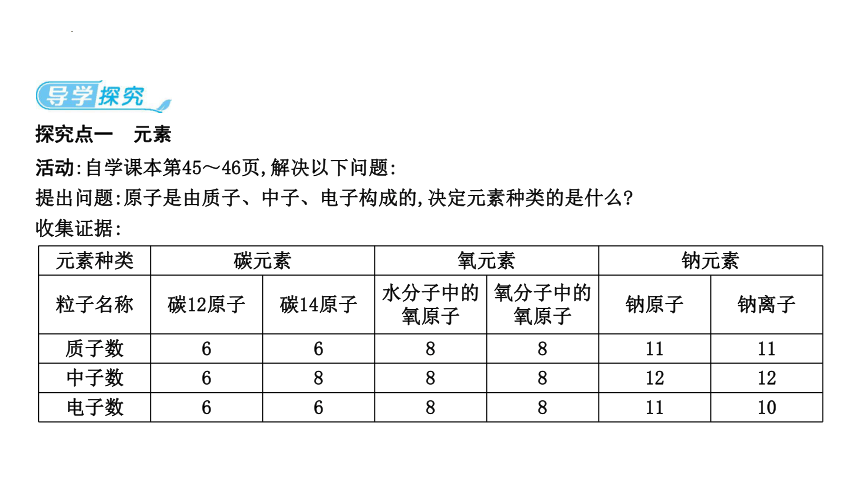
探究点一 元素
活动:自学课本第45~46页,解决以下问题:
提出问题:原子是由质子、中子、电子构成的,决定元素种类的是什么
收集证据:
元素种类 碳元素 氧元素 钠元素
粒子名称 碳12原子 碳14原子 水分子中的氧原子 氧分子中的氧原子 钠原子 钠离子
质子数 6 6 8 8 11 11
中子数 6 8 8 8 12 12
电子数 6 6 8 8 11 10
获得结论:
1. 决定元素的种类。
同种元素的原子, 一定相同;不同种元素的原子, 一定不同。
2.元素的概念:具有 的 的总称;既然是总称,元素只论 ,不论 ,用来描述物质的组成。
合作共建:
项目 元素 原子
区别 元素是 (填“宏观”或“微观”)概念, (填“能”或“不能”)论种类, (填“能”或“不能”)表示个数 原子是 (填“宏观”或“微观”)概念, (填“能”或“不能”)论种类, (填“能”或“不能”)表示个数
适用 范围 元素应用于描述物质的 原子应用于描述物质的 或分子的
联系 元素是质子数相同的一类原子的总称 原子是元素的最小单元
质子数
质子数
质子数
相同质子数
一类原子
种类
个数
宏观
能
不能
微观
能
能
组成
构成
构成
[例1] 中国自行研制的、具有自主知识产权的大型客机C919于2022年9月29日获得民航管理局颁发的合格证书。该客机部分机身采用了铝锂合金,铝元素与锂元素的本质区别是( )
A.中子数不同
B.质子数不同
C.最外层电子数不同
D.相对原子质量不同
B
描述物质组成时,宏观描述要说“由××元素组成”;微观描述要说“由××粒子(如分子、原子、离子)构成”。
探究点二 单质和化合物
活动1:请写出氧气、水、二氧化碳、过氧化氢等物质的化学式。
氧气 、水 、二氧化碳 、过氧化氢 。
O2
H2O
CO2
H2O2
[思考]以上均属于纯净物,以上这些纯净物由几种元素组成 能否对这些物质进行分类 分类的依据是什么
答案:氧气只由一种元素组成;水、二氧化碳、过氧化氢由两种元素组成。依据元素组成的种类,题述纯净物可分为单质和化合物。氧气属于单质;水、二氧化碳、过氧化氢属于化 合物。
活动2:请对单质和化合物的定义作出简要的归纳。
项目 分类角度 概念 举例
纯净物 单质 组成纯净物的元素种类是否相同 只由 元素组成的纯净物 氧气、臭氧、氢气、镁等
化合物 由 元素组成的纯净物 水、氧化镁、氯化钠等
一种
两种或两种以上
[例2] (2022柳州)分类是一种重要的化学观念。下列物质属于单质的是( )
A.硫(S) B.硝酸(HNO3)
C.硫酸铜(CuSO4) D.氢氧化钾(KOH)
A
(1)由同种元素组成的物质不一定是单质,如氧气和臭氧组成的物质中只含有氧元素,但属于混合物;因此,由一种元素组成的物质可能是单质、纯净物或混合物,但一定不是化合物。
(2)同一种元素可以存在于不同物质中,如氧气和二氧化碳中均含有氧元素。
探究点三 元素符号
活动:自学课本第46~47页元素符号,回答下列问题。
1.元素可用统一的符号来表示,这种符号叫 ,它的书写规则是(1)由一个字母表示的元素符号,字母 。(2)由两个字母表示的元素符号,第一个字母 ,第二个字母 。
2.元素符号的意义:既表示 (宏观意义),还可表示 (微观意义)。
例:N表示的意义有 和 。
如果在元素符号前面添加数字,就只表示该元素的原子个数,不能表示该元素。如H既表示氢元素又能表示一个氢原子,而2H只能表示 ,3Fe表示 ,若要表示5个镁原子可写为 。
3.元素在自然界中的分布并不均匀,按质量计算地壳里元素含量由高到低的顺序依次是
,地壳中含量最多的金属元素是 。
元素符号
大写
大写
小写
这种元素
该元素的一个原子
氮元素
1个氮原子
2个氢原子
3个铁原子
5Mg
氧、硅、铝、铁、钙等
铝
[例3] 符号“N”表示的意义有( )
①氮元素 ②氮分子 ③一个氮元素 ④一个氮原子 ⑤氮气
A.①④ B.③④
C.④⑤ D.①②③④
A
元素符号的意义
(1)宏观意义:表示一种元素。
(2)微观意义
①表示一个原子。
②符号前面若有数字,则只能表示该原子的个数,如2H表示2个氢原子,不能说是2个氢元素。
③元素符号也可以表示离子,在元素符号的右上角,先标电荷数,再标电性,如镁离子表示为Mg2+,电荷数为1时,省略不写,如Na+、Cl-。
质子数
氧、硅、铝、铁、钙
知识点一 元素
1.(2022青岛)某品牌饼干的营养成分表中标有钠、钙、铁的含量,这里的“钠、钙、铁”指的是( )
A.分子 B.原子 C.单质 D.元素
2.(2022乐山)下表是生物细胞中的部分元素及其组成,其中属于金属元素的是( )
D
C
选项 元素符号 质量分数
A N 3%
B P 1%
C K 0.35%
D S 0.25%
知识点二 单质和化合物
4.(2022泰安期中)现有①空气,②四氧化三铁,③泥水,④二氧化碳,⑤液态氧,⑥水,共六种物质,按要求填入对应序号。
(1)属于混合物的是 。
(2)属于纯净物的是 。
(3)属于化合物的是 。
C
①③
②④⑤⑥
②④⑥
知识点三 元素符号及其意义
5.(2023开封月考)下列元素符号中首字母相同的一组是( )
A.氢、硅、氦 B.氟、铁、磷
C.钙、氯、碳 D.氮、钠、镁
6.元素符号的意义:
(1)宏观上表示 ,如“N”表示 ,“O”表示 。每种元素只能有一种元素符号。
(2)微观上表示这种元素的 ,如“N”表示 ,“O”表示 。如果物质直接由原子构成,则该元素符号还表示一种物质,如“Fe”表示铁这种物质。
C
一种元素
氮元素
氧元素
一个原子
1个氮原子
1个氧原子
课时2 元素周期表
初步认识元素周期表。
1.1869年,俄国化学家 编制了第一张元素周期表。
2.在元素周期表中有 个横行, 个纵行。每个横行叫一个 ,每个纵行叫一个 (8、9、10纵行共同组成一个族)。
3.原子序数= = = 。
4.元素周期表中每一格包含的信息:
门捷列夫
7
18
周期
族
核电荷数
核内质子数
核外电子数
技巧点拨
探究点 元素周期表
认真阅读课本,仔细观察课本最后一页“元素周期表”,回答下列问题。
(1)你对元素周期表是如何认识的
①最早发现和编制者:1869年,俄国化学家 发现了元素周期律并编制了第一张元素周期表。
②排列:如今的元素周期表是把目前已发现并被正式命名的元素按照原子核内 由小到大的顺序排列而成的。
③结构:共 个横行, 个纵行,每一个横行叫作一个 ,每一个纵行叫作一个族(8、9、10三个纵行共同组成一个族)。
④原子序数:元素周期表中每一种元素都有一个序号,称为原子序数。它的数值等于其原子核内 。
门捷列夫
质子数
7
18
周期
质子数
(2)试着写出图中各部分的意义。
注:原子序数=核内 。
原子序数
元素符号
元素名称
相对原子质量
质子数
[例题] (2022南宁)如图是元素周期表的一部分,下列说法错误的是( )
B
甲
7 N 氮 14.01 乙 丙 10 Ne
氖
20.18
A.甲元素的符号是He
B.原子序数:乙>丙>甲
C.氮元素的相对原子质量是14.01
D.氖原子的结构示意图为
(1)元素周期表中原子核外电子层数即为该原子所在的周期数。
(2)同一族中,从上到下元素的原子最外层电子数相同,电子层数依次递增。
7
18
16
知识点 元素周期表
1.(2022河南)元素周期表是学习化学的工具。发现元素周期律并编制元素周期表的化学家是( )
A.拉瓦锡 B.道尔顿
C.门捷列夫 D.阿伏加德罗
2.如图是四种元素的原子结构示意图及氟元素在元素周期表中的信息。根据图示回答下列 问题。
(1)与A化学性质相似的原子是 (填字母,下同)。
(2)具有相对稳定结构的原子是 。
(3)C元素在元素周期表中位于第 周期。
(4)根据E图示所给信息,推出氟元素原子的核外电子总数为 。
C
D
B
三
9
3.(2022百色)如图中的①、②分别是钠元素、氯元素在周期表中的信息,A、B、C、D是四种粒子的结构示意图。请你回答下列问题:
(1)钠元素的原子序数为 ,氯元素的相对原子质量为 。
(2)示意图D中的x= 。
(3)A、B、C、D中属于同种元素的粒子是 (填字母)。
(4)已知A和B两种粒子的化学性质相似,是由于 。
(5)C粒子属于 (填“阴”或“阳”)离子。
11
35.45
8
BC
它们原子的最外层电子数相同
阴
第四节 元素
课时1 元素与元素符号
1.认识物质是由元素组成的,知道质子数相同的一类原子属于同种元素。
2.初步形成基于元素和分子、原子认识物质及其变化的视角,建立认识物质的宏观和微观视角之间的关联,知道物质的性质与组成、结构有关。
一、元素与元素符号
1.元素:把具有 的原子归为一类,每一类原子称为一种元素。
2.元素符号:国际上规定每种元素都采用 的符号来表示,这种符号叫作元素符号。
二、单质和化合物
1.单质:只由 种元素组成的 。
2.化合物:由 元素组成的 。
相同质子数
统一
一
纯净物
两种或两种以上
纯净物
技巧点拨
(1)分子、原子、元素、物质之间的关系
(2)元素符号前面添加数字时只具有微观意义,即只表示 n个原子。
(3)元素只讲种类,不讲个数。
探究点一 元素
活动:自学课本第45~46页,解决以下问题:
提出问题:原子是由质子、中子、电子构成的,决定元素种类的是什么
收集证据:
元素种类 碳元素 氧元素 钠元素
粒子名称 碳12原子 碳14原子 水分子中的氧原子 氧分子中的氧原子 钠原子 钠离子
质子数 6 6 8 8 11 11
中子数 6 8 8 8 12 12
电子数 6 6 8 8 11 10
获得结论:
1. 决定元素的种类。
同种元素的原子, 一定相同;不同种元素的原子, 一定不同。
2.元素的概念:具有 的 的总称;既然是总称,元素只论 ,不论 ,用来描述物质的组成。
合作共建:
项目 元素 原子
区别 元素是 (填“宏观”或“微观”)概念, (填“能”或“不能”)论种类, (填“能”或“不能”)表示个数 原子是 (填“宏观”或“微观”)概念, (填“能”或“不能”)论种类, (填“能”或“不能”)表示个数
适用 范围 元素应用于描述物质的 原子应用于描述物质的 或分子的
联系 元素是质子数相同的一类原子的总称 原子是元素的最小单元
质子数
质子数
质子数
相同质子数
一类原子
种类
个数
宏观
能
不能
微观
能
能
组成
构成
构成
[例1] 中国自行研制的、具有自主知识产权的大型客机C919于2022年9月29日获得民航管理局颁发的合格证书。该客机部分机身采用了铝锂合金,铝元素与锂元素的本质区别是( )
A.中子数不同
B.质子数不同
C.最外层电子数不同
D.相对原子质量不同
B
描述物质组成时,宏观描述要说“由××元素组成”;微观描述要说“由××粒子(如分子、原子、离子)构成”。
探究点二 单质和化合物
活动1:请写出氧气、水、二氧化碳、过氧化氢等物质的化学式。
氧气 、水 、二氧化碳 、过氧化氢 。
O2
H2O
CO2
H2O2
[思考]以上均属于纯净物,以上这些纯净物由几种元素组成 能否对这些物质进行分类 分类的依据是什么
答案:氧气只由一种元素组成;水、二氧化碳、过氧化氢由两种元素组成。依据元素组成的种类,题述纯净物可分为单质和化合物。氧气属于单质;水、二氧化碳、过氧化氢属于化 合物。
活动2:请对单质和化合物的定义作出简要的归纳。
项目 分类角度 概念 举例
纯净物 单质 组成纯净物的元素种类是否相同 只由 元素组成的纯净物 氧气、臭氧、氢气、镁等
化合物 由 元素组成的纯净物 水、氧化镁、氯化钠等
一种
两种或两种以上
[例2] (2022柳州)分类是一种重要的化学观念。下列物质属于单质的是( )
A.硫(S) B.硝酸(HNO3)
C.硫酸铜(CuSO4) D.氢氧化钾(KOH)
A
(1)由同种元素组成的物质不一定是单质,如氧气和臭氧组成的物质中只含有氧元素,但属于混合物;因此,由一种元素组成的物质可能是单质、纯净物或混合物,但一定不是化合物。
(2)同一种元素可以存在于不同物质中,如氧气和二氧化碳中均含有氧元素。
探究点三 元素符号
活动:自学课本第46~47页元素符号,回答下列问题。
1.元素可用统一的符号来表示,这种符号叫 ,它的书写规则是(1)由一个字母表示的元素符号,字母 。(2)由两个字母表示的元素符号,第一个字母 ,第二个字母 。
2.元素符号的意义:既表示 (宏观意义),还可表示 (微观意义)。
例:N表示的意义有 和 。
如果在元素符号前面添加数字,就只表示该元素的原子个数,不能表示该元素。如H既表示氢元素又能表示一个氢原子,而2H只能表示 ,3Fe表示 ,若要表示5个镁原子可写为 。
3.元素在自然界中的分布并不均匀,按质量计算地壳里元素含量由高到低的顺序依次是
,地壳中含量最多的金属元素是 。
元素符号
大写
大写
小写
这种元素
该元素的一个原子
氮元素
1个氮原子
2个氢原子
3个铁原子
5Mg
氧、硅、铝、铁、钙等
铝
[例3] 符号“N”表示的意义有( )
①氮元素 ②氮分子 ③一个氮元素 ④一个氮原子 ⑤氮气
A.①④ B.③④
C.④⑤ D.①②③④
A
元素符号的意义
(1)宏观意义:表示一种元素。
(2)微观意义
①表示一个原子。
②符号前面若有数字,则只能表示该原子的个数,如2H表示2个氢原子,不能说是2个氢元素。
③元素符号也可以表示离子,在元素符号的右上角,先标电荷数,再标电性,如镁离子表示为Mg2+,电荷数为1时,省略不写,如Na+、Cl-。
质子数
氧、硅、铝、铁、钙
知识点一 元素
1.(2022青岛)某品牌饼干的营养成分表中标有钠、钙、铁的含量,这里的“钠、钙、铁”指的是( )
A.分子 B.原子 C.单质 D.元素
2.(2022乐山)下表是生物细胞中的部分元素及其组成,其中属于金属元素的是( )
D
C
选项 元素符号 质量分数
A N 3%
B P 1%
C K 0.35%
D S 0.25%
知识点二 单质和化合物
4.(2022泰安期中)现有①空气,②四氧化三铁,③泥水,④二氧化碳,⑤液态氧,⑥水,共六种物质,按要求填入对应序号。
(1)属于混合物的是 。
(2)属于纯净物的是 。
(3)属于化合物的是 。
C
①③
②④⑤⑥
②④⑥
知识点三 元素符号及其意义
5.(2023开封月考)下列元素符号中首字母相同的一组是( )
A.氢、硅、氦 B.氟、铁、磷
C.钙、氯、碳 D.氮、钠、镁
6.元素符号的意义:
(1)宏观上表示 ,如“N”表示 ,“O”表示 。每种元素只能有一种元素符号。
(2)微观上表示这种元素的 ,如“N”表示 ,“O”表示 。如果物质直接由原子构成,则该元素符号还表示一种物质,如“Fe”表示铁这种物质。
C
一种元素
氮元素
氧元素
一个原子
1个氮原子
1个氧原子
课时2 元素周期表
初步认识元素周期表。
1.1869年,俄国化学家 编制了第一张元素周期表。
2.在元素周期表中有 个横行, 个纵行。每个横行叫一个 ,每个纵行叫一个 (8、9、10纵行共同组成一个族)。
3.原子序数= = = 。
4.元素周期表中每一格包含的信息:
门捷列夫
7
18
周期
族
核电荷数
核内质子数
核外电子数
技巧点拨
探究点 元素周期表
认真阅读课本,仔细观察课本最后一页“元素周期表”,回答下列问题。
(1)你对元素周期表是如何认识的
①最早发现和编制者:1869年,俄国化学家 发现了元素周期律并编制了第一张元素周期表。
②排列:如今的元素周期表是把目前已发现并被正式命名的元素按照原子核内 由小到大的顺序排列而成的。
③结构:共 个横行, 个纵行,每一个横行叫作一个 ,每一个纵行叫作一个族(8、9、10三个纵行共同组成一个族)。
④原子序数:元素周期表中每一种元素都有一个序号,称为原子序数。它的数值等于其原子核内 。
门捷列夫
质子数
7
18
周期
质子数
(2)试着写出图中各部分的意义。
注:原子序数=核内 。
原子序数
元素符号
元素名称
相对原子质量
质子数
[例题] (2022南宁)如图是元素周期表的一部分,下列说法错误的是( )
B
甲
7 N 氮 14.01 乙 丙 10 Ne
氖
20.18
A.甲元素的符号是He
B.原子序数:乙>丙>甲
C.氮元素的相对原子质量是14.01
D.氖原子的结构示意图为
(1)元素周期表中原子核外电子层数即为该原子所在的周期数。
(2)同一族中,从上到下元素的原子最外层电子数相同,电子层数依次递增。
7
18
16
知识点 元素周期表
1.(2022河南)元素周期表是学习化学的工具。发现元素周期律并编制元素周期表的化学家是( )
A.拉瓦锡 B.道尔顿
C.门捷列夫 D.阿伏加德罗
2.如图是四种元素的原子结构示意图及氟元素在元素周期表中的信息。根据图示回答下列 问题。
(1)与A化学性质相似的原子是 (填字母,下同)。
(2)具有相对稳定结构的原子是 。
(3)C元素在元素周期表中位于第 周期。
(4)根据E图示所给信息,推出氟元素原子的核外电子总数为 。
C
D
B
三
9
3.(2022百色)如图中的①、②分别是钠元素、氯元素在周期表中的信息,A、B、C、D是四种粒子的结构示意图。请你回答下列问题:
(1)钠元素的原子序数为 ,氯元素的相对原子质量为 。
(2)示意图D中的x= 。
(3)A、B、C、D中属于同种元素的粒子是 (填字母)。
(4)已知A和B两种粒子的化学性质相似,是由于 。
(5)C粒子属于 (填“阴”或“阳”)离子。
11
35.45
8
BC
它们原子的最外层电子数相同
阴
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
