到实验室去 化学实验基本技能训练(二) 课件(共22张PPT)---2023--2024学年九年级化学鲁教版上册
文档属性
| 名称 | 到实验室去 化学实验基本技能训练(二) 课件(共22张PPT)---2023--2024学年九年级化学鲁教版上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 633.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-21 00:00:00 | ||
图片预览





文档简介
(共22张PPT)
到实验室去:化学实验基本技能训练(二)
学会简单仪器的使用及连接等实验基本操作。
[实验目的]
1.初步学会使用托盘天平(或电子秤)、量筒等仪器。
2.学会物质的称量、仪器的连接、装置气密性的检验和仪器的洗涤等实验技能。
[实验用品]
1.仪器:托盘天平(或电子秤)、量筒、试管、烧杯、试管刷等。
2.药品:食盐、蒸馏水等。
[实验过程]
实验一 物质的称量
1.固体药品的称量(用托盘天平称量)
称量原理:当天平达到平衡时,左盘上的质量=右盘上的质量+游码质量。
称量时:应先 ,称量时称量物放在 盘,砝码放在 盘,有时需拨动 。
为了不使托盘天平受到污染和损坏,应在两个托盘上各放 ,易潮解或有腐蚀性的药品要放在 或表面皿等玻璃器皿中称量,如氢氧化钠。
调节托盘天平平衡
左
右
游码
一张相同质量的纸片
烧杯
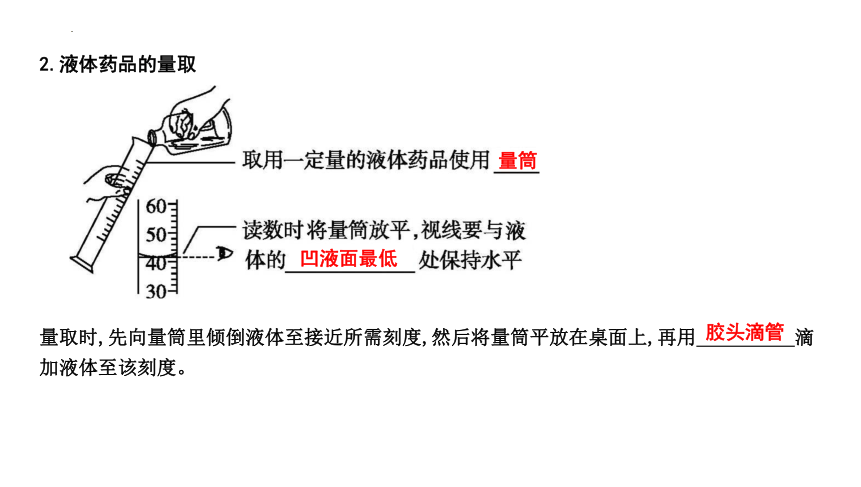
2.液体药品的量取
量取时,先向量筒里倾倒液体至接近所需刻度,然后将量筒平放在桌面上,再用 滴加液体至该刻度。
量筒
凹液面最低
胶头滴管
量筒不能加热,不能用作反应容器。
实验二 仪器的连接与洗涤
1.连接方法
玻璃管、橡皮塞、胶皮管的连接:
(1)将玻璃管插入胶皮管时,关键掌握两个字——润、转,即玻璃管一端用水 ,插入过程中应稍稍 插入(如下图左)。
(2)用橡皮塞塞住试管时,一手持试管,一手持橡皮塞,稍稍用力转动塞入(如下图右)。
润湿
用力转动
在玻璃管上套上胶皮管 用橡皮塞塞住试管
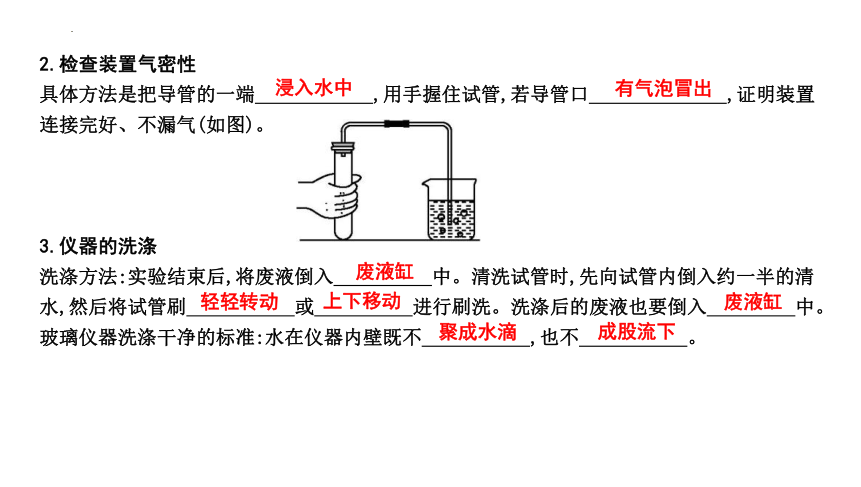
2.检查装置气密性
具体方法是把导管的一端 ,用手握住试管,若导管口 ,证明装置连接完好、不漏气(如图)。
3.仪器的洗涤
洗涤方法:实验结束后,将废液倒入 中。清洗试管时,先向试管内倒入约一半的清水,然后将试管刷 或 进行刷洗。洗涤后的废液也要倒入 中。
玻璃仪器洗涤干净的标准:水在仪器内壁既不 ,也不 。
浸入水中
有气泡冒出
废液缸
轻轻转动
上下移动
废液缸
聚成水滴
成股流下
[拓展探究]
1.用托盘天平称量物质时,若物质和砝码的位置放反了,读取物质的质量的数值比实际值偏大还是偏小(称量过程中使用游码)
答案:偏大。因为读数时,称得的质量是m砝码+m游码,但物质、砝码放反了,物质实际的质量是
m砝码-m游码,所以读取物质的质量的数值比实际值偏大。
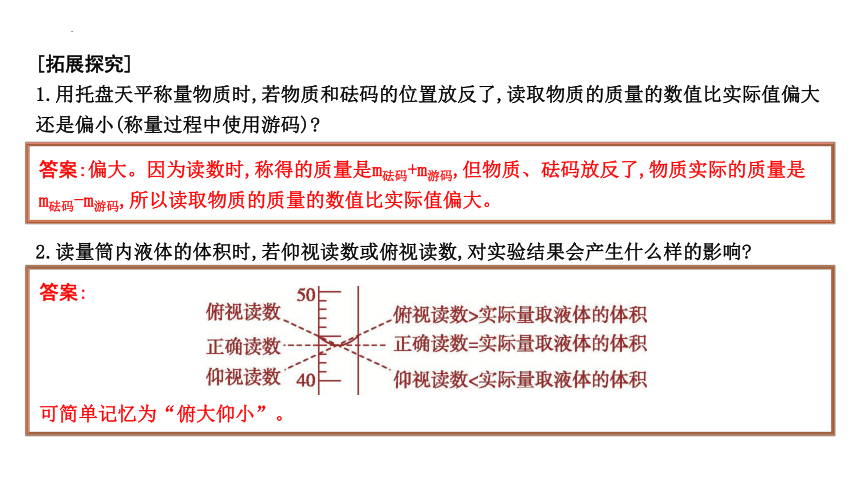
2.读量筒内液体的体积时,若仰视读数或俯视读数,对实验结果会产生什么样的影响
答案:
可简单记忆为“俯大仰小”。
[实战演练]
1.某同学测定的下列数据不合理的是( )
A.用温度计测得某液体的温度为23 ℃
B.用50 mL量筒量取了4.34 mL的水
C.用托盘天平称得某烧杯的质量为46.8 g
D.用10 mL的量筒量取了5.0 mL的水
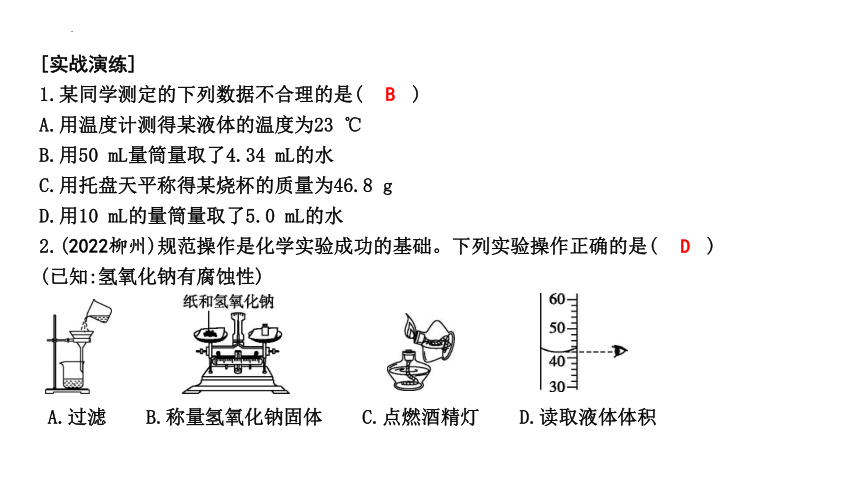
2.(2022柳州)规范操作是化学实验成功的基础。下列实验操作正确的是( )
(已知:氢氧化钠有腐蚀性)
B
D
A.过滤 B.称量氢氧化钠固体 C.点燃酒精灯 D.读取液体体积
3.(2023兴化月考)某学生在实验室练习用量筒量取液体,量筒放平稳且面对刻度,先是仰视液面读数为40 mL,倒出部分液体后,又俯视液面,读数为30 mL,则该学生实际倒出液体的体积为( )
A.大于10 mL B.小于10 mL
C.等于10 mL D.无法判断
4.化学实验必须严格按规定操作,否则可能导致实验失败或人身伤害。请填写下列错误的操作或错误操作可能造成的不良后果。
A
错误的操作 可能造成的不良后果
(1)给试管里的液体加热时,试管靠近灯芯
(2) 量取5 mL液体,实际5.4 mL
(3)向燃着的酒精灯内添加酒精
(4)砝码与药品位置颠倒了 称取6.8 g固体,实际只有 g(1 g以下用游码)
试管底部炸裂
仰视读数量取5 mL液体
引起火灾
5.2
5.根据下列实验示意图回答相关问题:
甲 称量金属块的质量 乙 量取液体体积
丙 检查装置气密性 丁 加热固体
(1)图甲中除了砝码和金属块位置放反了,还有一处明显的错误是 ;称量前需要调节天平平衡,游码归零,如发现横梁指针向左偏,此时应将平衡螺母向 (填“左”或“右”)调;若左盘中的砝码及游码指示位置如图所示,则金属块的质量为 g。
(2)指出图乙中两处错误:① ;② 。如量取42 mL 水,应选择 (填“50 mL”或“100 mL”)量筒。
(3)小亮同学用图丙所示方法检查该装置气密性,他没有看到导管口有气泡冒出,因此判断该装置漏气,你认为他的判断 (填“合理”或“不合理”),说明理由: _
_
。
(4)改正图丁中两处错误:① ;② 。
用手拿砝码
右
42.6
胶头滴管伸入量筒内
仰视读数
50 mL
不合理
长颈漏斗下
端没有液封,用手捂住锥形瓶,受热后气体膨胀,气体会沿长颈漏斗逸出,导致看不到导管口
有气泡
试管口应略向下倾斜
应用酒精灯外焰加热
实践活动一 水质检测及自制净水器
活动一 知道水质检测的部分内容,了解生活用水标准
1.新版《生活饮用水卫生标准》(简称新国标)中水质检测指标从原来的35项增加到106项。对供水各环节的水质提出了更高的要求。
(1)新国标在无机物指标中修订了镉、铅等的限量。这里的镉、铅指的是 (填字母)。
A.原子 B.分子
C.元素 D.单质
(2)新国标中消毒剂由1项增至4项,加入了对用臭氧(O3)、二氧化氯(ClO2)和氯胺(NH2Cl)消毒的规定。
①臭氧在消毒过程中转化为氧气。臭氧转化为氧气属于 (填“物理”或“化学”)变化。
②臭氧、二氧化氯和氯胺三种物质中属于含氧化合物的是 。
C
化学
二氧化氯(或ClO2)
(3)以下是某市水环境监测中心2023年5月发布的本市境内××河三个不同河段水资源质量状况中的一部分内容:
①主要污染指标表述的文字中,涉及的元素有 (写出两种元素符号即可)等。
②请你举出一种防治水体污染的措施: 。
N、P
河段编号 水质类别 主要污染指标 质量状况
甲 Ⅱ — 良好
乙 Ⅳ 汞 一般
丙 劣Ⅴ 磷、氨、氮等 较差
废水处理达标后排放
活动二 掌握常用的净水方法及其原理和作用
2.天然水的人工净化流程如图甲所示:
沉降
吸附
甲
乙
(1)请选用下列“关键词”填写上述流程方框内空白处。
沉降 蒸发 吸附
(2)过滤可除去 杂质。
(3)在过滤操作中,要注意“一贴、二低、三靠”,“二低”指的是 、
。
(4)某同学采用如图乙所示装置进行过滤。图中还缺少的一种仪器是 ,其作用是
;装置组装存在的一处错误是 ;操作中,他发现过滤速率太慢,可能的原因是 _
(合理即可)。
难溶性
滤纸边缘低于漏斗边缘
液面低于滤纸边缘
玻璃棒
引流
漏斗下端未靠在烧杯内壁上
难溶性杂质将滤纸空隙堵塞(或滤纸与漏斗内壁贴得不紧有气泡等)
活动三 制作简易净水器
3.(2022佳木斯期中)如图是某同学制作的简易净水器,请回答下列有关问题:
(1)小卵石、石英砂和蓬松棉的作用是 ,活性炭的作用是 。
(2)净化后得到的水是硬水还是软水 你认为可以用 检验。
(3)长期饮用硬水对健康不利,要降低水的硬度,生活中可采取 的方法。
(4)给自来水消毒常用的物质是 (合理即可)。
过滤 ,除去水中的部分不溶性杂质
吸附水中的色素和异味
肥皂水
煮沸
氯气
实践活动二 制作模型并展示科学家探索物质组成与结构的历程
活动一 认识物质的构成,初步认识分子、原子、离子
1.探秘物质的构成
科学理论的建立与发展是一代代科学家不懈努力的结果。人们对物质构成的认识,经历了漫长的探索过程。
(1)原子的构成:汤姆森、卢瑟福等科学家都是根据实验证据进行推理,再用原子模型来表征原子的内部结构。
①汤姆森之前,科学家对原子的认识是 。1897年,汤姆森在实验中发现所有原子都能释放出一种带负电的粒子,这种粒子就是 。如果你在当时的实验现场,根据这一实验结果,你推理获得的结论是 _
。
②卢瑟福等科学家在汤姆森研究的基础上,根据α粒子轰击金箔实验结论,提出了原子的
模型。
③在化学变化中,构成原子的 不变, 可变。
原子是构成物质的最小粒子,不可再分
电子
原子可分,原子内部存在带
正电荷的粒子
核式
原子核(或质子和中子)
核外电子(或电子)
(2)分子的构成:十九世纪初,科学家们提出早期的分子学说,部分观点如下:
观点1:一切物质都由分子构成,分子由原子构成。
观点2:单质分子由相同种类原子构成,化合物分子由不同种类原子构成。
观点3:分子不能用物理方法分割,化学方法可使它解离。
观点4:分子质量等于组成它的原子质量总和。
根据以上材料回答问题:
①按现代分子理论,观点1是否正确 。
②从元素角度谈谈你对观点2的认识: 。
③根据观点3,从微观角度分析“氢气和氧气反应生成水”,反应中发生改变的粒子是
(用符号表示,下同),不变的粒子是 。
④原子、分子质量很小,为计算和使用方便引入相对原子质量,结合观点4判断下列说法正确的是 (填字母序号)。
A.相对原子质量是采用以小比小使数值变大的计量原理
B.相对原子质量是一个原子的质量与一个碳12原子质量的1/12的比值
C.1个分子质量一定大于1个原子质量
不正确
单质由同种元素组成,化合物由不同种元素组成
H2、O2
H、O
AB
(3)离子的构成:2019年度诺贝尔化学奖授予在可充电锂离子电池研究领域做出突出贡献的三位科学家。
①锂(Li)的原子结构示意图如图甲所示,锂在化学反应中易 电子,形成 (填离子符号)。
②某种可充电锂离子电池以钴酸锂( LiCoO2)为正极,以碳素材料为负极。钴酸锂属于
(填“单质” 或“化合物”)。
失
Li+
化合物
甲 锂原子结构示意图 乙 原子结构示意图
(4)万物皆原子,原子是构成一切化学物质的基本单元。图乙是氢、氖、钠和氯的原子结构示意图。请你以氖气、氯化氢和氯化钠三种物质为例,从原子直接或间接构成物质的角度,简要谈谈你对“原子是构成一切化学物质的基本单元”的理解: _
_
_
。
能直接构成物质的粒子有分子、原子、离子。氖原子可以直接构成氖气;氢原子和氯原子(通过共用电子对)先构成氯化氢分子,再间接构成氯化氢这种物质;氯原子和钠原子(通过得失电子)先变成氯离子和钠离子,再间接构成氯化钠这种物质
活动二 构成物质的粒子及化学反应的微观模型
2.认识水分子的变化
小明设计了图甲、图乙两个实验。请回答下列有关问题:
(1)从微观上看,构成水的微观粒子的模型是 (填字母)。
C
甲
乙
(2)从微观的角度分析,图甲实验中发生的变化是 ;图乙实验中发生的变化是 。
(3)图乙实验中,一段时间后试管b中得到的物质是 (填化学符号),检验该物质的方法是 。
(4)请试着画出电解水的微观示意图:
,此变化中改变的粒子是 ,不变的粒子是
,由此可知,分子和原子的根本区别是 ,保持水的化学性质的粒子是 。
水分子的间隔和排列方式
水分子中氢、氧原子在通电的情况下,重新结合生成氢分子和氧分子
O2
将带火星的木条靠近气体,若木条复燃,则气体为氧气
水分子
氢原子、氧原子
化学变化中,分子改变,原子不变
水分子
到实验室去:化学实验基本技能训练(二)
学会简单仪器的使用及连接等实验基本操作。
[实验目的]
1.初步学会使用托盘天平(或电子秤)、量筒等仪器。
2.学会物质的称量、仪器的连接、装置气密性的检验和仪器的洗涤等实验技能。
[实验用品]
1.仪器:托盘天平(或电子秤)、量筒、试管、烧杯、试管刷等。
2.药品:食盐、蒸馏水等。
[实验过程]
实验一 物质的称量
1.固体药品的称量(用托盘天平称量)
称量原理:当天平达到平衡时,左盘上的质量=右盘上的质量+游码质量。
称量时:应先 ,称量时称量物放在 盘,砝码放在 盘,有时需拨动 。
为了不使托盘天平受到污染和损坏,应在两个托盘上各放 ,易潮解或有腐蚀性的药品要放在 或表面皿等玻璃器皿中称量,如氢氧化钠。
调节托盘天平平衡
左
右
游码
一张相同质量的纸片
烧杯
2.液体药品的量取
量取时,先向量筒里倾倒液体至接近所需刻度,然后将量筒平放在桌面上,再用 滴加液体至该刻度。
量筒
凹液面最低
胶头滴管
量筒不能加热,不能用作反应容器。
实验二 仪器的连接与洗涤
1.连接方法
玻璃管、橡皮塞、胶皮管的连接:
(1)将玻璃管插入胶皮管时,关键掌握两个字——润、转,即玻璃管一端用水 ,插入过程中应稍稍 插入(如下图左)。
(2)用橡皮塞塞住试管时,一手持试管,一手持橡皮塞,稍稍用力转动塞入(如下图右)。
润湿
用力转动
在玻璃管上套上胶皮管 用橡皮塞塞住试管
2.检查装置气密性
具体方法是把导管的一端 ,用手握住试管,若导管口 ,证明装置连接完好、不漏气(如图)。
3.仪器的洗涤
洗涤方法:实验结束后,将废液倒入 中。清洗试管时,先向试管内倒入约一半的清水,然后将试管刷 或 进行刷洗。洗涤后的废液也要倒入 中。
玻璃仪器洗涤干净的标准:水在仪器内壁既不 ,也不 。
浸入水中
有气泡冒出
废液缸
轻轻转动
上下移动
废液缸
聚成水滴
成股流下
[拓展探究]
1.用托盘天平称量物质时,若物质和砝码的位置放反了,读取物质的质量的数值比实际值偏大还是偏小(称量过程中使用游码)
答案:偏大。因为读数时,称得的质量是m砝码+m游码,但物质、砝码放反了,物质实际的质量是
m砝码-m游码,所以读取物质的质量的数值比实际值偏大。
2.读量筒内液体的体积时,若仰视读数或俯视读数,对实验结果会产生什么样的影响
答案:
可简单记忆为“俯大仰小”。
[实战演练]
1.某同学测定的下列数据不合理的是( )
A.用温度计测得某液体的温度为23 ℃
B.用50 mL量筒量取了4.34 mL的水
C.用托盘天平称得某烧杯的质量为46.8 g
D.用10 mL的量筒量取了5.0 mL的水
2.(2022柳州)规范操作是化学实验成功的基础。下列实验操作正确的是( )
(已知:氢氧化钠有腐蚀性)
B
D
A.过滤 B.称量氢氧化钠固体 C.点燃酒精灯 D.读取液体体积
3.(2023兴化月考)某学生在实验室练习用量筒量取液体,量筒放平稳且面对刻度,先是仰视液面读数为40 mL,倒出部分液体后,又俯视液面,读数为30 mL,则该学生实际倒出液体的体积为( )
A.大于10 mL B.小于10 mL
C.等于10 mL D.无法判断
4.化学实验必须严格按规定操作,否则可能导致实验失败或人身伤害。请填写下列错误的操作或错误操作可能造成的不良后果。
A
错误的操作 可能造成的不良后果
(1)给试管里的液体加热时,试管靠近灯芯
(2) 量取5 mL液体,实际5.4 mL
(3)向燃着的酒精灯内添加酒精
(4)砝码与药品位置颠倒了 称取6.8 g固体,实际只有 g(1 g以下用游码)
试管底部炸裂
仰视读数量取5 mL液体
引起火灾
5.2
5.根据下列实验示意图回答相关问题:
甲 称量金属块的质量 乙 量取液体体积
丙 检查装置气密性 丁 加热固体
(1)图甲中除了砝码和金属块位置放反了,还有一处明显的错误是 ;称量前需要调节天平平衡,游码归零,如发现横梁指针向左偏,此时应将平衡螺母向 (填“左”或“右”)调;若左盘中的砝码及游码指示位置如图所示,则金属块的质量为 g。
(2)指出图乙中两处错误:① ;② 。如量取42 mL 水,应选择 (填“50 mL”或“100 mL”)量筒。
(3)小亮同学用图丙所示方法检查该装置气密性,他没有看到导管口有气泡冒出,因此判断该装置漏气,你认为他的判断 (填“合理”或“不合理”),说明理由: _
_
。
(4)改正图丁中两处错误:① ;② 。
用手拿砝码
右
42.6
胶头滴管伸入量筒内
仰视读数
50 mL
不合理
长颈漏斗下
端没有液封,用手捂住锥形瓶,受热后气体膨胀,气体会沿长颈漏斗逸出,导致看不到导管口
有气泡
试管口应略向下倾斜
应用酒精灯外焰加热
实践活动一 水质检测及自制净水器
活动一 知道水质检测的部分内容,了解生活用水标准
1.新版《生活饮用水卫生标准》(简称新国标)中水质检测指标从原来的35项增加到106项。对供水各环节的水质提出了更高的要求。
(1)新国标在无机物指标中修订了镉、铅等的限量。这里的镉、铅指的是 (填字母)。
A.原子 B.分子
C.元素 D.单质
(2)新国标中消毒剂由1项增至4项,加入了对用臭氧(O3)、二氧化氯(ClO2)和氯胺(NH2Cl)消毒的规定。
①臭氧在消毒过程中转化为氧气。臭氧转化为氧气属于 (填“物理”或“化学”)变化。
②臭氧、二氧化氯和氯胺三种物质中属于含氧化合物的是 。
C
化学
二氧化氯(或ClO2)
(3)以下是某市水环境监测中心2023年5月发布的本市境内××河三个不同河段水资源质量状况中的一部分内容:
①主要污染指标表述的文字中,涉及的元素有 (写出两种元素符号即可)等。
②请你举出一种防治水体污染的措施: 。
N、P
河段编号 水质类别 主要污染指标 质量状况
甲 Ⅱ — 良好
乙 Ⅳ 汞 一般
丙 劣Ⅴ 磷、氨、氮等 较差
废水处理达标后排放
活动二 掌握常用的净水方法及其原理和作用
2.天然水的人工净化流程如图甲所示:
沉降
吸附
甲
乙
(1)请选用下列“关键词”填写上述流程方框内空白处。
沉降 蒸发 吸附
(2)过滤可除去 杂质。
(3)在过滤操作中,要注意“一贴、二低、三靠”,“二低”指的是 、
。
(4)某同学采用如图乙所示装置进行过滤。图中还缺少的一种仪器是 ,其作用是
;装置组装存在的一处错误是 ;操作中,他发现过滤速率太慢,可能的原因是 _
(合理即可)。
难溶性
滤纸边缘低于漏斗边缘
液面低于滤纸边缘
玻璃棒
引流
漏斗下端未靠在烧杯内壁上
难溶性杂质将滤纸空隙堵塞(或滤纸与漏斗内壁贴得不紧有气泡等)
活动三 制作简易净水器
3.(2022佳木斯期中)如图是某同学制作的简易净水器,请回答下列有关问题:
(1)小卵石、石英砂和蓬松棉的作用是 ,活性炭的作用是 。
(2)净化后得到的水是硬水还是软水 你认为可以用 检验。
(3)长期饮用硬水对健康不利,要降低水的硬度,生活中可采取 的方法。
(4)给自来水消毒常用的物质是 (合理即可)。
过滤 ,除去水中的部分不溶性杂质
吸附水中的色素和异味
肥皂水
煮沸
氯气
实践活动二 制作模型并展示科学家探索物质组成与结构的历程
活动一 认识物质的构成,初步认识分子、原子、离子
1.探秘物质的构成
科学理论的建立与发展是一代代科学家不懈努力的结果。人们对物质构成的认识,经历了漫长的探索过程。
(1)原子的构成:汤姆森、卢瑟福等科学家都是根据实验证据进行推理,再用原子模型来表征原子的内部结构。
①汤姆森之前,科学家对原子的认识是 。1897年,汤姆森在实验中发现所有原子都能释放出一种带负电的粒子,这种粒子就是 。如果你在当时的实验现场,根据这一实验结果,你推理获得的结论是 _
。
②卢瑟福等科学家在汤姆森研究的基础上,根据α粒子轰击金箔实验结论,提出了原子的
模型。
③在化学变化中,构成原子的 不变, 可变。
原子是构成物质的最小粒子,不可再分
电子
原子可分,原子内部存在带
正电荷的粒子
核式
原子核(或质子和中子)
核外电子(或电子)
(2)分子的构成:十九世纪初,科学家们提出早期的分子学说,部分观点如下:
观点1:一切物质都由分子构成,分子由原子构成。
观点2:单质分子由相同种类原子构成,化合物分子由不同种类原子构成。
观点3:分子不能用物理方法分割,化学方法可使它解离。
观点4:分子质量等于组成它的原子质量总和。
根据以上材料回答问题:
①按现代分子理论,观点1是否正确 。
②从元素角度谈谈你对观点2的认识: 。
③根据观点3,从微观角度分析“氢气和氧气反应生成水”,反应中发生改变的粒子是
(用符号表示,下同),不变的粒子是 。
④原子、分子质量很小,为计算和使用方便引入相对原子质量,结合观点4判断下列说法正确的是 (填字母序号)。
A.相对原子质量是采用以小比小使数值变大的计量原理
B.相对原子质量是一个原子的质量与一个碳12原子质量的1/12的比值
C.1个分子质量一定大于1个原子质量
不正确
单质由同种元素组成,化合物由不同种元素组成
H2、O2
H、O
AB
(3)离子的构成:2019年度诺贝尔化学奖授予在可充电锂离子电池研究领域做出突出贡献的三位科学家。
①锂(Li)的原子结构示意图如图甲所示,锂在化学反应中易 电子,形成 (填离子符号)。
②某种可充电锂离子电池以钴酸锂( LiCoO2)为正极,以碳素材料为负极。钴酸锂属于
(填“单质” 或“化合物”)。
失
Li+
化合物
甲 锂原子结构示意图 乙 原子结构示意图
(4)万物皆原子,原子是构成一切化学物质的基本单元。图乙是氢、氖、钠和氯的原子结构示意图。请你以氖气、氯化氢和氯化钠三种物质为例,从原子直接或间接构成物质的角度,简要谈谈你对“原子是构成一切化学物质的基本单元”的理解: _
_
_
。
能直接构成物质的粒子有分子、原子、离子。氖原子可以直接构成氖气;氢原子和氯原子(通过共用电子对)先构成氯化氢分子,再间接构成氯化氢这种物质;氯原子和钠原子(通过得失电子)先变成氯离子和钠离子,再间接构成氯化钠这种物质
活动二 构成物质的粒子及化学反应的微观模型
2.认识水分子的变化
小明设计了图甲、图乙两个实验。请回答下列有关问题:
(1)从微观上看,构成水的微观粒子的模型是 (填字母)。
C
甲
乙
(2)从微观的角度分析,图甲实验中发生的变化是 ;图乙实验中发生的变化是 。
(3)图乙实验中,一段时间后试管b中得到的物质是 (填化学符号),检验该物质的方法是 。
(4)请试着画出电解水的微观示意图:
,此变化中改变的粒子是 ,不变的粒子是
,由此可知,分子和原子的根本区别是 ,保持水的化学性质的粒子是 。
水分子的间隔和排列方式
水分子中氢、氧原子在通电的情况下,重新结合生成氢分子和氧分子
O2
将带火星的木条靠近气体,若木条复燃,则气体为氧气
水分子
氢原子、氧原子
化学变化中,分子改变,原子不变
水分子
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
