化学人教版(2019)必修第一册4.1原子结构 元素周期表(共31张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册4.1原子结构 元素周期表(共31张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-21 00:00:00 | ||
图片预览





文档简介
(共31张PPT)
人教版必修第一册
学
第一课时 原子结构、元素周期表
第四章 物质结构 元素周期律
人教版必修第一册
学
第一部分 原子的核外电子排布
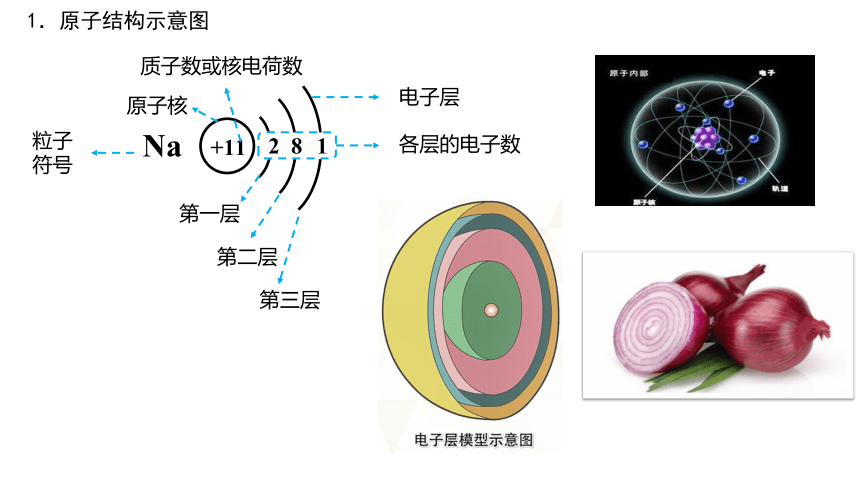
1.原子结构示意图
+11
2 8 1
原子核
质子数或核电荷数
第三层
各层的电子数
Na
粒子符号
电子层
第二层
第一层
原子核
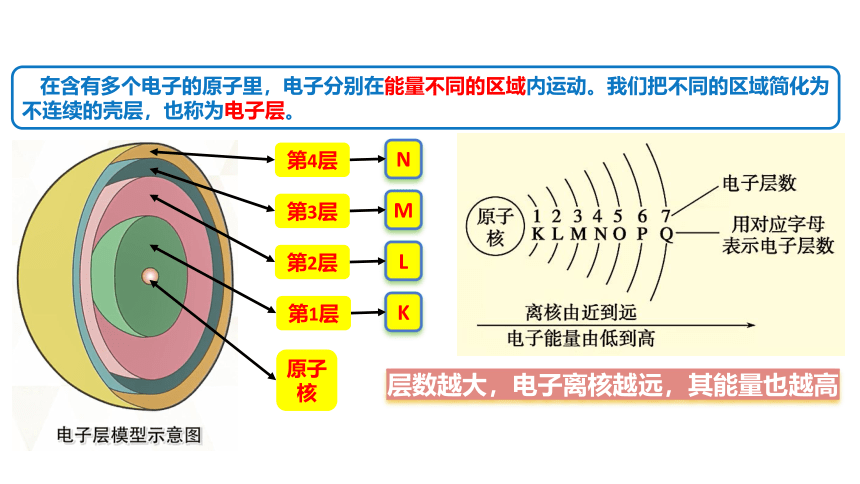
第1层
第2层
第3层
第4层
N
M
L
K
在含有多个电子的原子里,电子分别在能量不同的区域内运动。我们把不同的区域简化为不连续的壳层,也称为电子层。
层数越大,电子离核越远,其能量也越高
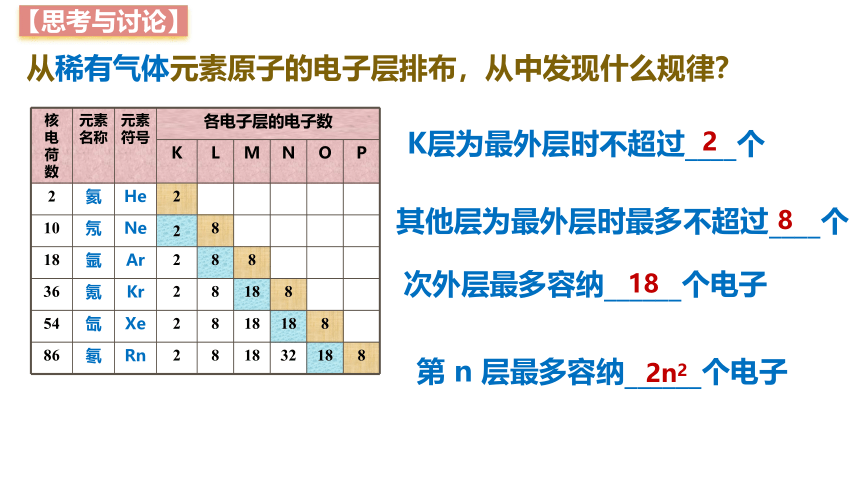
【思考与讨论】
核电荷数 元素名称 元素符号 各电子层的电子数 K L M N O P
2 氦 He 2
10 氖 Ne 2 8
18 氩 Ar 2 8 8
36 氪 Kr 2 8 18 8
54 氙 Xe 2 8 18 18 8
86 氡 Rn 2 8 18 32 18 8
从稀有气体元素原子的电子层排布,从中发现什么规律?
K层为最外层时不超过____个
2
其他层为最外层时最多不超过____个
8
次外层最多容纳______个电子
18
第 n 层最多容纳______个电子
2n2
1)各电子层最多容纳_______个电子
2)最外层电子数不超过_____个
(K层为最外层时不超过______个)
3)次外层(倒数第二层)电子数不超过_____个
K层为次外层时不超过__个,L层为次外层时不超过_ 个)
4)倒数第三层电子数不超过______个
2n2
8
2
18
2
8
32
【总结】
电子总是尽可能先从_____排起,当一层_____后再填充下一层,即按K→L→M……顺序排列。
内层
充满
以上几条规律相互联系和制约,
如K原子为
而不能写成
因为尽管第三层最多可排2×9=18个,但作为最外层不能超过8个。
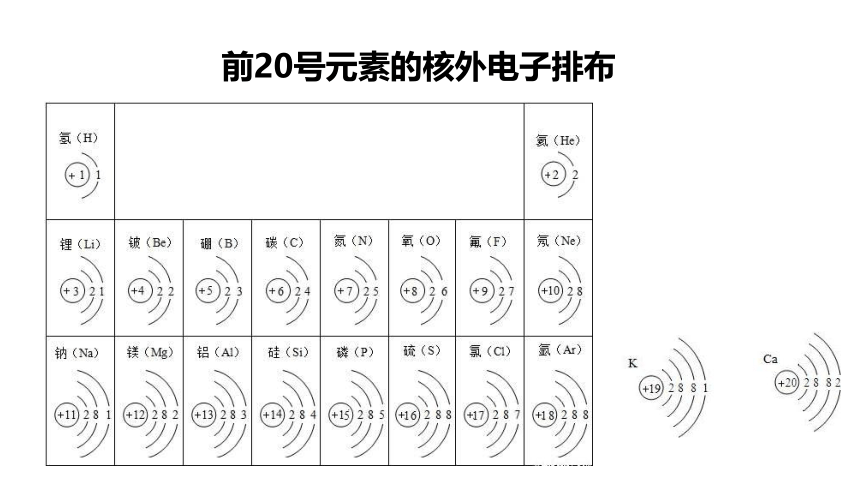
前20号元素的核外电子排布
人教版必修第一册
学
第二部分 元素周期表的结构
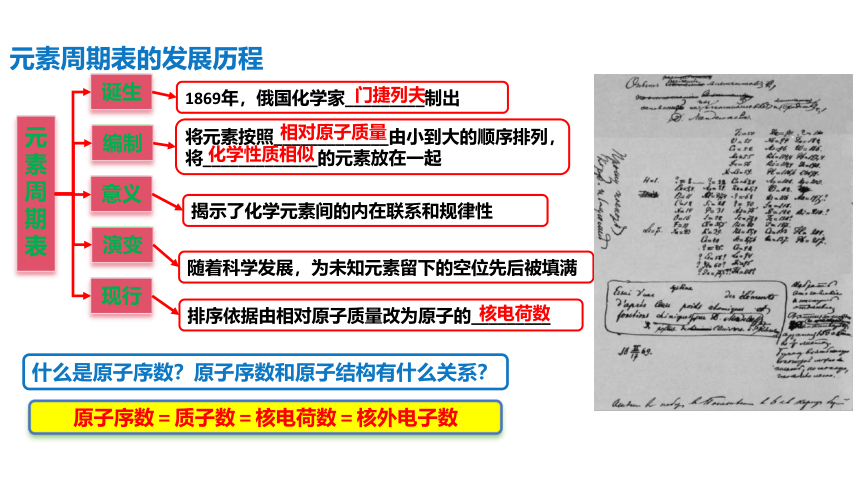
元素周期表的发展历程
元素周期表
诞生
编制
意义
揭示了化学元素间的内在联系和规律性
演变
现行
随着科学发展,为未知元素留下的空位先后被填满
1869年,俄国化学家_________制出
门捷列夫
将元素按照_____________由小到大的顺序排列,将_____________的元素放在一起
相对原子质量
化学性质相似
排序依据由相对原子质量改为原子的_________
核电荷数
原子序数=质子数=核电荷数=核外电子数
什么是原子序数?原子序数和原子结构有什么关系?
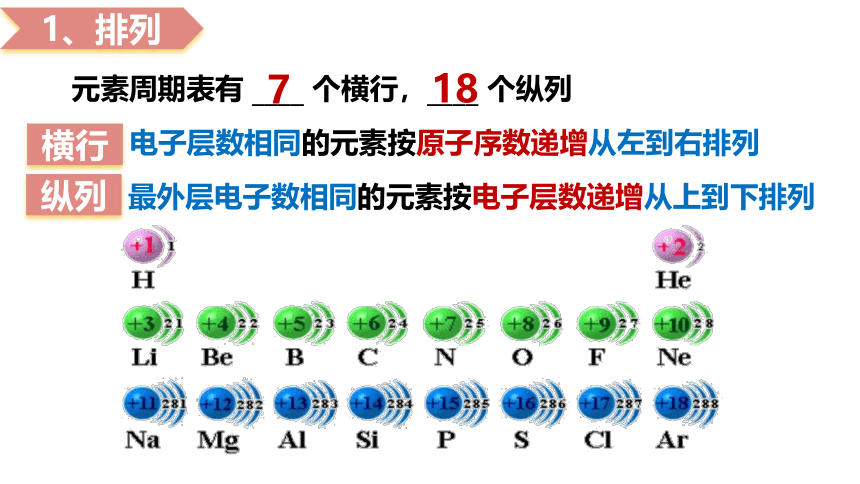
1、排列
电子层数相同的元素按原子序数递增从左到右排列
最外层电子数相同的元素按电子层数递增从上到下排列
纵列
横行
元素周期表有 ____ 个横行,____ 个纵列
7
18
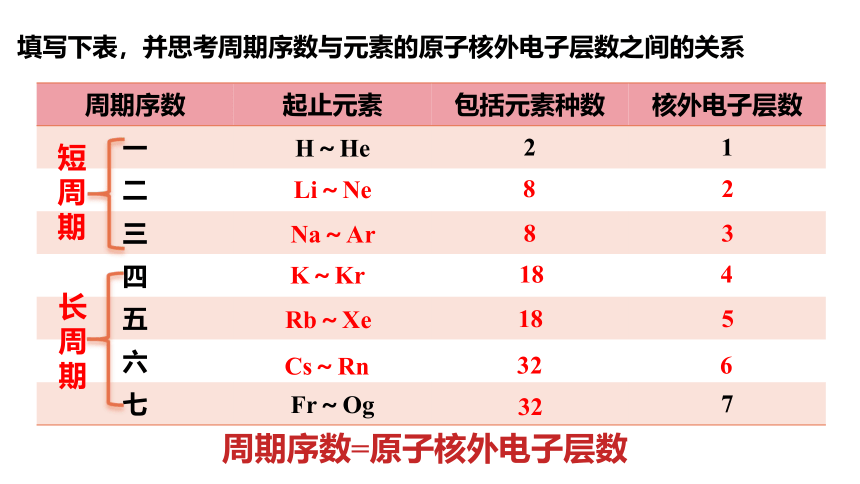
填写下表,并思考周期序数与元素的原子核外电子层数之间的关系
周期序数 起止元素 包括元素种数 核外电子层数
一 H~He 2 1
二
三
四
五
六
七 Fr~Og 7
Li~Ne
8
2
Na~Ar
8
3
K~Kr
18
4
Rb~Xe
18
5
Cs~Rn
32
6
32
周期序数=原子核外电子层数
短周期
长周期
2、周期
每一个横行叫做一个周期,共____个周期。
思考与讨论
1. 周期序数与原子核外电子层数有什么关系?
周期序数 = 电子层数
7
第一周期
第二周期
第三周期
每一个周期含多少种元素?
【思考与讨论】
元素种数
2
8
8
18
18
32
32
短周期:1-3周期
长周期:4-7周期
2、周期
七个周期,三短四长
7个周期
一二三四五六七
2种元素
8种元素
8种元素
18种元素
18种元素
32种元素
32种元素
短周期
长周期
2
稀有气体元素
原子序数
10
18
36
54
86
118
元素种类
周期数
1~3 周期
4~7 周期
3 、 族
每一个纵列叫做一个族;共____个纵列,____个族。
18
16
思考与讨论
每个纵列中的 A、B、0、Ⅷ 的含义?一共有多少个族?
85
84
83
82
81
53
52
51
50
49
35
34
33
32
31
17
16
15
14
13
9
8
7
6
5
88
87
56
55
38
37
20
19
12
11
4
3
1
A主族:7个
112
111
107
106
105
104
89-103
80
79
75
74
73
72
57-71
48
47
43
42
41
40
39
30
29
25
24
23
22
21
B副族:7个
110
109
108
78
77
76
46
45
44
28
27
26
VIII族
86
54
36
18
10
2
0族
稀有气体元素
七主、七副、0 和 八三
3 、 族
第ⅠA 族(除H外):
碱金属元素
第 ⅦA 族:
卤族元素
过渡元素
(均为金属元素)
3 、 族
主族序数 = 最外层电子数
+11
2
8
1
+1
1
+19
2
8
8
1
+3
2
1
Li
Na
K
H
第ⅠA族
+12
2
8
2
+20
2
8
8
2
+4
2
2
第 ⅡA 族
+13
2
8
3
+31
2
8
18
3
+5
2
3
第 ⅢA 族
元素的信息
铁
※3d64s2
55.85
元素符号
元素名称
相对原子质量
26 Fe
原子序数
原子序数=核电荷数=质子数=核外电子数
元素周期表中的元素信息
【归纳总结】
三短、四长、七周期;18纵列、16族;
七主、七副、0 和 Ⅷ;8、9、10列为Ⅷ族;
每逢二三分主副;镧系锕系都在ⅢB住。
元素周期表结构记忆口诀
(1)电子层数与最外层电子数相等的元素有___________;
(2)最外层电子数是电子层数2倍的元素有___________;
(3)最外层电子数是电子层数3倍的元素有___________;
【练习1】
1-20号元素中:
H、
Be、
Al
He、
C、
S
O
(4)最外层电子数与次外层电子数相等的元素有________;
(5)最外层电子数是次外层电子数2倍的元素是_________;
(6)最外层电子数是次外层电子数3倍的元素是_________;
(7)次外层电子数是最外层电子数2倍的元素有_________;
(8)内层电子总数是最外层电子数2倍的元素有_________;
【练习2】
Be、
1-20号元素中:
Ar
C
O
Li、
Si
Li、
P
[解析] 设A原子L、M层电子数分别为x、y,依题意,A、B两原子的电子层结构见表。
B原子的M层至少有3个电子,
因而其L层的电子数必然是8,求得x=4。
对A原子来说,L层有4个电子时只能是最外层,即y=0,y+3=3。
因此,这两个原子分别为碳原子和铝原子,故D项正确。
今有A、B两种原子,A原子的M层比B原子的M层少3个电子,B原子的L层电子数恰为A原子L层电子数的2倍,A和B分别是( )
A.硅原子和钠原子 B.硼原子和氢原子 C.氯原子和碳原子 D.碳原子和铝原子
电子层 K L M
A原子 2 x y
B原子 2 2x y+3
D
练习5:有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且均小于20,其中只有X、Z是金属元素,V和Z元素原子的最外层都只有一个电子,W和Y元素原子的最外层电子数相等,且W元素原子L层电子数是K层电子数的3倍,X元素原子的最外层电子数是Y元素原子最外层电子数的一半。由此可推知。 V:____ 、W: ____ 、X: ____、 Y: ____、 Z: ____。(填元素符号)
课堂练习
H
O
Al
S
K
练习4:已知A、B、C三种元素的原子中,质子数:AA:_______ 、 B:_______ 、 C:_______ 。
碳 C
硅 Si
氯 Cl
人教版必修第一册
学
第四部分 确定主族元素在元素周期表中的位置
2.确定周期数
因为116大于86小于118, 知该元素位于第 周期。
推算原子序数为116的元素在元素周期表中的位置。
86
118
步骤:
1.查找第六周期、第七周期0族元素的原子序数分别为
3.确定族序数
因为118-116=2,由0族向左推2个纵行,
知该元素位于第 族。
VIA
七
0族定位法
第五周期 ⅦA族
[习题]已知某主族元素的原子结构示意图如下,判断其位于第几周期,第几族?
思考:Cl的位置的描述:
第三周期第VIIA族
第四周期 ⅠA族
(2021·上海市控江中学高二期中)81号元素所在周期和族是( )
A.第六周期ⅣA族
B.第六周期ⅢB族
C.第七周期0族
D.第六周期ⅢA族
D
(2020·上海交大附中高二期中)下列各表是元素周期表中的一部分,表中数字表示的是原子序号与其在周期表中的位置相符合的是
D
心情不好~~~
作业好多~~~
人教版必修第一册
学
第一课时 原子结构、元素周期表
第四章 物质结构 元素周期律
人教版必修第一册
学
第一部分 原子的核外电子排布
1.原子结构示意图
+11
2 8 1
原子核
质子数或核电荷数
第三层
各层的电子数
Na
粒子符号
电子层
第二层
第一层
原子核
第1层
第2层
第3层
第4层
N
M
L
K
在含有多个电子的原子里,电子分别在能量不同的区域内运动。我们把不同的区域简化为不连续的壳层,也称为电子层。
层数越大,电子离核越远,其能量也越高
【思考与讨论】
核电荷数 元素名称 元素符号 各电子层的电子数 K L M N O P
2 氦 He 2
10 氖 Ne 2 8
18 氩 Ar 2 8 8
36 氪 Kr 2 8 18 8
54 氙 Xe 2 8 18 18 8
86 氡 Rn 2 8 18 32 18 8
从稀有气体元素原子的电子层排布,从中发现什么规律?
K层为最外层时不超过____个
2
其他层为最外层时最多不超过____个
8
次外层最多容纳______个电子
18
第 n 层最多容纳______个电子
2n2
1)各电子层最多容纳_______个电子
2)最外层电子数不超过_____个
(K层为最外层时不超过______个)
3)次外层(倒数第二层)电子数不超过_____个
K层为次外层时不超过__个,L层为次外层时不超过_ 个)
4)倒数第三层电子数不超过______个
2n2
8
2
18
2
8
32
【总结】
电子总是尽可能先从_____排起,当一层_____后再填充下一层,即按K→L→M……顺序排列。
内层
充满
以上几条规律相互联系和制约,
如K原子为
而不能写成
因为尽管第三层最多可排2×9=18个,但作为最外层不能超过8个。
前20号元素的核外电子排布
人教版必修第一册
学
第二部分 元素周期表的结构
元素周期表的发展历程
元素周期表
诞生
编制
意义
揭示了化学元素间的内在联系和规律性
演变
现行
随着科学发展,为未知元素留下的空位先后被填满
1869年,俄国化学家_________制出
门捷列夫
将元素按照_____________由小到大的顺序排列,将_____________的元素放在一起
相对原子质量
化学性质相似
排序依据由相对原子质量改为原子的_________
核电荷数
原子序数=质子数=核电荷数=核外电子数
什么是原子序数?原子序数和原子结构有什么关系?
1、排列
电子层数相同的元素按原子序数递增从左到右排列
最外层电子数相同的元素按电子层数递增从上到下排列
纵列
横行
元素周期表有 ____ 个横行,____ 个纵列
7
18
填写下表,并思考周期序数与元素的原子核外电子层数之间的关系
周期序数 起止元素 包括元素种数 核外电子层数
一 H~He 2 1
二
三
四
五
六
七 Fr~Og 7
Li~Ne
8
2
Na~Ar
8
3
K~Kr
18
4
Rb~Xe
18
5
Cs~Rn
32
6
32
周期序数=原子核外电子层数
短周期
长周期
2、周期
每一个横行叫做一个周期,共____个周期。
思考与讨论
1. 周期序数与原子核外电子层数有什么关系?
周期序数 = 电子层数
7
第一周期
第二周期
第三周期
每一个周期含多少种元素?
【思考与讨论】
元素种数
2
8
8
18
18
32
32
短周期:1-3周期
长周期:4-7周期
2、周期
七个周期,三短四长
7个周期
一二三四五六七
2种元素
8种元素
8种元素
18种元素
18种元素
32种元素
32种元素
短周期
长周期
2
稀有气体元素
原子序数
10
18
36
54
86
118
元素种类
周期数
1~3 周期
4~7 周期
3 、 族
每一个纵列叫做一个族;共____个纵列,____个族。
18
16
思考与讨论
每个纵列中的 A、B、0、Ⅷ 的含义?一共有多少个族?
85
84
83
82
81
53
52
51
50
49
35
34
33
32
31
17
16
15
14
13
9
8
7
6
5
88
87
56
55
38
37
20
19
12
11
4
3
1
A主族:7个
112
111
107
106
105
104
89-103
80
79
75
74
73
72
57-71
48
47
43
42
41
40
39
30
29
25
24
23
22
21
B副族:7个
110
109
108
78
77
76
46
45
44
28
27
26
VIII族
86
54
36
18
10
2
0族
稀有气体元素
七主、七副、0 和 八三
3 、 族
第ⅠA 族(除H外):
碱金属元素
第 ⅦA 族:
卤族元素
过渡元素
(均为金属元素)
3 、 族
主族序数 = 最外层电子数
+11
2
8
1
+1
1
+19
2
8
8
1
+3
2
1
Li
Na
K
H
第ⅠA族
+12
2
8
2
+20
2
8
8
2
+4
2
2
第 ⅡA 族
+13
2
8
3
+31
2
8
18
3
+5
2
3
第 ⅢA 族
元素的信息
铁
※3d64s2
55.85
元素符号
元素名称
相对原子质量
26 Fe
原子序数
原子序数=核电荷数=质子数=核外电子数
元素周期表中的元素信息
【归纳总结】
三短、四长、七周期;18纵列、16族;
七主、七副、0 和 Ⅷ;8、9、10列为Ⅷ族;
每逢二三分主副;镧系锕系都在ⅢB住。
元素周期表结构记忆口诀
(1)电子层数与最外层电子数相等的元素有___________;
(2)最外层电子数是电子层数2倍的元素有___________;
(3)最外层电子数是电子层数3倍的元素有___________;
【练习1】
1-20号元素中:
H、
Be、
Al
He、
C、
S
O
(4)最外层电子数与次外层电子数相等的元素有________;
(5)最外层电子数是次外层电子数2倍的元素是_________;
(6)最外层电子数是次外层电子数3倍的元素是_________;
(7)次外层电子数是最外层电子数2倍的元素有_________;
(8)内层电子总数是最外层电子数2倍的元素有_________;
【练习2】
Be、
1-20号元素中:
Ar
C
O
Li、
Si
Li、
P
[解析] 设A原子L、M层电子数分别为x、y,依题意,A、B两原子的电子层结构见表。
B原子的M层至少有3个电子,
因而其L层的电子数必然是8,求得x=4。
对A原子来说,L层有4个电子时只能是最外层,即y=0,y+3=3。
因此,这两个原子分别为碳原子和铝原子,故D项正确。
今有A、B两种原子,A原子的M层比B原子的M层少3个电子,B原子的L层电子数恰为A原子L层电子数的2倍,A和B分别是( )
A.硅原子和钠原子 B.硼原子和氢原子 C.氯原子和碳原子 D.碳原子和铝原子
电子层 K L M
A原子 2 x y
B原子 2 2x y+3
D
练习5:有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且均小于20,其中只有X、Z是金属元素,V和Z元素原子的最外层都只有一个电子,W和Y元素原子的最外层电子数相等,且W元素原子L层电子数是K层电子数的3倍,X元素原子的最外层电子数是Y元素原子最外层电子数的一半。由此可推知。 V:____ 、W: ____ 、X: ____、 Y: ____、 Z: ____。(填元素符号)
课堂练习
H
O
Al
S
K
练习4:已知A、B、C三种元素的原子中,质子数:A
碳 C
硅 Si
氯 Cl
人教版必修第一册
学
第四部分 确定主族元素在元素周期表中的位置
2.确定周期数
因为116大于86小于118, 知该元素位于第 周期。
推算原子序数为116的元素在元素周期表中的位置。
86
118
步骤:
1.查找第六周期、第七周期0族元素的原子序数分别为
3.确定族序数
因为118-116=2,由0族向左推2个纵行,
知该元素位于第 族。
VIA
七
0族定位法
第五周期 ⅦA族
[习题]已知某主族元素的原子结构示意图如下,判断其位于第几周期,第几族?
思考:Cl的位置的描述:
第三周期第VIIA族
第四周期 ⅠA族
(2021·上海市控江中学高二期中)81号元素所在周期和族是( )
A.第六周期ⅣA族
B.第六周期ⅢB族
C.第七周期0族
D.第六周期ⅢA族
D
(2020·上海交大附中高二期中)下列各表是元素周期表中的一部分,表中数字表示的是原子序号与其在周期表中的位置相符合的是
D
心情不好~~~
作业好多~~~
