2023—2024学年人教版(五四学制)化学九年级全一册第3单元 酸和碱 分层题(含答案)
文档属性
| 名称 | 2023—2024学年人教版(五四学制)化学九年级全一册第3单元 酸和碱 分层题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 314.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-23 00:00:00 | ||
图片预览



文档简介
2023—2024学年人教版(五四学制)化学九年级全一册第3单元 酸和碱 分层题含答案
人教版(五四学制)第3单元 酸和碱
一、选择题。
1、用焊锡进行焊接时,为了清除金属表面的锈,焊接处要滴几滴( )
A. 食盐 B. 盐酸 C. 蒸馏水 D. 烧碱
2、有关中和反应的说法一定正确的是( )
A.反应物均须溶于水 B.有沉淀生成
C.有气体生成 D.有盐生成
3、某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的关系如图,下列说法正确的是( )
A. HCl和MgCl2一定存在
B. NaOH、H2SO4和MgCl2一定不存在
C. HCl和H2SO4一定存在
D. HCl一定存在,NaOH、H2SO4一定不存在,MgCl2可能存在
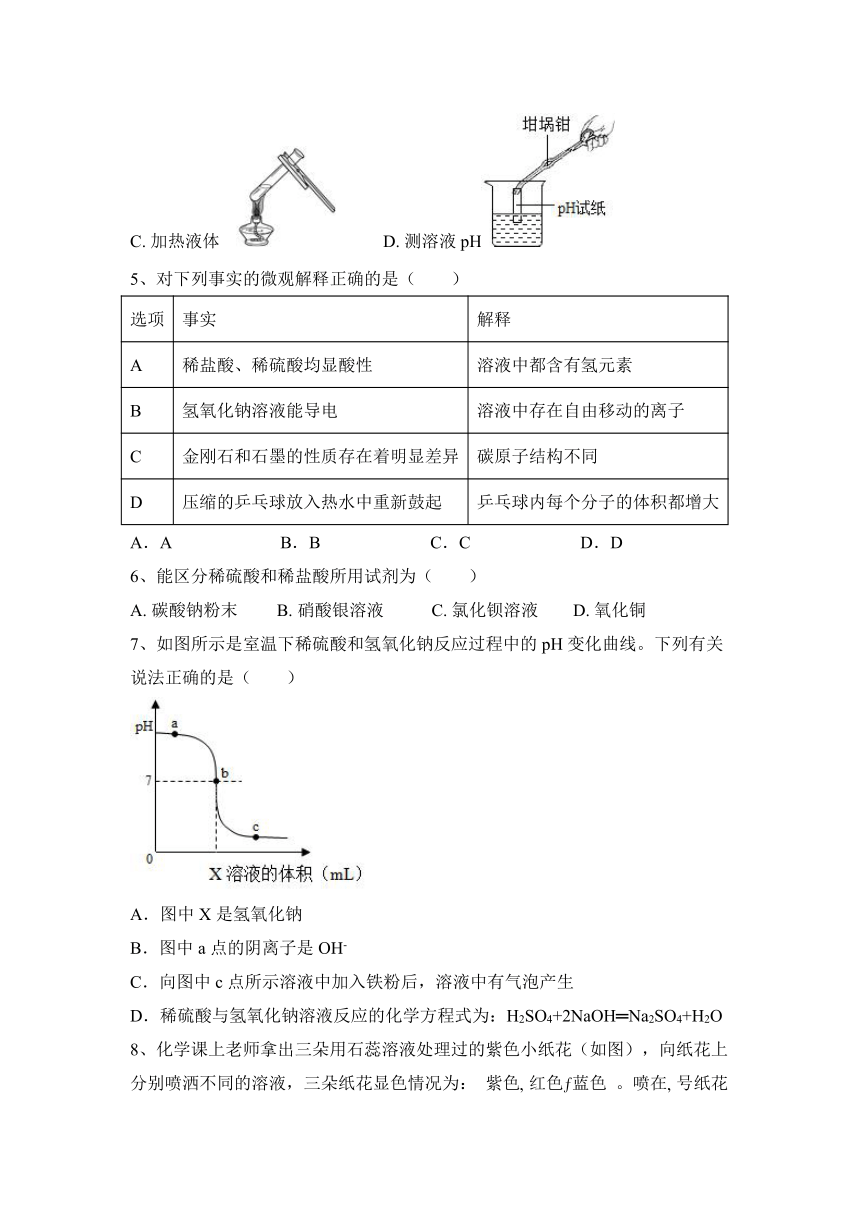
4、下列实验操作中,正确的是( )
A. 闻气味 B. 滴加液体
C. 加热液体 D. 测溶液pH
5、对下列事实的微观解释正确的是( )
选项 事实 解释
A 稀盐酸、稀硫酸均显酸性 溶液中都含有氢元素
B 氢氧化钠溶液能导电 溶液中存在自由移动的离子
C 金刚石和石墨的性质存在着明显差异 碳原子结构不同
D 压缩的乒乓球放入热水中重新鼓起 乒乓球内每个分子的体积都增大
A.A B.B C.C D.D
6、能区分稀硫酸和稀盐酸所用试剂为( )
A. 碳酸钠粉末 B. 硝酸银溶液 C. 氯化钡溶液 D. 氧化铜
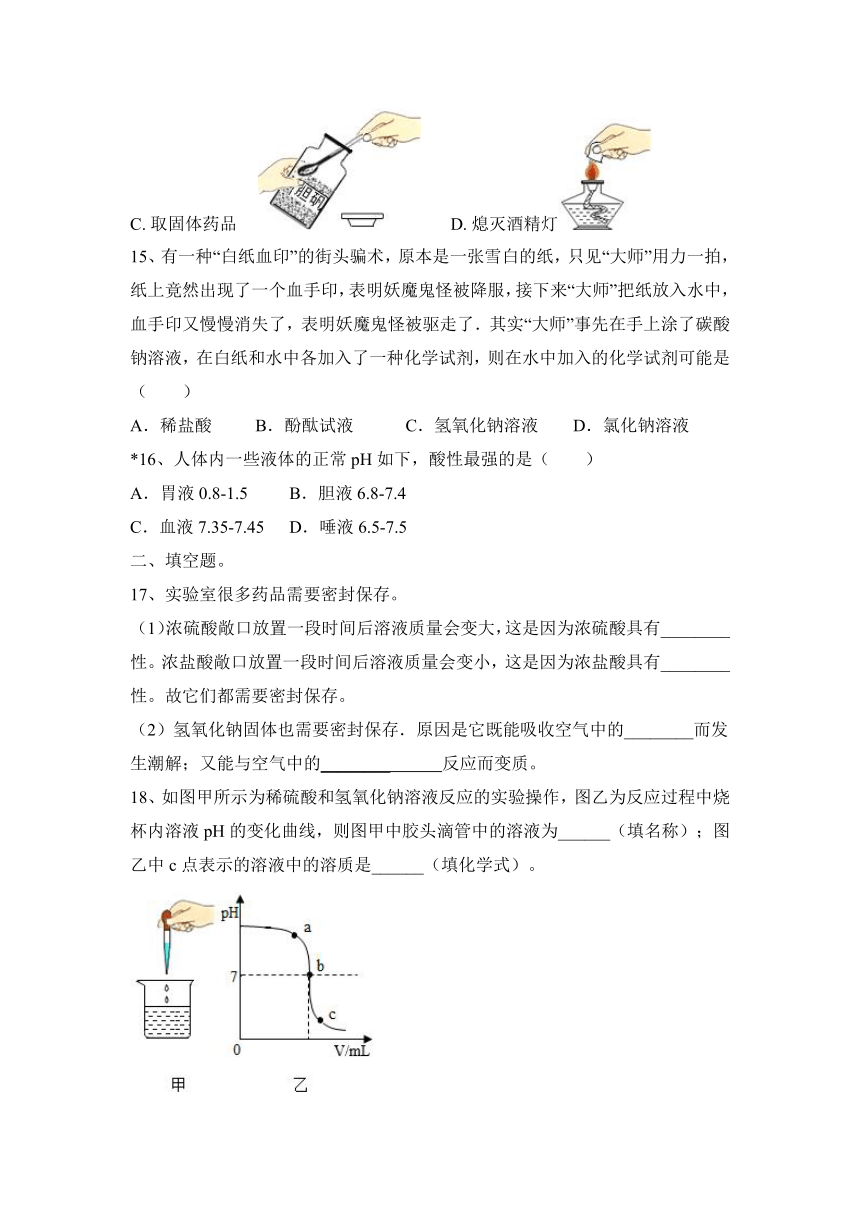
7、如图所示是室温下稀硫酸和氢氧化钠反应过程中的pH变化曲线。下列有关说法正确的是( )
A.图中X是氢氧化钠
B.图中a点的阴离子是OH-
C.向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
D.稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4+2NaOH═Na2SO4+H2O
8、化学课上老师拿出三朵用石蕊溶液处理过的紫色小纸花(如图),向纸花上分别喷洒不同的溶液,三朵纸花显色情况为: 紫色 红色 蓝色 。喷在 号纸花上的溶液可能是( )
A. 氢氧化钠 B. 氯化钠 C. 碳酸钠 D. 稀盐酸
9、人体不同器官的体液会保持相对稳定的酸碱度范围。由下表可知:以下叙述中正确的是( )
体液 血液 唾液 胃液
pH 7.35~7.45 6.6~7.2 0.9~1.5
A. 人的血液一定呈碱性 B. 人的胃液一定能使紫色石蕊试液变成蓝色
C. 人的唾液一定呈酸性 D. 用pH试纸能精确测定以上体液的pH
10、下列物质能使紫色石蕊试液变红的是( )
A.胃液 B.氨水 C.蔗糖水 D.pH约为7.8的鸡蛋清
11、下列物质的溶液能使酚酞试液变红色的是( )
A. B. C. D. 的水溶液
12、下列反应,属于中和反应的是( )
A.Ca(OH)2+CO2=CaCO3↓+H2O B.CuO+2HCl=CuCl2+H2O
C.Cu(OH)2+H2SO4=CuSO4+2H2O D.AgNO3+HCl=AgCl↓+HNO3
13、碱溶液中都含有OH-,因此不同碱变现出一些共同的性质,下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A. 能与盐酸反应生成水 B. 能使紫色石蕊溶液变蓝色
C. 能与Na2SO4溶液反应生成BaSO4沉淀 D. 能与CO2反应生成水
14、下列基本实验操作正确的是( )
A. 检查气密性 B. 测量溶液的pH
C. 取固体药品 D. 熄灭酒精灯
15、有一种“白纸血印”的街头骗术,原本是一张雪白的纸,只见“大师”用力一拍,纸上竟然出现了一个血手印,表明妖魔鬼怪被降服,接下来“大师”把纸放入水中,血手印又慢慢消失了,表明妖魔鬼怪被驱走了.其实“大师”事先在手上涂了碳酸钠溶液,在白纸和水中各加入了一种化学试剂,则在水中加入的化学试剂可能是( )
A.稀盐酸 B.酚酞试液 C.氢氧化钠溶液 D.氯化钠溶液
*16、人体内一些液体的正常pH如下,酸性最强的是( )
A.胃液0.8-1.5 B.胆液6.8-7.4
C.血液7.35-7.45 D.唾液6.5-7.5
二、填空题。
17、实验室很多药品需要密封保存。
(1)浓硫酸敞口放置一段时间后溶液质量会变大,这是因为浓硫酸具有________性。浓盐酸敞口放置一段时间后溶液质量会变小,这是因为浓盐酸具有________性。故它们都需要密封保存。
(2)氢氧化钠固体也需要密封保存.原因是它既能吸收空气中的________而发生潮解;又能与空气中的________ 反应而变质。
18、如图甲所示为稀硫酸和氢氧化钠溶液反应的实验操作,图乙为反应过程中烧杯内溶液pH的变化曲线,则图甲中胶头滴管中的溶液为______(填名称);图乙中c点表示的溶液中的溶质是______(填化学式)。
19、某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示。请分析下表,并回答下列问题:
试剂 稀盐酸 食醋 蔗糖水 蒸馏水 肥皂水 烧碱溶液 石灰水
颜色 红 红 黄 黄 绿 绿 绿
(1)该花汁________(填“可以”或“不可以”)作酸碱指示剂。
(2)蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒.要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的________。
(3)烧碱溶液中含有的阴离子符号为:________。
20、小亮在做“盐酸中和氢氧化钠溶液”实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.请你和他一起探究: 提出猜想:所得溶液可能呈________性。
设计实验验证你的猜想:
实验操作 实验现象 结论
________ 。 ________ 。 ________ 。
21、选择H、C、Cl、S 、O、Ca六种元素中的适当元素,组成符合下列要求的物质,将化学式填在空格中:
(1)相对分子质量最小的氧化物
(2)用于改良酸性土壤的碱
(3)实验室中用来干燥CO2气体的干燥剂
三、实验题。
22、氢氧化钙的性质:
实验步骤 (1)向两支试管中各加入相同量的氢氧化钙粉末(用药匙的柄把一端挑一点),然后各加入水,振荡;再各滴入1~2滴酚酞溶液,观察现象;(2)继续向其中一支试管中加入约水,振荡;(3)向另一支试管加入约稀盐酸,振荡;比较两支试管中的现象
实验现象 (1)______ ;(2)______ ;(3)______ 。
化学方程式 ______ 。
结论:氢氧化钙______溶于水,其水溶液呈______;氢氧化钙粉末______与盐酸发生反应。
23、某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂。此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质的成分进行探究。
(1)写出该中和反应的化学方程式________ 。
(2)探究烧杯内溶液中溶质的成分:
【提出问题】
该烧杯内的溶液中溶质是什么?
【进行猜想】
(A)溶质可能是CaCl2与Ca(OH)2
(B)溶质可能只是CaCl2
(C)溶质可能是CaCl2与盐酸
【实验探究】
①小明从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液。振荡.观察到酚酞试液不变色。于是他排除了猜想(A),你认为他排除猜想(A)的理由是________ 。
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
实验步骤 预计现象 预计结论
取少量反应后的溶液于试管中,
逐滴加入碳酸钠溶液。 ________ 。 猜想(B)正确
________ 。 猜想(C)正确
通过以上探究,最后确定猜想(C)正确。
【反思与拓展】
要想处理烧杯内溶液使其只有CaCl2溶液,最好向溶液中加入过量________, 充分反应后过滤即可。
四、实验探究题。
24、根据下列图示,回答相关问题:
(1)实验一:滴加液体试剂的仪器名称是 ,实验中所测溶液pH的数值将 (选填 “偏大”“偏小”或“不变”)。
(2)实验二:燃着的酒精灯的作用是 ,玻璃管中发生反应的化学方程式 。
(3)实验三:检验所用水是否属于软水,可使用的物质是 ,制好的汽水打开瓶盖后有大量气体逸出,其主要原因是 。
2023—2024学年人教版(五四学制)化学九年级全一册第3单元 酸和碱 分层题含答案
人教版(五四学制)第3单元 酸和碱
一、选择题。
1、用焊锡进行焊接时,为了清除金属表面的锈,焊接处要滴几滴( )
A. 食盐 B. 盐酸 C. 蒸馏水 D. 烧碱
【答案】B
2、有关中和反应的说法一定正确的是( )
A.反应物均须溶于水 B.有沉淀生成
C.有气体生成 D.有盐生成
【答案】D
3、某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的关系如图,下列说法正确的是( )
A. HCl和MgCl2一定存在
B. NaOH、H2SO4和MgCl2一定不存在
C. HCl和H2SO4一定存在
D. HCl一定存在,NaOH、H2SO4一定不存在,MgCl2可能存在
【答案】A
4、下列实验操作中,正确的是( )
A. 闻气味 B. 滴加液体
C. 加热液体 D. 测溶液pH
【答案】C
5、对下列事实的微观解释正确的是( )
选项 事实 解释
A 稀盐酸、稀硫酸均显酸性 溶液中都含有氢元素
B 氢氧化钠溶液能导电 溶液中存在自由移动的离子
C 金刚石和石墨的性质存在着明显差异 碳原子结构不同
D 压缩的乒乓球放入热水中重新鼓起 乒乓球内每个分子的体积都增大
A.A B.B C.C D.D
【答案】B
6、能区分稀硫酸和稀盐酸所用试剂为( )
A. 碳酸钠粉末 B. 硝酸银溶液 C. 氯化钡溶液 D. 氧化铜
【答案】C
7、如图所示是室温下稀硫酸和氢氧化钠反应过程中的pH变化曲线。下列有关说法正确的是( )
A.图中X是氢氧化钠
B.图中a点的阴离子是OH-
C.向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
D.稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4+2NaOH═Na2SO4+H2O
【答案】C
8、化学课上老师拿出三朵用石蕊溶液处理过的紫色小纸花(如图),向纸花上分别喷洒不同的溶液,三朵纸花显色情况为: 紫色 红色 蓝色 。喷在 号纸花上的溶液可能是( )
A. 氢氧化钠 B. 氯化钠 C. 碳酸钠 D. 稀盐酸
【答案】D
9、人体不同器官的体液会保持相对稳定的酸碱度范围。由下表可知:以下叙述中正确的是( )
体液 血液 唾液 胃液
pH 7.35~7.45 6.6~7.2 0.9~1.5
A. 人的血液一定呈碱性 B. 人的胃液一定能使紫色石蕊试液变成蓝色
C. 人的唾液一定呈酸性 D. 用pH试纸能精确测定以上体液的pH
【答案】A
10、下列物质能使紫色石蕊试液变红的是( )
A.胃液 B.氨水 C.蔗糖水 D.pH约为7.8的鸡蛋清
【答案】A
11、下列物质的溶液能使酚酞试液变红色的是( )
A. B. C. D. 的水溶液
【答案】A
12、下列反应,属于中和反应的是( )
A.Ca(OH)2+CO2=CaCO3↓+H2O B.CuO+2HCl=CuCl2+H2O
C.Cu(OH)2+H2SO4=CuSO4+2H2O D.AgNO3+HCl=AgCl↓+HNO3
【答案】C
13、碱溶液中都含有OH-,因此不同碱变现出一些共同的性质,下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A. 能与盐酸反应生成水 B. 能使紫色石蕊溶液变蓝色
C. 能与Na2SO4溶液反应生成BaSO4沉淀 D. 能与CO2反应生成水
【答案】C
14、下列基本实验操作正确的是( )
A. 检查气密性 B. 测量溶液的pH
C. 取固体药品 D. 熄灭酒精灯
【答案】D
15、有一种“白纸血印”的街头骗术,原本是一张雪白的纸,只见“大师”用力一拍,纸上竟然出现了一个血手印,表明妖魔鬼怪被降服,接下来“大师”把纸放入水中,血手印又慢慢消失了,表明妖魔鬼怪被驱走了.其实“大师”事先在手上涂了碳酸钠溶液,在白纸和水中各加入了一种化学试剂,则在水中加入的化学试剂可能是( )
A.稀盐酸 B.酚酞试液 C.氢氧化钠溶液 D.氯化钠溶液
【答案】B
*16、人体内一些液体的正常pH如下,酸性最强的是( )
A.胃液0.8-1.5 B.胆液6.8-7.4
C.血液7.35-7.45 D.唾液6.5-7.5
【答案】A
二、填空题。
17、实验室很多药品需要密封保存。
(1)浓硫酸敞口放置一段时间后溶液质量会变大,这是因为浓硫酸具有________性。浓盐酸敞口放置一段时间后溶液质量会变小,这是因为浓盐酸具有________性。故它们都需要密封保存。
(2)氢氧化钠固体也需要密封保存.原因是它既能吸收空气中的________而发生潮解;又能与空气中的________ 反应而变质。
【答案】(1)吸水性;挥发性 (2)水分;二氧化碳
18、如图甲所示为稀硫酸和氢氧化钠溶液反应的实验操作,图乙为反应过程中烧杯内溶液pH的变化曲线,则图甲中胶头滴管中的溶液为______(填名称);图乙中c点表示的溶液中的溶质是______(填化学式)。
【答案】稀硫酸 Na2SO4、H2SO4
19、某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示。请分析下表,并回答下列问题:
试剂 稀盐酸 食醋 蔗糖水 蒸馏水 肥皂水 烧碱溶液 石灰水
颜色 红 红 黄 黄 绿 绿 绿
(1)该花汁________(填“可以”或“不可以”)作酸碱指示剂。
(2)蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒.要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的________。
(3)烧碱溶液中含有的阴离子符号为:________。
【答案】(1)可以 (2)肥皂水 (3)OH-
20、小亮在做“盐酸中和氢氧化钠溶液”实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.请你和他一起探究: 提出猜想:所得溶液可能呈________性。
设计实验验证你的猜想:
实验操作 实验现象 结论
________ 。 ________ 。 ________ 。
【答案】碱;取少量混合液于试管中,再滴入几滴紫色石蕊溶液;溶液变蓝色;所得溶液呈碱性
21、选择H、C、Cl、S 、O、Ca六种元素中的适当元素,组成符合下列要求的物质,将化学式填在空格中:
(1)相对分子质量最小的氧化物
(2)用于改良酸性土壤的碱
(3)实验室中用来干燥CO2气体的干燥剂
【答案】H2O Ca(OH)2 H2SO4
三、实验题。
22、氢氧化钙的性质:
实验步骤 (1)向两支试管中各加入相同量的氢氧化钙粉末(用药匙的柄把一端挑一点),然后各加入水,振荡;再各滴入1~2滴酚酞溶液,观察现象;(2)继续向其中一支试管中加入约水,振荡;(3)向另一支试管加入约稀盐酸,振荡;比较两支试管中的现象
实验现象 (1)______ ;(2)______ ;(3)______ 。
化学方程式 ______ 。
结论:氢氧化钙______溶于水,其水溶液呈______;氢氧化钙粉末______与盐酸发生反应。
【答案】溶液变红,试管底部有少量粉末剩余
试管底部还有少量粉末未溶解
加盐酸的试管中溶液逐渐就成无色,粉末完全消失
Ca(OH)2+2HCl=CaCl2+2H2O 微 碱性 能
23、某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂。此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质的成分进行探究。
(1)写出该中和反应的化学方程式________ 。
(2)探究烧杯内溶液中溶质的成分:
【提出问题】
该烧杯内的溶液中溶质是什么?
【进行猜想】
(A)溶质可能是CaCl2与Ca(OH)2
(B)溶质可能只是CaCl2
(C)溶质可能是CaCl2与盐酸
【实验探究】
①小明从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液。振荡.观察到酚酞试液不变色。于是他排除了猜想(A),你认为他排除猜想(A)的理由是________ 。
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
实验步骤 预计现象 预计结论
取少量反应后的溶液于试管中,
逐滴加入碳酸钠溶液。 ________ 。 猜想(B)正确
________ 。 猜想(C)正确
通过以上探究,最后确定猜想(C)正确。
【反思与拓展】
要想处理烧杯内溶液使其只有CaCl2溶液,最好向溶液中加入过量________, 充分反应后过滤即可。
【答案】Ca(OH)2+2HCl=CaCl2+2H2O ;
酚酞溶液不变色,说明溶液不呈碱性,而猜想(A) 的溶液呈碱性,所以猜想(A)可以排除 ;
只有白色沉淀产生 ;先有气泡产生,后有白色沉淀产生 ;碳酸钙
四、实验探究题。
24、根据下列图示,回答相关问题:
(1)实验一:滴加液体试剂的仪器名称是 ,实验中所测溶液pH的数值将 (选填 “偏大”“偏小”或“不变”)。
(2)实验二:燃着的酒精灯的作用是 ,玻璃管中发生反应的化学方程式 。
(3)实验三:检验所用水是否属于软水,可使用的物质是 ,制好的汽水打开瓶盖后有大量气体逸出,其主要原因是 。
【答案】(1)胶头滴管 偏小
(2)点燃未反应的一氧化碳,进行尾气处理,防止其污染空气
(3)肥皂水 气压减小,二氧化碳的溶解度减小,大量二氧化碳逸出
人教版(五四学制)第3单元 酸和碱
一、选择题。
1、用焊锡进行焊接时,为了清除金属表面的锈,焊接处要滴几滴( )
A. 食盐 B. 盐酸 C. 蒸馏水 D. 烧碱
2、有关中和反应的说法一定正确的是( )
A.反应物均须溶于水 B.有沉淀生成
C.有气体生成 D.有盐生成
3、某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的关系如图,下列说法正确的是( )
A. HCl和MgCl2一定存在
B. NaOH、H2SO4和MgCl2一定不存在
C. HCl和H2SO4一定存在
D. HCl一定存在,NaOH、H2SO4一定不存在,MgCl2可能存在
4、下列实验操作中,正确的是( )
A. 闻气味 B. 滴加液体
C. 加热液体 D. 测溶液pH
5、对下列事实的微观解释正确的是( )
选项 事实 解释
A 稀盐酸、稀硫酸均显酸性 溶液中都含有氢元素
B 氢氧化钠溶液能导电 溶液中存在自由移动的离子
C 金刚石和石墨的性质存在着明显差异 碳原子结构不同
D 压缩的乒乓球放入热水中重新鼓起 乒乓球内每个分子的体积都增大
A.A B.B C.C D.D
6、能区分稀硫酸和稀盐酸所用试剂为( )
A. 碳酸钠粉末 B. 硝酸银溶液 C. 氯化钡溶液 D. 氧化铜
7、如图所示是室温下稀硫酸和氢氧化钠反应过程中的pH变化曲线。下列有关说法正确的是( )
A.图中X是氢氧化钠
B.图中a点的阴离子是OH-
C.向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
D.稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4+2NaOH═Na2SO4+H2O
8、化学课上老师拿出三朵用石蕊溶液处理过的紫色小纸花(如图),向纸花上分别喷洒不同的溶液,三朵纸花显色情况为: 紫色 红色 蓝色 。喷在 号纸花上的溶液可能是( )
A. 氢氧化钠 B. 氯化钠 C. 碳酸钠 D. 稀盐酸
9、人体不同器官的体液会保持相对稳定的酸碱度范围。由下表可知:以下叙述中正确的是( )
体液 血液 唾液 胃液
pH 7.35~7.45 6.6~7.2 0.9~1.5
A. 人的血液一定呈碱性 B. 人的胃液一定能使紫色石蕊试液变成蓝色
C. 人的唾液一定呈酸性 D. 用pH试纸能精确测定以上体液的pH
10、下列物质能使紫色石蕊试液变红的是( )
A.胃液 B.氨水 C.蔗糖水 D.pH约为7.8的鸡蛋清
11、下列物质的溶液能使酚酞试液变红色的是( )
A. B. C. D. 的水溶液
12、下列反应,属于中和反应的是( )
A.Ca(OH)2+CO2=CaCO3↓+H2O B.CuO+2HCl=CuCl2+H2O
C.Cu(OH)2+H2SO4=CuSO4+2H2O D.AgNO3+HCl=AgCl↓+HNO3
13、碱溶液中都含有OH-,因此不同碱变现出一些共同的性质,下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A. 能与盐酸反应生成水 B. 能使紫色石蕊溶液变蓝色
C. 能与Na2SO4溶液反应生成BaSO4沉淀 D. 能与CO2反应生成水
14、下列基本实验操作正确的是( )
A. 检查气密性 B. 测量溶液的pH
C. 取固体药品 D. 熄灭酒精灯
15、有一种“白纸血印”的街头骗术,原本是一张雪白的纸,只见“大师”用力一拍,纸上竟然出现了一个血手印,表明妖魔鬼怪被降服,接下来“大师”把纸放入水中,血手印又慢慢消失了,表明妖魔鬼怪被驱走了.其实“大师”事先在手上涂了碳酸钠溶液,在白纸和水中各加入了一种化学试剂,则在水中加入的化学试剂可能是( )
A.稀盐酸 B.酚酞试液 C.氢氧化钠溶液 D.氯化钠溶液
*16、人体内一些液体的正常pH如下,酸性最强的是( )
A.胃液0.8-1.5 B.胆液6.8-7.4
C.血液7.35-7.45 D.唾液6.5-7.5
二、填空题。
17、实验室很多药品需要密封保存。
(1)浓硫酸敞口放置一段时间后溶液质量会变大,这是因为浓硫酸具有________性。浓盐酸敞口放置一段时间后溶液质量会变小,这是因为浓盐酸具有________性。故它们都需要密封保存。
(2)氢氧化钠固体也需要密封保存.原因是它既能吸收空气中的________而发生潮解;又能与空气中的________ 反应而变质。
18、如图甲所示为稀硫酸和氢氧化钠溶液反应的实验操作,图乙为反应过程中烧杯内溶液pH的变化曲线,则图甲中胶头滴管中的溶液为______(填名称);图乙中c点表示的溶液中的溶质是______(填化学式)。
19、某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示。请分析下表,并回答下列问题:
试剂 稀盐酸 食醋 蔗糖水 蒸馏水 肥皂水 烧碱溶液 石灰水
颜色 红 红 黄 黄 绿 绿 绿
(1)该花汁________(填“可以”或“不可以”)作酸碱指示剂。
(2)蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒.要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的________。
(3)烧碱溶液中含有的阴离子符号为:________。
20、小亮在做“盐酸中和氢氧化钠溶液”实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.请你和他一起探究: 提出猜想:所得溶液可能呈________性。
设计实验验证你的猜想:
实验操作 实验现象 结论
________ 。 ________ 。 ________ 。
21、选择H、C、Cl、S 、O、Ca六种元素中的适当元素,组成符合下列要求的物质,将化学式填在空格中:
(1)相对分子质量最小的氧化物
(2)用于改良酸性土壤的碱
(3)实验室中用来干燥CO2气体的干燥剂
三、实验题。
22、氢氧化钙的性质:
实验步骤 (1)向两支试管中各加入相同量的氢氧化钙粉末(用药匙的柄把一端挑一点),然后各加入水,振荡;再各滴入1~2滴酚酞溶液,观察现象;(2)继续向其中一支试管中加入约水,振荡;(3)向另一支试管加入约稀盐酸,振荡;比较两支试管中的现象
实验现象 (1)______ ;(2)______ ;(3)______ 。
化学方程式 ______ 。
结论:氢氧化钙______溶于水,其水溶液呈______;氢氧化钙粉末______与盐酸发生反应。
23、某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂。此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质的成分进行探究。
(1)写出该中和反应的化学方程式________ 。
(2)探究烧杯内溶液中溶质的成分:
【提出问题】
该烧杯内的溶液中溶质是什么?
【进行猜想】
(A)溶质可能是CaCl2与Ca(OH)2
(B)溶质可能只是CaCl2
(C)溶质可能是CaCl2与盐酸
【实验探究】
①小明从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液。振荡.观察到酚酞试液不变色。于是他排除了猜想(A),你认为他排除猜想(A)的理由是________ 。
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
实验步骤 预计现象 预计结论
取少量反应后的溶液于试管中,
逐滴加入碳酸钠溶液。 ________ 。 猜想(B)正确
________ 。 猜想(C)正确
通过以上探究,最后确定猜想(C)正确。
【反思与拓展】
要想处理烧杯内溶液使其只有CaCl2溶液,最好向溶液中加入过量________, 充分反应后过滤即可。
四、实验探究题。
24、根据下列图示,回答相关问题:
(1)实验一:滴加液体试剂的仪器名称是 ,实验中所测溶液pH的数值将 (选填 “偏大”“偏小”或“不变”)。
(2)实验二:燃着的酒精灯的作用是 ,玻璃管中发生反应的化学方程式 。
(3)实验三:检验所用水是否属于软水,可使用的物质是 ,制好的汽水打开瓶盖后有大量气体逸出,其主要原因是 。
2023—2024学年人教版(五四学制)化学九年级全一册第3单元 酸和碱 分层题含答案
人教版(五四学制)第3单元 酸和碱
一、选择题。
1、用焊锡进行焊接时,为了清除金属表面的锈,焊接处要滴几滴( )
A. 食盐 B. 盐酸 C. 蒸馏水 D. 烧碱
【答案】B
2、有关中和反应的说法一定正确的是( )
A.反应物均须溶于水 B.有沉淀生成
C.有气体生成 D.有盐生成
【答案】D
3、某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的关系如图,下列说法正确的是( )
A. HCl和MgCl2一定存在
B. NaOH、H2SO4和MgCl2一定不存在
C. HCl和H2SO4一定存在
D. HCl一定存在,NaOH、H2SO4一定不存在,MgCl2可能存在
【答案】A
4、下列实验操作中,正确的是( )
A. 闻气味 B. 滴加液体
C. 加热液体 D. 测溶液pH
【答案】C
5、对下列事实的微观解释正确的是( )
选项 事实 解释
A 稀盐酸、稀硫酸均显酸性 溶液中都含有氢元素
B 氢氧化钠溶液能导电 溶液中存在自由移动的离子
C 金刚石和石墨的性质存在着明显差异 碳原子结构不同
D 压缩的乒乓球放入热水中重新鼓起 乒乓球内每个分子的体积都增大
A.A B.B C.C D.D
【答案】B
6、能区分稀硫酸和稀盐酸所用试剂为( )
A. 碳酸钠粉末 B. 硝酸银溶液 C. 氯化钡溶液 D. 氧化铜
【答案】C
7、如图所示是室温下稀硫酸和氢氧化钠反应过程中的pH变化曲线。下列有关说法正确的是( )
A.图中X是氢氧化钠
B.图中a点的阴离子是OH-
C.向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
D.稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4+2NaOH═Na2SO4+H2O
【答案】C
8、化学课上老师拿出三朵用石蕊溶液处理过的紫色小纸花(如图),向纸花上分别喷洒不同的溶液,三朵纸花显色情况为: 紫色 红色 蓝色 。喷在 号纸花上的溶液可能是( )
A. 氢氧化钠 B. 氯化钠 C. 碳酸钠 D. 稀盐酸
【答案】D
9、人体不同器官的体液会保持相对稳定的酸碱度范围。由下表可知:以下叙述中正确的是( )
体液 血液 唾液 胃液
pH 7.35~7.45 6.6~7.2 0.9~1.5
A. 人的血液一定呈碱性 B. 人的胃液一定能使紫色石蕊试液变成蓝色
C. 人的唾液一定呈酸性 D. 用pH试纸能精确测定以上体液的pH
【答案】A
10、下列物质能使紫色石蕊试液变红的是( )
A.胃液 B.氨水 C.蔗糖水 D.pH约为7.8的鸡蛋清
【答案】A
11、下列物质的溶液能使酚酞试液变红色的是( )
A. B. C. D. 的水溶液
【答案】A
12、下列反应,属于中和反应的是( )
A.Ca(OH)2+CO2=CaCO3↓+H2O B.CuO+2HCl=CuCl2+H2O
C.Cu(OH)2+H2SO4=CuSO4+2H2O D.AgNO3+HCl=AgCl↓+HNO3
【答案】C
13、碱溶液中都含有OH-,因此不同碱变现出一些共同的性质,下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A. 能与盐酸反应生成水 B. 能使紫色石蕊溶液变蓝色
C. 能与Na2SO4溶液反应生成BaSO4沉淀 D. 能与CO2反应生成水
【答案】C
14、下列基本实验操作正确的是( )
A. 检查气密性 B. 测量溶液的pH
C. 取固体药品 D. 熄灭酒精灯
【答案】D
15、有一种“白纸血印”的街头骗术,原本是一张雪白的纸,只见“大师”用力一拍,纸上竟然出现了一个血手印,表明妖魔鬼怪被降服,接下来“大师”把纸放入水中,血手印又慢慢消失了,表明妖魔鬼怪被驱走了.其实“大师”事先在手上涂了碳酸钠溶液,在白纸和水中各加入了一种化学试剂,则在水中加入的化学试剂可能是( )
A.稀盐酸 B.酚酞试液 C.氢氧化钠溶液 D.氯化钠溶液
【答案】B
*16、人体内一些液体的正常pH如下,酸性最强的是( )
A.胃液0.8-1.5 B.胆液6.8-7.4
C.血液7.35-7.45 D.唾液6.5-7.5
【答案】A
二、填空题。
17、实验室很多药品需要密封保存。
(1)浓硫酸敞口放置一段时间后溶液质量会变大,这是因为浓硫酸具有________性。浓盐酸敞口放置一段时间后溶液质量会变小,这是因为浓盐酸具有________性。故它们都需要密封保存。
(2)氢氧化钠固体也需要密封保存.原因是它既能吸收空气中的________而发生潮解;又能与空气中的________ 反应而变质。
【答案】(1)吸水性;挥发性 (2)水分;二氧化碳
18、如图甲所示为稀硫酸和氢氧化钠溶液反应的实验操作,图乙为反应过程中烧杯内溶液pH的变化曲线,则图甲中胶头滴管中的溶液为______(填名称);图乙中c点表示的溶液中的溶质是______(填化学式)。
【答案】稀硫酸 Na2SO4、H2SO4
19、某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示。请分析下表,并回答下列问题:
试剂 稀盐酸 食醋 蔗糖水 蒸馏水 肥皂水 烧碱溶液 石灰水
颜色 红 红 黄 黄 绿 绿 绿
(1)该花汁________(填“可以”或“不可以”)作酸碱指示剂。
(2)蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒.要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的________。
(3)烧碱溶液中含有的阴离子符号为:________。
【答案】(1)可以 (2)肥皂水 (3)OH-
20、小亮在做“盐酸中和氢氧化钠溶液”实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.请你和他一起探究: 提出猜想:所得溶液可能呈________性。
设计实验验证你的猜想:
实验操作 实验现象 结论
________ 。 ________ 。 ________ 。
【答案】碱;取少量混合液于试管中,再滴入几滴紫色石蕊溶液;溶液变蓝色;所得溶液呈碱性
21、选择H、C、Cl、S 、O、Ca六种元素中的适当元素,组成符合下列要求的物质,将化学式填在空格中:
(1)相对分子质量最小的氧化物
(2)用于改良酸性土壤的碱
(3)实验室中用来干燥CO2气体的干燥剂
【答案】H2O Ca(OH)2 H2SO4
三、实验题。
22、氢氧化钙的性质:
实验步骤 (1)向两支试管中各加入相同量的氢氧化钙粉末(用药匙的柄把一端挑一点),然后各加入水,振荡;再各滴入1~2滴酚酞溶液,观察现象;(2)继续向其中一支试管中加入约水,振荡;(3)向另一支试管加入约稀盐酸,振荡;比较两支试管中的现象
实验现象 (1)______ ;(2)______ ;(3)______ 。
化学方程式 ______ 。
结论:氢氧化钙______溶于水,其水溶液呈______;氢氧化钙粉末______与盐酸发生反应。
【答案】溶液变红,试管底部有少量粉末剩余
试管底部还有少量粉末未溶解
加盐酸的试管中溶液逐渐就成无色,粉末完全消失
Ca(OH)2+2HCl=CaCl2+2H2O 微 碱性 能
23、某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂。此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质的成分进行探究。
(1)写出该中和反应的化学方程式________ 。
(2)探究烧杯内溶液中溶质的成分:
【提出问题】
该烧杯内的溶液中溶质是什么?
【进行猜想】
(A)溶质可能是CaCl2与Ca(OH)2
(B)溶质可能只是CaCl2
(C)溶质可能是CaCl2与盐酸
【实验探究】
①小明从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液。振荡.观察到酚酞试液不变色。于是他排除了猜想(A),你认为他排除猜想(A)的理由是________ 。
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
实验步骤 预计现象 预计结论
取少量反应后的溶液于试管中,
逐滴加入碳酸钠溶液。 ________ 。 猜想(B)正确
________ 。 猜想(C)正确
通过以上探究,最后确定猜想(C)正确。
【反思与拓展】
要想处理烧杯内溶液使其只有CaCl2溶液,最好向溶液中加入过量________, 充分反应后过滤即可。
【答案】Ca(OH)2+2HCl=CaCl2+2H2O ;
酚酞溶液不变色,说明溶液不呈碱性,而猜想(A) 的溶液呈碱性,所以猜想(A)可以排除 ;
只有白色沉淀产生 ;先有气泡产生,后有白色沉淀产生 ;碳酸钙
四、实验探究题。
24、根据下列图示,回答相关问题:
(1)实验一:滴加液体试剂的仪器名称是 ,实验中所测溶液pH的数值将 (选填 “偏大”“偏小”或“不变”)。
(2)实验二:燃着的酒精灯的作用是 ,玻璃管中发生反应的化学方程式 。
(3)实验三:检验所用水是否属于软水,可使用的物质是 ,制好的汽水打开瓶盖后有大量气体逸出,其主要原因是 。
【答案】(1)胶头滴管 偏小
(2)点燃未反应的一氧化碳,进行尾气处理,防止其污染空气
(3)肥皂水 气压减小,二氧化碳的溶解度减小,大量二氧化碳逸出
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
