2.4化学反应的调控 课件(16张)2023-2024学年高二上学期化学人教版(2019)选择性必修1
文档属性
| 名称 | 2.4化学反应的调控 课件(16张)2023-2024学年高二上学期化学人教版(2019)选择性必修1 |
|
|
| 格式 | pptx | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-25 00:00:00 | ||
图片预览







文档简介
(共16张PPT)
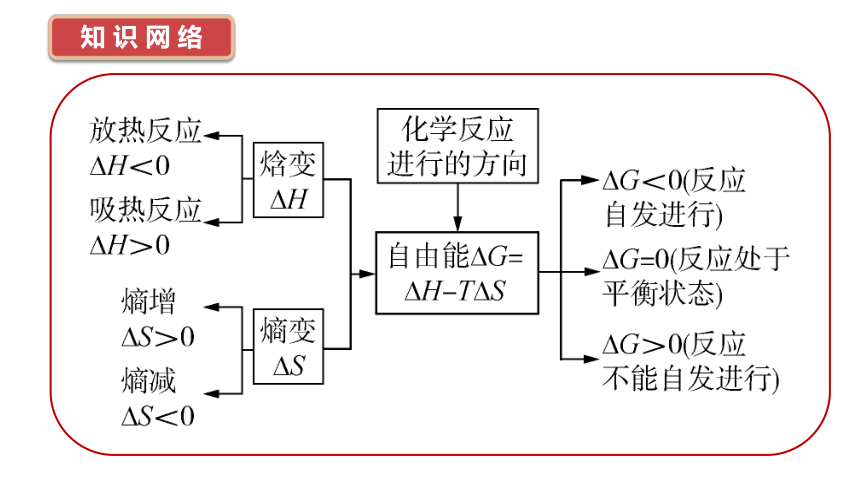
知 识 网 络
第四节 化学反应的调控
第二章 化学反应速率与化学平衡
授课人:
氨是重要的无机化工产品之一,在国民经济中占有重要地位,其中约有80%氨用来生产化学肥料,主要用于制造氮肥和复合肥料,例如尿素、硝酸铵、磷酸铵、氯化铵以及各种含氮复合肥;20%为其它化工产品的原料,如硝酸、各种含氮的无机盐及有机中间体、聚酰胺纤维和丁腈橡胶等都需要氨作为原料。
为什么要设计合成氨?
工业合成氨是人类科学技术的一项重大突破。
本节课将以合成氨反应为例,讨论化学反应条件的选择与优化。
结合数据,分析哪个反应更适合工业固氮?
从化学反应速率和化学平衡两个角度,分析合适的调控方法。
反应很慢(破坏氮氮三键需要很高的能量),但升高温度会导致反应 AG>0 使得氨气又分解。在1000°C时,合成氨只占到混合气体的0.01,根本没有意义。
合成目标:提高反应速率 提高转化率
反应条件:浓度、温度、压强、催化剂
如何选择反应条件以增大合成氨的反应速率,提高平衡混合物中氨的含量?
对合成氨反应的影响 影 响 因 素
浓度 温度 压强 催化剂
增大合成氨的反应速率
提高平衡混合物中氨的含量
增大
增大
增大
使用
增大
降低
增大
无影响
合成氨反应是放热的、气体体积缩小的可逆反应。
请分析合成氨工业中N2和H2的最佳投料比。
图1 一定条件下平衡混合气中
NH3的体积分数与N2和H2投料比的关系
当 N2 和 H2 的物质的量之比约为 1 : 3 时,平衡混合气中 NH3 的体积分数最大,因此 N2 和 H2 的最佳投料比为
适当增大廉价原料(N2)的量,可以提高昂贵原料(H2)的转化率。
在温度与压强的最佳条件下,平衡混合物中氨的含量仍不高怎么办
温度/℃ 氨的含量/%
0.1MPa 10 MPa 20 MPa 30 MPa 60 MPa 100 MPa
200 15.3 81.5 86.4 89.9 95.4 98.8
300 2.20 52.0 64.2 71.0 84.2 92.6
400 0.40 25.1 38.2 47.0 65.2 79.8
500 0.10 10.6 19.1 26.4 42.2 57.5
600 0.05 4.50 9.10 13.8 23.1 31.4
合成氨工业采用迅速冷却法,使气态氨变为液氨后及时从混合物中分离。
表2-2 不同条件下,合成氨反应达到化学平衡时反应混合物中氨的含量(体积分数)
维持反应物浓度需要更多原料,如何降低原料成本?
循环工艺:未反应的N2和H2进行循环利用,能达到提高转化率、降低成本的目的。
原料
循环
利用
分离产物
分析表中数据,应如何选择反应条件以提高平衡混合物中氨的含量?
温度/℃ 氨的含量/%
0.1MPa 10 MPa 20 MPa 30 MPa 60 MPa 100 MPa
200 15.3 81.5 86.4 89.9 95.4 98.8
300 2.20 52.0 64.2 71.0 84.2 92.6
400 0.40 25.1 38.2 47.0 65.2 79.8
500 0.10 10.6 19.1 26.4 42.2 57.5
600 0.05 4.50 9.10 13.8 23.1 31.4
表2-2 不同条件下,合成氨反应达到化学平衡时反应混合物中氨的含量(体积分数)
分析表中数据:压强相等时,温度越低,平衡时氨的含量越高;
温度相等时,压强越大,平衡时氨的含量越高。
降温
加压
合成氨工业中一般采用的压强为10-30 Mpa,为什么不采用>30 Mpa的压强?
压强越大,对材料的强度和设备的制造要求也越高,需要的动力也越大,这会加大生产投资,可能降低综合经济效益。
图2-11 400℃下平衡时的体积分数
随压强的变化示意图
压强增大,氨的含量增大,合成氨的反应速率加快。
选择生产条件的原则:既要注意理论上的需要,又要注意实际操作上的可能性。
【平衡、速率角度相一致】
合成氨工业中一般采用的温度为400-500℃,为什么不采用<400℃的温度?
温度太低,反应速率太小,达到平衡所需的时间变长,不经济。
图2-12 10MPa下平衡时氨的体积分数
随温度的变化示意图
升高温度,合成氨的反应速率加快,但氨的含量减小。
【平衡、速率角度相矛盾】
选择生产条件的原则:综合考虑影响化学反应速率和化学平衡的因素,寻找合适且符合实际需求的生产条件。
在高温高压下N2和H2的反应仍然十分缓慢,请提出合适的方法解决上述问题。
可以加入合适的催化剂,以改变反应历程,从而降低反应的活化能,使反应物能较快地发生反应。
图4 合成氨催化反应图解
目前合成氨工业中普遍使用的是以铁为主体的多成分催化剂,又称铁触媒。
铁触媒在500°C左右时的活性最大,这也是合成氨一般选择400-500°C进行的重要原因。
如何协调温度和催化剂对合成氨反应速率调控的一致性?
选择生产条件的原则:既要注意温度、催化剂对速率影响的一致性,
又要注意催化剂活性对温度的限制。
原料
循环
利用
分离产物
防止催化剂“中毒”,原料气必须经过净化
催化剂活性
最大
总结合成氨常用的生产条件。
合成氨常用的生产条件:
压强:10 - 30 Mpa
温度:400 - 500℃
使用催化剂
将氨及时分离出来
原料气循环使用
总结工业生产中调控化学反应的一般思路和方法。
可自发
优先考虑催化剂
大大提高转化率
温度、浓度、压强等
知 识 网 络
第四节 化学反应的调控
第二章 化学反应速率与化学平衡
授课人:
氨是重要的无机化工产品之一,在国民经济中占有重要地位,其中约有80%氨用来生产化学肥料,主要用于制造氮肥和复合肥料,例如尿素、硝酸铵、磷酸铵、氯化铵以及各种含氮复合肥;20%为其它化工产品的原料,如硝酸、各种含氮的无机盐及有机中间体、聚酰胺纤维和丁腈橡胶等都需要氨作为原料。
为什么要设计合成氨?
工业合成氨是人类科学技术的一项重大突破。
本节课将以合成氨反应为例,讨论化学反应条件的选择与优化。
结合数据,分析哪个反应更适合工业固氮?
从化学反应速率和化学平衡两个角度,分析合适的调控方法。
反应很慢(破坏氮氮三键需要很高的能量),但升高温度会导致反应 AG>0 使得氨气又分解。在1000°C时,合成氨只占到混合气体的0.01,根本没有意义。
合成目标:提高反应速率 提高转化率
反应条件:浓度、温度、压强、催化剂
如何选择反应条件以增大合成氨的反应速率,提高平衡混合物中氨的含量?
对合成氨反应的影响 影 响 因 素
浓度 温度 压强 催化剂
增大合成氨的反应速率
提高平衡混合物中氨的含量
增大
增大
增大
使用
增大
降低
增大
无影响
合成氨反应是放热的、气体体积缩小的可逆反应。
请分析合成氨工业中N2和H2的最佳投料比。
图1 一定条件下平衡混合气中
NH3的体积分数与N2和H2投料比的关系
当 N2 和 H2 的物质的量之比约为 1 : 3 时,平衡混合气中 NH3 的体积分数最大,因此 N2 和 H2 的最佳投料比为
适当增大廉价原料(N2)的量,可以提高昂贵原料(H2)的转化率。
在温度与压强的最佳条件下,平衡混合物中氨的含量仍不高怎么办
温度/℃ 氨的含量/%
0.1MPa 10 MPa 20 MPa 30 MPa 60 MPa 100 MPa
200 15.3 81.5 86.4 89.9 95.4 98.8
300 2.20 52.0 64.2 71.0 84.2 92.6
400 0.40 25.1 38.2 47.0 65.2 79.8
500 0.10 10.6 19.1 26.4 42.2 57.5
600 0.05 4.50 9.10 13.8 23.1 31.4
合成氨工业采用迅速冷却法,使气态氨变为液氨后及时从混合物中分离。
表2-2 不同条件下,合成氨反应达到化学平衡时反应混合物中氨的含量(体积分数)
维持反应物浓度需要更多原料,如何降低原料成本?
循环工艺:未反应的N2和H2进行循环利用,能达到提高转化率、降低成本的目的。
原料
循环
利用
分离产物
分析表中数据,应如何选择反应条件以提高平衡混合物中氨的含量?
温度/℃ 氨的含量/%
0.1MPa 10 MPa 20 MPa 30 MPa 60 MPa 100 MPa
200 15.3 81.5 86.4 89.9 95.4 98.8
300 2.20 52.0 64.2 71.0 84.2 92.6
400 0.40 25.1 38.2 47.0 65.2 79.8
500 0.10 10.6 19.1 26.4 42.2 57.5
600 0.05 4.50 9.10 13.8 23.1 31.4
表2-2 不同条件下,合成氨反应达到化学平衡时反应混合物中氨的含量(体积分数)
分析表中数据:压强相等时,温度越低,平衡时氨的含量越高;
温度相等时,压强越大,平衡时氨的含量越高。
降温
加压
合成氨工业中一般采用的压强为10-30 Mpa,为什么不采用>30 Mpa的压强?
压强越大,对材料的强度和设备的制造要求也越高,需要的动力也越大,这会加大生产投资,可能降低综合经济效益。
图2-11 400℃下平衡时的体积分数
随压强的变化示意图
压强增大,氨的含量增大,合成氨的反应速率加快。
选择生产条件的原则:既要注意理论上的需要,又要注意实际操作上的可能性。
【平衡、速率角度相一致】
合成氨工业中一般采用的温度为400-500℃,为什么不采用<400℃的温度?
温度太低,反应速率太小,达到平衡所需的时间变长,不经济。
图2-12 10MPa下平衡时氨的体积分数
随温度的变化示意图
升高温度,合成氨的反应速率加快,但氨的含量减小。
【平衡、速率角度相矛盾】
选择生产条件的原则:综合考虑影响化学反应速率和化学平衡的因素,寻找合适且符合实际需求的生产条件。
在高温高压下N2和H2的反应仍然十分缓慢,请提出合适的方法解决上述问题。
可以加入合适的催化剂,以改变反应历程,从而降低反应的活化能,使反应物能较快地发生反应。
图4 合成氨催化反应图解
目前合成氨工业中普遍使用的是以铁为主体的多成分催化剂,又称铁触媒。
铁触媒在500°C左右时的活性最大,这也是合成氨一般选择400-500°C进行的重要原因。
如何协调温度和催化剂对合成氨反应速率调控的一致性?
选择生产条件的原则:既要注意温度、催化剂对速率影响的一致性,
又要注意催化剂活性对温度的限制。
原料
循环
利用
分离产物
防止催化剂“中毒”,原料气必须经过净化
催化剂活性
最大
总结合成氨常用的生产条件。
合成氨常用的生产条件:
压强:10 - 30 Mpa
温度:400 - 500℃
使用催化剂
将氨及时分离出来
原料气循环使用
总结工业生产中调控化学反应的一般思路和方法。
可自发
优先考虑催化剂
大大提高转化率
温度、浓度、压强等
