第三章第一节第1课时 铁及其性质 课件(25张PPT)2023-2024学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 第三章第一节第1课时 铁及其性质 课件(25张PPT)2023-2024学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 34.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-26 00:00:00 | ||
图片预览








文档简介
(共25张PPT)
第三章 铁 金属材料
第一节 铁及其化合物
第1课时
3
1
本节重、难点
铁元素在自然界中的存在形态
铁的化学性质
2
铁的物理性质
4
铁的重要用途
古代铁炉
补铁剂
铁锅
高铁
铁元素在中华文化的足迹
古代铁文化
人类最早使用的铁,是来自太空的陨铁
1978年,北京商代遗址中出土一件铁刃铜钺,
其刃部一度被误认为是古代人工冶炼的熟铁。
后来北京钢铁学院对这件器物作了全面的考察,
确定其刃部实为陨铁锻制。
陨
铁
铜
钺
铁在自然界中可以以_____形态存在,但主要以____价和____价_______的形态存在,地壳中含量居第___位,仅次于氧、硅和铝。
单质
1)存在:
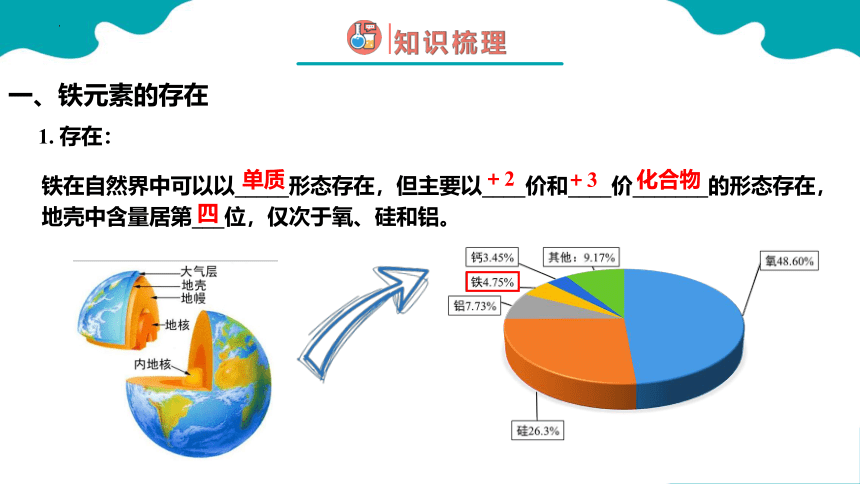
一、铁元素的存在
一、铁元素的存在
铁在自然界中可以以_____形态存在,但主要以____价和____价_______的形态存在,地壳中含量居第___位,仅次于氧、硅和铝。
单质
+2
+3
化合物
1. 存在:
赤铁矿Fe2O3
菱铁矿FeCO3
磁铁矿Fe3O4
黄铁矿FeS2
铁在自然界中可以以_____形态存在,但主要以____价和____价_______的形态存在,地壳中含量居第___位,仅次于氧、硅和铝。
单质
+2
+3
化合物
四
1. 存在:
一、铁元素的存在
春秋初年秦国的铜柄铁剑
我国目前发现最早的人工冶铁制品
战国时期最大的铁器
长方形铁炉
2. 使用
古代铁文化
一、铁元素的存在
二、 铁的物理性质
铁有_____性、_____性、_____性,但其导电性不如________,铁还能被______吸引。其熔、沸点较____,熔点:1 535 ℃、沸点:2 750 ℃,密度:7.86 g·cm-3。
延展
导热
导电
铜和铝
磁体
高
铁皮
铁锅
电极
铁 钠
非金属单质 2Na + Cl2 2NaCl
4Na + O2 = 2Na2O
2Na + O2 Na2O2
酸 2Na + H2SO4= Na2SO4 + H2↑
盐溶液 2Na + CuSO4 +2H2O =
Na2SO4 + Cu(OH)2 + H2↑
水 2Na + 2H2O = 2NaOH + H2↑
金属单质一般与什么物质反应?
非金属单质,水、酸、盐溶液等
三、 铁的化学性质
三、铁的化学性质——还原性
1. 与某些非金属单质反应
化学性质 化学方程式举例
①Fe与非金属单质反应
铁丝在氧气中燃烧
铁丝在氯气中燃烧
铁丝与硫磺的反应
2. 与酸反应
化学性质 化学方程式
②Fe与非氧化性酸反应(H2SO4)
Fe+H2SO4===FeSO4+H2↑
铁丝与稀硫酸反应
三、铁的化学性质——还原性
3.与盐溶液反应
化学性质 化学方程式举例
③Fe与盐溶液反应(CuSO4)
Fe+CuSO4===Cu+FeSO4
铁丝与硫酸铜反应
三、铁的化学性质——还原性
化学性质 化学方程式举例
①Fe与非金属单质反应
②Fe与非氧化性酸反应(H2SO4)
③Fe与盐溶液反应(CuSO4)
Fe在反应中作_____剂,遇到较强的_____剂(如Cl2等)生成____价铁的化合物,遇到较弱的_____剂(如稀硫酸等)生成____价铁的化合物。
Fe+H2SO4===FeSO4+H2↑
Fe+CuSO4===Cu+FeSO4
还原
氧化
+3
氧化
+2
结 论:
4. 还原性小结
三、铁的化学性质——还原性
炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,这是为什么?
近代铁文化 ———
近代工业炼铁
3CO+Fe2O3 2Fe+3CO2
高温
冶炼原理:
生活经验告诉我们,在常温下,铁与水是不发生反应的。那么,在高温下,铁能否与水发生反应呢
5. 铁与水的反应
三、铁的化学性质——还原性
思考:铁会与冷水、热水反应吗?
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
H2O(g)
冷H2O
热H2O
查阅资料:金属与水的反应如下
三、铁的化学性质
5. 铁与水的反应
不反应
5. 铁与水的反应
由已学知识预测:
相关物质的性质
还原 铁粉 FeO Fe2O3 Fe3O4 Fe(OH)2 Fe(OH)3
黑色 黑色 红棕色 黑色 白色 红褐色
受热 不分解 受热 不分解 受热 不分解 受热 不分解 不稳定 500 ℃
分解为Fe2O3
2Na + 2H2O = 2NaOH + H2
Mg + 2H2O(热) = Mg(OH)2 + H2
Fe + H2O(g) Fe2O3 + H2
高温
实验探究
探究:有人设计了如图所示的装置,进行还原铁粉与水蒸气反应的实验。请讨论以下两种方案,哪种方案更好呢
三、铁的化学性质
5. 铁与水的反应
方案一
方案二
肥皂液
五水硫酸铜
还原铁粉
5. 铁粉与水蒸气的反应
实验装置
操作现象 用火柴点燃肥皂液,听到_____声,证明生成了______。
实验结论 在高温下,铁能与水蒸气反应,化学方程式为
_____________________________________________________。
爆鸣
H2
肥皂液
还原铁粉
五水硫酸铜
作用是受热时提供反应所需的水蒸气。
食品脱氧剂
补铁剂
补铁剂
印刷电路板
现代铁文化
铁为我们日常生活带来的改变
四、铁的重要用途
1.将一枚洁净的铁钉浸入稀硫酸中,下列叙述正确的是( )
①铁钉表面产生气泡 ②溶液由无色逐渐变为浅绿色
③铁钉的质量减轻 ④溶液的质量减轻
A.②③ B.①②④ C.①②③ D.①②③④
C
2.下列说法不正确的是( )
A.铁与纯氧气和水蒸气反应都能生成四氧化三铁
B.铁在高温下与水蒸气的反应是置换反应
C.铁与盐酸反应生成氯化铁和氢气
D.铁与盐酸或水蒸气反应,都做还原剂
C
A.反应生成FeO
B.湿棉花的主要作用是冷却试管,防止炸裂
C.肥皂液的主要作用是检验生成的H2
D.铁粉与水蒸气反应后,可立即用磁铁将剩余铁粉分离出来
3.还原铁粉与水蒸气反应的装置如图所示,下列有关该实验的说法正确的是( )
C
铁
铁元素的存在及使用
铁的物理性质
铁的化学性质
第一节
铁及其化合物
第1课时
五、课堂总结
铁的重要用途
THANKS
谢谢聆听
第三章 铁 金属材料
第一节 铁及其化合物
第1课时
3
1
本节重、难点
铁元素在自然界中的存在形态
铁的化学性质
2
铁的物理性质
4
铁的重要用途
古代铁炉
补铁剂
铁锅
高铁
铁元素在中华文化的足迹
古代铁文化
人类最早使用的铁,是来自太空的陨铁
1978年,北京商代遗址中出土一件铁刃铜钺,
其刃部一度被误认为是古代人工冶炼的熟铁。
后来北京钢铁学院对这件器物作了全面的考察,
确定其刃部实为陨铁锻制。
陨
铁
铜
钺
铁在自然界中可以以_____形态存在,但主要以____价和____价_______的形态存在,地壳中含量居第___位,仅次于氧、硅和铝。
单质
1)存在:
一、铁元素的存在
一、铁元素的存在
铁在自然界中可以以_____形态存在,但主要以____价和____价_______的形态存在,地壳中含量居第___位,仅次于氧、硅和铝。
单质
+2
+3
化合物
1. 存在:
赤铁矿Fe2O3
菱铁矿FeCO3
磁铁矿Fe3O4
黄铁矿FeS2
铁在自然界中可以以_____形态存在,但主要以____价和____价_______的形态存在,地壳中含量居第___位,仅次于氧、硅和铝。
单质
+2
+3
化合物
四
1. 存在:
一、铁元素的存在
春秋初年秦国的铜柄铁剑
我国目前发现最早的人工冶铁制品
战国时期最大的铁器
长方形铁炉
2. 使用
古代铁文化
一、铁元素的存在
二、 铁的物理性质
铁有_____性、_____性、_____性,但其导电性不如________,铁还能被______吸引。其熔、沸点较____,熔点:1 535 ℃、沸点:2 750 ℃,密度:7.86 g·cm-3。
延展
导热
导电
铜和铝
磁体
高
铁皮
铁锅
电极
铁 钠
非金属单质 2Na + Cl2 2NaCl
4Na + O2 = 2Na2O
2Na + O2 Na2O2
酸 2Na + H2SO4= Na2SO4 + H2↑
盐溶液 2Na + CuSO4 +2H2O =
Na2SO4 + Cu(OH)2 + H2↑
水 2Na + 2H2O = 2NaOH + H2↑
金属单质一般与什么物质反应?
非金属单质,水、酸、盐溶液等
三、 铁的化学性质
三、铁的化学性质——还原性
1. 与某些非金属单质反应
化学性质 化学方程式举例
①Fe与非金属单质反应
铁丝在氧气中燃烧
铁丝在氯气中燃烧
铁丝与硫磺的反应
2. 与酸反应
化学性质 化学方程式
②Fe与非氧化性酸反应(H2SO4)
Fe+H2SO4===FeSO4+H2↑
铁丝与稀硫酸反应
三、铁的化学性质——还原性
3.与盐溶液反应
化学性质 化学方程式举例
③Fe与盐溶液反应(CuSO4)
Fe+CuSO4===Cu+FeSO4
铁丝与硫酸铜反应
三、铁的化学性质——还原性
化学性质 化学方程式举例
①Fe与非金属单质反应
②Fe与非氧化性酸反应(H2SO4)
③Fe与盐溶液反应(CuSO4)
Fe在反应中作_____剂,遇到较强的_____剂(如Cl2等)生成____价铁的化合物,遇到较弱的_____剂(如稀硫酸等)生成____价铁的化合物。
Fe+H2SO4===FeSO4+H2↑
Fe+CuSO4===Cu+FeSO4
还原
氧化
+3
氧化
+2
结 论:
4. 还原性小结
三、铁的化学性质——还原性
炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,不得留有水,这是为什么?
近代铁文化 ———
近代工业炼铁
3CO+Fe2O3 2Fe+3CO2
高温
冶炼原理:
生活经验告诉我们,在常温下,铁与水是不发生反应的。那么,在高温下,铁能否与水发生反应呢
5. 铁与水的反应
三、铁的化学性质——还原性
思考:铁会与冷水、热水反应吗?
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
H2O(g)
冷H2O
热H2O
查阅资料:金属与水的反应如下
三、铁的化学性质
5. 铁与水的反应
不反应
5. 铁与水的反应
由已学知识预测:
相关物质的性质
还原 铁粉 FeO Fe2O3 Fe3O4 Fe(OH)2 Fe(OH)3
黑色 黑色 红棕色 黑色 白色 红褐色
受热 不分解 受热 不分解 受热 不分解 受热 不分解 不稳定 500 ℃
分解为Fe2O3
2Na + 2H2O = 2NaOH + H2
Mg + 2H2O(热) = Mg(OH)2 + H2
Fe + H2O(g) Fe2O3 + H2
高温
实验探究
探究:有人设计了如图所示的装置,进行还原铁粉与水蒸气反应的实验。请讨论以下两种方案,哪种方案更好呢
三、铁的化学性质
5. 铁与水的反应
方案一
方案二
肥皂液
五水硫酸铜
还原铁粉
5. 铁粉与水蒸气的反应
实验装置
操作现象 用火柴点燃肥皂液,听到_____声,证明生成了______。
实验结论 在高温下,铁能与水蒸气反应,化学方程式为
_____________________________________________________。
爆鸣
H2
肥皂液
还原铁粉
五水硫酸铜
作用是受热时提供反应所需的水蒸气。
食品脱氧剂
补铁剂
补铁剂
印刷电路板
现代铁文化
铁为我们日常生活带来的改变
四、铁的重要用途
1.将一枚洁净的铁钉浸入稀硫酸中,下列叙述正确的是( )
①铁钉表面产生气泡 ②溶液由无色逐渐变为浅绿色
③铁钉的质量减轻 ④溶液的质量减轻
A.②③ B.①②④ C.①②③ D.①②③④
C
2.下列说法不正确的是( )
A.铁与纯氧气和水蒸气反应都能生成四氧化三铁
B.铁在高温下与水蒸气的反应是置换反应
C.铁与盐酸反应生成氯化铁和氢气
D.铁与盐酸或水蒸气反应,都做还原剂
C
A.反应生成FeO
B.湿棉花的主要作用是冷却试管,防止炸裂
C.肥皂液的主要作用是检验生成的H2
D.铁粉与水蒸气反应后,可立即用磁铁将剩余铁粉分离出来
3.还原铁粉与水蒸气反应的装置如图所示,下列有关该实验的说法正确的是( )
C
铁
铁元素的存在及使用
铁的物理性质
铁的化学性质
第一节
铁及其化合物
第1课时
五、课堂总结
铁的重要用途
THANKS
谢谢聆听
