3.1.3 铁盐和亚铁盐 说课课件 (24张)2023-2024学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 3.1.3 铁盐和亚铁盐 说课课件 (24张)2023-2024学年高一上学期化学人教版(2019)必修第一册 |  | |
| 格式 | pptx | ||
| 文件大小 | 8.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-26 10:03:41 | ||
图片预览




文档简介
(共24张PPT)
第三章 第一节 第3课时
铁盐和亚铁盐
探究补铁剂硫酸亚铁片的奥秘
说课人:XXX
人教版(2019版)必修第一册
说课内容
1
2
3
4
教材分析
学情分析
教法与学法分析
教学与评价目标
5
6
教学与评价思路
教学过程
1-1.教材内容的地位和作用
铁盐和亚铁盐
前面已经掌握实验操作基本方法,对物质的分类、离子反应、氧化还原反应有一定的认识。
为学习元素周期律、物质结构打下基础
承上启下
1-2.教学重、难点分析
重点
难点
铁离子和亚铁离子的转化
铁离子的检验,铁离子和亚铁离子的转化
通过实验探究方式突出重点
通过让学生分组实验方式突破难点
心理特征
学生已具备一定的实验操作能力,归纳概括能力和分析问题能力,但是缺乏对知识进行主动探究和建构的能力。
能力水平
知识储备
处于青春期的高中生们思维活跃、好奇心强,对未知事物具有强烈的好奇心,对实验探究充满兴趣,但自主学习意识不强。
学生在初中已初步接触过铁及其化合物的知识,在本教材中学生对物质的分类、离子反应、氧化还原反应也具有一定的认识。
实验探究法
多媒体教学
生活情境引入
观察辨析
合作探究
讨论交流
学法
教法
①通过实验探究认识铁离子和亚铁离子的鉴别及相互转化,巩固加深对氧化还原反应的认识,并提高实验探究能力和动手操作能力。
②通过实验验证硫酸亚铁片中含有亚铁离子,建立鉴别亚铁离子与铁离子的模型,培养学生证据推理与模型认知的核心素养。
③通过设计实验方案,探究久置空气中的硫酸亚铁片中是否部分变质的方案,学以致用,培养学生科学探究与创新意识的核心素养。
教学目标:
①通过对硫酸亚铁片中含有亚铁离子的验证,以及硫酸亚铁片补铁奥秘的探究,诊断并发展学生对实验探究的定性水平。
②通过对亚铁离子与铁离子转化的探究实验设计方案的交流与点评,诊断并发展学生对氧化还原反应本质的认识阶梯和认识思路的结构化水平。
③通过探究久置空气中的硫酸亚铁片是否部分变质的实验方案设计的点评与交流,诊断并发展学生对化学价值的认识水平。
评价目标:
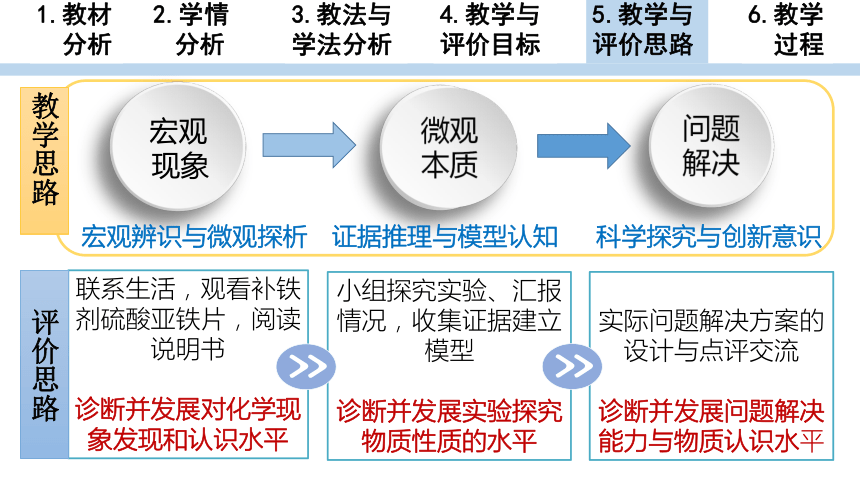
联系生活,观看补铁剂硫酸亚铁片,阅读说明书
诊断并发展对化学现象发现和认识水平
小组探究实验、汇报情况,收集证据建立模型
诊断并发展实验探究物质性质的水平
实际问题解决方案的设计与点评交流
诊断并发展问题解决能力与物质认识水平
宏观
现象
宏观辨识与微观探析
微观
本质
问题
解决
教学思路
评价思路
证据推理与模型认知
科学探究与创新意识
创设情境
引入新课
激发学生
学习兴趣
总结练习
布置作业
实验探究1
课堂练习和课后练习,巩固所学知识
实验探究2
Fe2+
Fe3+
培养学生的实验探究精神与动手能力
进一步培养学生小组合作探究能力与表达交流能力
铁盐和亚铁盐
二、Fe3+的检验:
Fe3+ +3SCN- Fe(SCN)3
(血红色络合物)
三、Fe2+与Fe3+的相互转换:
Fe2+
Fe3+
氧化剂
还原剂
一、Fe2+和Fe3+的鉴别:
观察法、加碱法、加硫氰化钾法
高中课程标准人教版化学必修一
第三章《有机化合物》第二节第3课时
铁盐和亚铁盐
授课人:
5号选手
探究补铁剂硫酸亚铁片的奥秘
硫酸亚铁片说明书
请思考:
1.如何证明硫酸亚铁中含有的是Fe2+而不是Fe3+
2.硫酸亚铁片为何不应与浓茶同服?
3.为什么维生素C与硫酸亚铁片同服有助于吸收?
Fe2+和Fe3+的鉴别
Fe2+ Fe3+
还有没有其他方法?
1.观察法
溶液为浅绿色
溶液为黄色
2.加碱法
生成白色絮状沉淀,很快变灰绿色,最后变红褐色
生成红褐色沉淀
会有什么现象?
血红色络合物
Fe3+ +3SCN- Fe(SCN)3
纸片事先被喷洒了硫氰
化钾溶液(KSCN)
木刀背后贴着吸有Fe3+
溶液的胶头滴管
魔术揭秘:
魔术演示:木刀刺纸片
道具:纸片、小木刀
纸片流血了!
KSCN溶液
Fe3+
滴入KSCN溶液
FeCl3溶液
FeCl2溶液
请两名同学分别演示往FeCl2溶液和FeCl3溶液中滴加1-2滴硫氰化钾溶液,台下的同学注意观察实验现象并做好记录。
溶液由黄色变为血红色
同学们都掌握这种检验Fe3+的方法了吗?那么现在有几种方法鉴别Fe2+和Fe3+了呢?
溶液无明显现象
Fe2+和Fe3+的鉴别模型
Fe2+ Fe3+
1.观察法
2.加碱法
溶液为浅绿色
溶液为黄色
生成白色絮状沉淀,很快变灰绿色,最后变红褐色
生成红褐色沉淀
3.加硫氰化钾法
溶液由黄色变为血红色
溶液无明显现象
任务:请同学们分组利用这三种方法当一位质检员,探究硫酸亚铁片的质量如何,是否真的含Fe2+
第一组 (用观察法) 第二组 (用加碱法) 第三组
(用加硫氰化钾法)
实验现象
能当质检员:探究硫酸亚铁片是否含Fe2+,请分小组搜集证据
证据一
证据二
证据三
将硫酸亚铁片粉末用蒸馏水溶解后,溶液为浅绿色
将硫酸亚铁片粉末用蒸馏水溶解后,加入适量NaOH溶液,生成白色絮状沉淀,很快变灰绿色,最后变红褐色
将硫酸亚铁片粉末用蒸馏水溶解后,加入1-2滴KSCN溶液,无明显现象
质量合格
又有什么现象呢?敬请期待~
茶水变墨水,又变回了茶水!
Fe2+与Fe3+是可以相互转换的
说明:
魔术演示:神奇的茶水
道具:茶水、玻璃棒
茶水里含大量的单宁酸,其遇到亚铁离子生成单宁酸亚铁很快被氧化成单宁酸铁的络合物而呈蓝黑色,从而使茶水变成墨水。而维生素C能将铁离子还原成亚铁离子,因此溶液的蓝黑色消失,又显现出茶水的颜色。
魔术揭秘:
Fe2+与Fe3+的相互转换:
氧化剂 还原剂
新制氯水、过氧化氢溶液、酸性高锰酸钾溶液 铁粉、铜粉、CO、
氢气、KI溶液
Fe3+
请同学们依据提供的氧化剂与还原剂设计实验方案探究Fe2+与Fe3+的相互转换~
还原剂
氧化剂
Fe2+
实验室常见氧化剂与还原剂
3、从氧化还原角度认识了二价铁和三价铁之间的转化关系,探究了补铁剂硫酸亚铁片中蕴藏的奥秘。
观察法、加碱法、加硫氰化钾法
Fe3+ +3SCN- Fe(SCN)3
1、检验铁离子的新的方法——加硫氰化钾法
(血红色络合物)
2、完善了Fe2+和Fe3+的鉴别方法
为了检测某氯化亚铁溶液是否变质,可向溶液
中加入( )
A.NaOH溶液 B.铁片
C.KSCN溶液 D.石蕊溶液
√
C
一、练习册1~5题。
二、拓展作业:
请同学们设计实验方案探究暴露在空气中已久的硫酸亚铁片是否部分变质。
苦了!
感谢各位专家评委
您们辛苦了
第三章 第一节 第3课时
铁盐和亚铁盐
探究补铁剂硫酸亚铁片的奥秘
说课人:XXX
人教版(2019版)必修第一册
说课内容
1
2
3
4
教材分析
学情分析
教法与学法分析
教学与评价目标
5
6
教学与评价思路
教学过程
1-1.教材内容的地位和作用
铁盐和亚铁盐
前面已经掌握实验操作基本方法,对物质的分类、离子反应、氧化还原反应有一定的认识。
为学习元素周期律、物质结构打下基础
承上启下
1-2.教学重、难点分析
重点
难点
铁离子和亚铁离子的转化
铁离子的检验,铁离子和亚铁离子的转化
通过实验探究方式突出重点
通过让学生分组实验方式突破难点
心理特征
学生已具备一定的实验操作能力,归纳概括能力和分析问题能力,但是缺乏对知识进行主动探究和建构的能力。
能力水平
知识储备
处于青春期的高中生们思维活跃、好奇心强,对未知事物具有强烈的好奇心,对实验探究充满兴趣,但自主学习意识不强。
学生在初中已初步接触过铁及其化合物的知识,在本教材中学生对物质的分类、离子反应、氧化还原反应也具有一定的认识。
实验探究法
多媒体教学
生活情境引入
观察辨析
合作探究
讨论交流
学法
教法
①通过实验探究认识铁离子和亚铁离子的鉴别及相互转化,巩固加深对氧化还原反应的认识,并提高实验探究能力和动手操作能力。
②通过实验验证硫酸亚铁片中含有亚铁离子,建立鉴别亚铁离子与铁离子的模型,培养学生证据推理与模型认知的核心素养。
③通过设计实验方案,探究久置空气中的硫酸亚铁片中是否部分变质的方案,学以致用,培养学生科学探究与创新意识的核心素养。
教学目标:
①通过对硫酸亚铁片中含有亚铁离子的验证,以及硫酸亚铁片补铁奥秘的探究,诊断并发展学生对实验探究的定性水平。
②通过对亚铁离子与铁离子转化的探究实验设计方案的交流与点评,诊断并发展学生对氧化还原反应本质的认识阶梯和认识思路的结构化水平。
③通过探究久置空气中的硫酸亚铁片是否部分变质的实验方案设计的点评与交流,诊断并发展学生对化学价值的认识水平。
评价目标:
联系生活,观看补铁剂硫酸亚铁片,阅读说明书
诊断并发展对化学现象发现和认识水平
小组探究实验、汇报情况,收集证据建立模型
诊断并发展实验探究物质性质的水平
实际问题解决方案的设计与点评交流
诊断并发展问题解决能力与物质认识水平
宏观
现象
宏观辨识与微观探析
微观
本质
问题
解决
教学思路
评价思路
证据推理与模型认知
科学探究与创新意识
创设情境
引入新课
激发学生
学习兴趣
总结练习
布置作业
实验探究1
课堂练习和课后练习,巩固所学知识
实验探究2
Fe2+
Fe3+
培养学生的实验探究精神与动手能力
进一步培养学生小组合作探究能力与表达交流能力
铁盐和亚铁盐
二、Fe3+的检验:
Fe3+ +3SCN- Fe(SCN)3
(血红色络合物)
三、Fe2+与Fe3+的相互转换:
Fe2+
Fe3+
氧化剂
还原剂
一、Fe2+和Fe3+的鉴别:
观察法、加碱法、加硫氰化钾法
高中课程标准人教版化学必修一
第三章《有机化合物》第二节第3课时
铁盐和亚铁盐
授课人:
5号选手
探究补铁剂硫酸亚铁片的奥秘
硫酸亚铁片说明书
请思考:
1.如何证明硫酸亚铁中含有的是Fe2+而不是Fe3+
2.硫酸亚铁片为何不应与浓茶同服?
3.为什么维生素C与硫酸亚铁片同服有助于吸收?
Fe2+和Fe3+的鉴别
Fe2+ Fe3+
还有没有其他方法?
1.观察法
溶液为浅绿色
溶液为黄色
2.加碱法
生成白色絮状沉淀,很快变灰绿色,最后变红褐色
生成红褐色沉淀
会有什么现象?
血红色络合物
Fe3+ +3SCN- Fe(SCN)3
纸片事先被喷洒了硫氰
化钾溶液(KSCN)
木刀背后贴着吸有Fe3+
溶液的胶头滴管
魔术揭秘:
魔术演示:木刀刺纸片
道具:纸片、小木刀
纸片流血了!
KSCN溶液
Fe3+
滴入KSCN溶液
FeCl3溶液
FeCl2溶液
请两名同学分别演示往FeCl2溶液和FeCl3溶液中滴加1-2滴硫氰化钾溶液,台下的同学注意观察实验现象并做好记录。
溶液由黄色变为血红色
同学们都掌握这种检验Fe3+的方法了吗?那么现在有几种方法鉴别Fe2+和Fe3+了呢?
溶液无明显现象
Fe2+和Fe3+的鉴别模型
Fe2+ Fe3+
1.观察法
2.加碱法
溶液为浅绿色
溶液为黄色
生成白色絮状沉淀,很快变灰绿色,最后变红褐色
生成红褐色沉淀
3.加硫氰化钾法
溶液由黄色变为血红色
溶液无明显现象
任务:请同学们分组利用这三种方法当一位质检员,探究硫酸亚铁片的质量如何,是否真的含Fe2+
第一组 (用观察法) 第二组 (用加碱法) 第三组
(用加硫氰化钾法)
实验现象
能当质检员:探究硫酸亚铁片是否含Fe2+,请分小组搜集证据
证据一
证据二
证据三
将硫酸亚铁片粉末用蒸馏水溶解后,溶液为浅绿色
将硫酸亚铁片粉末用蒸馏水溶解后,加入适量NaOH溶液,生成白色絮状沉淀,很快变灰绿色,最后变红褐色
将硫酸亚铁片粉末用蒸馏水溶解后,加入1-2滴KSCN溶液,无明显现象
质量合格
又有什么现象呢?敬请期待~
茶水变墨水,又变回了茶水!
Fe2+与Fe3+是可以相互转换的
说明:
魔术演示:神奇的茶水
道具:茶水、玻璃棒
茶水里含大量的单宁酸,其遇到亚铁离子生成单宁酸亚铁很快被氧化成单宁酸铁的络合物而呈蓝黑色,从而使茶水变成墨水。而维生素C能将铁离子还原成亚铁离子,因此溶液的蓝黑色消失,又显现出茶水的颜色。
魔术揭秘:
Fe2+与Fe3+的相互转换:
氧化剂 还原剂
新制氯水、过氧化氢溶液、酸性高锰酸钾溶液 铁粉、铜粉、CO、
氢气、KI溶液
Fe3+
请同学们依据提供的氧化剂与还原剂设计实验方案探究Fe2+与Fe3+的相互转换~
还原剂
氧化剂
Fe2+
实验室常见氧化剂与还原剂
3、从氧化还原角度认识了二价铁和三价铁之间的转化关系,探究了补铁剂硫酸亚铁片中蕴藏的奥秘。
观察法、加碱法、加硫氰化钾法
Fe3+ +3SCN- Fe(SCN)3
1、检验铁离子的新的方法——加硫氰化钾法
(血红色络合物)
2、完善了Fe2+和Fe3+的鉴别方法
为了检测某氯化亚铁溶液是否变质,可向溶液
中加入( )
A.NaOH溶液 B.铁片
C.KSCN溶液 D.石蕊溶液
√
C
一、练习册1~5题。
二、拓展作业:
请同学们设计实验方案探究暴露在空气中已久的硫酸亚铁片是否部分变质。
苦了!
感谢各位专家评委
您们辛苦了
