2023-2024学年九年级化学上册(人教版)5.1.2化学方程式 质量守恒定律应用课件(共17张PPT)
文档属性
| 名称 | 2023-2024学年九年级化学上册(人教版)5.1.2化学方程式 质量守恒定律应用课件(共17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-26 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
第五单元 课题1 质量守恒定律
课时2 化学方程式 质量守恒定律应用
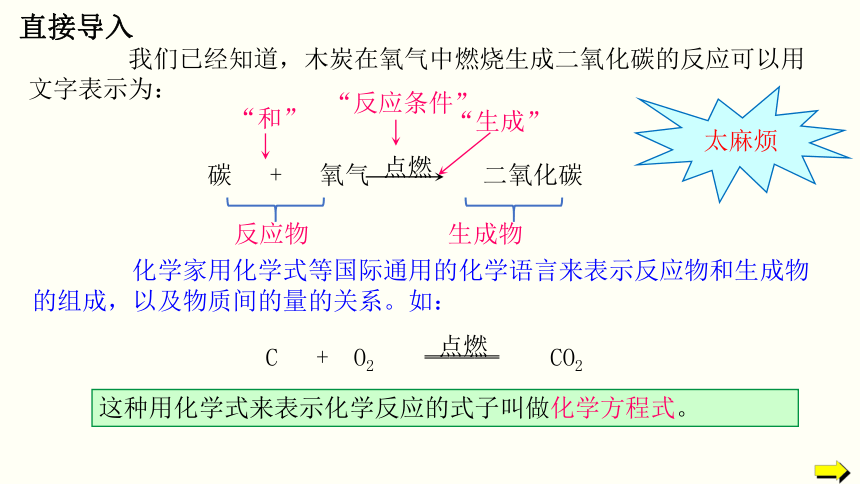
我们已经知道,木炭在氧气中燃烧生成二氧化碳的反应可以用文字表示为:
碳 + 氧气 二氧化碳
点燃
反应物
生成物
“和”
“生成”
“反应条件”
C + O2 ═══ CO2
点燃
太麻烦
化学家用化学式等国际通用的化学语言来表示反应物和生成物的组成,以及物质间的量的关系。如:
这种用化学式来表示化学反应的式子叫做化学方程式。
直接导入
学习目标
1.化学方程式的定义及意义。(重点)
2、掌握质量守恒定律的应用。
一 .化学方程式及其意义
化学式
阅读课本第96页,了解什么是化学方程式及其包含的信息,完成有关问题:
1.化学方程式:用__________来表示化学反应的式子。“+”读作________,“=”读作____________。
化学方程式
客观事实 反应物
生成物
反应条件
和
生成
C和O2(或碳和氧气)
CO2(或二氧化碳)
H2O(或水)
H2和O2(或氢气和氧气)
C + O2 CO2
点燃
2H2O 2H2↑+O2↑
通电
2.化学方程式包含的信息:
点燃
通电
观察与思考
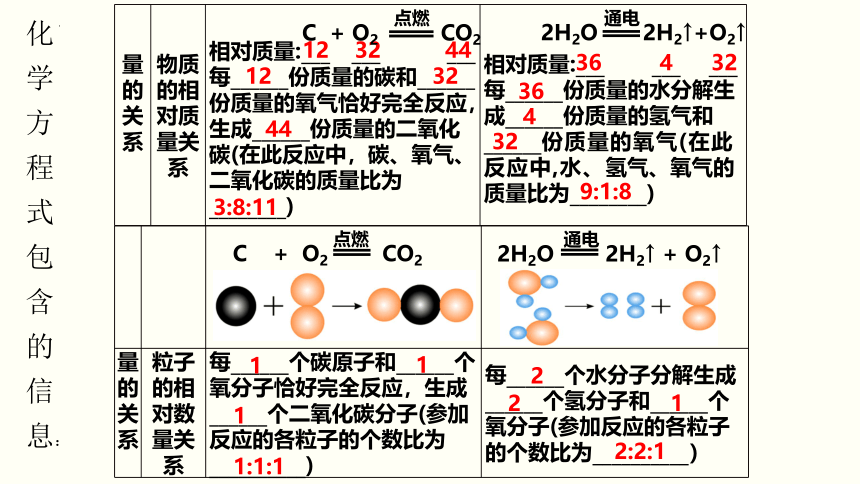
量的关系 物质的相对质量关系 相对质量:___ ___ ___ 每______份质量的碳和______份质量的氧气恰好完全反应,生成______份质量的二氧化碳(在此反应中,碳、氧气、二氧化碳的质量比为________)
相对质量:___ ___ ___
每______份质量的水分解生成______份质量的氢气和______份质量的氧气(在此反应中,水、氢气、氧气的质量比为________)
12 32 44
36 4 32
12
32
44
3:8:11
36
4
32
9:1:8
C + O2 CO2
点燃
2H2O 2H2↑+O2↑
通电
量的关系 粒子的相对数量关系 每______个碳原子和______个氧分子恰好完全反应,生成______个二氧化碳分子(参加反应的各粒子的个数比为__________) 每______个水分子分解生成______个氢分子和______个氧分子(参加反应的各粒子的个数比为__________)
1
1
1
1:1:1
2
2
1
2:2:1
C + O2 CO2
点燃
2H2O 2H2↑ + O2↑
通电
化学方程式包含的信息:
点拨
1.化学计量数指化学方程式中化学式前面的数字,如上述反应中H2的化学计量数为2,O2的化学计量数为1。
2.如果反应物(或生成物)都是气体,化学方程式还能表示它们在反应时的体积比,体积比等于化学计量数之比。如 ,水通电分解生成氢气和氧气的体积比为2︰1。
2H2 ↑ +
O2 ↑
通电
2H2O
二、质量守恒定律的应用
应用 1 推断某反应物,生成物的元素组成(依据化学反应前后元素种类不变)。
应用 2 推断未知物的化学式(依据化学反应前后原子种类、原子数目均不变)。
应用 3 推断物质的化学计量数或其之比(依据化学反应前后元素种类、物质总质量、原子数目均不变)。
应用 4 解释化学反应前后物质的质量变化及质量差,确定某一物质的质量(参加反应的各物质的质量总和等于反应生成的各物质的质量总和)。
观察与思考
三、微观示意图
微观反应示意图解题策略:
(2)若小球代表的原子已知,则可以根据反应示意图写出反应的化学方程式;若小球代表的原子未知,则根据原子的种类和数目不变进行配平,然后根据反应特征判断基本反应类型。
(3)根据化学方程式或质量守恒定律判断元素的种类、原子种类和个数、分子种类和个数是否发生变化。
(4)利用化学反应中小球的移动判断化学反应的实质。
(1)抵消化学反应前后相同的物质(即由相同小球组成,且结构也相同的物质)。
课堂小结:
1、化学方程式的意义(3个)
(1)表示反应物、生成物以及反应条件。
(2)表示各反应物与生成物的粒子个数比。
(化学计量数比)
(3)表示反应物与生成物的质量比。
2、质量守恒定律的应用
课堂检测
1.关于2CO+O2 2CO2的叙述正确的是 ( )
A.一氧化碳加氧气点燃等于二氧化碳
B.一氧化碳和氧气在点燃的条件下反应生成二氧化碳
C.两个一氧化碳分子加一个氧分子等于两个二氧化碳分子
D.2 g一氧化碳和1 g氧气反应生成2 g二氧化碳
2.草酸亚铁晶体(FeC2O4·2H2O)是生产锂电池的原料。当草酸亚铁晶体受热分解时,其产物不可能是 ( )
A.FeO B.CO2 C.H2O D.SO2
B
D
3.大多数动植物进行呼吸作用时发生反应:X+6O2 6CO2+6H2O,动植物利用该反应释放的能量维持生命活动。X的化学式为 ( )
A.C6H12 B.C6H12O C.C6H12O6 D.C6H12O8
4.在一密闭容器中发生某反应,容器中各物质的质量变化如表所示。下列判断正确的是( )
A.x等于90
B.b可能是单质
C.参加反应的a与c的质量比为7∶8
D.d一定是该反应的催化剂
C
物质 a b c d
反应前的质量/g 40 40 32 10
反应后的质量/g 12 x 0 10
C
5.某化合物在氧气中完全的消耗了7.2g氧气,只生成了6.6g二氧化碳和4.05g水,则该化合物( )
A.含有碳、氢、氧三种元素
B.含有碳、氢两种元素
C.含有碳、氧两种元素
D.含有碳、氢元素,可能含有氧元素
6.硅是重要的半导体材料,X+H2 3HCl+Si(高纯)是工业制硅流程中的化学反应之一。下列说法错误的是 ( )
A.反应前后元素种类不变 B.反应前后元素的化合价有变化
C.X的化学式是SiHCl2 D.生成物的质量比为219∶56
A
C
7.下列四个化学方程式中,同时符合四位同学描述的是( )
A.S+O2 SO2
B.2H2+O2 2H2O
C.CH4+2O2 CO2+2H2O
D.2C+O2 2CO
B
直击中考
1.(2023年北京市中考化学真题)下列关于 的说法正确的是( )
A.该反应属于置换反应
B.该反应前后分子的个数不变
C.生成的H2O与O2的分子个数比为2:1
D.参加反应的H2O2与生成的O2的质量比为17:4
2.(2023年辽宁省铁岭市、葫芦岛市中考化学真题)侯德榜发明的侯氏制碱法为我国化学工业作出了杰出的贡献。其主要反应为:,其中X的化学式是( )
A.NaCl B.
C.NaClO D.
C
A
3.(2023年湖北省鄂州市中考化学真题)密闭容器里有甲、乙、丙、丁四种物质在一定条件下反应,测得反应前及反应过程中的某个时刻各物质的质量分数如图所示。下列说法不正确的是( )
A.b=8%
B.丁可能是该反应的催化剂
C.参加反应的甲和乙的质量比为5:1
D.该反应可以表示工业合成氨:N2+3H2 2NH3
C
4.(2023年四川省凉山州中考化学真题)学习化学既要“见著知微”,又要“见微知著”。下图是某化学反应的微观示意图,下列说法错误的是( )
A.该反应属于化合反应
B.参加反应的两物质分子个数比为3:4
C.由该反应可知,燃烧不一定需要氧气参加
D.由该反应可知,化学反应前后原子的种类和数目不变
B
5.(2023年山东省威海市中考化学真题)建立模型是学习化学的重要方法。如图是某反应的微观示意图,下列说法正确的是( )
A.甲物质中氮元素的化合价为+3
B.该反应前后分子数目不发生改变
C.该反应前后涉及的化合物有3种
D.参加反应的甲、乙的质量比等于生成的丙、丁的质量比17:45
C
第五单元 课题1 质量守恒定律
课时2 化学方程式 质量守恒定律应用
我们已经知道,木炭在氧气中燃烧生成二氧化碳的反应可以用文字表示为:
碳 + 氧气 二氧化碳
点燃
反应物
生成物
“和”
“生成”
“反应条件”
C + O2 ═══ CO2
点燃
太麻烦
化学家用化学式等国际通用的化学语言来表示反应物和生成物的组成,以及物质间的量的关系。如:
这种用化学式来表示化学反应的式子叫做化学方程式。
直接导入
学习目标
1.化学方程式的定义及意义。(重点)
2、掌握质量守恒定律的应用。
一 .化学方程式及其意义
化学式
阅读课本第96页,了解什么是化学方程式及其包含的信息,完成有关问题:
1.化学方程式:用__________来表示化学反应的式子。“+”读作________,“=”读作____________。
化学方程式
客观事实 反应物
生成物
反应条件
和
生成
C和O2(或碳和氧气)
CO2(或二氧化碳)
H2O(或水)
H2和O2(或氢气和氧气)
C + O2 CO2
点燃
2H2O 2H2↑+O2↑
通电
2.化学方程式包含的信息:
点燃
通电
观察与思考
量的关系 物质的相对质量关系 相对质量:___ ___ ___ 每______份质量的碳和______份质量的氧气恰好完全反应,生成______份质量的二氧化碳(在此反应中,碳、氧气、二氧化碳的质量比为________)
相对质量:___ ___ ___
每______份质量的水分解生成______份质量的氢气和______份质量的氧气(在此反应中,水、氢气、氧气的质量比为________)
12 32 44
36 4 32
12
32
44
3:8:11
36
4
32
9:1:8
C + O2 CO2
点燃
2H2O 2H2↑+O2↑
通电
量的关系 粒子的相对数量关系 每______个碳原子和______个氧分子恰好完全反应,生成______个二氧化碳分子(参加反应的各粒子的个数比为__________) 每______个水分子分解生成______个氢分子和______个氧分子(参加反应的各粒子的个数比为__________)
1
1
1
1:1:1
2
2
1
2:2:1
C + O2 CO2
点燃
2H2O 2H2↑ + O2↑
通电
化学方程式包含的信息:
点拨
1.化学计量数指化学方程式中化学式前面的数字,如上述反应中H2的化学计量数为2,O2的化学计量数为1。
2.如果反应物(或生成物)都是气体,化学方程式还能表示它们在反应时的体积比,体积比等于化学计量数之比。如 ,水通电分解生成氢气和氧气的体积比为2︰1。
2H2 ↑ +
O2 ↑
通电
2H2O
二、质量守恒定律的应用
应用 1 推断某反应物,生成物的元素组成(依据化学反应前后元素种类不变)。
应用 2 推断未知物的化学式(依据化学反应前后原子种类、原子数目均不变)。
应用 3 推断物质的化学计量数或其之比(依据化学反应前后元素种类、物质总质量、原子数目均不变)。
应用 4 解释化学反应前后物质的质量变化及质量差,确定某一物质的质量(参加反应的各物质的质量总和等于反应生成的各物质的质量总和)。
观察与思考
三、微观示意图
微观反应示意图解题策略:
(2)若小球代表的原子已知,则可以根据反应示意图写出反应的化学方程式;若小球代表的原子未知,则根据原子的种类和数目不变进行配平,然后根据反应特征判断基本反应类型。
(3)根据化学方程式或质量守恒定律判断元素的种类、原子种类和个数、分子种类和个数是否发生变化。
(4)利用化学反应中小球的移动判断化学反应的实质。
(1)抵消化学反应前后相同的物质(即由相同小球组成,且结构也相同的物质)。
课堂小结:
1、化学方程式的意义(3个)
(1)表示反应物、生成物以及反应条件。
(2)表示各反应物与生成物的粒子个数比。
(化学计量数比)
(3)表示反应物与生成物的质量比。
2、质量守恒定律的应用
课堂检测
1.关于2CO+O2 2CO2的叙述正确的是 ( )
A.一氧化碳加氧气点燃等于二氧化碳
B.一氧化碳和氧气在点燃的条件下反应生成二氧化碳
C.两个一氧化碳分子加一个氧分子等于两个二氧化碳分子
D.2 g一氧化碳和1 g氧气反应生成2 g二氧化碳
2.草酸亚铁晶体(FeC2O4·2H2O)是生产锂电池的原料。当草酸亚铁晶体受热分解时,其产物不可能是 ( )
A.FeO B.CO2 C.H2O D.SO2
B
D
3.大多数动植物进行呼吸作用时发生反应:X+6O2 6CO2+6H2O,动植物利用该反应释放的能量维持生命活动。X的化学式为 ( )
A.C6H12 B.C6H12O C.C6H12O6 D.C6H12O8
4.在一密闭容器中发生某反应,容器中各物质的质量变化如表所示。下列判断正确的是( )
A.x等于90
B.b可能是单质
C.参加反应的a与c的质量比为7∶8
D.d一定是该反应的催化剂
C
物质 a b c d
反应前的质量/g 40 40 32 10
反应后的质量/g 12 x 0 10
C
5.某化合物在氧气中完全的消耗了7.2g氧气,只生成了6.6g二氧化碳和4.05g水,则该化合物( )
A.含有碳、氢、氧三种元素
B.含有碳、氢两种元素
C.含有碳、氧两种元素
D.含有碳、氢元素,可能含有氧元素
6.硅是重要的半导体材料,X+H2 3HCl+Si(高纯)是工业制硅流程中的化学反应之一。下列说法错误的是 ( )
A.反应前后元素种类不变 B.反应前后元素的化合价有变化
C.X的化学式是SiHCl2 D.生成物的质量比为219∶56
A
C
7.下列四个化学方程式中,同时符合四位同学描述的是( )
A.S+O2 SO2
B.2H2+O2 2H2O
C.CH4+2O2 CO2+2H2O
D.2C+O2 2CO
B
直击中考
1.(2023年北京市中考化学真题)下列关于 的说法正确的是( )
A.该反应属于置换反应
B.该反应前后分子的个数不变
C.生成的H2O与O2的分子个数比为2:1
D.参加反应的H2O2与生成的O2的质量比为17:4
2.(2023年辽宁省铁岭市、葫芦岛市中考化学真题)侯德榜发明的侯氏制碱法为我国化学工业作出了杰出的贡献。其主要反应为:,其中X的化学式是( )
A.NaCl B.
C.NaClO D.
C
A
3.(2023年湖北省鄂州市中考化学真题)密闭容器里有甲、乙、丙、丁四种物质在一定条件下反应,测得反应前及反应过程中的某个时刻各物质的质量分数如图所示。下列说法不正确的是( )
A.b=8%
B.丁可能是该反应的催化剂
C.参加反应的甲和乙的质量比为5:1
D.该反应可以表示工业合成氨:N2+3H2 2NH3
C
4.(2023年四川省凉山州中考化学真题)学习化学既要“见著知微”,又要“见微知著”。下图是某化学反应的微观示意图,下列说法错误的是( )
A.该反应属于化合反应
B.参加反应的两物质分子个数比为3:4
C.由该反应可知,燃烧不一定需要氧气参加
D.由该反应可知,化学反应前后原子的种类和数目不变
B
5.(2023年山东省威海市中考化学真题)建立模型是学习化学的重要方法。如图是某反应的微观示意图,下列说法正确的是( )
A.甲物质中氮元素的化合价为+3
B.该反应前后分子数目不发生改变
C.该反应前后涉及的化合物有3种
D.参加反应的甲、乙的质量比等于生成的丙、丁的质量比17:45
C
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
