2.3.1物质的量课件(共17张PPT)2023-2024学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 2.3.1物质的量课件(共17张PPT)2023-2024学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 7.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-26 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
物质的量
第二章 第三节 第1课时
物质的量的单位——摩尔
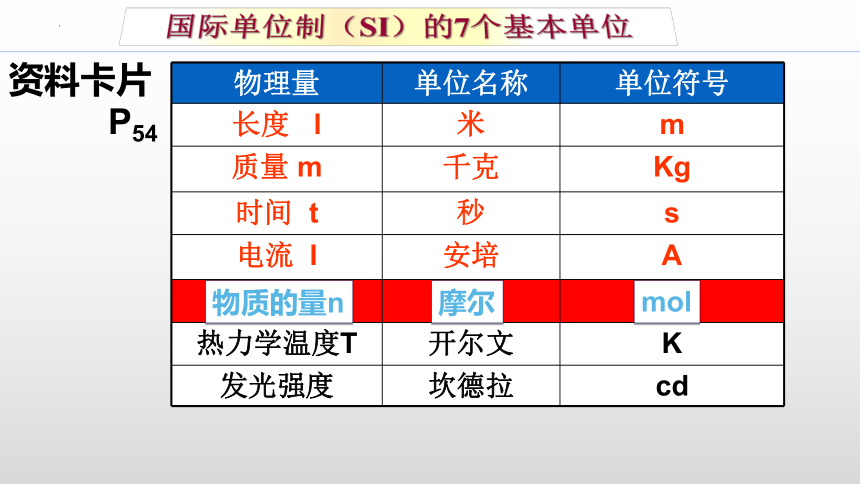
物理量 单位名称 单位符号
长度 l 米 m
质量 m 千克 Kg
时间 t 秒 s
电流 I 安培 A
热力学温度T 开尔文 K
发光强度 坎德拉 cd
国际单位制(SI)的7个基本单位
物质的量n
摩尔
mol
资料卡片
P54
【任务一】物质的量
1、定义:表示 的集合体。
2、符号: 。
3、单位: 简称: ,符号为: 。
阅读课本P53第三段,完成下面的填空。
一定数目粒子
n
摩尔
摩
mol
{
原子、分子、离子、原子团、
电子、质子 、中子等微观粒子
C、用摩尔为单位表示某物质的物质的量时,必须指明物质微粒的名称、符号或化学式。如:1 mol H、1 mol H+、 1 mol H2 ,不能用 “1 mol 氢”这样含糊无意义的表示。
D、 物质的量的数值可以是整数,也可以是小数。
A、“物质的量”是一个物理量的全称,是一个专有名词;
是衡量一定微观粒子数目集体的物理量。
不能理解成物质的数量或质量。
B、摩尔只能描述原子、分子、离子、原子团、质子、中子和电子等微观粒子,不能描述宏观物质。
4、注意事项:
思考:判断下列说法是否正确
(A)1 mol氧
(B)1 molH
(C)2 mol大米
(D)H2SO4的物质量为3mol
(E)二氧化碳的摩尔数是0.5
必须指明微粒的种类,是氧原子、氧分子还是氧离子
1mol 氢原子
大米是宏观物质
物质的量不能拆开
“摩尔”是“物质的量”的单位,两者不能混淆,应该是二氧化碳分子的物质的量是0.5mol或者是0.5摩尔二氧化碳分子。
一打生蚝几个?
1 mol的衡量标准
宏观物质
微观粒子
二
1 mol的衡量标准
1、定义
把1 mol任何微粒所含的微粒数为阿伏加德罗常数
2、符号:NA
【任务二】阿伏伽德罗常数
3、数值
NA≈ 6.02×1023 mol-1
约等于
近似值
二
4、微观粒子数、物质的量、NA之间的关系
n
=
N
NA
物质的量
(单位:mol)
微粒数
(单位:个)
阿伏加德罗常数
(单位:mol-1)
N = n × NA
【任务二】阿伏伽德罗常数
1mol H2O中有多少H和O
1个 H2O由2个H和1个O构成
2个 H2O由4个H和2个O构成
6.02×1023个 H2O
由2×6.02×1023个H和6.02×1023个O构成
【任务二】阿伏伽德罗常数
例1:下列关于阿伏加德罗常数的说法正确的是( )
A.阿伏加德罗常数是一个纯数,没有单位
B.阿伏加德罗常数就是6.02×1023
C.阿伏加德罗常数是指1 mol 的任何粒子的粒子数
D.阿伏加德罗常数的值为6.02×1023 mol-1
C
评价任务二
【例2】填空
(1)3 mol Na2CO3含有 个钠离子, 个碳酸根离子。
(2)6.02×1023个碳原子有 mol 碳原子。
(3)1个 CO2中含有 个质子, 个电子,2mol CO2中质子的物质的量为 ,质子数为 ,电子数为 。
(4)0.1molNa+含有 个电子;0.1molOH—中含有 个电子。
(5)0.1 mol Na2CO3·10H2O含有 个氢原子、含有 个氧原子和 mol原子。
评价任务一、二
那么单位物质的量的微粒与其所具有的质量又有什么关系呢?
粒子符号 相对分子质量 每个粒子的质量(g/个) 1摩物质含有的粒子数(个) 1摩物质质量(g)
C 12 1.993X10-23
Fe 56 9.302X10-23
H2SO4 98 1.628X10-22
H2O 18 2.990X10-23
Na+ 23 3.821X10-23
OH- 17 2.824X10-23
NA
NA
NA
NA
NA
NA
12
56
98
18
23
17
1 mol任何粒子或物质的质量(g)在数值上= 相对分子质量或相对原子质量
1、定义
符号:M 单位:g/mol
单位物质的量的物质所具有的质量叫做摩尔质量
b. 数值上等于物质的“相对分子质量或相对原子质量”
2、理解
a. 1 mol 物质的质量
分子:相对分子质量;原子:相对原子质量;离子:不考虑电子质量
表示方法:M(NaCl) = 58.5 g/mol
【任务三】摩尔质量
1 mol Fe的质量是:________
1 mol Fe2+的质量是: ________
1 mol Fe3+的质量是: ________
3、n、m、M之间的关系
2 mol Fe的质量是:________
10 mol Fe的质量是: ________
n
=
m
M
物质的量
物质的质量
摩尔质量
【任务三】摩尔质量
物质的量
(n)
质量
(m)
粒子数
(N)
M×
÷M
×NA
NA÷
宏观量
微观量
“桥梁”
原子数、分子数、离子数、原子团数、电子数、质子数中子数等
【示例】
常温下,48 g O2与O3的混合物中含有_____NA个氧原子
34 g OH- 中含有的电子数为_______NA
20
3
【例3】49 g H2SO4的物质的量是多少?所含H2SO4分子的个数是多少?
M (H2SO4) = 98 g/mol
m (H2SO4)
n (H2SO4) =
M (H2SO4)
49 g
98 g/mol
= 0.5 mol
N (H2SO4) =
= 0.5 mol×6.02×1023mol-1
n (H2SO4)×NA
= 3.01×1023
=
评价任务三
【例4】填空题
(1)39g过氧化钠的物质的量是 mol;
(2)1.5 mol 硫酸的质量是 g,其中含有 mol O ,
其质量是 g;
(3)0.01 mol 某物质的质量是1.08 g,此物质的摩尔质量为 ;
(4)71 g Na2SO4中含 molNa+ , 个Na+ 。
评价任务三
物质的量
第二章 第三节 第1课时
物质的量的单位——摩尔
物理量 单位名称 单位符号
长度 l 米 m
质量 m 千克 Kg
时间 t 秒 s
电流 I 安培 A
热力学温度T 开尔文 K
发光强度 坎德拉 cd
国际单位制(SI)的7个基本单位
物质的量n
摩尔
mol
资料卡片
P54
【任务一】物质的量
1、定义:表示 的集合体。
2、符号: 。
3、单位: 简称: ,符号为: 。
阅读课本P53第三段,完成下面的填空。
一定数目粒子
n
摩尔
摩
mol
{
原子、分子、离子、原子团、
电子、质子 、中子等微观粒子
C、用摩尔为单位表示某物质的物质的量时,必须指明物质微粒的名称、符号或化学式。如:1 mol H、1 mol H+、 1 mol H2 ,不能用 “1 mol 氢”这样含糊无意义的表示。
D、 物质的量的数值可以是整数,也可以是小数。
A、“物质的量”是一个物理量的全称,是一个专有名词;
是衡量一定微观粒子数目集体的物理量。
不能理解成物质的数量或质量。
B、摩尔只能描述原子、分子、离子、原子团、质子、中子和电子等微观粒子,不能描述宏观物质。
4、注意事项:
思考:判断下列说法是否正确
(A)1 mol氧
(B)1 molH
(C)2 mol大米
(D)H2SO4的物质量为3mol
(E)二氧化碳的摩尔数是0.5
必须指明微粒的种类,是氧原子、氧分子还是氧离子
1mol 氢原子
大米是宏观物质
物质的量不能拆开
“摩尔”是“物质的量”的单位,两者不能混淆,应该是二氧化碳分子的物质的量是0.5mol或者是0.5摩尔二氧化碳分子。
一打生蚝几个?
1 mol的衡量标准
宏观物质
微观粒子
二
1 mol的衡量标准
1、定义
把1 mol任何微粒所含的微粒数为阿伏加德罗常数
2、符号:NA
【任务二】阿伏伽德罗常数
3、数值
NA≈ 6.02×1023 mol-1
约等于
近似值
二
4、微观粒子数、物质的量、NA之间的关系
n
=
N
NA
物质的量
(单位:mol)
微粒数
(单位:个)
阿伏加德罗常数
(单位:mol-1)
N = n × NA
【任务二】阿伏伽德罗常数
1mol H2O中有多少H和O
1个 H2O由2个H和1个O构成
2个 H2O由4个H和2个O构成
6.02×1023个 H2O
由2×6.02×1023个H和6.02×1023个O构成
【任务二】阿伏伽德罗常数
例1:下列关于阿伏加德罗常数的说法正确的是( )
A.阿伏加德罗常数是一个纯数,没有单位
B.阿伏加德罗常数就是6.02×1023
C.阿伏加德罗常数是指1 mol 的任何粒子的粒子数
D.阿伏加德罗常数的值为6.02×1023 mol-1
C
评价任务二
【例2】填空
(1)3 mol Na2CO3含有 个钠离子, 个碳酸根离子。
(2)6.02×1023个碳原子有 mol 碳原子。
(3)1个 CO2中含有 个质子, 个电子,2mol CO2中质子的物质的量为 ,质子数为 ,电子数为 。
(4)0.1molNa+含有 个电子;0.1molOH—中含有 个电子。
(5)0.1 mol Na2CO3·10H2O含有 个氢原子、含有 个氧原子和 mol原子。
评价任务一、二
那么单位物质的量的微粒与其所具有的质量又有什么关系呢?
粒子符号 相对分子质量 每个粒子的质量(g/个) 1摩物质含有的粒子数(个) 1摩物质质量(g)
C 12 1.993X10-23
Fe 56 9.302X10-23
H2SO4 98 1.628X10-22
H2O 18 2.990X10-23
Na+ 23 3.821X10-23
OH- 17 2.824X10-23
NA
NA
NA
NA
NA
NA
12
56
98
18
23
17
1 mol任何粒子或物质的质量(g)在数值上= 相对分子质量或相对原子质量
1、定义
符号:M 单位:g/mol
单位物质的量的物质所具有的质量叫做摩尔质量
b. 数值上等于物质的“相对分子质量或相对原子质量”
2、理解
a. 1 mol 物质的质量
分子:相对分子质量;原子:相对原子质量;离子:不考虑电子质量
表示方法:M(NaCl) = 58.5 g/mol
【任务三】摩尔质量
1 mol Fe的质量是:________
1 mol Fe2+的质量是: ________
1 mol Fe3+的质量是: ________
3、n、m、M之间的关系
2 mol Fe的质量是:________
10 mol Fe的质量是: ________
n
=
m
M
物质的量
物质的质量
摩尔质量
【任务三】摩尔质量
物质的量
(n)
质量
(m)
粒子数
(N)
M×
÷M
×NA
NA÷
宏观量
微观量
“桥梁”
原子数、分子数、离子数、原子团数、电子数、质子数中子数等
【示例】
常温下,48 g O2与O3的混合物中含有_____NA个氧原子
34 g OH- 中含有的电子数为_______NA
20
3
【例3】49 g H2SO4的物质的量是多少?所含H2SO4分子的个数是多少?
M (H2SO4) = 98 g/mol
m (H2SO4)
n (H2SO4) =
M (H2SO4)
49 g
98 g/mol
= 0.5 mol
N (H2SO4) =
= 0.5 mol×6.02×1023mol-1
n (H2SO4)×NA
= 3.01×1023
=
评价任务三
【例4】填空题
(1)39g过氧化钠的物质的量是 mol;
(2)1.5 mol 硫酸的质量是 g,其中含有 mol O ,
其质量是 g;
(3)0.01 mol 某物质的质量是1.08 g,此物质的摩尔质量为 ;
(4)71 g Na2SO4中含 molNa+ , 个Na+ 。
评价任务三
