1.1.2有机化合物中的共价键、同分异构现象课件(共35张PPT)2023-2024学年下学期高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 1.1.2有机化合物中的共价键、同分异构现象课件(共35张PPT)2023-2024学年下学期高二化学人教版(2019)选择性必修3 |
|
|
| 格式 | pptx | ||
| 文件大小 | 7.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-26 00:00:00 | ||
图片预览










文档简介
(共35张PPT)
第一章 有机化合物的结构特点与研究方法
第一节 有机化合物的结构特点
第2课时 有机化合物中的共价键 同分异构现象
【温故知新】
在有机化合物分子中,碳原子通过共用电子对与其他原子相连接形成不同类型的共价键,共价键的类型和极性对有机化合物的性质有很大的影响。你还记得共价键可以怎样分类吗?
【思考与讨论】请同学们从以上三个分类角度分析甲烷、乙烯的化学键类型。
共价键
极性键
非极性键
共价键
单键
三键
双键
共价键
σ键
π键
一、有机化合物中的共价键
甲烷
极性键
4个碳氢单键
4个σ键
sp3杂化
甲烷分子中的σ键
C原子的4个sp3杂化轨道与4个H原子的1s轨道以“头碰头”的形式重叠形成。
如何形成?
1、共价键的类型
乙烯
含极性键 和 非极性键
4个碳氢单键 和 1个碳碳双键
5个σ键 1个π键
sp2杂化
σ键
π键
乙烯分子中的σ键和π键
如何形成?
C原子2个sp2杂化轨道与H原子的1s轨道及另一个C原子的sp2杂化轨道以“头碰头”的形式重叠形成σ键; C原子未参与杂化的p轨道以“肩并肩”的形式重叠形成π键。
一、认识有机化合物中的共价键
【思考与交流】分析乙炔中的化学键类型,并从化学键的角度解释甲烷、乙烯、乙炔在性质上的差异性。
甲烷分子中含有C—H σ键,能发生取代反应;乙烯和乙炔分子的双键和三键中含有π键,它们都能发生加成反应。
含极性键 和 非极性键
2个碳氢单键 和 1个碳碳三键
3个σ键 2个π键
(1)一般情况下,有机化合物中的单键是σ键,双键中含有一个σ键和一个π键,三键中含有一个σ键和两个π键。
(3)共价键类型与反应类型密切相关。
(2)π键与σ键的轨道重叠程度不同,所以强度不同,一般π键稳定性更弱。通过σ键连接的原子或原子团可以绕键轴旋转,通过π键连接的原子或原子团不能绕键轴旋转。
【小结】有机化合物中的共价键
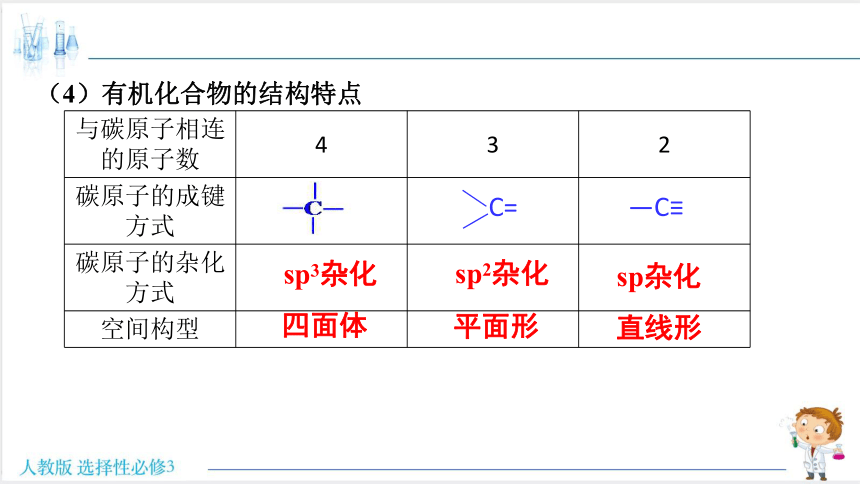
(4)有机化合物的结构特点
与碳原子相连的原子数 4 3 2
碳原子的成键方式
碳原子的杂化方式
空间构型
C=
—C≡
sp3杂化
sp2杂化
sp杂化
四面体
平面形
直线形
由于不同的成键原子间电负性的差异,共用电子对会发生偏移。成键原子间电负性差异越大,共价键极性越强,在反应中越容易发生断裂。因此有机化合物的官能团及其邻近的化学键往往是发生化学反应的活性部位。
【思考与交流】如何理解共价键的极性?共价键的极性强弱与化学键的稳定性有什么关系?
实验1-1
向两只分别盛有蒸馏水和无水乙醇的烧杯中各加入同样大小的钠(约绿豆大),观察现象。
实验1-1
水和钠 无水乙醇和钠
实验原理
实验现象
剧烈程度
剧烈程度:H2O>CH3CH2OH
2Na+2H2O=2NaOH+H2↑
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
浮、熔、游、响、红
钠沉入底部,有气体产生,最终钠粒消失,液体仍为无色透明。
2、共价键的极性与有机反应
1、为什么乙醇与钠能发生反应放出氢气?
原因在于乙醇分子中的氢氧键极性较强,能够发生断裂
2、同样条件下,为什么乙醇与钠的反应没有水与钠的反应剧烈?
这是由于受乙基的影响,乙醇分子中氢氧键的极性比水分子中氢氧键的极性弱。
基团之间的相互影响使官能团中化学键的极性发生变化,从而影响官能团和物质的性质。
【思考与交流】
由于羟基中氧原子的电负性较大,乙醇分子中的碳氧键极性也较强,在乙醇与氢溴酸的反应中,碳氧键发生了断裂。
共价键的断裂需要吸收能量,而且有机化合物分子中共价键断裂的位置存在多种可能。相对无机反应,有机反应一般反应速率较小,副反应较多,产物比较复杂。
H—C—C—O—H+H—Br
H
H
H
H
△
H—C—C—Br+H2O
H
H
H
H
2、共价键的极性与有机反应
取代反应
大本练习册P9
应用体验
1.碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如图。下列有关该物质的说法不正确的是( )
A.分子式为C3H4O3
B.分子中σ键与π键个数之比为10∶1
C.分子中既有极性键也有非极性键
D.分子中碳原子的杂化方式全部为sp2杂化
D
大本练习册P9
应用体验
2.丙烯颜料是一种非常方便使用的手绘颜料。下列关于丙烯(CH3—CH=CH2)的说法正确的是( )
A.丙烯分子中3个碳原子在同一直线上
B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子中不存在非极性键
D.一个丙烯分子中有8个σ键、1个π键
D
大本练习册P9
应用体验
3.科学家在-100 ℃的低温下合成了一种烃X,X分子的球棍模型如图所示。
(1)X的分子式为 。
(2)X分子中每个碳原子均形成4个化学键,则X分子中含有 个σ键,
个π键。
(3)1 mol X在一定条件下可与 mol H2发生反应(假设环状结构不变)。
C5H4
10
2
2
大本练习册P9
应用体验
4.相同条件下金属钠和水反应与金属钠和无水乙醇反应相比,前者较为剧烈的原因是( )
A.水是无机物,乙醇是有机化合物
B.水的相对分子质量小,乙醇的相对分子质量大
C.乙醇分子中羟基与乙基相连,受乙基影响,乙醇分子中的羟基不如水分子中的羟基活泼
D.水是电解质,乙醇是非电解质
C
大本练习册P9
应用体验
5.共价键的类型和极性与有机化合物的性质存在紧密联系。下列说法错误的是( )
A.一般仅含σ键的烃易发生取代反应,含有π键的烃易发生加成反应
B.一般共价键极性越强,在反应中越容易发生断裂
C.有机化合物分子中基团之间的相互影响不会影响官能团和物质的性质
D.乙醇分子和水分子中的氧氢键极性不同,所以乙醇和水分别与钠反应的剧烈程度不同
C
戊烷(C5H12)的三种同分异构体的结构。
异戊烷
正戊烷
新戊烷
物质名称 正戊烷 异戊烷 新戊烷
结构简式
相同点
不同点
CH3CH2CH2CH2CH3
(CH3)2CHCH2CH3
C(CH3)4
思考与讨论
分子式相同,化学性质相似
碳骨架不同(碳原子间的连接顺序不同),物理性质不同,支链越多,沸点越低。
1.同分异构现象:
具有相同的分子式,但具有不同的结构的现象。
2.同分异构体:
具有同分异构现象的化合物互为同分异构体。
一般情况下,有机化合物分子中的碳原子数目越多,其同分异构体的数目也越多。
碳原子数 1 2 3 4 5 6 7 8 9 10
同分异体数 1 1 1 2 3 5 9 18 35 75
熟记7个碳以内烷烃对应的同分异构体数:
二、有机化合物的同分异构现象
3.同分异构现象的分类
同分异构现象
构造异构
立体异构
碳架异构
顺反异构
对映异构
位置异构
官能团异构
碳骨架不同
官能团的位置不同
官能团种类不同
CH3—CH2—CH2—CH3
异丁烷
CH3—CH—CH3
CH3
正丁烷
1-丁烯
2-丁烯
CH2=CH—CH2—CH3
1
2
3
4
CH3—CH=CH—CH3
1
2
3
4
Cl
Cl
Cl
Cl
Cl
Cl
邻二氯苯
间二氯苯
对二氯苯
H—C—C—OH
H
H
H
H
H—C—O—C—H
H
H
H
H
乙醇
二甲醚
4.构造异构现象的书写
(1)碳架异构
主链由长到短,
支链由整到散,
位置由心到边,
排布对邻间。
减碳法
【尝试应用】1.写出C6H14的所有同分异构体的结构简式
(1)确定碳链
(2)补写氢原子
①最多碳,成直链
②摘一碳,挂中间;往边排,不到端
C—C—C—C—C
C—C—C—C—C
C
C
等效碳不重排
CH3—CH2—CH—CH2—CH3
CH3
CH3—CH—CH2—CH2—CH3
CH3
主链由长到短,
支链由整到散,
位置由心到边,
排布对邻间。
甲基不能连接在主链的两端
(1)确定碳链
(2)补写氢原子
从主链上取下来的碳原子数,要少于主链所剩碳原子数。
③摘两碳,整到散;两支链,对邻间
C—C—C—C
C
C
C—C—C—C
C
C
CH3—C—CH2—CH3
CH3
CH3
CH3—CH—CH—CH3
CH3
CH3
乙基不能连接在主链第二位碳
(2)位置异构
先写出具有此C原子数的烷烃的碳架异构,再根据碳链的对称性,将官能团插入碳链中,最后用氢原子补足碳的四个价键。
。
①插入法(适用于烯烃、炔烃、酯等)
【尝试应用】2.书写烯烃C4H8的同分异构体。
C-C-C-C
C-C-C
C
碳链异构
位置异构
C=C-C-C
C- C = C-C
C=C-C
C
CH3- CH = CH-CH3
CH2 = CH- CH2-CH3
CH2=C-CH3
CH3
②等效氢法(适用于一元醇、一元卤代烃)
(2)位置异构
一元取代物的种类数=等效氢的种类数
①同一碳原子上的氢原子等效;
②同一碳原子上所连接甲基上的氢原子等效;
CH3
CH3-C-CH3
CH3
③处于对称位置上的氢原子等效
CH3CH2CH2CH2CH3
① ② ③ ② ①
b
b
b
b
a
a
a
a
②等效氢法(适用于一元醇、一元卤代烃)
先写出与给定烷基的碳原子数相同的烷烃的碳架异构,再判断等效氢的种类数。
(2)位置异构
一元取代物的种类数=等效氢的种类数
【尝试应用】3.书写分子式C5H12O的醇的同分异构体。
熟记:
-C3H7 2种
-C4H9 4种
-C5H11 8种
(2)位置异构
③定一移一法(适用于二元取代物)
【尝试应用】4.书写分子式C7H7Cl含苯环的同分异构体。
(3)官能团异构
序号
类别
通式
1
单烯烃
环烷烃
2
炔烃
二烯烃
3
饱和一元脂肪醇
饱和醚
4
饱和一元脂肪醛
酮
5
饱和羧酸
酯
CnH2n
CnH2n-2
CnH2n+2O
CnH2nO
CnH2nO2
常见的官能团异构
思路:先官能团异构,再碳架异构,最后位置异构
(1)官能团异构
【尝试应用】5.分子式为C3H8O的所有有机化合物。
(2)碳架异构
(3) 位置异构(用↑表示羟基(-OH)或 “-O-”的连接位置)
C-C -C
↑
↑
C-C -C
↑
醇
醚
一般按碳架异构→位置异构→官能团异构的顺序书写。
例:(以C4H10O为例且只写出骨架与官能团)
①碳架异构
C—C—C—C
②位置异构
③官能团异构
C—O—C—C—C
C—C—O—C—C
4.构造异构现象的书写
二、有机化合物的同分异构现象
同分异构现象
构造异构
立体异构
碳架异构
顺反异构
对映异构
位置异构
官能团异构
降碳对称法
插入法
通式相同的物质
等效氢法
烯烃部分继续学习
手性碳原子的判断
定一移一法
大本练习册P10
应用体验
1.已知下列有机化合物:
大本练习册P10
应用体验
(1)其中互为同分异构体的是 。
(2)其中属于碳架异构的是 。
(3)其中属于位置异构的是 。
(4)其中属于官能团异构的是 。
(5)其中属于同一种物质的是 。
①②③④⑦⑧
①
②
③④⑦⑧
⑤
大本练习册P10
应用体验
2.试写出分子式为C4H8且属于烯烃的同分异构体的结构简式。
大本练习册P10
应用体验
3.试写出分子式为C4H9Cl的同分异构体的结构简式。
第一章 有机化合物的结构特点与研究方法
第一节 有机化合物的结构特点
第2课时 有机化合物中的共价键 同分异构现象
【温故知新】
在有机化合物分子中,碳原子通过共用电子对与其他原子相连接形成不同类型的共价键,共价键的类型和极性对有机化合物的性质有很大的影响。你还记得共价键可以怎样分类吗?
【思考与讨论】请同学们从以上三个分类角度分析甲烷、乙烯的化学键类型。
共价键
极性键
非极性键
共价键
单键
三键
双键
共价键
σ键
π键
一、有机化合物中的共价键
甲烷
极性键
4个碳氢单键
4个σ键
sp3杂化
甲烷分子中的σ键
C原子的4个sp3杂化轨道与4个H原子的1s轨道以“头碰头”的形式重叠形成。
如何形成?
1、共价键的类型
乙烯
含极性键 和 非极性键
4个碳氢单键 和 1个碳碳双键
5个σ键 1个π键
sp2杂化
σ键
π键
乙烯分子中的σ键和π键
如何形成?
C原子2个sp2杂化轨道与H原子的1s轨道及另一个C原子的sp2杂化轨道以“头碰头”的形式重叠形成σ键; C原子未参与杂化的p轨道以“肩并肩”的形式重叠形成π键。
一、认识有机化合物中的共价键
【思考与交流】分析乙炔中的化学键类型,并从化学键的角度解释甲烷、乙烯、乙炔在性质上的差异性。
甲烷分子中含有C—H σ键,能发生取代反应;乙烯和乙炔分子的双键和三键中含有π键,它们都能发生加成反应。
含极性键 和 非极性键
2个碳氢单键 和 1个碳碳三键
3个σ键 2个π键
(1)一般情况下,有机化合物中的单键是σ键,双键中含有一个σ键和一个π键,三键中含有一个σ键和两个π键。
(3)共价键类型与反应类型密切相关。
(2)π键与σ键的轨道重叠程度不同,所以强度不同,一般π键稳定性更弱。通过σ键连接的原子或原子团可以绕键轴旋转,通过π键连接的原子或原子团不能绕键轴旋转。
【小结】有机化合物中的共价键
(4)有机化合物的结构特点
与碳原子相连的原子数 4 3 2
碳原子的成键方式
碳原子的杂化方式
空间构型
C=
—C≡
sp3杂化
sp2杂化
sp杂化
四面体
平面形
直线形
由于不同的成键原子间电负性的差异,共用电子对会发生偏移。成键原子间电负性差异越大,共价键极性越强,在反应中越容易发生断裂。因此有机化合物的官能团及其邻近的化学键往往是发生化学反应的活性部位。
【思考与交流】如何理解共价键的极性?共价键的极性强弱与化学键的稳定性有什么关系?
实验1-1
向两只分别盛有蒸馏水和无水乙醇的烧杯中各加入同样大小的钠(约绿豆大),观察现象。
实验1-1
水和钠 无水乙醇和钠
实验原理
实验现象
剧烈程度
剧烈程度:H2O>CH3CH2OH
2Na+2H2O=2NaOH+H2↑
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
浮、熔、游、响、红
钠沉入底部,有气体产生,最终钠粒消失,液体仍为无色透明。
2、共价键的极性与有机反应
1、为什么乙醇与钠能发生反应放出氢气?
原因在于乙醇分子中的氢氧键极性较强,能够发生断裂
2、同样条件下,为什么乙醇与钠的反应没有水与钠的反应剧烈?
这是由于受乙基的影响,乙醇分子中氢氧键的极性比水分子中氢氧键的极性弱。
基团之间的相互影响使官能团中化学键的极性发生变化,从而影响官能团和物质的性质。
【思考与交流】
由于羟基中氧原子的电负性较大,乙醇分子中的碳氧键极性也较强,在乙醇与氢溴酸的反应中,碳氧键发生了断裂。
共价键的断裂需要吸收能量,而且有机化合物分子中共价键断裂的位置存在多种可能。相对无机反应,有机反应一般反应速率较小,副反应较多,产物比较复杂。
H—C—C—O—H+H—Br
H
H
H
H
△
H—C—C—Br+H2O
H
H
H
H
2、共价键的极性与有机反应
取代反应
大本练习册P9
应用体验
1.碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如图。下列有关该物质的说法不正确的是( )
A.分子式为C3H4O3
B.分子中σ键与π键个数之比为10∶1
C.分子中既有极性键也有非极性键
D.分子中碳原子的杂化方式全部为sp2杂化
D
大本练习册P9
应用体验
2.丙烯颜料是一种非常方便使用的手绘颜料。下列关于丙烯(CH3—CH=CH2)的说法正确的是( )
A.丙烯分子中3个碳原子在同一直线上
B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子中不存在非极性键
D.一个丙烯分子中有8个σ键、1个π键
D
大本练习册P9
应用体验
3.科学家在-100 ℃的低温下合成了一种烃X,X分子的球棍模型如图所示。
(1)X的分子式为 。
(2)X分子中每个碳原子均形成4个化学键,则X分子中含有 个σ键,
个π键。
(3)1 mol X在一定条件下可与 mol H2发生反应(假设环状结构不变)。
C5H4
10
2
2
大本练习册P9
应用体验
4.相同条件下金属钠和水反应与金属钠和无水乙醇反应相比,前者较为剧烈的原因是( )
A.水是无机物,乙醇是有机化合物
B.水的相对分子质量小,乙醇的相对分子质量大
C.乙醇分子中羟基与乙基相连,受乙基影响,乙醇分子中的羟基不如水分子中的羟基活泼
D.水是电解质,乙醇是非电解质
C
大本练习册P9
应用体验
5.共价键的类型和极性与有机化合物的性质存在紧密联系。下列说法错误的是( )
A.一般仅含σ键的烃易发生取代反应,含有π键的烃易发生加成反应
B.一般共价键极性越强,在反应中越容易发生断裂
C.有机化合物分子中基团之间的相互影响不会影响官能团和物质的性质
D.乙醇分子和水分子中的氧氢键极性不同,所以乙醇和水分别与钠反应的剧烈程度不同
C
戊烷(C5H12)的三种同分异构体的结构。
异戊烷
正戊烷
新戊烷
物质名称 正戊烷 异戊烷 新戊烷
结构简式
相同点
不同点
CH3CH2CH2CH2CH3
(CH3)2CHCH2CH3
C(CH3)4
思考与讨论
分子式相同,化学性质相似
碳骨架不同(碳原子间的连接顺序不同),物理性质不同,支链越多,沸点越低。
1.同分异构现象:
具有相同的分子式,但具有不同的结构的现象。
2.同分异构体:
具有同分异构现象的化合物互为同分异构体。
一般情况下,有机化合物分子中的碳原子数目越多,其同分异构体的数目也越多。
碳原子数 1 2 3 4 5 6 7 8 9 10
同分异体数 1 1 1 2 3 5 9 18 35 75
熟记7个碳以内烷烃对应的同分异构体数:
二、有机化合物的同分异构现象
3.同分异构现象的分类
同分异构现象
构造异构
立体异构
碳架异构
顺反异构
对映异构
位置异构
官能团异构
碳骨架不同
官能团的位置不同
官能团种类不同
CH3—CH2—CH2—CH3
异丁烷
CH3—CH—CH3
CH3
正丁烷
1-丁烯
2-丁烯
CH2=CH—CH2—CH3
1
2
3
4
CH3—CH=CH—CH3
1
2
3
4
Cl
Cl
Cl
Cl
Cl
Cl
邻二氯苯
间二氯苯
对二氯苯
H—C—C—OH
H
H
H
H
H—C—O—C—H
H
H
H
H
乙醇
二甲醚
4.构造异构现象的书写
(1)碳架异构
主链由长到短,
支链由整到散,
位置由心到边,
排布对邻间。
减碳法
【尝试应用】1.写出C6H14的所有同分异构体的结构简式
(1)确定碳链
(2)补写氢原子
①最多碳,成直链
②摘一碳,挂中间;往边排,不到端
C—C—C—C—C
C—C—C—C—C
C
C
等效碳不重排
CH3—CH2—CH—CH2—CH3
CH3
CH3—CH—CH2—CH2—CH3
CH3
主链由长到短,
支链由整到散,
位置由心到边,
排布对邻间。
甲基不能连接在主链的两端
(1)确定碳链
(2)补写氢原子
从主链上取下来的碳原子数,要少于主链所剩碳原子数。
③摘两碳,整到散;两支链,对邻间
C—C—C—C
C
C
C—C—C—C
C
C
CH3—C—CH2—CH3
CH3
CH3
CH3—CH—CH—CH3
CH3
CH3
乙基不能连接在主链第二位碳
(2)位置异构
先写出具有此C原子数的烷烃的碳架异构,再根据碳链的对称性,将官能团插入碳链中,最后用氢原子补足碳的四个价键。
。
①插入法(适用于烯烃、炔烃、酯等)
【尝试应用】2.书写烯烃C4H8的同分异构体。
C-C-C-C
C-C-C
C
碳链异构
位置异构
C=C-C-C
C- C = C-C
C=C-C
C
CH3- CH = CH-CH3
CH2 = CH- CH2-CH3
CH2=C-CH3
CH3
②等效氢法(适用于一元醇、一元卤代烃)
(2)位置异构
一元取代物的种类数=等效氢的种类数
①同一碳原子上的氢原子等效;
②同一碳原子上所连接甲基上的氢原子等效;
CH3
CH3-C-CH3
CH3
③处于对称位置上的氢原子等效
CH3CH2CH2CH2CH3
① ② ③ ② ①
b
b
b
b
a
a
a
a
②等效氢法(适用于一元醇、一元卤代烃)
先写出与给定烷基的碳原子数相同的烷烃的碳架异构,再判断等效氢的种类数。
(2)位置异构
一元取代物的种类数=等效氢的种类数
【尝试应用】3.书写分子式C5H12O的醇的同分异构体。
熟记:
-C3H7 2种
-C4H9 4种
-C5H11 8种
(2)位置异构
③定一移一法(适用于二元取代物)
【尝试应用】4.书写分子式C7H7Cl含苯环的同分异构体。
(3)官能团异构
序号
类别
通式
1
单烯烃
环烷烃
2
炔烃
二烯烃
3
饱和一元脂肪醇
饱和醚
4
饱和一元脂肪醛
酮
5
饱和羧酸
酯
CnH2n
CnH2n-2
CnH2n+2O
CnH2nO
CnH2nO2
常见的官能团异构
思路:先官能团异构,再碳架异构,最后位置异构
(1)官能团异构
【尝试应用】5.分子式为C3H8O的所有有机化合物。
(2)碳架异构
(3) 位置异构(用↑表示羟基(-OH)或 “-O-”的连接位置)
C-C -C
↑
↑
C-C -C
↑
醇
醚
一般按碳架异构→位置异构→官能团异构的顺序书写。
例:(以C4H10O为例且只写出骨架与官能团)
①碳架异构
C—C—C—C
②位置异构
③官能团异构
C—O—C—C—C
C—C—O—C—C
4.构造异构现象的书写
二、有机化合物的同分异构现象
同分异构现象
构造异构
立体异构
碳架异构
顺反异构
对映异构
位置异构
官能团异构
降碳对称法
插入法
通式相同的物质
等效氢法
烯烃部分继续学习
手性碳原子的判断
定一移一法
大本练习册P10
应用体验
1.已知下列有机化合物:
大本练习册P10
应用体验
(1)其中互为同分异构体的是 。
(2)其中属于碳架异构的是 。
(3)其中属于位置异构的是 。
(4)其中属于官能团异构的是 。
(5)其中属于同一种物质的是 。
①②③④⑦⑧
①
②
③④⑦⑧
⑤
大本练习册P10
应用体验
2.试写出分子式为C4H8且属于烯烃的同分异构体的结构简式。
大本练习册P10
应用体验
3.试写出分子式为C4H9Cl的同分异构体的结构简式。
