4.1 原子结构与元素周期表 同步练习题(含解析) 2023-2024学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 4.1 原子结构与元素周期表 同步练习题(含解析) 2023-2024学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 188.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-27 00:00:00 | ||
图片预览


文档简介
4.1 原子结构与元素周期表 同步练习题
一、选择题
1.下列说法错误的是
A.元素在自然界中的存在形式有原子、分子或离子
B.在化学变化中,分子可以再分,离子和原子不可以再分
C.同一种元素可能有多种不同原子,同一种原子也可能形成不同的离子
D.酸性氧化物不一定是非金属氧化物
2.元素周期律和周期表对化学研究有一定的指导作用,人们运用周期律,在周期表中一定的区域内寻找特定性质的物质,下列有关研究方向的叙述错误的是
A.在主族金属元素中寻找耐高温的合金材料
B.在过渡金属元素中寻找化工生产中的高效催化剂
C.非金属元素的化合物进行研究合成新农药
D.在金属与非金属的分界线附近寻找新型的半导体材料
3.下列表示不正确的是
A.氯离子结构示意图: B.I的中子数是:74
C.镁原子结构示意图: D.明矾化学式:KAl(SO4)2
4.医学界通过标记的发现了一种的羧酸衍生物,这种羧酸衍生物在特定条件下可以通过断裂DNA抑制艾滋病毒的繁殖。下列有关的说法正确的是
A.与互为同位素 B.原子核内中子数为6
C.、、属于不同的核素 D.、互为同素异形体
5.2020年11月,我国发射的“嫦娥五号”飞船成功着陆月球,据科学家推测,月球的土壤吸附着数百万吨的,在地球上复元素主要以的形式存在,下列有关和的说法正确的是
A.属于同一种核素 B.比少一个质子
C.与互为同素异形体 D.和互为同位素
6.下列元素中,属于第三周期的是
A.H B.N C.O D.Cl
7.某元素原子的结构示意图如下,下列关于该元素的说法不正确的是
A.元素符号是K B.属于金属元素
C.在化学反应中易失电子 D.位于元素周期表第四周期第ⅡA族
8.分类法是学习化学的重要方法。下列物质或变化不能按照对应的分类标准归类的是
选项 物质或变化 分类标准
A 、、CaO 碱性氧化物
B 石墨、金刚石、 同素异形体
C ,、 碳酸盐
D 钢铁生锈、食物变质、纸张燃烧 化学变化
A.A B.B C.C D.D
二、非选择题
9.回答下列问题
(1)1.204×1024个CO2分子的摩尔质量是 。
(2)用NA表示阿伏加德罗常数的值,则0.3 mol HF中所含质子数与 个CH4中所含质子数相等。
10.碘元素的一种核素可用于治疗肿瘤。该核素的质子数为 ,中子数为 ,质量数为 ,核外电子数为 。
11.下表是元素周期表的一部分,针对所给的元素,完成下列各小题。
主族 周期 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2 C N O
3 Na Al Si S Cl
(1)第3周期中金属性最强的元素是 (填元素名称) 。
(2)C、N和O原子半径由小到大的顺序的是 。
(3)第3周期中气态氢化物最稳定的是 (填化学式) 。
(4)Si是带来人类文明的重要元素之一,其氧化物化学式是 。
(5)铝是大自然赐予人类的宝物。它的一个用途是发生铝热反应,冶炼某些难熔金属,写出与Fe2O3反应的化学方程式 。
(6)S元素形成的氢化物与其氧化物相遇后的现象是 。
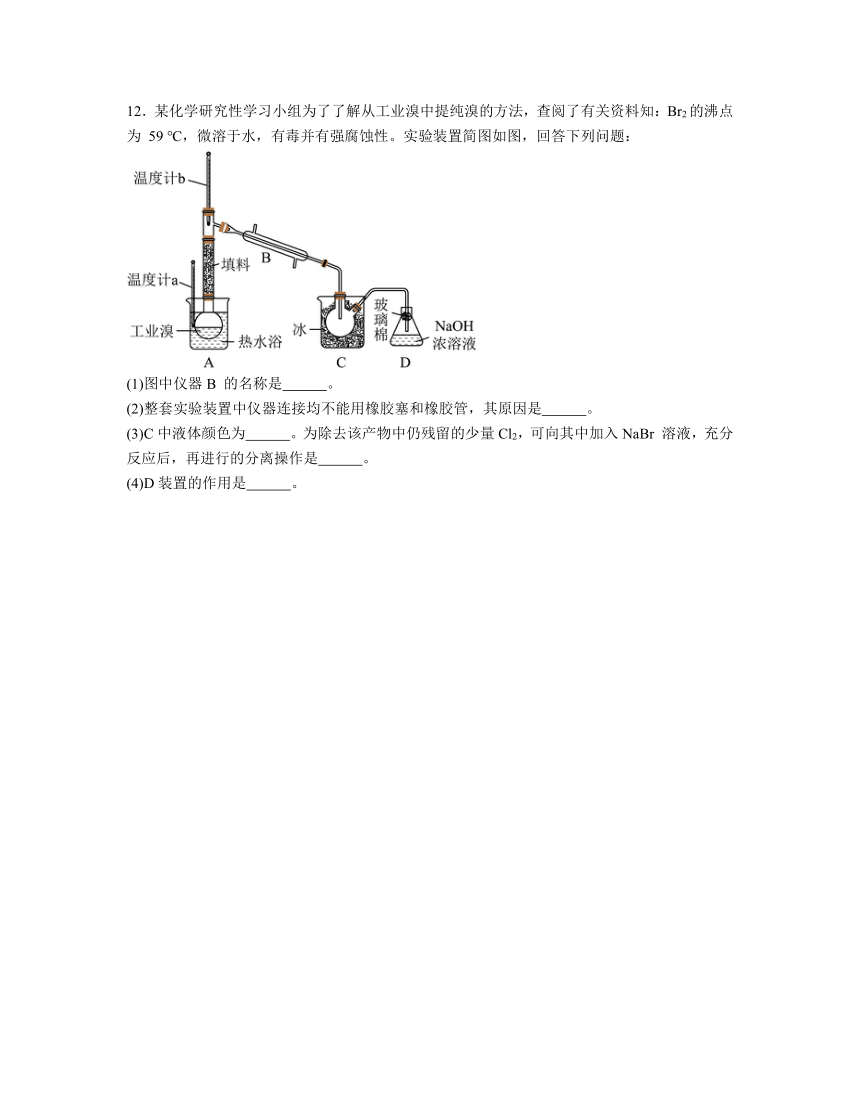
12.某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为 59 ℃,微溶于水,有毒并有强腐蚀性。实验装置简图如图,回答下列问题:
(1)图中仪器B 的名称是 。
(2)整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 。
(3)C中液体颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr 溶液,充分反应后,再进行的分离操作是 。
(4)D装置的作用是 。
【参考答案】
一、选择题
1.B
解析:A.元素在自然界中的存在形式有原子、分子或离子,A正确;
B.化学变化中分子可以再分,原子不能再分,B错误;
C.同一种元素可能有多种不同原子,如氢元素存在3种同位素,同一种原子也可能形成不同的离子,如铁有二价和三价铁离子,C正确;
D.Mn2O7为金属氧化物,是酸性氧化物,D正确;
故选B。
2.A
解析:A.在过渡金属元素中寻找耐高温的合金材料,A错误;
B.在过渡金属元素中有些元素具有良好的催化性能,在此寻找化工生产中的高效催化剂,B正确;
C.第ⅤA、ⅥA、ⅦA族的一些非金属元素可用于制取农药,故可以对非金属元素的化合物进行研究合成新农药,C正确;
D.在金属与非金属的分界线附近元素有的具有良好的半导体性能,故在此寻找新型的半导体材料大,D正确;
故选A。
3.D
解析:A.氯离子核电荷数为17,核外电子分三层、分别为2、8、8个, 氯离子结构示意图正确,A正确;
B. I的中子数是127-53=74,B正确;
C.镁原子核电荷数为12,核外电子分三层、分别为2、8、2个,镁原子结构示意图正确,C正确;
D. 明矾为结晶水合物,化学式:KAl(SO4)2·12H2O,D不正确;
答案选D。
4.C
解析:A.质子数相同而中子数不同的同一元素的不同原子互称为同位素,14C与14N不互为同位素,A错误;
B.14C原子核内中子数为14-6=8,B错误;
C.核素是指具有一定数目质子和一定数目中子的一种原子,12C、13C、14C属于不同的核素,C正确;
D.14C60、12C60是碳元素的同种单质,D错误;
故选C。
5.D
解析:A. 质子数相同、中子数不同,是同种元素的不同核素,A错误;
B. 比的质子均为2,中子数=质量数-质子数,比的中子数少1,B错误;
C.同种元素的不同单质互为同素异形体,与为两种核素、氦由单原子直接构成,但对应的气体均为氦气、不互为同素异形体,C错误;
D. 和质子数相同、中子数不同,是同种元素的不同核素,互称为同位素,D正确;
答案选D。
6.D
解析:A.H原子序数是1,属于第一周期,A错误;
B.N原子序数是7,属于第二周期,B错误;
C.O原子序数是8,属于第二周期,C错误;
D.Cl原子序数是17,属于第三周期,D正确;
故选D。
7.D
【分析】某元素原子的结构示意图为,该元素为K;据此分析解题。
解析:A.据分析可知,该元素元素符号是K,故A正确;
B.K属于金属元素,故B正确;
C.K最外层只有一个电子,在化学反应中易失电子,故C正确;
D.K位于元素周期表第四周期第ⅠA族,故D错误;
故答案选D。
8.A
解析:A.属于酸性氧化物,故A错误;
B.石墨、金刚石、均为碳元素形成的单质,互为同素异形体,故B正确;
C.,、都是由碳酸根和金属阳离子形成的盐,均属于碳酸盐,故C正确;
D.钢铁生锈、食物变质、纸张燃烧的过程中均有新物质生成,均属于化学变化,故D正确;
故答案选A。
二、非选择题
9.(1)44 g mol-1
(2)0.3NA
解析:(1)二氧化碳的摩尔质量是以g/mol为单位,在数值上等于其相对分子质量,即为44 g mol-1,与二氧化碳的多少无关;
(2)氟化氢和甲烷分子中都含有10个质子,故0.3 mol HF中所含质子数0.3molCH4中所含质子数相等,即0.3NA。
10.72 125 53
解析:核素符合左下角为质子数、左上角为质量数,则该核素的质子数为53,中子数=质量数-质子数=125-53=72,质量数为125,核外电子数等于质子数=53。
11.Na O<N<C HCl SiO2 2Al+ Fe2O3 Al2O3 +2Fe 有淡黄色沉淀生成
解析:(1)同周期元素,从左到右元素的金属性依次减弱,则第3周期中金属性最强的元素是Na元素,故答案为:Na;
(2) 同周期元素,从左到右原子半径依次减小,C、N和O原子半径由小到大的顺序为O<N<C,故答案为:O<N<C;
(3)元素的非金属性越强,氢化物的稳定性越强,同周期元素,从左到右非金属性依次增强,则第3周期中气态氢化物最稳定的是HCl,故答案为:HCl;
(4)Si元素的氧化物为二氧化硅,化学式为SiO2,故答案为:SiO2;
(5)铝与氧化铁在高温下发生铝热反应生成铁和氧化铝,反应的化学方程式为2Al+ Fe2O3 Al2O3 +2Fe,故答案为:2Al+ Fe2O3 Al2O3 +2Fe;
(6)具有还原性的氢硫酸溶液与具有氧化性的二氧化硫反应生成硫和水,反应中有淡黄色沉淀生成,故答案为:有淡黄色沉淀生成。
12.冷凝管 溴具有强腐蚀性,可以腐蚀橡胶 深红棕色 蒸馏 吸收溴蒸气,防止污染环境
解析:(1)图中仪器B的名称是冷凝管,故答案为:冷凝管;
(2)溴具有强腐蚀性,会腐蚀橡胶,故答案为:溴具有强腐蚀性,可以腐蚀橡胶;
(3)C中收集到大量的液溴,液溴为深红棕色液体,产物中残留少量Cl2,加入NaBr溶液,充分反应(2NaBr+ Cl2=2NaCl +Br2),此时得到大量的液溴和氯化钠的水溶液,由于二者沸点相差很大,采用蒸馏进行分离提纯,故答案为:深红棕色;蒸馏;
(4)溴易挥发且有毒,可用NaOH溶液吸收溴蒸汽,防止污染环境,故答案为:吸收溴蒸气,防止污染环境
一、选择题
1.下列说法错误的是
A.元素在自然界中的存在形式有原子、分子或离子
B.在化学变化中,分子可以再分,离子和原子不可以再分
C.同一种元素可能有多种不同原子,同一种原子也可能形成不同的离子
D.酸性氧化物不一定是非金属氧化物
2.元素周期律和周期表对化学研究有一定的指导作用,人们运用周期律,在周期表中一定的区域内寻找特定性质的物质,下列有关研究方向的叙述错误的是
A.在主族金属元素中寻找耐高温的合金材料
B.在过渡金属元素中寻找化工生产中的高效催化剂
C.非金属元素的化合物进行研究合成新农药
D.在金属与非金属的分界线附近寻找新型的半导体材料
3.下列表示不正确的是
A.氯离子结构示意图: B.I的中子数是:74
C.镁原子结构示意图: D.明矾化学式:KAl(SO4)2
4.医学界通过标记的发现了一种的羧酸衍生物,这种羧酸衍生物在特定条件下可以通过断裂DNA抑制艾滋病毒的繁殖。下列有关的说法正确的是
A.与互为同位素 B.原子核内中子数为6
C.、、属于不同的核素 D.、互为同素异形体
5.2020年11月,我国发射的“嫦娥五号”飞船成功着陆月球,据科学家推测,月球的土壤吸附着数百万吨的,在地球上复元素主要以的形式存在,下列有关和的说法正确的是
A.属于同一种核素 B.比少一个质子
C.与互为同素异形体 D.和互为同位素
6.下列元素中,属于第三周期的是
A.H B.N C.O D.Cl
7.某元素原子的结构示意图如下,下列关于该元素的说法不正确的是
A.元素符号是K B.属于金属元素
C.在化学反应中易失电子 D.位于元素周期表第四周期第ⅡA族
8.分类法是学习化学的重要方法。下列物质或变化不能按照对应的分类标准归类的是
选项 物质或变化 分类标准
A 、、CaO 碱性氧化物
B 石墨、金刚石、 同素异形体
C ,、 碳酸盐
D 钢铁生锈、食物变质、纸张燃烧 化学变化
A.A B.B C.C D.D
二、非选择题
9.回答下列问题
(1)1.204×1024个CO2分子的摩尔质量是 。
(2)用NA表示阿伏加德罗常数的值,则0.3 mol HF中所含质子数与 个CH4中所含质子数相等。
10.碘元素的一种核素可用于治疗肿瘤。该核素的质子数为 ,中子数为 ,质量数为 ,核外电子数为 。
11.下表是元素周期表的一部分,针对所给的元素,完成下列各小题。
主族 周期 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2 C N O
3 Na Al Si S Cl
(1)第3周期中金属性最强的元素是 (填元素名称) 。
(2)C、N和O原子半径由小到大的顺序的是 。
(3)第3周期中气态氢化物最稳定的是 (填化学式) 。
(4)Si是带来人类文明的重要元素之一,其氧化物化学式是 。
(5)铝是大自然赐予人类的宝物。它的一个用途是发生铝热反应,冶炼某些难熔金属,写出与Fe2O3反应的化学方程式 。
(6)S元素形成的氢化物与其氧化物相遇后的现象是 。
12.某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为 59 ℃,微溶于水,有毒并有强腐蚀性。实验装置简图如图,回答下列问题:
(1)图中仪器B 的名称是 。
(2)整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 。
(3)C中液体颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr 溶液,充分反应后,再进行的分离操作是 。
(4)D装置的作用是 。
【参考答案】
一、选择题
1.B
解析:A.元素在自然界中的存在形式有原子、分子或离子,A正确;
B.化学变化中分子可以再分,原子不能再分,B错误;
C.同一种元素可能有多种不同原子,如氢元素存在3种同位素,同一种原子也可能形成不同的离子,如铁有二价和三价铁离子,C正确;
D.Mn2O7为金属氧化物,是酸性氧化物,D正确;
故选B。
2.A
解析:A.在过渡金属元素中寻找耐高温的合金材料,A错误;
B.在过渡金属元素中有些元素具有良好的催化性能,在此寻找化工生产中的高效催化剂,B正确;
C.第ⅤA、ⅥA、ⅦA族的一些非金属元素可用于制取农药,故可以对非金属元素的化合物进行研究合成新农药,C正确;
D.在金属与非金属的分界线附近元素有的具有良好的半导体性能,故在此寻找新型的半导体材料大,D正确;
故选A。
3.D
解析:A.氯离子核电荷数为17,核外电子分三层、分别为2、8、8个, 氯离子结构示意图正确,A正确;
B. I的中子数是127-53=74,B正确;
C.镁原子核电荷数为12,核外电子分三层、分别为2、8、2个,镁原子结构示意图正确,C正确;
D. 明矾为结晶水合物,化学式:KAl(SO4)2·12H2O,D不正确;
答案选D。
4.C
解析:A.质子数相同而中子数不同的同一元素的不同原子互称为同位素,14C与14N不互为同位素,A错误;
B.14C原子核内中子数为14-6=8,B错误;
C.核素是指具有一定数目质子和一定数目中子的一种原子,12C、13C、14C属于不同的核素,C正确;
D.14C60、12C60是碳元素的同种单质,D错误;
故选C。
5.D
解析:A. 质子数相同、中子数不同,是同种元素的不同核素,A错误;
B. 比的质子均为2,中子数=质量数-质子数,比的中子数少1,B错误;
C.同种元素的不同单质互为同素异形体,与为两种核素、氦由单原子直接构成,但对应的气体均为氦气、不互为同素异形体,C错误;
D. 和质子数相同、中子数不同,是同种元素的不同核素,互称为同位素,D正确;
答案选D。
6.D
解析:A.H原子序数是1,属于第一周期,A错误;
B.N原子序数是7,属于第二周期,B错误;
C.O原子序数是8,属于第二周期,C错误;
D.Cl原子序数是17,属于第三周期,D正确;
故选D。
7.D
【分析】某元素原子的结构示意图为,该元素为K;据此分析解题。
解析:A.据分析可知,该元素元素符号是K,故A正确;
B.K属于金属元素,故B正确;
C.K最外层只有一个电子,在化学反应中易失电子,故C正确;
D.K位于元素周期表第四周期第ⅠA族,故D错误;
故答案选D。
8.A
解析:A.属于酸性氧化物,故A错误;
B.石墨、金刚石、均为碳元素形成的单质,互为同素异形体,故B正确;
C.,、都是由碳酸根和金属阳离子形成的盐,均属于碳酸盐,故C正确;
D.钢铁生锈、食物变质、纸张燃烧的过程中均有新物质生成,均属于化学变化,故D正确;
故答案选A。
二、非选择题
9.(1)44 g mol-1
(2)0.3NA
解析:(1)二氧化碳的摩尔质量是以g/mol为单位,在数值上等于其相对分子质量,即为44 g mol-1,与二氧化碳的多少无关;
(2)氟化氢和甲烷分子中都含有10个质子,故0.3 mol HF中所含质子数0.3molCH4中所含质子数相等,即0.3NA。
10.72 125 53
解析:核素符合左下角为质子数、左上角为质量数,则该核素的质子数为53,中子数=质量数-质子数=125-53=72,质量数为125,核外电子数等于质子数=53。
11.Na O<N<C HCl SiO2 2Al+ Fe2O3 Al2O3 +2Fe 有淡黄色沉淀生成
解析:(1)同周期元素,从左到右元素的金属性依次减弱,则第3周期中金属性最强的元素是Na元素,故答案为:Na;
(2) 同周期元素,从左到右原子半径依次减小,C、N和O原子半径由小到大的顺序为O<N<C,故答案为:O<N<C;
(3)元素的非金属性越强,氢化物的稳定性越强,同周期元素,从左到右非金属性依次增强,则第3周期中气态氢化物最稳定的是HCl,故答案为:HCl;
(4)Si元素的氧化物为二氧化硅,化学式为SiO2,故答案为:SiO2;
(5)铝与氧化铁在高温下发生铝热反应生成铁和氧化铝,反应的化学方程式为2Al+ Fe2O3 Al2O3 +2Fe,故答案为:2Al+ Fe2O3 Al2O3 +2Fe;
(6)具有还原性的氢硫酸溶液与具有氧化性的二氧化硫反应生成硫和水,反应中有淡黄色沉淀生成,故答案为:有淡黄色沉淀生成。
12.冷凝管 溴具有强腐蚀性,可以腐蚀橡胶 深红棕色 蒸馏 吸收溴蒸气,防止污染环境
解析:(1)图中仪器B的名称是冷凝管,故答案为:冷凝管;
(2)溴具有强腐蚀性,会腐蚀橡胶,故答案为:溴具有强腐蚀性,可以腐蚀橡胶;
(3)C中收集到大量的液溴,液溴为深红棕色液体,产物中残留少量Cl2,加入NaBr溶液,充分反应(2NaBr+ Cl2=2NaCl +Br2),此时得到大量的液溴和氯化钠的水溶液,由于二者沸点相差很大,采用蒸馏进行分离提纯,故答案为:深红棕色;蒸馏;
(4)溴易挥发且有毒,可用NaOH溶液吸收溴蒸汽,防止污染环境,故答案为:吸收溴蒸气,防止污染环境
