沪教版化学九上层级提分练1.2.2 物质的组成与构成 物质的用途制法(含解析)
文档属性
| 名称 | 沪教版化学九上层级提分练1.2.2 物质的组成与构成 物质的用途制法(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 208.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-27 00:00:00 | ||
图片预览




文档简介
1.2.2 物质的组成与结构 物质的用途与制法
【基础训练】
1.空气中含量较多且化学性质不活泼的气体是( )
A.氮气 B.氧气 C.水蒸气 D.二氧化碳
2.空气中含很多成分,其中含量较少,常用作保护气的是( )
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
3.下列物质的用途主要利用其化学性质的是( )
A.钨用于造灯泡中的灯丝 B.金刚石可用来裁玻璃
C.氢气用于填充探空气球 D.碳素墨水用于书写档案
4.关于测定空气中氧气含量的实验,下列说法正确的是( )
A.实验前止水夹没有夹紧
B.将红磷换成木炭进行实验
C.待装置冷却至室温后,再打开止水夹
D.点燃红磷缓慢伸入集气瓶中后,再塞紧瓶塞
【能力提升】
1.下列物质的用途主要利用其化学性质的是( )
A.钨用于造灯泡中的灯丝 B.金刚石可用来裁玻璃
C.氢气用于填充探空气球 D.碳素墨水用于书写档案
2.下列物质的用途主要利用其物理性质的是( )
A.酒精用作燃料 B.石墨用作电极
C.小苏打用于治疗胃酸过多 D.熟石灰用来改良酸性土壤
3.空气是一种复杂的混合物,含有氮气、氧气、二氧化碳、稀有气体等成分,下列说法错误的是( )
A.氧气可用于化工生产、航空航天、医疗急救等领域
B.医疗上可在液氮冷冻麻醉条件下做手术
C.因为二氧化碳能与水反应生成碳酸,所以二氧化碳能造成酸雨
D.庆祝节假日时,美丽的霓虹灯与稀有气体的应用有关
4.下列实验装置中不能用来测定空气中氧气含量的是( )
A. B.
C. D.
5.研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置。请根据图示实验回答下列问题:
(1)闭合电源开关,可以观察到白磷 。
(2)装置冷却到室温时,可观察到U型管内左侧液面 。
(3)通过这个实验得出的结论是 。
(4)此实验还可推知反应后剩余气体的两点性质是: 。
(5)评价优点: 。
【拓展培优】
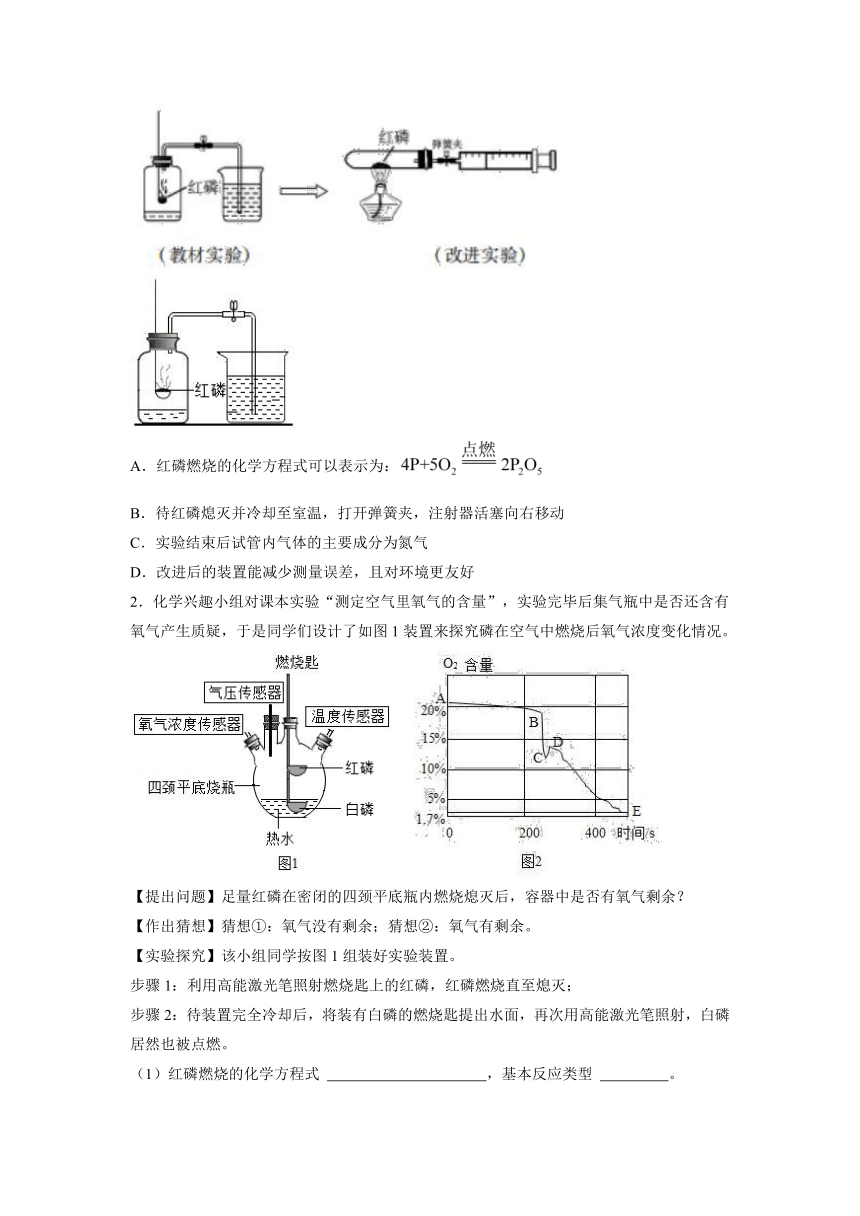
1.为测定空气中氧气的含量,某同学将教材实验进行改进,改进后的实验装置如图所示,(部分夹持装置已忽略),实验时引燃红磷后便熄灭酒精灯。下列有关改进实验的说法不正确的是( )
A.红磷燃烧的化学方程式可以表示为:
B.待红磷熄灭并冷却至室温,打开弹簧夹,注射器活塞向右移动
C.实验结束后试管内气体的主要成分为氮气
D.改进后的装置能减少测量误差,且对环境更友好
2.化学兴趣小组对课本实验“测定空气里氧气的含量”,实验完毕后集气瓶中是否还含有氧气产生质疑,于是同学们设计了如图1装置来探究磷在空气中燃烧后氧气浓度变化情况。
【提出问题】足量红磷在密闭的四颈平底瓶内燃烧熄灭后,容器中是否有氧气剩余?
【作出猜想】猜想①:氧气没有剩余;猜想②:氧气有剩余。
【实验探究】该小组同学按图1组装好实验装置。
步骤1:利用高能激光笔照射燃烧匙上的红磷,红磷燃烧直至熄灭;
步骤2:待装置完全冷却后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被点燃。
(1)红磷燃烧的化学方程式 ,基本反应类型 。
(2)兴趣小组通过实验分析思考,得出了“不同物质燃烧,需要的氧气浓度不一样”的结论由此联想到课本实验: (填物质名称)在空气中不能燃烧,但在氧气中剧烈燃烧、火星四射。
(3)图2是该小组同学从开始实验到最后装置冷却后的整个实验过程中,用传感器测量容器内氧气浓度变化的曲线图;在图2中 (填“A、B、C、D、E”)点时红磷燃烧熄灭;白磷开始燃烧至燃烧结束对应的曲线为 段(用图2中字母表示)。
【实验结论】
(4)根据上述实验现象及数据分析,得出结论如下:猜想 正确。
【拓展延伸】
(5)红磷燃烧产物P2O5与瓶底的热水发生反应,生成磷酸(H3PO4),其反应的化学方程式为 。
【反思与评价】
(6)课本上用红磷燃烧的方法 (填“能”或“不能”)精确地测量空气中氧气的含量,理由是 。
答案解析
【基础训练】
1.空气中含量较多且化学性质不活泼的气体是( )
A.氮气 B.氧气 C.水蒸气 D.二氧化碳
【答案】A
【解析】空气是一种天然资源,混合均匀,相对稳定,氮气在空气中含量较多,在常温下化学性质极不活泼,一般不与其他物质发生化学反应。
故选A。
2.空气中含很多成分,其中含量较少,常用作保护气的是( )
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
【答案】D
【解析】空气中含很多成分,常用作保护气是氮气和稀有气体,且含量较少的是稀有气体;
答案:D。
3.下列物质的用途主要利用其化学性质的是( )
A.钨用于造灯泡中的灯丝 B.金刚石可用来裁玻璃
C.氢气用于填充探空气球 D.碳素墨水用于书写档案
【答案】D
【解析】A.钨用于造灯泡中的灯丝,是利用钨熔点高的物理性质,此选项不符合题意;
B.金刚石可用来裁玻璃,是利用金刚石硬度大的物理性质,此选项不符合题意;
C.氢气用于填充探空气球,是利用氢气密度小的物理性质,此选项不符合题意;
D.碳素墨水用于书写档案,是利用碳常温下化学性质稳定的化学性质,此选项符合题意。
故选D。
4.关于测定空气中氧气含量的实验,下列说法正确的是( )
A.实验前止水夹没有夹紧
B.将红磷换成木炭进行实验
C.待装置冷却至室温后,再打开止水夹
D.点燃红磷缓慢伸入集气瓶中后,再塞紧瓶塞
【答案】C
【解析】
A.若做该实验时,止水夹没有夹紧,会使集气瓶内的空气受热通过导管进入空气中,因此集气瓶内的气体减少的量包括消耗的氧气及逸出的空气,会使瓶内的气体比实际氧气减少的多,因此会使水倒流超过五分之一,造成结果偏大,此选项错误;
B.木炭在空气中燃烧生成二氧化碳气体,虽然能除去氧气,但却增加了新的气体,没有形成压强差,不能用来测定空气中氧气含量,此选项错误;
C.待装置冷却至室温后才能打开止水夹,以防止剩余的气体在受热状态下,处于膨胀状态,占据了部分水的体积,造成结果偏小,此选项正确;
D.点燃后的红磷必须迅速伸入集气瓶中,塞紧瓶塞,否则瓶内气体逸出,造成实验误差,此选项错误。
故选C。
【能力提升】
1.下列物质的用途主要利用其化学性质的是( )
A.钨用于造灯泡中的灯丝 B.金刚石可用来裁玻璃
C.氢气用于填充探空气球 D.碳素墨水用于书写档案
【答案】D
【解析】A.钨用于造灯泡中的灯丝,是利用钨熔点高的物理性质,此选项不符合题意;
B.金刚石可用来裁玻璃,是利用金刚石硬度大的物理性质,此选项不符合题意;
C.氢气用于填充探空气球,是利用氢气密度小的物理性质,此选项不符合题意;
D.碳素墨水用于书写档案,是利用碳常温下化学性质稳定的化学性质,此选项符合题意。
故选D。
2.下列物质的用途主要利用其物理性质的是( )
A.酒精用作燃料 B.石墨用作电极
C.小苏打用于治疗胃酸过多 D.熟石灰用来改良酸性土壤
【答案】B
【解析】A.酒精用作燃料是因为酒精能燃烧,可溶性属于酒精的化学性质,不符合题意;
B.石墨能导电故石墨用作电极,能导电是石墨的物理性质,符合题意;
C.小苏打用于治疗胃酸过多,是利用小苏打即碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,利用了其化学性质,不符合题意;
D.熟石灰用来改良酸性土壤是利用熟石灰能与酸发生中和反应,利用了其化学性质,不符合题意;
答案为:B。
3.空气是一种复杂的混合物,含有氮气、氧气、二氧化碳、稀有气体等成分,下列说法错误的是( )
A.氧气可用于化工生产、航空航天、医疗急救等领域
B.医疗上可在液氮冷冻麻醉条件下做手术
C.因为二氧化碳能与水反应生成碳酸,所以二氧化碳能造成酸雨
D.庆祝节假日时,美丽的霓虹灯与稀有气体的应用有关
【答案】C
【解析】A.氧气具有支持燃烧的性质,可用于化工生产、航空航天、医疗急救等领域,故说法正确;
B.氮气可以制造低温环境,可用于医疗上可在液氨冷冻麻醉条件下做手术,故说法正确;
C.二氧化碳能与水反应生成碳酸,二氧化碳能制作碳酸饮料,二氧化硫溶于水并与水发生反应生成亚硫酸,二氧化硫能造成酸雨,故说法错误;
D.稀有气体在通电条件下发出各种颜色的光源,所以美丽的霓虹灯与稀有气体的应用有关,故说法正确。
故选C。
4.下列实验装置中不能用来测定空气中氧气含量的是( )
A. B.
C. D.
【答案】C
【解析】
在装有空气的密闭容器中,欲用燃烧法测定空气中氧气含量,该实验一般要注意以下几点:①装置的气密性好;②所用药品必须是足量;③读数时一定要冷却到原温度;④所选除氧剂要具备以下特征:本身能够在空气中燃烧;本身的状态为非气体;生成的物质为非气态;据此进行分析判断。
A.图中所示装置,红磷燃烧消耗氧气使装置内气体体积减少,压强减小,能用于测定空气中氧气含量,故选项错误;
B.图中所示装置,用凸透镜引燃红磷,红磷燃烧消耗氧气使装置内气体体积减少,压强减小,能用于测定空气中氧气含量,故选项错误;
C.木炭在空气中燃烧生成二氧化碳气体或者一氧化碳气体甚至是两者的混合气体,虽除去氧气,而增加了新的气体,不能用来测定空气中氧气含量,故选项正确;
D.热水提供的热量引燃白磷,白磷燃烧消耗氧气使装置内气体体积减少,压强减小,使活塞左移,能用于测定空气中氧气含量,故选项错误。
故选:C。
5.研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置。请根据图示实验回答下列问题:
(1)闭合电源开关,可以观察到白磷 。
(2)装置冷却到室温时,可观察到U型管内左侧液面 。
(3)通过这个实验得出的结论是 。
(4)此实验还可推知反应后剩余气体的两点性质是: 。
(5)评价优点: 。
【答案】燃烧,产生白烟,放热;上升至1刻度处;氧气约占空气总体积的五分之一;难溶于水,不能燃烧也不支持燃烧;实验结果更准确、更环保。
【解析】(1)闭合电源开关,可以观察到白磷燃烧,产生白烟,放热。
故填:燃烧,产生白烟,放热。
(2)装置冷却到室温时,可观察到U型管内左侧液面上升至1刻度处。
故填:上升至1刻度处。
(3)通过这个实验得出的结论是氧气约占空气总体积的五分之一。
故填:氧气约占空气总体积的五分之一。
(4)此实验还可推知反应后剩余气体的两点性质是难溶于水,不能燃烧、也不支持燃烧。
故填:难溶于水,不能燃烧也不支持燃烧。
(5)优点是防止了燃烧匙伸入集气瓶中时导致的部分气体受热膨胀逸出,实验结果更准确,同时防止了反应生成的五氧化二磷扩散到空气中污染环境。
故填:实验结果更准确、更环保。
【拓展培优】
1.为测定空气中氧气的含量,某同学将教材实验进行改进,改进后的实验装置如图所示,(部分夹持装置已忽略),实验时引燃红磷后便熄灭酒精灯。下列有关改进实验的说法不正确的是( )
A.红磷燃烧的化学方程式可以表示为:
B.待红磷熄灭并冷却至室温,打开弹簧夹,注射器活塞向右移动
C.实验结束后试管内气体的主要成分为氮气
D.改进后的装置能减少测量误差,且对环境更友好
【答案】B
【解析】A.红磷燃烧的化学方程式可以表示为:,正确;
B.待红磷熄灭并冷却至室温,打开弹簧夹,注射器内压强变小,所以注射器活塞向左移动,选项错误;
C.实验结束后试管内气体的主要成分为氮气,氧气与红磷反应,正确;
D.改进后的装置能减少测量误差,且对环境更友好,正确。
故选:B。
2.化学兴趣小组对课本实验“测定空气里氧气的含量”,实验完毕后集气瓶中是否还含有氧气产生质疑,于是同学们设计了如图1装置来探究磷在空气中燃烧后氧气浓度变化情况。
【提出问题】足量红磷在密闭的四颈平底瓶内燃烧熄灭后,容器中是否有氧气剩余?
【作出猜想】猜想①:氧气没有剩余;猜想②:氧气有剩余。
【实验探究】该小组同学按图1组装好实验装置。
步骤1:利用高能激光笔照射燃烧匙上的红磷,红磷燃烧直至熄灭;
步骤2:待装置完全冷却后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被点燃。
(1)红磷燃烧的化学方程式 ,基本反应类型 。
(2)兴趣小组通过实验分析思考,得出了“不同物质燃烧,需要的氧气浓度不一样”的结论由此联想到课本实验: (填物质名称)在空气中不能燃烧,但在氧气中剧烈燃烧、火星四射。
(3)图2是该小组同学从开始实验到最后装置冷却后的整个实验过程中,用传感器测量容器内氧气浓度变化的曲线图;在图2中 (填“A、B、C、D、E”)点时红磷燃烧熄灭;白磷开始燃烧至燃烧结束对应的曲线为 段(用图2中字母表示)。
【实验结论】
(4)根据上述实验现象及数据分析,得出结论如下:猜想 正确。
【拓展延伸】
(5)红磷燃烧产物P2O5与瓶底的热水发生反应,生成磷酸(H3PO4),其反应的化学方程式为 。
【反思与评价】
(6)课本上用红磷燃烧的方法 (填“能”或“不能”)精确地测量空气中氧气的含量,理由是 。
【答案】(1)4P+5O22P2O5;化合反应 (2)铁。(3)C;D﹣E。(4)②。
(5)P2O5+3H2O(热)=2H3PO4。(6)不能;红磷不能把集气瓶中的氧气耗尽。
【解析】磷燃烧只能够消耗空气中的氧气,氧气消耗后,容器中的气压减小,在外界大气压作用下,水进入容器,进入容器中的水的体积即为容器中空气中的氧气体积,进一步可以计算出空气中氧气的含量。
磷燃烧能够消耗空气中的氧气,氧气消耗后,容器中的气压减小,在外界大气压作用下,容器内体积减小,减少的体积即为容器中空气中的氧气体积,进一步可以计算出空气中氧气的含量。
(1)红磷燃烧的化学方程式:4P+5O22P2O5,基本反应类型是化合反应。
故答案为:4P+5O22P2O5;化合反应。
(2)铁在空气中不能燃烧,但在氧气中剧烈燃烧、火星四射。故答案为:铁。
(3)在图2中C点时红磷燃烧熄灭;白磷开始燃烧至燃烧结束对应的曲线为D﹣E段。
故答案为:C;D﹣E。
(4)根据上述实验现象及数据分析,得出结论如下:猜想②正确。故答案为:②。
(5)红磷燃烧产物P2O5与瓶底的热水发生反应,生成磷酸(H3PO4),其反应的化学方程式为:P2O5+3H2O(热)=2H3PO4。故答案为:P2O5+3H2O(热)=2H3PO4。
(6)课本上用红磷燃烧的方法不能精确地测量空气中氧气的含量,理由是红磷不能把集气瓶中的氧气耗尽。
故答案为:不能;红磷不能把集气瓶中的氧气耗尽。
【基础训练】
1.空气中含量较多且化学性质不活泼的气体是( )
A.氮气 B.氧气 C.水蒸气 D.二氧化碳
2.空气中含很多成分,其中含量较少,常用作保护气的是( )
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
3.下列物质的用途主要利用其化学性质的是( )
A.钨用于造灯泡中的灯丝 B.金刚石可用来裁玻璃
C.氢气用于填充探空气球 D.碳素墨水用于书写档案
4.关于测定空气中氧气含量的实验,下列说法正确的是( )
A.实验前止水夹没有夹紧
B.将红磷换成木炭进行实验
C.待装置冷却至室温后,再打开止水夹
D.点燃红磷缓慢伸入集气瓶中后,再塞紧瓶塞
【能力提升】
1.下列物质的用途主要利用其化学性质的是( )
A.钨用于造灯泡中的灯丝 B.金刚石可用来裁玻璃
C.氢气用于填充探空气球 D.碳素墨水用于书写档案
2.下列物质的用途主要利用其物理性质的是( )
A.酒精用作燃料 B.石墨用作电极
C.小苏打用于治疗胃酸过多 D.熟石灰用来改良酸性土壤
3.空气是一种复杂的混合物,含有氮气、氧气、二氧化碳、稀有气体等成分,下列说法错误的是( )
A.氧气可用于化工生产、航空航天、医疗急救等领域
B.医疗上可在液氮冷冻麻醉条件下做手术
C.因为二氧化碳能与水反应生成碳酸,所以二氧化碳能造成酸雨
D.庆祝节假日时,美丽的霓虹灯与稀有气体的应用有关
4.下列实验装置中不能用来测定空气中氧气含量的是( )
A. B.
C. D.
5.研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置。请根据图示实验回答下列问题:
(1)闭合电源开关,可以观察到白磷 。
(2)装置冷却到室温时,可观察到U型管内左侧液面 。
(3)通过这个实验得出的结论是 。
(4)此实验还可推知反应后剩余气体的两点性质是: 。
(5)评价优点: 。
【拓展培优】
1.为测定空气中氧气的含量,某同学将教材实验进行改进,改进后的实验装置如图所示,(部分夹持装置已忽略),实验时引燃红磷后便熄灭酒精灯。下列有关改进实验的说法不正确的是( )
A.红磷燃烧的化学方程式可以表示为:
B.待红磷熄灭并冷却至室温,打开弹簧夹,注射器活塞向右移动
C.实验结束后试管内气体的主要成分为氮气
D.改进后的装置能减少测量误差,且对环境更友好
2.化学兴趣小组对课本实验“测定空气里氧气的含量”,实验完毕后集气瓶中是否还含有氧气产生质疑,于是同学们设计了如图1装置来探究磷在空气中燃烧后氧气浓度变化情况。
【提出问题】足量红磷在密闭的四颈平底瓶内燃烧熄灭后,容器中是否有氧气剩余?
【作出猜想】猜想①:氧气没有剩余;猜想②:氧气有剩余。
【实验探究】该小组同学按图1组装好实验装置。
步骤1:利用高能激光笔照射燃烧匙上的红磷,红磷燃烧直至熄灭;
步骤2:待装置完全冷却后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被点燃。
(1)红磷燃烧的化学方程式 ,基本反应类型 。
(2)兴趣小组通过实验分析思考,得出了“不同物质燃烧,需要的氧气浓度不一样”的结论由此联想到课本实验: (填物质名称)在空气中不能燃烧,但在氧气中剧烈燃烧、火星四射。
(3)图2是该小组同学从开始实验到最后装置冷却后的整个实验过程中,用传感器测量容器内氧气浓度变化的曲线图;在图2中 (填“A、B、C、D、E”)点时红磷燃烧熄灭;白磷开始燃烧至燃烧结束对应的曲线为 段(用图2中字母表示)。
【实验结论】
(4)根据上述实验现象及数据分析,得出结论如下:猜想 正确。
【拓展延伸】
(5)红磷燃烧产物P2O5与瓶底的热水发生反应,生成磷酸(H3PO4),其反应的化学方程式为 。
【反思与评价】
(6)课本上用红磷燃烧的方法 (填“能”或“不能”)精确地测量空气中氧气的含量,理由是 。
答案解析
【基础训练】
1.空气中含量较多且化学性质不活泼的气体是( )
A.氮气 B.氧气 C.水蒸气 D.二氧化碳
【答案】A
【解析】空气是一种天然资源,混合均匀,相对稳定,氮气在空气中含量较多,在常温下化学性质极不活泼,一般不与其他物质发生化学反应。
故选A。
2.空气中含很多成分,其中含量较少,常用作保护气的是( )
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
【答案】D
【解析】空气中含很多成分,常用作保护气是氮气和稀有气体,且含量较少的是稀有气体;
答案:D。
3.下列物质的用途主要利用其化学性质的是( )
A.钨用于造灯泡中的灯丝 B.金刚石可用来裁玻璃
C.氢气用于填充探空气球 D.碳素墨水用于书写档案
【答案】D
【解析】A.钨用于造灯泡中的灯丝,是利用钨熔点高的物理性质,此选项不符合题意;
B.金刚石可用来裁玻璃,是利用金刚石硬度大的物理性质,此选项不符合题意;
C.氢气用于填充探空气球,是利用氢气密度小的物理性质,此选项不符合题意;
D.碳素墨水用于书写档案,是利用碳常温下化学性质稳定的化学性质,此选项符合题意。
故选D。
4.关于测定空气中氧气含量的实验,下列说法正确的是( )
A.实验前止水夹没有夹紧
B.将红磷换成木炭进行实验
C.待装置冷却至室温后,再打开止水夹
D.点燃红磷缓慢伸入集气瓶中后,再塞紧瓶塞
【答案】C
【解析】
A.若做该实验时,止水夹没有夹紧,会使集气瓶内的空气受热通过导管进入空气中,因此集气瓶内的气体减少的量包括消耗的氧气及逸出的空气,会使瓶内的气体比实际氧气减少的多,因此会使水倒流超过五分之一,造成结果偏大,此选项错误;
B.木炭在空气中燃烧生成二氧化碳气体,虽然能除去氧气,但却增加了新的气体,没有形成压强差,不能用来测定空气中氧气含量,此选项错误;
C.待装置冷却至室温后才能打开止水夹,以防止剩余的气体在受热状态下,处于膨胀状态,占据了部分水的体积,造成结果偏小,此选项正确;
D.点燃后的红磷必须迅速伸入集气瓶中,塞紧瓶塞,否则瓶内气体逸出,造成实验误差,此选项错误。
故选C。
【能力提升】
1.下列物质的用途主要利用其化学性质的是( )
A.钨用于造灯泡中的灯丝 B.金刚石可用来裁玻璃
C.氢气用于填充探空气球 D.碳素墨水用于书写档案
【答案】D
【解析】A.钨用于造灯泡中的灯丝,是利用钨熔点高的物理性质,此选项不符合题意;
B.金刚石可用来裁玻璃,是利用金刚石硬度大的物理性质,此选项不符合题意;
C.氢气用于填充探空气球,是利用氢气密度小的物理性质,此选项不符合题意;
D.碳素墨水用于书写档案,是利用碳常温下化学性质稳定的化学性质,此选项符合题意。
故选D。
2.下列物质的用途主要利用其物理性质的是( )
A.酒精用作燃料 B.石墨用作电极
C.小苏打用于治疗胃酸过多 D.熟石灰用来改良酸性土壤
【答案】B
【解析】A.酒精用作燃料是因为酒精能燃烧,可溶性属于酒精的化学性质,不符合题意;
B.石墨能导电故石墨用作电极,能导电是石墨的物理性质,符合题意;
C.小苏打用于治疗胃酸过多,是利用小苏打即碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,利用了其化学性质,不符合题意;
D.熟石灰用来改良酸性土壤是利用熟石灰能与酸发生中和反应,利用了其化学性质,不符合题意;
答案为:B。
3.空气是一种复杂的混合物,含有氮气、氧气、二氧化碳、稀有气体等成分,下列说法错误的是( )
A.氧气可用于化工生产、航空航天、医疗急救等领域
B.医疗上可在液氮冷冻麻醉条件下做手术
C.因为二氧化碳能与水反应生成碳酸,所以二氧化碳能造成酸雨
D.庆祝节假日时,美丽的霓虹灯与稀有气体的应用有关
【答案】C
【解析】A.氧气具有支持燃烧的性质,可用于化工生产、航空航天、医疗急救等领域,故说法正确;
B.氮气可以制造低温环境,可用于医疗上可在液氨冷冻麻醉条件下做手术,故说法正确;
C.二氧化碳能与水反应生成碳酸,二氧化碳能制作碳酸饮料,二氧化硫溶于水并与水发生反应生成亚硫酸,二氧化硫能造成酸雨,故说法错误;
D.稀有气体在通电条件下发出各种颜色的光源,所以美丽的霓虹灯与稀有气体的应用有关,故说法正确。
故选C。
4.下列实验装置中不能用来测定空气中氧气含量的是( )
A. B.
C. D.
【答案】C
【解析】
在装有空气的密闭容器中,欲用燃烧法测定空气中氧气含量,该实验一般要注意以下几点:①装置的气密性好;②所用药品必须是足量;③读数时一定要冷却到原温度;④所选除氧剂要具备以下特征:本身能够在空气中燃烧;本身的状态为非气体;生成的物质为非气态;据此进行分析判断。
A.图中所示装置,红磷燃烧消耗氧气使装置内气体体积减少,压强减小,能用于测定空气中氧气含量,故选项错误;
B.图中所示装置,用凸透镜引燃红磷,红磷燃烧消耗氧气使装置内气体体积减少,压强减小,能用于测定空气中氧气含量,故选项错误;
C.木炭在空气中燃烧生成二氧化碳气体或者一氧化碳气体甚至是两者的混合气体,虽除去氧气,而增加了新的气体,不能用来测定空气中氧气含量,故选项正确;
D.热水提供的热量引燃白磷,白磷燃烧消耗氧气使装置内气体体积减少,压强减小,使活塞左移,能用于测定空气中氧气含量,故选项错误。
故选:C。
5.研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置。请根据图示实验回答下列问题:
(1)闭合电源开关,可以观察到白磷 。
(2)装置冷却到室温时,可观察到U型管内左侧液面 。
(3)通过这个实验得出的结论是 。
(4)此实验还可推知反应后剩余气体的两点性质是: 。
(5)评价优点: 。
【答案】燃烧,产生白烟,放热;上升至1刻度处;氧气约占空气总体积的五分之一;难溶于水,不能燃烧也不支持燃烧;实验结果更准确、更环保。
【解析】(1)闭合电源开关,可以观察到白磷燃烧,产生白烟,放热。
故填:燃烧,产生白烟,放热。
(2)装置冷却到室温时,可观察到U型管内左侧液面上升至1刻度处。
故填:上升至1刻度处。
(3)通过这个实验得出的结论是氧气约占空气总体积的五分之一。
故填:氧气约占空气总体积的五分之一。
(4)此实验还可推知反应后剩余气体的两点性质是难溶于水,不能燃烧、也不支持燃烧。
故填:难溶于水,不能燃烧也不支持燃烧。
(5)优点是防止了燃烧匙伸入集气瓶中时导致的部分气体受热膨胀逸出,实验结果更准确,同时防止了反应生成的五氧化二磷扩散到空气中污染环境。
故填:实验结果更准确、更环保。
【拓展培优】
1.为测定空气中氧气的含量,某同学将教材实验进行改进,改进后的实验装置如图所示,(部分夹持装置已忽略),实验时引燃红磷后便熄灭酒精灯。下列有关改进实验的说法不正确的是( )
A.红磷燃烧的化学方程式可以表示为:
B.待红磷熄灭并冷却至室温,打开弹簧夹,注射器活塞向右移动
C.实验结束后试管内气体的主要成分为氮气
D.改进后的装置能减少测量误差,且对环境更友好
【答案】B
【解析】A.红磷燃烧的化学方程式可以表示为:,正确;
B.待红磷熄灭并冷却至室温,打开弹簧夹,注射器内压强变小,所以注射器活塞向左移动,选项错误;
C.实验结束后试管内气体的主要成分为氮气,氧气与红磷反应,正确;
D.改进后的装置能减少测量误差,且对环境更友好,正确。
故选:B。
2.化学兴趣小组对课本实验“测定空气里氧气的含量”,实验完毕后集气瓶中是否还含有氧气产生质疑,于是同学们设计了如图1装置来探究磷在空气中燃烧后氧气浓度变化情况。
【提出问题】足量红磷在密闭的四颈平底瓶内燃烧熄灭后,容器中是否有氧气剩余?
【作出猜想】猜想①:氧气没有剩余;猜想②:氧气有剩余。
【实验探究】该小组同学按图1组装好实验装置。
步骤1:利用高能激光笔照射燃烧匙上的红磷,红磷燃烧直至熄灭;
步骤2:待装置完全冷却后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被点燃。
(1)红磷燃烧的化学方程式 ,基本反应类型 。
(2)兴趣小组通过实验分析思考,得出了“不同物质燃烧,需要的氧气浓度不一样”的结论由此联想到课本实验: (填物质名称)在空气中不能燃烧,但在氧气中剧烈燃烧、火星四射。
(3)图2是该小组同学从开始实验到最后装置冷却后的整个实验过程中,用传感器测量容器内氧气浓度变化的曲线图;在图2中 (填“A、B、C、D、E”)点时红磷燃烧熄灭;白磷开始燃烧至燃烧结束对应的曲线为 段(用图2中字母表示)。
【实验结论】
(4)根据上述实验现象及数据分析,得出结论如下:猜想 正确。
【拓展延伸】
(5)红磷燃烧产物P2O5与瓶底的热水发生反应,生成磷酸(H3PO4),其反应的化学方程式为 。
【反思与评价】
(6)课本上用红磷燃烧的方法 (填“能”或“不能”)精确地测量空气中氧气的含量,理由是 。
【答案】(1)4P+5O22P2O5;化合反应 (2)铁。(3)C;D﹣E。(4)②。
(5)P2O5+3H2O(热)=2H3PO4。(6)不能;红磷不能把集气瓶中的氧气耗尽。
【解析】磷燃烧只能够消耗空气中的氧气,氧气消耗后,容器中的气压减小,在外界大气压作用下,水进入容器,进入容器中的水的体积即为容器中空气中的氧气体积,进一步可以计算出空气中氧气的含量。
磷燃烧能够消耗空气中的氧气,氧气消耗后,容器中的气压减小,在外界大气压作用下,容器内体积减小,减少的体积即为容器中空气中的氧气体积,进一步可以计算出空气中氧气的含量。
(1)红磷燃烧的化学方程式:4P+5O22P2O5,基本反应类型是化合反应。
故答案为:4P+5O22P2O5;化合反应。
(2)铁在空气中不能燃烧,但在氧气中剧烈燃烧、火星四射。故答案为:铁。
(3)在图2中C点时红磷燃烧熄灭;白磷开始燃烧至燃烧结束对应的曲线为D﹣E段。
故答案为:C;D﹣E。
(4)根据上述实验现象及数据分析,得出结论如下:猜想②正确。故答案为:②。
(5)红磷燃烧产物P2O5与瓶底的热水发生反应,生成磷酸(H3PO4),其反应的化学方程式为:P2O5+3H2O(热)=2H3PO4。故答案为:P2O5+3H2O(热)=2H3PO4。
(6)课本上用红磷燃烧的方法不能精确地测量空气中氧气的含量,理由是红磷不能把集气瓶中的氧气耗尽。
故答案为:不能;红磷不能把集气瓶中的氧气耗尽。
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
