2024北京课改化学九年级下学期课时练--专项素养综合全练(一) 溶解度曲线的应用
文档属性
| 名称 | 2024北京课改化学九年级下学期课时练--专项素养综合全练(一) 溶解度曲线的应用 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-01 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2024北京课改化学九年级下学期
专项素养综合全练(一)
溶解度曲线的应用
1.(2023湖南株洲中考)下图为KNO3和NaCl两种固体的溶解度曲线。下列有关说法正确的是 ( )
①0 ℃时,溶解度:KNO3>NaCl
②t1 ℃时,KNO3和NaCl的溶解度相等
③温度由0 ℃→t1 ℃,NaCl的溶解度逐渐减小
④t2 ℃时,饱和溶液中溶质的质量分数:KNO3>NaCl
A.①② B.②④
C.①③ D.③④
2.(2023海南儋州一中二模)氢氧化钙的溶解度曲线如图所示。下列说法正确的是 ( )
A.氢氧化钙的溶解度随温度升高而增大
B.30 ℃时,100 g水中最多溶解0.15 g氢氧化钙
C.将60 ℃时氢氧化钙的饱和溶液降低温度至20 ℃,有晶体析出
D.将30 ℃时氢氧化钙的饱和溶液升高温度至70 ℃,溶液的溶质质量分数不变
3.(2022广东实验中学期末)打开碳酸饮料的瓶盖,能听到“咝”的一声,有气体冲出,下列图示能解释这个现象的是 ( )
A B
C D
4.(2023新疆中考)碳酸钠和氯化钠的溶解度曲线如下图所示,下列说法错误的是 ( )
A.氯化钠的溶解度随温度升高而增大
B.b点表示t2 ℃时碳酸钠和氯化钠的溶解度相等
C.t1 ℃时,将20 g氯化钠放入50 g水中,充分溶解后得到70 g溶液
D.t3 ℃时,可通过升高温度的方法使接近饱和的碳酸钠溶液变为饱和溶液
5.(2023湖南永州中考)甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )
A.阴影部分的任意点表明甲、乙两种溶液都是饱和溶液
B.P点时,甲、乙两种溶液的溶质质量分数相等
C.t2 ℃时,在100 g水中加入60 g甲,形成不饱和溶液
D.t1 ℃时,将甲、乙的饱和溶液升温至t2 ℃,溶液的溶质质量分数:甲>乙
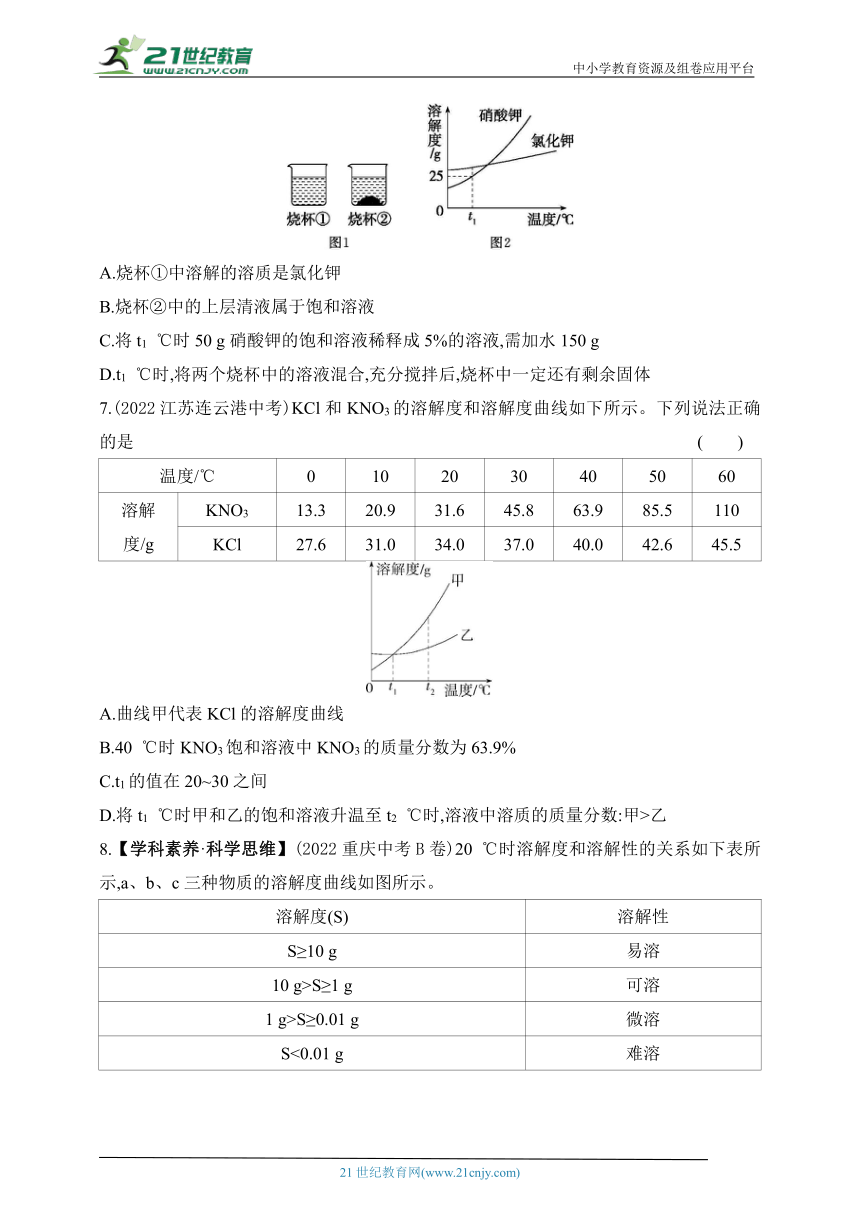
6.(2023山东济宁中考)t1 ℃时,将等质量的硝酸钾和氯化钾分别加入盛有100 g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。下列说法错误的是 ( )
A.烧杯①中溶解的溶质是氯化钾
B.烧杯②中的上层清液属于饱和溶液
C.将t1 ℃时50 g硝酸钾的饱和溶液稀释成5%的溶液,需加水150 g
D.t1 ℃时,将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
7.(2022江苏连云港中考)KCl和KNO3的溶解度和溶解度曲线如下所示。下列说法正确的是 ( )
温度/℃ 0 10 20 30 40 50 60
溶解 度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110
KCl 27.6 31.0 34.0 37.0 40.0 42.6 45.5
A.曲线甲代表KCl的溶解度曲线
B.40 ℃时KNO3饱和溶液中KNO3的质量分数为63.9%
C.t1的值在20~30之间
D.将t1 ℃时甲和乙的饱和溶液升温至t2 ℃时,溶液中溶质的质量分数:甲>乙
8.【学科素养·科学思维】(2022重庆中考B卷)20 ℃时溶解度和溶解性的关系如下表所示,a、b、c三种物质的溶解度曲线如图所示。
溶解度(S) 溶解性
S≥10 g 易溶
10 g>S≥1 g 可溶
1 g>S≥0.01 g 微溶
S<0.01 g 难溶
(1)20 ℃时a、b两物质的溶解性均为 溶。
(2)c在水中的溶解度随温度的变化趋势与 相似(填序号)。
A.KNO3 B.NaCl C.Ca(OH)2
(3)某温度时,将b的饱和溶液升温 (填“一定”或“不一定”)能形成不饱和溶液。
(4)关于a、b溶液说法正确的是 (填序号)。
A.20 ℃时,可配制质量分数为25%的a溶液
B.使60 ℃的a饱和溶液析出晶体的方法不止一种
C.阴影区域(不包括b曲线上的点)对应的b溶液为饱和溶液
答案全解全析
1.B 0 ℃时,溶解度:KNO3NaCl,④正确。
2.B 由题图可知,氢氧化钙的溶解度随温度的升高而减小,A错误;30 ℃时,氢氧化钙的溶解度为0.15 g,即此时100 g水中最多溶解0.15 g氢氧化钙,B正确;氢氧化钙的溶解度随温度的降低而增大,将60 ℃时氢氧化钙的饱和溶液降温,变为不饱和溶液,C错误;将30 ℃时的氢氧化钙饱和溶液升温,会析出晶体,溶液的溶质质量分数减小,D错误。
3.D 打开碳酸饮料的瓶盖,有气体冲出,是因为打开瓶盖时,瓶内的压强减小,二氧化碳气体的溶解度随之减小,二氧化碳逸出。
4.C t1 ℃时氯化钠的溶解度是36 g,将20 g氯化钠放入50 g水中,只能溶解18 g,得到68 g溶液,C错误。
5.B 阴影部分的任意点表明甲溶液是饱和溶液,乙溶液是不饱和溶液,A错误;P点时,甲、乙两种物质的溶解度相等,所以溶液的溶质质量分数相等,B正确;t2 ℃时,甲物质的溶解度小于50 g,所以此时在100 g水中加入60 g甲,固体未完全溶解,形成饱和溶液,C错误;t1 ℃时,甲物质的溶解度小于乙物质的溶解度,饱和溶液的溶质质量分数:甲<乙,甲、乙的饱和溶液升温至t2 ℃,溶质、溶剂质量不变,所以溶液的溶质质量分数仍为甲<乙,D错误。
6.D t1 ℃时,氯化钾的溶解度大于硝酸钾,结合题图1可知,烧杯①中溶解的溶质是氯化钾,A正确;烧杯②中的上层清液属于饱和溶液,B正确;将t1 ℃时50 g硝酸钾的饱和溶液(溶质质量是50 g×=10 g)稀释成5%的溶液,需加水的质量是-50 g=150 g,C正确;t1 ℃时,将两个烧杯中的溶液混合,充分搅拌后,烧杯中没有固体剩余,D错误。
7.C 分析题表中的数据可知,0 ℃时,KCl的溶解度大于KNO3的溶解度,所以曲线乙代表KCl的溶解度曲线,A错误;40 ℃时KNO3的溶解度是63.9 g,其饱和溶液中 KNO3的质量分数为×100%≈39%,B错误;t1 ℃时,甲、乙两物质的溶解度相等,所以t1的值在20~30之间,C正确;t1 ℃时,甲、乙两物质的溶解度相等,甲和乙的饱和溶液的溶质质量分数相等,升温至t2 ℃时,溶质、溶剂质量均不变,所以溶液中溶质的质量分数:甲=乙,D错误。
8.(1)易 (2)C (3)不一定 (4)B
解析 (1)20 ℃时,a和b的溶解度都是25 g,都属于易溶物质。(2)硝酸钾的溶解度随温度的升高而增大;氯化钠的溶解度随温度升高变化不大,但是不会随温度升高而减小;氢氧化钙的溶解度随温度的升高而减小,故选C。(3)b的溶解度随温度升高先增大后减小,因此将b的饱和溶液升温不一定能得到不饱和溶液。(4)20 ℃时,a物质的溶解度为25 g,其饱和溶液的溶质质量分数为×100%=20%,因此不能配制该温度下质量分数为25%的a溶液,A错误;使60 ℃的a饱和溶液析出晶体的方法可以是降低温度或恒温蒸发溶剂,B正确;阴影区域(不包括b曲线上的点)在b曲线以下,因此表示b物质的不饱和溶液,C错误。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024北京课改化学九年级下学期
专项素养综合全练(一)
溶解度曲线的应用
1.(2023湖南株洲中考)下图为KNO3和NaCl两种固体的溶解度曲线。下列有关说法正确的是 ( )
①0 ℃时,溶解度:KNO3>NaCl
②t1 ℃时,KNO3和NaCl的溶解度相等
③温度由0 ℃→t1 ℃,NaCl的溶解度逐渐减小
④t2 ℃时,饱和溶液中溶质的质量分数:KNO3>NaCl
A.①② B.②④
C.①③ D.③④
2.(2023海南儋州一中二模)氢氧化钙的溶解度曲线如图所示。下列说法正确的是 ( )
A.氢氧化钙的溶解度随温度升高而增大
B.30 ℃时,100 g水中最多溶解0.15 g氢氧化钙
C.将60 ℃时氢氧化钙的饱和溶液降低温度至20 ℃,有晶体析出
D.将30 ℃时氢氧化钙的饱和溶液升高温度至70 ℃,溶液的溶质质量分数不变
3.(2022广东实验中学期末)打开碳酸饮料的瓶盖,能听到“咝”的一声,有气体冲出,下列图示能解释这个现象的是 ( )
A B
C D
4.(2023新疆中考)碳酸钠和氯化钠的溶解度曲线如下图所示,下列说法错误的是 ( )
A.氯化钠的溶解度随温度升高而增大
B.b点表示t2 ℃时碳酸钠和氯化钠的溶解度相等
C.t1 ℃时,将20 g氯化钠放入50 g水中,充分溶解后得到70 g溶液
D.t3 ℃时,可通过升高温度的方法使接近饱和的碳酸钠溶液变为饱和溶液
5.(2023湖南永州中考)甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )
A.阴影部分的任意点表明甲、乙两种溶液都是饱和溶液
B.P点时,甲、乙两种溶液的溶质质量分数相等
C.t2 ℃时,在100 g水中加入60 g甲,形成不饱和溶液
D.t1 ℃时,将甲、乙的饱和溶液升温至t2 ℃,溶液的溶质质量分数:甲>乙
6.(2023山东济宁中考)t1 ℃时,将等质量的硝酸钾和氯化钾分别加入盛有100 g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。下列说法错误的是 ( )
A.烧杯①中溶解的溶质是氯化钾
B.烧杯②中的上层清液属于饱和溶液
C.将t1 ℃时50 g硝酸钾的饱和溶液稀释成5%的溶液,需加水150 g
D.t1 ℃时,将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
7.(2022江苏连云港中考)KCl和KNO3的溶解度和溶解度曲线如下所示。下列说法正确的是 ( )
温度/℃ 0 10 20 30 40 50 60
溶解 度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110
KCl 27.6 31.0 34.0 37.0 40.0 42.6 45.5
A.曲线甲代表KCl的溶解度曲线
B.40 ℃时KNO3饱和溶液中KNO3的质量分数为63.9%
C.t1的值在20~30之间
D.将t1 ℃时甲和乙的饱和溶液升温至t2 ℃时,溶液中溶质的质量分数:甲>乙
8.【学科素养·科学思维】(2022重庆中考B卷)20 ℃时溶解度和溶解性的关系如下表所示,a、b、c三种物质的溶解度曲线如图所示。
溶解度(S) 溶解性
S≥10 g 易溶
10 g>S≥1 g 可溶
1 g>S≥0.01 g 微溶
S<0.01 g 难溶
(1)20 ℃时a、b两物质的溶解性均为 溶。
(2)c在水中的溶解度随温度的变化趋势与 相似(填序号)。
A.KNO3 B.NaCl C.Ca(OH)2
(3)某温度时,将b的饱和溶液升温 (填“一定”或“不一定”)能形成不饱和溶液。
(4)关于a、b溶液说法正确的是 (填序号)。
A.20 ℃时,可配制质量分数为25%的a溶液
B.使60 ℃的a饱和溶液析出晶体的方法不止一种
C.阴影区域(不包括b曲线上的点)对应的b溶液为饱和溶液
答案全解全析
1.B 0 ℃时,溶解度:KNO3
2.B 由题图可知,氢氧化钙的溶解度随温度的升高而减小,A错误;30 ℃时,氢氧化钙的溶解度为0.15 g,即此时100 g水中最多溶解0.15 g氢氧化钙,B正确;氢氧化钙的溶解度随温度的降低而增大,将60 ℃时氢氧化钙的饱和溶液降温,变为不饱和溶液,C错误;将30 ℃时的氢氧化钙饱和溶液升温,会析出晶体,溶液的溶质质量分数减小,D错误。
3.D 打开碳酸饮料的瓶盖,有气体冲出,是因为打开瓶盖时,瓶内的压强减小,二氧化碳气体的溶解度随之减小,二氧化碳逸出。
4.C t1 ℃时氯化钠的溶解度是36 g,将20 g氯化钠放入50 g水中,只能溶解18 g,得到68 g溶液,C错误。
5.B 阴影部分的任意点表明甲溶液是饱和溶液,乙溶液是不饱和溶液,A错误;P点时,甲、乙两种物质的溶解度相等,所以溶液的溶质质量分数相等,B正确;t2 ℃时,甲物质的溶解度小于50 g,所以此时在100 g水中加入60 g甲,固体未完全溶解,形成饱和溶液,C错误;t1 ℃时,甲物质的溶解度小于乙物质的溶解度,饱和溶液的溶质质量分数:甲<乙,甲、乙的饱和溶液升温至t2 ℃,溶质、溶剂质量不变,所以溶液的溶质质量分数仍为甲<乙,D错误。
6.D t1 ℃时,氯化钾的溶解度大于硝酸钾,结合题图1可知,烧杯①中溶解的溶质是氯化钾,A正确;烧杯②中的上层清液属于饱和溶液,B正确;将t1 ℃时50 g硝酸钾的饱和溶液(溶质质量是50 g×=10 g)稀释成5%的溶液,需加水的质量是-50 g=150 g,C正确;t1 ℃时,将两个烧杯中的溶液混合,充分搅拌后,烧杯中没有固体剩余,D错误。
7.C 分析题表中的数据可知,0 ℃时,KCl的溶解度大于KNO3的溶解度,所以曲线乙代表KCl的溶解度曲线,A错误;40 ℃时KNO3的溶解度是63.9 g,其饱和溶液中 KNO3的质量分数为×100%≈39%,B错误;t1 ℃时,甲、乙两物质的溶解度相等,所以t1的值在20~30之间,C正确;t1 ℃时,甲、乙两物质的溶解度相等,甲和乙的饱和溶液的溶质质量分数相等,升温至t2 ℃时,溶质、溶剂质量均不变,所以溶液中溶质的质量分数:甲=乙,D错误。
8.(1)易 (2)C (3)不一定 (4)B
解析 (1)20 ℃时,a和b的溶解度都是25 g,都属于易溶物质。(2)硝酸钾的溶解度随温度的升高而增大;氯化钠的溶解度随温度升高变化不大,但是不会随温度升高而减小;氢氧化钙的溶解度随温度的升高而减小,故选C。(3)b的溶解度随温度升高先增大后减小,因此将b的饱和溶液升温不一定能得到不饱和溶液。(4)20 ℃时,a物质的溶解度为25 g,其饱和溶液的溶质质量分数为×100%=20%,因此不能配制该温度下质量分数为25%的a溶液,A错误;使60 ℃的a饱和溶液析出晶体的方法可以是降低温度或恒温蒸发溶剂,B正确;阴影区域(不包括b曲线上的点)在b曲线以下,因此表示b物质的不饱和溶液,C错误。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
