2024北京课改化学九年级下学期课时练--第1课时 盐酸、硫酸
文档属性
| 名称 | 2024北京课改化学九年级下学期课时练--第1课时 盐酸、硫酸 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-01 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2024北京课改化学九年级下学期
第11章 酸与碱
第二节 几种常见的酸
第1课时 盐酸、硫酸
基础过关全练
知识点1 盐酸
1.(2022北京东城二模)人体胃液中含有的物质是 ( )
A.盐酸 B.硫酸
C.氢氧化钠 D.碳酸钠
2.(2022江苏常州一模)浓盐酸露置在空气中,质量会减小,说明浓盐酸具有 ( )
A.酸性 B.吸水性 C.挥发性 D.腐蚀性
3.(2021北京中考)下列物质能除铁锈的是 ( )
A.盐酸 B.植物油
C.NaOH溶液 D.食盐水
4.盐酸在生产和生活中的用途很广,能与多种物质发生反应。下列物质与盐酸反应时,颜色变化不明显的是 ( )
5.【学科素养·化学观念】(2021广东广州越秀二模改编)盐酸是氯化氢气体的水溶液。下列有关说法正确的是 ( )
A.氯化氢气体由H+、Cl-构成
B.将氯化氢气体通入紫色石蕊试液中,石蕊试液变蓝
C.浓盐酸常用做干燥剂
D.工业上常用盐酸除铁锈
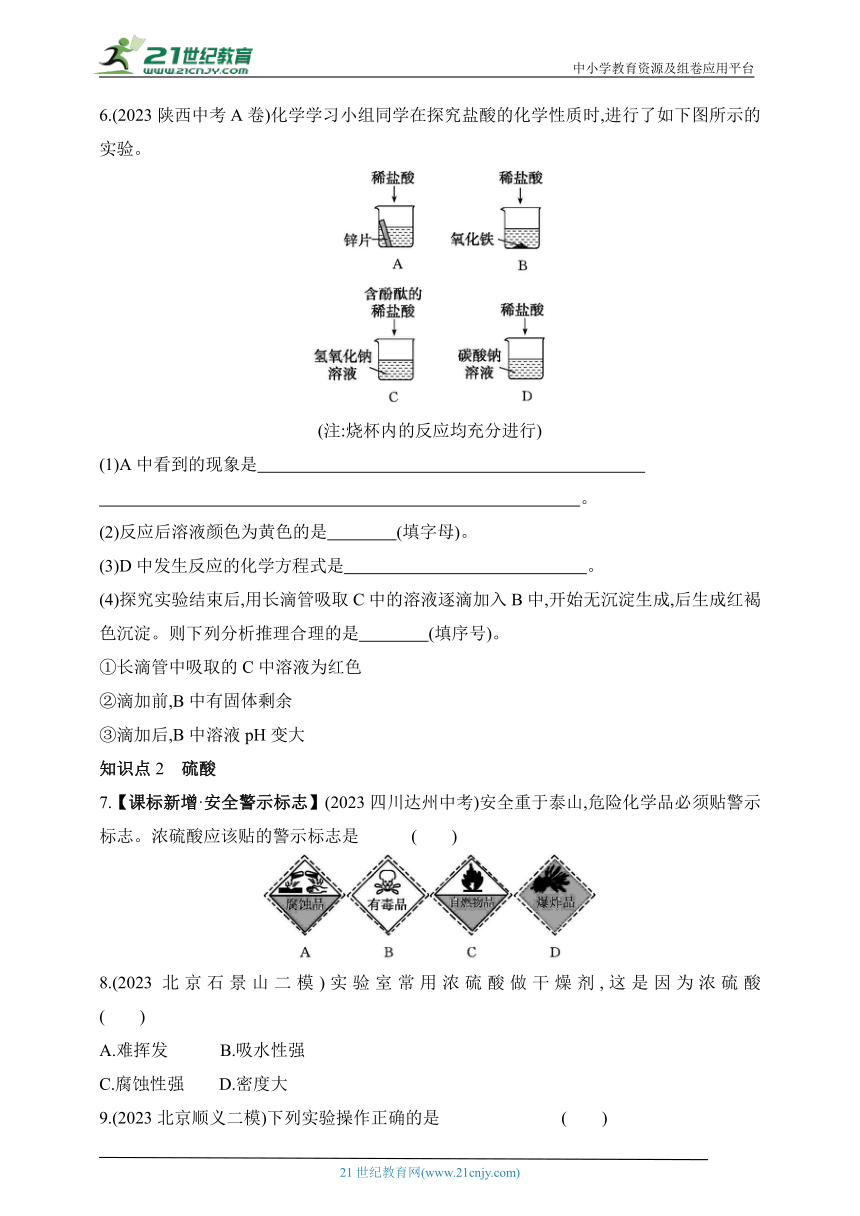
6.(2023陕西中考A卷)化学学习小组同学在探究盐酸的化学性质时,进行了如下图所示的实验。
(注:烧杯内的反应均充分进行)
(1)A中看到的现象是 。
(2)反应后溶液颜色为黄色的是 (填字母)。
(3)D中发生反应的化学方程式是 。
(4)探究实验结束后,用长滴管吸取C中的溶液逐滴加入B中,开始无沉淀生成,后生成红褐色沉淀。则下列分析推理合理的是 (填序号)。
①长滴管中吸取的C中溶液为红色
②滴加前,B中有固体剩余
③滴加后,B中溶液pH变大
知识点2 硫酸
7.【课标新增·安全警示标志】(2023四川达州中考)安全重于泰山,危险化学品必须贴警示标志。浓硫酸应该贴的警示标志是 ( )
8.(2023北京石景山二模)实验室常用浓硫酸做干燥剂,这是因为浓硫酸 ( )
A.难挥发 B.吸水性强
C.腐蚀性强 D.密度大
9.(2023北京顺义二模)下列实验操作正确的是 ( )
10.(2023安徽中考)硫酸是实验室常用的化学试剂。下列有关硫酸的说法,错误的是 ( )
A.稀硫酸和锌反应制取氢气
B.含硫酸的废液可用熟石灰中和处理
C.稀硫酸的密度比水小
D.蘸取浓硫酸的木棍会变黑
11.【教材变式·P57素材】下列试剂中,能区分稀硫酸和稀盐酸的是( )
A.酚酞溶液 B.石蕊溶液
C.NaCl溶液 D.Ba(NO3)2溶液
12.【跨学科·物理】(2023海南海口琼山二模)小军向水槽中缓缓滴加稀硫酸,观察到小灯泡的亮度变化情况:亮→暗→熄→亮。下列说法正确的是 ( )
A.实验中没有白色沉淀生成
B.灯泡熄灭时,水槽中的液体中不存在粒子
C.灯泡亮度发生变化只因为溶液中的H+、OH-的浓度改变
D.将稀硫酸换成稀盐酸观察到灯泡亮度变化情况不相同
13.氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸中的哪种粒子(H2O、H+、S)能使氧化铜溶解。请你和他一起通过Ⅰ、Ⅱ、Ⅲ三个实验完成这次探究活动。
(1)你提出的假设是 。
(2)通过实验Ⅰ可以证明 。
(3)要验证另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅲ中应该加入 。
(4)探究结果为 。你认为除稀硫酸外,还能够溶解氧化铜的一种常见物质是 。
14.(2022北京大兴一模)利用下图装置研究稀硫酸的性质。
(1)能证明H2SO4与NaOH发生反应的现象是 。
(2)试管2中发生反应的化学方程式为 。
(3)试管3反应后所得溶液中一定含有的溶质为 。
答案全解全析
基础过关全练
1.A 人体胃液中含有胃酸,其主要成分是盐酸。
2.C 浓盐酸露置在空气中,质量会减小,是因为浓盐酸具有挥发性。
3.A 铁锈的主要成分Fe2O3属于金属氧化物,能够与盐酸发生反应而被除去;植物油、NaOH溶液、食盐水均不能与铁锈发生反应。
4.C 稀盐酸显酸性,能使紫色石蕊溶液变成红色;氧化铁与盐酸反应生成氯化铁和水,溶液会变黄;稀盐酸与Ca(OH)2溶液反应无明显现象;稀盐酸与铁反应生成氯化亚铁和氢气,溶液变为浅绿色。故选C。
5.D 氯化氢气体是由氯化氢分子构成的,A错误;将氯化氢气体通入紫色石蕊试液中,氯化氢气体溶于水形成盐酸,使紫色石蕊试液变红,B错误;浓盐酸不具有吸水性,不能用做干燥剂,C错误;工业上常用盐酸除铁锈,D正确。
6.(1)锌片表面产生气泡(合理即可) (2)B (3)Na2CO3+2HCl 2NaCl+H2O+CO2↑ (4)①③
解析 (1)锌与稀盐酸反应生成氯化锌和氢气,锌片表面产生气泡,锌片逐渐溶解。(2)氧化铁与稀盐酸反应生成氯化铁和水,溶液颜色为黄色。(3)碳酸钠与盐酸反应生成氯化钠、二氧化碳和水,化学方程式为Na2CO3+2HCl 2NaCl+H2O+CO2↑。(4)实验结束后,用长滴管吸取C中的溶液逐滴加入B中,开始无沉淀生成,后生成红褐色沉淀,说明C中氢氧化钠过量,B中盐酸过量,氢氧化钠先与盐酸反应生成氯化钠和水,后与氯化铁反应生成氢氧化铁红褐色沉淀和氯化钠。C中氢氧化钠过量,溶液显碱性,可使酚酞变红,①正确;B中盐酸过量,氧化铁完全反应,②错误;滴加前,B中盐酸过量,显酸性,滴加后,氢氧化钠与盐酸反应,B中溶液pH变大,③正确。
7.A 浓硫酸有强烈的腐蚀性,属于腐蚀品,故选A。
8.B 浓硫酸具有很强的吸水性,实验室常用浓硫酸做干燥剂,故选B。
9.C 称量固体,应“左物右码”,A错误;加热液体时,应用酒精灯的外焰加热,B错误;稀释浓硫酸时,应把浓硫酸沿器壁缓慢地倒入水中,并用玻璃棒不断搅拌,C正确;不能将pH试纸浸入待测液中,以防污染待测液,D错误。
10.C 稀硫酸的密度比水大。
11.D 加入Ba(NO3)2溶液,有白色沉淀产生的是稀硫酸,无现象的是稀盐酸,故选D。
12.D 硫酸和氢氧化钡反应生成白色沉淀硫酸钡和水,A错误;灯泡熄灭时,硫酸和氢氧化钡恰好完全反应,此时水槽中的液体中只含有水分子,B错误;灯泡亮度发生变化是因为溶液中的氢氧根离子、钡离子、氢离子、硫酸根离子浓度改变,C错误;将稀硫酸换成稀盐酸观察到灯泡亮度变化情况不相同,是因为盐酸和氢氧化钡反应生成氯化钡和水,过程中不产生沉淀,D正确。
13.(1)稀硫酸中的H+使CuO溶解(合理即可) (2)H2O不能使CuO溶解 (3)硫酸钠溶液(合理即可) (4)稀硫酸中的H+可以使CuO溶解 稀盐酸(合理即可)
解析 本实验涉及H2O、H+、S三个变量,通过实验Ⅰ,能得出H2O不能使氧化铜溶解的结论。
(1)试管1中溶液红色褪去
(2)Fe2O3+3H2SO4(SO4)3+3H2O (3)Na2SO4
解析 (1)滴有酚酞的NaOH溶液呈红色,与足量H2SO4反应后,溶液变成无色。(2)稀硫酸与氧化铁反应生成硫酸铁和水,反应的化学方程式为Fe2O3+3H2SO4Fe2(SO4)3+3H2O。(3)试管3中的反应为H2SO4+2NaHCO3Na2SO4+2CO2↑+2H2O。若滴入少量的稀硫酸,NaHCO3未反应完,所得溶液中含有的溶质为Na2SO4、NaHCO3;若两者恰好完全反应,所得溶液中含有的溶质为Na2SO4;若稀硫酸过量,所得溶液中含有的溶质为Na2SO4、H2SO4。故反应后所得溶液中一定含有的溶质为Na2SO4。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024北京课改化学九年级下学期
第11章 酸与碱
第二节 几种常见的酸
第1课时 盐酸、硫酸
基础过关全练
知识点1 盐酸
1.(2022北京东城二模)人体胃液中含有的物质是 ( )
A.盐酸 B.硫酸
C.氢氧化钠 D.碳酸钠
2.(2022江苏常州一模)浓盐酸露置在空气中,质量会减小,说明浓盐酸具有 ( )
A.酸性 B.吸水性 C.挥发性 D.腐蚀性
3.(2021北京中考)下列物质能除铁锈的是 ( )
A.盐酸 B.植物油
C.NaOH溶液 D.食盐水
4.盐酸在生产和生活中的用途很广,能与多种物质发生反应。下列物质与盐酸反应时,颜色变化不明显的是 ( )
5.【学科素养·化学观念】(2021广东广州越秀二模改编)盐酸是氯化氢气体的水溶液。下列有关说法正确的是 ( )
A.氯化氢气体由H+、Cl-构成
B.将氯化氢气体通入紫色石蕊试液中,石蕊试液变蓝
C.浓盐酸常用做干燥剂
D.工业上常用盐酸除铁锈
6.(2023陕西中考A卷)化学学习小组同学在探究盐酸的化学性质时,进行了如下图所示的实验。
(注:烧杯内的反应均充分进行)
(1)A中看到的现象是 。
(2)反应后溶液颜色为黄色的是 (填字母)。
(3)D中发生反应的化学方程式是 。
(4)探究实验结束后,用长滴管吸取C中的溶液逐滴加入B中,开始无沉淀生成,后生成红褐色沉淀。则下列分析推理合理的是 (填序号)。
①长滴管中吸取的C中溶液为红色
②滴加前,B中有固体剩余
③滴加后,B中溶液pH变大
知识点2 硫酸
7.【课标新增·安全警示标志】(2023四川达州中考)安全重于泰山,危险化学品必须贴警示标志。浓硫酸应该贴的警示标志是 ( )
8.(2023北京石景山二模)实验室常用浓硫酸做干燥剂,这是因为浓硫酸 ( )
A.难挥发 B.吸水性强
C.腐蚀性强 D.密度大
9.(2023北京顺义二模)下列实验操作正确的是 ( )
10.(2023安徽中考)硫酸是实验室常用的化学试剂。下列有关硫酸的说法,错误的是 ( )
A.稀硫酸和锌反应制取氢气
B.含硫酸的废液可用熟石灰中和处理
C.稀硫酸的密度比水小
D.蘸取浓硫酸的木棍会变黑
11.【教材变式·P57素材】下列试剂中,能区分稀硫酸和稀盐酸的是( )
A.酚酞溶液 B.石蕊溶液
C.NaCl溶液 D.Ba(NO3)2溶液
12.【跨学科·物理】(2023海南海口琼山二模)小军向水槽中缓缓滴加稀硫酸,观察到小灯泡的亮度变化情况:亮→暗→熄→亮。下列说法正确的是 ( )
A.实验中没有白色沉淀生成
B.灯泡熄灭时,水槽中的液体中不存在粒子
C.灯泡亮度发生变化只因为溶液中的H+、OH-的浓度改变
D.将稀硫酸换成稀盐酸观察到灯泡亮度变化情况不相同
13.氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸中的哪种粒子(H2O、H+、S)能使氧化铜溶解。请你和他一起通过Ⅰ、Ⅱ、Ⅲ三个实验完成这次探究活动。
(1)你提出的假设是 。
(2)通过实验Ⅰ可以证明 。
(3)要验证另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅲ中应该加入 。
(4)探究结果为 。你认为除稀硫酸外,还能够溶解氧化铜的一种常见物质是 。
14.(2022北京大兴一模)利用下图装置研究稀硫酸的性质。
(1)能证明H2SO4与NaOH发生反应的现象是 。
(2)试管2中发生反应的化学方程式为 。
(3)试管3反应后所得溶液中一定含有的溶质为 。
答案全解全析
基础过关全练
1.A 人体胃液中含有胃酸,其主要成分是盐酸。
2.C 浓盐酸露置在空气中,质量会减小,是因为浓盐酸具有挥发性。
3.A 铁锈的主要成分Fe2O3属于金属氧化物,能够与盐酸发生反应而被除去;植物油、NaOH溶液、食盐水均不能与铁锈发生反应。
4.C 稀盐酸显酸性,能使紫色石蕊溶液变成红色;氧化铁与盐酸反应生成氯化铁和水,溶液会变黄;稀盐酸与Ca(OH)2溶液反应无明显现象;稀盐酸与铁反应生成氯化亚铁和氢气,溶液变为浅绿色。故选C。
5.D 氯化氢气体是由氯化氢分子构成的,A错误;将氯化氢气体通入紫色石蕊试液中,氯化氢气体溶于水形成盐酸,使紫色石蕊试液变红,B错误;浓盐酸不具有吸水性,不能用做干燥剂,C错误;工业上常用盐酸除铁锈,D正确。
6.(1)锌片表面产生气泡(合理即可) (2)B (3)Na2CO3+2HCl 2NaCl+H2O+CO2↑ (4)①③
解析 (1)锌与稀盐酸反应生成氯化锌和氢气,锌片表面产生气泡,锌片逐渐溶解。(2)氧化铁与稀盐酸反应生成氯化铁和水,溶液颜色为黄色。(3)碳酸钠与盐酸反应生成氯化钠、二氧化碳和水,化学方程式为Na2CO3+2HCl 2NaCl+H2O+CO2↑。(4)实验结束后,用长滴管吸取C中的溶液逐滴加入B中,开始无沉淀生成,后生成红褐色沉淀,说明C中氢氧化钠过量,B中盐酸过量,氢氧化钠先与盐酸反应生成氯化钠和水,后与氯化铁反应生成氢氧化铁红褐色沉淀和氯化钠。C中氢氧化钠过量,溶液显碱性,可使酚酞变红,①正确;B中盐酸过量,氧化铁完全反应,②错误;滴加前,B中盐酸过量,显酸性,滴加后,氢氧化钠与盐酸反应,B中溶液pH变大,③正确。
7.A 浓硫酸有强烈的腐蚀性,属于腐蚀品,故选A。
8.B 浓硫酸具有很强的吸水性,实验室常用浓硫酸做干燥剂,故选B。
9.C 称量固体,应“左物右码”,A错误;加热液体时,应用酒精灯的外焰加热,B错误;稀释浓硫酸时,应把浓硫酸沿器壁缓慢地倒入水中,并用玻璃棒不断搅拌,C正确;不能将pH试纸浸入待测液中,以防污染待测液,D错误。
10.C 稀硫酸的密度比水大。
11.D 加入Ba(NO3)2溶液,有白色沉淀产生的是稀硫酸,无现象的是稀盐酸,故选D。
12.D 硫酸和氢氧化钡反应生成白色沉淀硫酸钡和水,A错误;灯泡熄灭时,硫酸和氢氧化钡恰好完全反应,此时水槽中的液体中只含有水分子,B错误;灯泡亮度发生变化是因为溶液中的氢氧根离子、钡离子、氢离子、硫酸根离子浓度改变,C错误;将稀硫酸换成稀盐酸观察到灯泡亮度变化情况不相同,是因为盐酸和氢氧化钡反应生成氯化钡和水,过程中不产生沉淀,D正确。
13.(1)稀硫酸中的H+使CuO溶解(合理即可) (2)H2O不能使CuO溶解 (3)硫酸钠溶液(合理即可) (4)稀硫酸中的H+可以使CuO溶解 稀盐酸(合理即可)
解析 本实验涉及H2O、H+、S三个变量,通过实验Ⅰ,能得出H2O不能使氧化铜溶解的结论。
(1)试管1中溶液红色褪去
(2)Fe2O3+3H2SO4(SO4)3+3H2O (3)Na2SO4
解析 (1)滴有酚酞的NaOH溶液呈红色,与足量H2SO4反应后,溶液变成无色。(2)稀硫酸与氧化铁反应生成硫酸铁和水,反应的化学方程式为Fe2O3+3H2SO4Fe2(SO4)3+3H2O。(3)试管3中的反应为H2SO4+2NaHCO3Na2SO4+2CO2↑+2H2O。若滴入少量的稀硫酸,NaHCO3未反应完,所得溶液中含有的溶质为Na2SO4、NaHCO3;若两者恰好完全反应,所得溶液中含有的溶质为Na2SO4;若稀硫酸过量,所得溶液中含有的溶质为Na2SO4、H2SO4。故反应后所得溶液中一定含有的溶质为Na2SO4。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
