2024北京课改化学九年级下学期课时练--第11章综合检测
文档属性
| 名称 | 2024北京课改化学九年级下学期课时练--第11章综合检测 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-01 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2024北京课改化学九年级下学期
第11章·素养综合检测
(满分100分,限时40分钟)
一、选择题(每小题3分,共36分)
1.【新素材·传统习俗】(2023北京中考)重阳赏菊。菊花适合在弱酸性土壤中生长,下列土壤的pH最适合菊花生长的是 ( )
A.6.3 B.8.5 C.8.9 D.9.2
2.(2023北京东城一模)能用于改良酸性土壤的物质是 ( )
A.Ca(OH)2 B.NaCl C.NaOH D.CaCl2
3.(2023云南曲靖二模)植物的汁液可以用做酸碱指示剂,下表是牵牛花浸出液在不同条件下的显色情况,下列溶液中能使牵牛花浸出液变为蓝色的是 ( )
溶液 酸性溶液 中性溶液 碱性溶液
颜色 红色 紫色 蓝色
A.氢氧化钠溶液 B.碳酸
C.稀盐酸 D.硫酸钠溶液
4.食用松花蛋时常感到有涩味,是因为制作过程中用到了熟石灰等原料,为了减轻涩味,可在食用时添加 ( )
A.味精 B.食醋 C.酱油 D.食盐
5.(2023湖南郴州中考)下列图示的实验操作正确的是 ( )
6.(2022浙江嘉兴中考)一瓶存放较长时间的石灰水,瓶内壁附有一层白膜,下列有关说法错误的是 ( )
A.白膜都是氢氧化钙
B.白膜的形成与二氧化碳有关
C.白膜可用盐酸除去
D.试剂使用后应及时盖上瓶塞
7.(2023云南永善二模)如图是一些物质的近似pH。下列说法正确的是( )
A.酸性最强的是厨房清洁剂
B.苹果汁能够使无色酚酞溶液变红色
C.小苏打水比厨房清洁剂的碱性强
D.紫色石蕊溶液滴加在厨房清洁剂中,石蕊溶液变蓝
8.冬春季节,园林工人会给许多树的树干刷一段石灰浆,下列有关说法正确的是 ( )
A.石灰浆属于溶液
B.石灰浆的主要成分是CaO
C.石灰浆可以防止树木上的害虫生卵
D.一段时间后树干上的白色物质是Ca(OH)2
9.(2023浙江杭州中考)将过量盐酸加入一定质量的氢氧化钠溶液中,充分反应后得到溶液X。下列现象或事实描述不合理的是 ( )
A.溶液X显酸性
B.向X滴加少量硝酸银溶液无沉淀生成
C.向X滴加少量硫酸铜溶液无沉淀生成
D.向X加入锌粒有气体生成
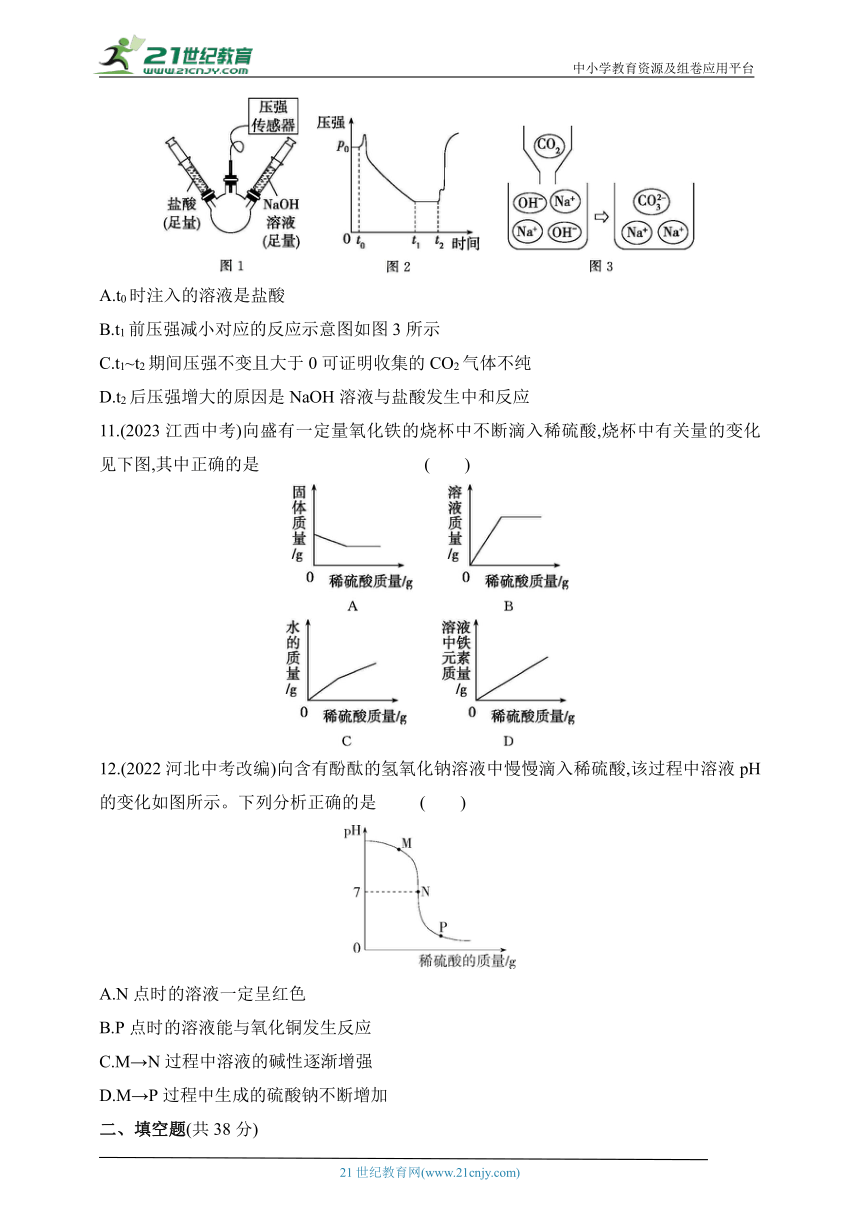
10.【数字化实验】(2023江苏连云港中考)在三颈烧瓶中用排空气法收集CO2气体,然后将三颈烧瓶与盛有盐酸、NaOH溶液的注射器和压强传感器密封连接(如图1)。检验气密性后,在t0时快速注入一种溶液,t2时快速注入第二种溶液,测得瓶内压强随时间变化曲线如图2。下列说法中正确的是 ( )
A.t0时注入的溶液是盐酸
B.t1前压强减小对应的反应示意图如图3所示
C.t1~t2期间压强不变且大于0可证明收集的CO2气体不纯
D.t2后压强增大的原因是NaOH溶液与盐酸发生中和反应
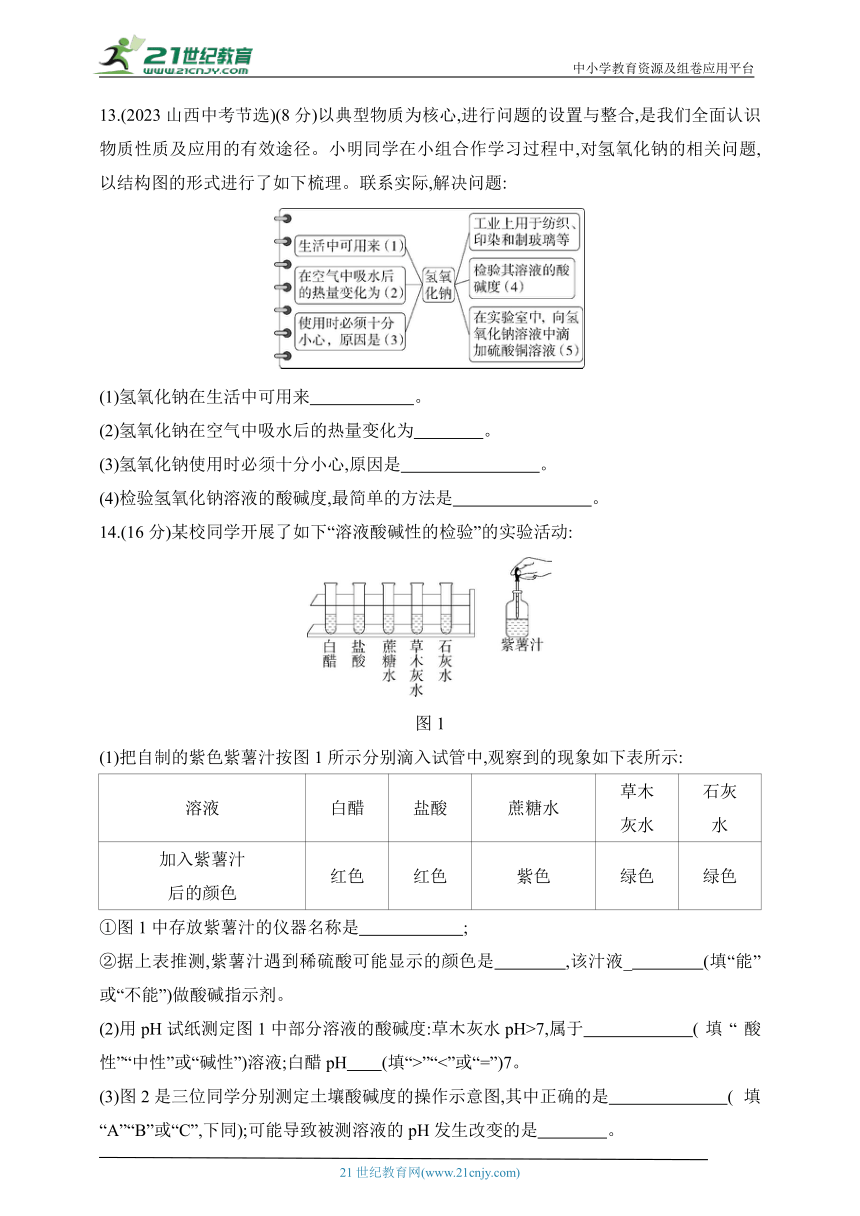
11.(2023江西中考)向盛有一定量氧化铁的烧杯中不断滴入稀硫酸,烧杯中有关量的变化见下图,其中正确的是 ( )
12.(2022河北中考改编)向含有酚酞的氢氧化钠溶液中慢慢滴入稀硫酸,该过程中溶液pH的变化如图所示。下列分析正确的是 ( )
A.N点时的溶液一定呈红色
B.P点时的溶液能与氧化铜发生反应
C.M→N过程中溶液的碱性逐渐增强
D.M→P过程中生成的硫酸钠不断增加
二、填空题(共38分)
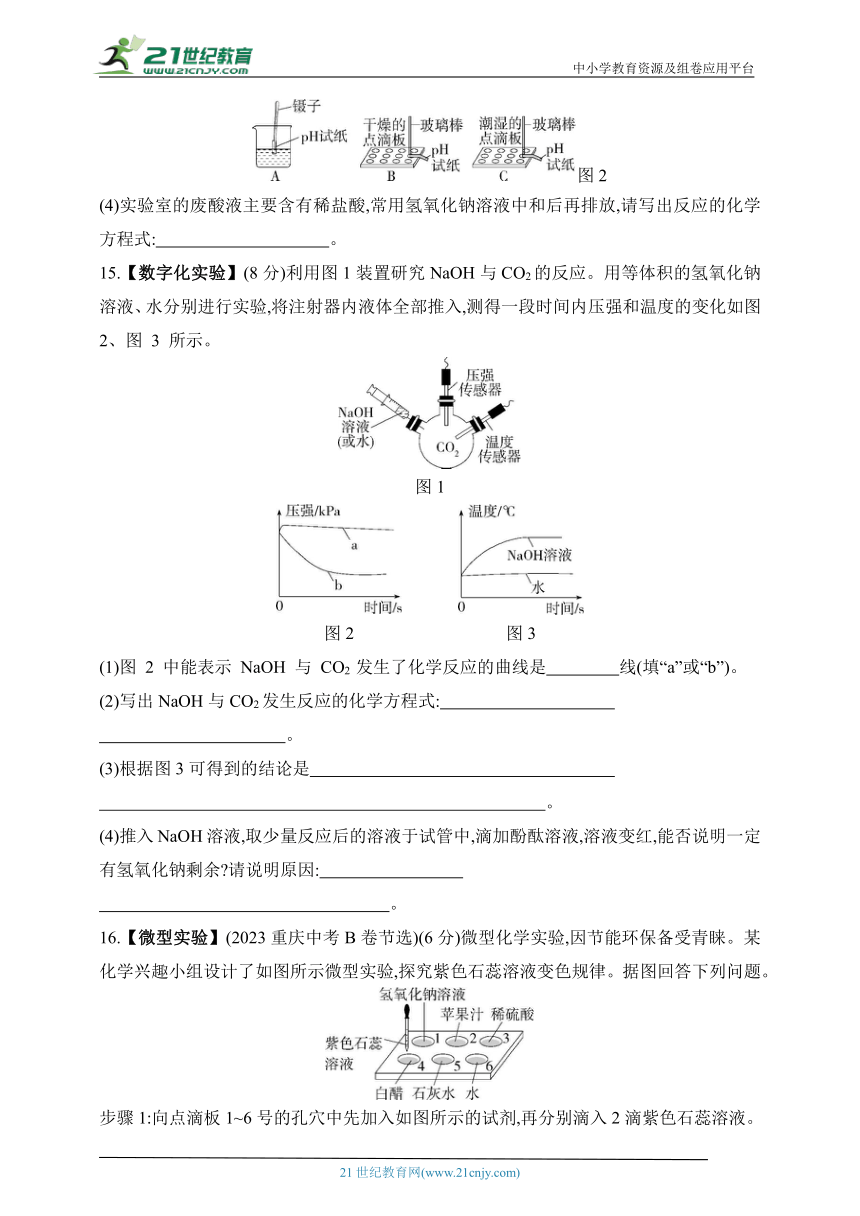
13.(2023山西中考节选)(8分)以典型物质为核心,进行问题的设置与整合,是我们全面认识物质性质及应用的有效途径。小明同学在小组合作学习过程中,对氢氧化钠的相关问题,以结构图的形式进行了如下梳理。联系实际,解决问题:
(1)氢氧化钠在生活中可用来 。
(2)氢氧化钠在空气中吸水后的热量变化为 。
(3)氢氧化钠使用时必须十分小心,原因是 。
(4)检验氢氧化钠溶液的酸碱度,最简单的方法是 。
14.(16分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:
图1
(1)把自制的紫色紫薯汁按图1所示分别滴入试管中,观察到的现象如下表所示:
溶液 白醋 盐酸 蔗糖水 草木 灰水 石灰 水
加入紫薯汁 后的颜色 红色 红色 紫色 绿色 绿色
①图1中存放紫薯汁的仪器名称是 ;
②据上表推测,紫薯汁遇到稀硫酸可能显示的颜色是 ,该汁液_ (填“能”或“不能”)做酸碱指示剂。
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”“中性”或“碱性”)溶液;白醋pH (填“>”“<”或“=”)7。
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 (填“A”“B”或“C”,下同);可能导致被测溶液的pH发生改变的是 。
图2
(4)实验室的废酸液主要含有稀盐酸,常用氢氧化钠溶液中和后再排放,请写出反应的化学方程式: 。
15.【数字化实验】(8分)利用图1装置研究NaOH与CO2的反应。用等体积的氢氧化钠溶液、水分别进行实验,将注射器内液体全部推入,测得一段时间内压强和温度的变化如图 2、图 3 所示。
图1
图2 图3
(1)图 2 中能表示 NaOH 与 CO2 发生了化学反应的曲线是 线(填“a”或“b”)。
(2)写出NaOH与CO2发生反应的化学方程式: 。
(3)根据图3可得到的结论是 。
(4)推入NaOH溶液,取少量反应后的溶液于试管中,滴加酚酞溶液,溶液变红,能否说明一定有氢氧化钠剩余 请说明原因: 。
16.【微型实验】(2023重庆中考B卷节选)(6分)微型化学实验,因节能环保备受青睐。某化学兴趣小组设计了如图所示微型实验,探究紫色石蕊溶液变色规律。据图回答下列问题。
步骤1:向点滴板1~6号的孔穴中先加入如图所示的试剂,再分别滴入2滴紫色石蕊溶液。6号孔穴中水的作用是 。
步骤2:将步骤1中所得的1号溶液和4号溶液互滴后溶液颜色发生明显变化,选出下列组合中互滴后溶液颜色有明显变化的是 (填序号)。
A.1号、5号 B.1号、3号
C.3号、4号 D.4号、5号
步骤3:重复步骤1,用吸管向5号孔穴吹入人呼出的气体,溶液表面出现白膜,写出反应的化学方程式: 。
三、实验探究题(共14分)
17.【学科素养·科学探究与实践】(2023四川达州中考)(14分)为了参加2023年5月举行的化学实验操作考试,各学校积极组织了实验操作训练。小姚同学完成了“稀盐酸、氢氧化钠溶液、蒸馏水的鉴别”实验,请你帮他完成实验报告的填写。
【实验题目】稀盐酸、氢氧化钠溶液、蒸馏水的鉴别
【实验目的】选择合适的指示剂鉴别稀盐酸、氢氧化钠溶液、蒸馏水。
【实验仪器】小试管5支、试管刷等。
【实验药品】随机编号为A、B、C的三种待测液,酚酞试液(装于滴瓶),石蕊试液(装于滴瓶)。
【实验过程】
实验步骤 实验现象 实验结论
①分别取A、B、C待测液1~2 mL于三支试管中,分别滴入1~2滴石蕊试液,振荡 B中的石蕊试液变 ,另外两支试管中的液体呈蓝色、紫色,但颜色相近 鉴别出B是 ,A、C无法准确鉴别
②另取A、C待测液1~2 mL于两支试管中,分别滴入1~2滴酚酞试液,振荡 C中的酚酞试液变 ,A中无明显现象 鉴别出C是 ,A是蒸馏水
【交流反思】小峰同学认为,只用酚酞试液也能完成该实验。他设计方案并完成了实验。
实验步骤 实验现象 实验结论
①分别取A、B、C待测液1~2 mL于三支试管中,分别滴入1~2滴酚酞试液,振荡 C中液体呈红色,A、B中无明显现象 鉴别出C
②将①中的红色液体分为两等份, 观察到其中一支试管有明显的现象: 发生反应的化学方程式为 ,鉴别出A、B
四、计算题(共12分)
18.(2023山东枣庄中考)(12分)为测定某硫酸溶液的溶质质量分数,实验小组设计了以下方案:在烧杯中加入该硫酸溶液100 g,然后向烧杯中逐滴加入氢氧化钡溶液,滴加的氢氧化钡溶液质量与生成沉淀的质量关系如图所示。请你帮其解决下列问题:
(1)恰好完全反应时,生成沉淀的质量为 g。
(2)求该硫酸溶液的溶质质量分数(写出计算过程)。
答案全解全析
1.A 菊花适合在弱酸性土壤中生长,土壤的pH=6.3时符合题意,故选A。
2.A 氢氧化钙是一种碱,能与酸反应,常用于改良酸性土壤;氯化钠、氯化钙溶液呈中性,不能用于改良酸性土壤;氢氧化钠具有强烈的腐蚀性,不能用于改良酸性土壤。
3.A 氢氧化钠溶液呈碱性,能使牵牛花浸出液显蓝色;碳酸、稀盐酸呈酸性,能使牵牛花浸出液显红色;硫酸钠溶液呈中性,能使牵牛花浸出液显紫色。故选A。
4.B 松花蛋有涩味,是因为制作过程中用到了熟石灰等原料,可利用中和反应原理,通过添加食醋减轻涩味。
5.C 用胶头滴管滴加液体时,胶头滴管应垂直悬空在试管口上方,A错误;用pH试纸测定溶液的pH时,应在白瓷板或玻璃片上放一小片pH试纸,用洁净干燥的玻璃棒蘸取待测液滴到pH试纸上,把试纸显示的颜色与标准比色板对照,读出pH,将pH试纸伸入待测液中会污染待测液,B错误;量筒读数时,视线要与量筒内液体凹液面的最低处保持水平,C正确;氢气的密度比空气的小,用向下排空气法收集,D错误。
6.A 由题意可知,二氧化碳与氢氧化钙反应生成碳酸钙沉淀,A错误,B正确;碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,白膜可用盐酸除去,C正确;为防止药品与空气中的成分发生化学反应,试剂使用后应及时盖上瓶塞,D正确。
7.D 厨房清洁剂的pH>7,显碱性,A错误;苹果汁的pH<7,显酸性,无色酚酞溶液遇酸性溶液不变色,B错误;pH>7溶液呈碱性,pH越大,溶液的碱性越强,小苏打水比厨房清洁剂的碱性弱,C错误;紫色石蕊溶液遇酸性溶液变红色,遇碱性溶液变蓝色,厨房清洁剂的pH>7,显碱性,能使紫色石蕊溶液变蓝色,D正确。
8.C 石灰浆是氢氧化钙的悬浊液,A错误;石灰浆的主要成分是氢氧化钙,B错误;石灰浆可以防止树木上的害虫生卵,C正确;氢氧化钙能与空气中的二氧化碳反应生成碳酸钙,所以一段时间后树干上的白色物质是CaCO3,D错误。
9.B 过量盐酸与一定质量的氢氧化钠溶液反应,生成氯化钠和水,溶液X中盐酸有剩余。溶液X显酸性,A正确;氯化钠、盐酸均能与硝酸银反应生成氯化银白色沉淀,B错误;氯化钠、盐酸均不与硫酸铜反应,C正确;盐酸与锌反应生成氢气,D正确。
10.C 由题图2可知,t0时注入的溶液是氢氧化钠溶液,二氧化碳与氢氧化钠反应生成碳酸钠和水,使瓶内气体体积减小,压强减小,A错误;t1前发生的反应是二氧化碳与氢氧化钠反应生成碳酸钠和水,题图3生成物中缺少水分子,B错误;t1~t2期间压强不变且大于0,可证明收集的CO2气体不纯,C正确;t2后压强增大的原因是碳酸钠与盐酸反应有二氧化碳气体生成,D错误。
11.C 向盛有一定量氧化铁的烧杯中不断滴入稀硫酸,氧化铁和稀硫酸反应生成硫酸铁和水。随着反应的进行,固体质量逐渐减小,至氧化铁完全反应,固体质量为0,A错误;反应过程中,溶液质量逐渐增大,至完全反应,继续加入稀硫酸,溶液质量继续增大,但增大幅度减小,B错误;随着反应进行,水的质量逐渐增大,至完全反应,继续加入稀硫酸,水的质量继续增大,但增大幅度减小,C正确;随着反应进行,溶液中铁元素质量逐渐增大,至氧化铁完全反应,不再发生改变,D错误。
12.B N点时溶液的pH等于7,呈中性,溶液呈无色,A错误。P点时溶液的pH小于7,显酸性,溶质是硫酸和硫酸钠,硫酸能与氧化铜发生反应,B正确。M→N过程中溶液pH逐渐减小,碱性逐渐变弱,C错误。M→N过程中,硫酸钠的质量逐渐增大;N→P过程中,硫酸钠的质量不变,D错误。
13.(1)去除油污(合理即可) (2)放热 (3)有强腐蚀性 (4)用pH试纸检测
解析 (1)氢氧化钠能与油脂反应,可用做炉具清洁剂;(2)氢氧化钠溶于水放热;(3)氢氧化钠具有强腐蚀性,使用氢氧化钠时必须十分小心;(4)检验溶液的酸碱度最简单的方法是使用pH试纸检测。
14.(1)①滴瓶 ②红色 能 (2)碱性 < (3)B C (4)NaOH+HClNaCl+H2O
解析 (1)①题图1中存放紫薯汁的仪器是滴瓶。②由题表中的信息可知,紫薯汁遇酸变红,因此其遇到稀硫酸显示的颜色是红色。(2)pH>7时溶液呈碱性,故草木灰水属于碱性溶液;白醋呈酸性,pH<7。(3)A操作会污染被测溶液;C操作相当于将被测溶液稀释,可能导致被测溶液的pH发生改变。
15.(1) b (2)CO2+2NaOHNa2CO3+H2O (3)二氧化碳溶于水温度无明显变化,氢氧化钠与二氧化碳的反应是放热反应(合理即可) (4)不能,因为碳酸钠溶液显碱性,也能使酚酞变红
解析 (1)二氧化碳与氢氧化钠发生化学反应,二氧化碳被大量消耗,装置内压强变化较大,对应曲线b。(2)二氧化碳与氢氧化钠反应生成碳酸钠与水,化学方程式为2NaOH+CO2Na2CO3+H2O。(3)从题图3中可以分析得出:二氧化碳溶于水时温度无明显变化,氢氧化钠与二氧化碳的反应是放热反应。(4)碱性溶液能使无色酚酞变红,氢氧化钠溶液和碳酸钠溶液都呈碱性,故无法判断溶液中是否存在氢氧化钠。
16.步骤1:进行对照 步骤2:BD 步骤3:CO2+Ca(OH)2 CaCO3↓+H2O
解析 步骤1:1~5号孔穴中的物质分别呈酸性或碱性,水呈中性,6号孔穴中水的作用是进行对照。步骤2:1号、5号都是碱溶液,互滴后溶液颜色没有明显变化;氢氧化钠能与硫酸反应生成硫酸钠和水,1号、3号互滴后溶液颜色有明显变化;3号、4号都是酸溶液,互滴后溶液颜色没有明显变化;白醋能与石灰水中的氢氧化钙反应,4号、5号互滴后溶液颜色有明显变化。步骤3:人呼出气体中的二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为CO2+Ca(OH)2 CaCO3↓+H2O。
17.【实验过程】①红 稀盐酸 ②红 氢氧化钠溶液 【交流反思】②分别滴入盛有A、B待测液的两支试管中 溶液的红色褪去 NaOH+HCl NaCl+H2O
解析 【实验过程】①稀盐酸能使石蕊试液变红,B为稀盐酸。②氢氧化钠溶液能使酚酞试液变红,C是氢氧化钠溶液。【交流反思】②在三种溶液中分别滴加酚酞试液,C中液体呈红色,即C是氢氧化钠溶液;盐酸和氢氧化钠溶液发生中和反应,氢氧化钠反应完全酚酞试液变为无色,故将①中的红色液体分为两等份,分别滴入盛有A、B待测液的两支试管中,能使溶液红色褪去的是稀盐酸;无明显变化的是蒸馏水。氢氧化钠和盐酸发生反应的化学方程式为NaOH+HCl NaCl+H2O。
18.(1)23.3
(2)解:设100 g该硫酸溶液中溶质的质量为x。
H2SO4+Ba(OH)2 BaSO4↓+2H2O
98 233
x 23.3 g
=
x=9.8 g
则该硫酸溶液的溶质质量分数为×100%=9.8%。
答:该硫酸溶液的溶质质量分数为9.8%。
解析 (1)由题图可知,恰好完全反应时,生成沉淀的质量为23.3 g。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024北京课改化学九年级下学期
第11章·素养综合检测
(满分100分,限时40分钟)
一、选择题(每小题3分,共36分)
1.【新素材·传统习俗】(2023北京中考)重阳赏菊。菊花适合在弱酸性土壤中生长,下列土壤的pH最适合菊花生长的是 ( )
A.6.3 B.8.5 C.8.9 D.9.2
2.(2023北京东城一模)能用于改良酸性土壤的物质是 ( )
A.Ca(OH)2 B.NaCl C.NaOH D.CaCl2
3.(2023云南曲靖二模)植物的汁液可以用做酸碱指示剂,下表是牵牛花浸出液在不同条件下的显色情况,下列溶液中能使牵牛花浸出液变为蓝色的是 ( )
溶液 酸性溶液 中性溶液 碱性溶液
颜色 红色 紫色 蓝色
A.氢氧化钠溶液 B.碳酸
C.稀盐酸 D.硫酸钠溶液
4.食用松花蛋时常感到有涩味,是因为制作过程中用到了熟石灰等原料,为了减轻涩味,可在食用时添加 ( )
A.味精 B.食醋 C.酱油 D.食盐
5.(2023湖南郴州中考)下列图示的实验操作正确的是 ( )
6.(2022浙江嘉兴中考)一瓶存放较长时间的石灰水,瓶内壁附有一层白膜,下列有关说法错误的是 ( )
A.白膜都是氢氧化钙
B.白膜的形成与二氧化碳有关
C.白膜可用盐酸除去
D.试剂使用后应及时盖上瓶塞
7.(2023云南永善二模)如图是一些物质的近似pH。下列说法正确的是( )
A.酸性最强的是厨房清洁剂
B.苹果汁能够使无色酚酞溶液变红色
C.小苏打水比厨房清洁剂的碱性强
D.紫色石蕊溶液滴加在厨房清洁剂中,石蕊溶液变蓝
8.冬春季节,园林工人会给许多树的树干刷一段石灰浆,下列有关说法正确的是 ( )
A.石灰浆属于溶液
B.石灰浆的主要成分是CaO
C.石灰浆可以防止树木上的害虫生卵
D.一段时间后树干上的白色物质是Ca(OH)2
9.(2023浙江杭州中考)将过量盐酸加入一定质量的氢氧化钠溶液中,充分反应后得到溶液X。下列现象或事实描述不合理的是 ( )
A.溶液X显酸性
B.向X滴加少量硝酸银溶液无沉淀生成
C.向X滴加少量硫酸铜溶液无沉淀生成
D.向X加入锌粒有气体生成
10.【数字化实验】(2023江苏连云港中考)在三颈烧瓶中用排空气法收集CO2气体,然后将三颈烧瓶与盛有盐酸、NaOH溶液的注射器和压强传感器密封连接(如图1)。检验气密性后,在t0时快速注入一种溶液,t2时快速注入第二种溶液,测得瓶内压强随时间变化曲线如图2。下列说法中正确的是 ( )
A.t0时注入的溶液是盐酸
B.t1前压强减小对应的反应示意图如图3所示
C.t1~t2期间压强不变且大于0可证明收集的CO2气体不纯
D.t2后压强增大的原因是NaOH溶液与盐酸发生中和反应
11.(2023江西中考)向盛有一定量氧化铁的烧杯中不断滴入稀硫酸,烧杯中有关量的变化见下图,其中正确的是 ( )
12.(2022河北中考改编)向含有酚酞的氢氧化钠溶液中慢慢滴入稀硫酸,该过程中溶液pH的变化如图所示。下列分析正确的是 ( )
A.N点时的溶液一定呈红色
B.P点时的溶液能与氧化铜发生反应
C.M→N过程中溶液的碱性逐渐增强
D.M→P过程中生成的硫酸钠不断增加
二、填空题(共38分)
13.(2023山西中考节选)(8分)以典型物质为核心,进行问题的设置与整合,是我们全面认识物质性质及应用的有效途径。小明同学在小组合作学习过程中,对氢氧化钠的相关问题,以结构图的形式进行了如下梳理。联系实际,解决问题:
(1)氢氧化钠在生活中可用来 。
(2)氢氧化钠在空气中吸水后的热量变化为 。
(3)氢氧化钠使用时必须十分小心,原因是 。
(4)检验氢氧化钠溶液的酸碱度,最简单的方法是 。
14.(16分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:
图1
(1)把自制的紫色紫薯汁按图1所示分别滴入试管中,观察到的现象如下表所示:
溶液 白醋 盐酸 蔗糖水 草木 灰水 石灰 水
加入紫薯汁 后的颜色 红色 红色 紫色 绿色 绿色
①图1中存放紫薯汁的仪器名称是 ;
②据上表推测,紫薯汁遇到稀硫酸可能显示的颜色是 ,该汁液_ (填“能”或“不能”)做酸碱指示剂。
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”“中性”或“碱性”)溶液;白醋pH (填“>”“<”或“=”)7。
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 (填“A”“B”或“C”,下同);可能导致被测溶液的pH发生改变的是 。
图2
(4)实验室的废酸液主要含有稀盐酸,常用氢氧化钠溶液中和后再排放,请写出反应的化学方程式: 。
15.【数字化实验】(8分)利用图1装置研究NaOH与CO2的反应。用等体积的氢氧化钠溶液、水分别进行实验,将注射器内液体全部推入,测得一段时间内压强和温度的变化如图 2、图 3 所示。
图1
图2 图3
(1)图 2 中能表示 NaOH 与 CO2 发生了化学反应的曲线是 线(填“a”或“b”)。
(2)写出NaOH与CO2发生反应的化学方程式: 。
(3)根据图3可得到的结论是 。
(4)推入NaOH溶液,取少量反应后的溶液于试管中,滴加酚酞溶液,溶液变红,能否说明一定有氢氧化钠剩余 请说明原因: 。
16.【微型实验】(2023重庆中考B卷节选)(6分)微型化学实验,因节能环保备受青睐。某化学兴趣小组设计了如图所示微型实验,探究紫色石蕊溶液变色规律。据图回答下列问题。
步骤1:向点滴板1~6号的孔穴中先加入如图所示的试剂,再分别滴入2滴紫色石蕊溶液。6号孔穴中水的作用是 。
步骤2:将步骤1中所得的1号溶液和4号溶液互滴后溶液颜色发生明显变化,选出下列组合中互滴后溶液颜色有明显变化的是 (填序号)。
A.1号、5号 B.1号、3号
C.3号、4号 D.4号、5号
步骤3:重复步骤1,用吸管向5号孔穴吹入人呼出的气体,溶液表面出现白膜,写出反应的化学方程式: 。
三、实验探究题(共14分)
17.【学科素养·科学探究与实践】(2023四川达州中考)(14分)为了参加2023年5月举行的化学实验操作考试,各学校积极组织了实验操作训练。小姚同学完成了“稀盐酸、氢氧化钠溶液、蒸馏水的鉴别”实验,请你帮他完成实验报告的填写。
【实验题目】稀盐酸、氢氧化钠溶液、蒸馏水的鉴别
【实验目的】选择合适的指示剂鉴别稀盐酸、氢氧化钠溶液、蒸馏水。
【实验仪器】小试管5支、试管刷等。
【实验药品】随机编号为A、B、C的三种待测液,酚酞试液(装于滴瓶),石蕊试液(装于滴瓶)。
【实验过程】
实验步骤 实验现象 实验结论
①分别取A、B、C待测液1~2 mL于三支试管中,分别滴入1~2滴石蕊试液,振荡 B中的石蕊试液变 ,另外两支试管中的液体呈蓝色、紫色,但颜色相近 鉴别出B是 ,A、C无法准确鉴别
②另取A、C待测液1~2 mL于两支试管中,分别滴入1~2滴酚酞试液,振荡 C中的酚酞试液变 ,A中无明显现象 鉴别出C是 ,A是蒸馏水
【交流反思】小峰同学认为,只用酚酞试液也能完成该实验。他设计方案并完成了实验。
实验步骤 实验现象 实验结论
①分别取A、B、C待测液1~2 mL于三支试管中,分别滴入1~2滴酚酞试液,振荡 C中液体呈红色,A、B中无明显现象 鉴别出C
②将①中的红色液体分为两等份, 观察到其中一支试管有明显的现象: 发生反应的化学方程式为 ,鉴别出A、B
四、计算题(共12分)
18.(2023山东枣庄中考)(12分)为测定某硫酸溶液的溶质质量分数,实验小组设计了以下方案:在烧杯中加入该硫酸溶液100 g,然后向烧杯中逐滴加入氢氧化钡溶液,滴加的氢氧化钡溶液质量与生成沉淀的质量关系如图所示。请你帮其解决下列问题:
(1)恰好完全反应时,生成沉淀的质量为 g。
(2)求该硫酸溶液的溶质质量分数(写出计算过程)。
答案全解全析
1.A 菊花适合在弱酸性土壤中生长,土壤的pH=6.3时符合题意,故选A。
2.A 氢氧化钙是一种碱,能与酸反应,常用于改良酸性土壤;氯化钠、氯化钙溶液呈中性,不能用于改良酸性土壤;氢氧化钠具有强烈的腐蚀性,不能用于改良酸性土壤。
3.A 氢氧化钠溶液呈碱性,能使牵牛花浸出液显蓝色;碳酸、稀盐酸呈酸性,能使牵牛花浸出液显红色;硫酸钠溶液呈中性,能使牵牛花浸出液显紫色。故选A。
4.B 松花蛋有涩味,是因为制作过程中用到了熟石灰等原料,可利用中和反应原理,通过添加食醋减轻涩味。
5.C 用胶头滴管滴加液体时,胶头滴管应垂直悬空在试管口上方,A错误;用pH试纸测定溶液的pH时,应在白瓷板或玻璃片上放一小片pH试纸,用洁净干燥的玻璃棒蘸取待测液滴到pH试纸上,把试纸显示的颜色与标准比色板对照,读出pH,将pH试纸伸入待测液中会污染待测液,B错误;量筒读数时,视线要与量筒内液体凹液面的最低处保持水平,C正确;氢气的密度比空气的小,用向下排空气法收集,D错误。
6.A 由题意可知,二氧化碳与氢氧化钙反应生成碳酸钙沉淀,A错误,B正确;碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,白膜可用盐酸除去,C正确;为防止药品与空气中的成分发生化学反应,试剂使用后应及时盖上瓶塞,D正确。
7.D 厨房清洁剂的pH>7,显碱性,A错误;苹果汁的pH<7,显酸性,无色酚酞溶液遇酸性溶液不变色,B错误;pH>7溶液呈碱性,pH越大,溶液的碱性越强,小苏打水比厨房清洁剂的碱性弱,C错误;紫色石蕊溶液遇酸性溶液变红色,遇碱性溶液变蓝色,厨房清洁剂的pH>7,显碱性,能使紫色石蕊溶液变蓝色,D正确。
8.C 石灰浆是氢氧化钙的悬浊液,A错误;石灰浆的主要成分是氢氧化钙,B错误;石灰浆可以防止树木上的害虫生卵,C正确;氢氧化钙能与空气中的二氧化碳反应生成碳酸钙,所以一段时间后树干上的白色物质是CaCO3,D错误。
9.B 过量盐酸与一定质量的氢氧化钠溶液反应,生成氯化钠和水,溶液X中盐酸有剩余。溶液X显酸性,A正确;氯化钠、盐酸均能与硝酸银反应生成氯化银白色沉淀,B错误;氯化钠、盐酸均不与硫酸铜反应,C正确;盐酸与锌反应生成氢气,D正确。
10.C 由题图2可知,t0时注入的溶液是氢氧化钠溶液,二氧化碳与氢氧化钠反应生成碳酸钠和水,使瓶内气体体积减小,压强减小,A错误;t1前发生的反应是二氧化碳与氢氧化钠反应生成碳酸钠和水,题图3生成物中缺少水分子,B错误;t1~t2期间压强不变且大于0,可证明收集的CO2气体不纯,C正确;t2后压强增大的原因是碳酸钠与盐酸反应有二氧化碳气体生成,D错误。
11.C 向盛有一定量氧化铁的烧杯中不断滴入稀硫酸,氧化铁和稀硫酸反应生成硫酸铁和水。随着反应的进行,固体质量逐渐减小,至氧化铁完全反应,固体质量为0,A错误;反应过程中,溶液质量逐渐增大,至完全反应,继续加入稀硫酸,溶液质量继续增大,但增大幅度减小,B错误;随着反应进行,水的质量逐渐增大,至完全反应,继续加入稀硫酸,水的质量继续增大,但增大幅度减小,C正确;随着反应进行,溶液中铁元素质量逐渐增大,至氧化铁完全反应,不再发生改变,D错误。
12.B N点时溶液的pH等于7,呈中性,溶液呈无色,A错误。P点时溶液的pH小于7,显酸性,溶质是硫酸和硫酸钠,硫酸能与氧化铜发生反应,B正确。M→N过程中溶液pH逐渐减小,碱性逐渐变弱,C错误。M→N过程中,硫酸钠的质量逐渐增大;N→P过程中,硫酸钠的质量不变,D错误。
13.(1)去除油污(合理即可) (2)放热 (3)有强腐蚀性 (4)用pH试纸检测
解析 (1)氢氧化钠能与油脂反应,可用做炉具清洁剂;(2)氢氧化钠溶于水放热;(3)氢氧化钠具有强腐蚀性,使用氢氧化钠时必须十分小心;(4)检验溶液的酸碱度最简单的方法是使用pH试纸检测。
14.(1)①滴瓶 ②红色 能 (2)碱性 < (3)B C (4)NaOH+HClNaCl+H2O
解析 (1)①题图1中存放紫薯汁的仪器是滴瓶。②由题表中的信息可知,紫薯汁遇酸变红,因此其遇到稀硫酸显示的颜色是红色。(2)pH>7时溶液呈碱性,故草木灰水属于碱性溶液;白醋呈酸性,pH<7。(3)A操作会污染被测溶液;C操作相当于将被测溶液稀释,可能导致被测溶液的pH发生改变。
15.(1) b (2)CO2+2NaOHNa2CO3+H2O (3)二氧化碳溶于水温度无明显变化,氢氧化钠与二氧化碳的反应是放热反应(合理即可) (4)不能,因为碳酸钠溶液显碱性,也能使酚酞变红
解析 (1)二氧化碳与氢氧化钠发生化学反应,二氧化碳被大量消耗,装置内压强变化较大,对应曲线b。(2)二氧化碳与氢氧化钠反应生成碳酸钠与水,化学方程式为2NaOH+CO2Na2CO3+H2O。(3)从题图3中可以分析得出:二氧化碳溶于水时温度无明显变化,氢氧化钠与二氧化碳的反应是放热反应。(4)碱性溶液能使无色酚酞变红,氢氧化钠溶液和碳酸钠溶液都呈碱性,故无法判断溶液中是否存在氢氧化钠。
16.步骤1:进行对照 步骤2:BD 步骤3:CO2+Ca(OH)2 CaCO3↓+H2O
解析 步骤1:1~5号孔穴中的物质分别呈酸性或碱性,水呈中性,6号孔穴中水的作用是进行对照。步骤2:1号、5号都是碱溶液,互滴后溶液颜色没有明显变化;氢氧化钠能与硫酸反应生成硫酸钠和水,1号、3号互滴后溶液颜色有明显变化;3号、4号都是酸溶液,互滴后溶液颜色没有明显变化;白醋能与石灰水中的氢氧化钙反应,4号、5号互滴后溶液颜色有明显变化。步骤3:人呼出气体中的二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为CO2+Ca(OH)2 CaCO3↓+H2O。
17.【实验过程】①红 稀盐酸 ②红 氢氧化钠溶液 【交流反思】②分别滴入盛有A、B待测液的两支试管中 溶液的红色褪去 NaOH+HCl NaCl+H2O
解析 【实验过程】①稀盐酸能使石蕊试液变红,B为稀盐酸。②氢氧化钠溶液能使酚酞试液变红,C是氢氧化钠溶液。【交流反思】②在三种溶液中分别滴加酚酞试液,C中液体呈红色,即C是氢氧化钠溶液;盐酸和氢氧化钠溶液发生中和反应,氢氧化钠反应完全酚酞试液变为无色,故将①中的红色液体分为两等份,分别滴入盛有A、B待测液的两支试管中,能使溶液红色褪去的是稀盐酸;无明显变化的是蒸馏水。氢氧化钠和盐酸发生反应的化学方程式为NaOH+HCl NaCl+H2O。
18.(1)23.3
(2)解:设100 g该硫酸溶液中溶质的质量为x。
H2SO4+Ba(OH)2 BaSO4↓+2H2O
98 233
x 23.3 g
=
x=9.8 g
则该硫酸溶液的溶质质量分数为×100%=9.8%。
答:该硫酸溶液的溶质质量分数为9.8%。
解析 (1)由题图可知,恰好完全反应时,生成沉淀的质量为23.3 g。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
