2024北京课改化学九年级下学期课时练--期中素养综合测试
文档属性
| 名称 | 2024北京课改化学九年级下学期课时练--期中素养综合测试 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-01 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
2024北京课改化学九年级下学期
期中素养综合测试
(满分100分,限时60分钟)
一、选择题(每小题3分,共36分)
1.(2023辽宁抚顺、本溪、辽阳中考)厨房里的下列物质放入水中,能形成溶液的是 ( )
A.面粉 B.白糖
C.植物油 D.辣椒面
2.(2023北京东城二模)铝能加工成铝箔,说明铝具有良好的 ( )
A.导热性 B.延展性
C.导电性 D.抗腐蚀性
3.(2023湖北宜昌中考)实验室配制一定溶质质量分数的氯化钠溶液,下列操作错误的是( )
4.下列有关金属资源的利用与防护不合理的是 ( )
A.经常用钢丝球擦洗铝锅表面,保持洁净
B.在钢铁表面喷油漆可防止生锈
C.废旧金属的回收利用,是保护金属资源的有效途径之一
D.改变金属的组成和结构,铸造成合金材料可优化其性能
5.【跨学科·语文】《吕氏春秋》记载:“金(即铜单质)柔锡(即锡单质)柔,合两柔则为刚(即坚硬)。”这句话说明合金具有的特性是 ( )
A.合金的熔点一般比其组分金属低
B.合金的硬度一般比其组分金属大
C.合金的抗腐蚀性一般比其组分金属强
D.合金的耐磨性一般比其组分金属好
6.(2023湖南衡阳中考)溶液具有广泛的用途,与人们的生活息息相关。下列有关溶液的说法正确的是 ( )
A.凡是均一、稳定的液体一定是溶液
B.饱和溶液一定比不饱和溶液的浓度大
C.硝酸铵固体在溶于水形成溶液的过程中,吸收热量
D.降低饱和溶液的温度后,溶液中溶质的质量分数一定减小
7.(2023四川自贡中考)现有体积大小相同的三种金属X、Y、Z,分别放入三份溶质质量分数相等的足量稀硫酸中,X不发生反应,Y、Z反应生成氢气的质量与反应时间的关系如图所示。X、Y、Z的金属活动性顺序正确的是 ( )
A.X>Y>Z B.X>Z>Y C.Y>Z>X D.Z>Y>X
8.(2023江苏苏州中考)铁是应用最广泛的金属。下列有关说法正确的是 ( )
A.炼铁原理是用合适的物质将单质铁转化为氧化铁
B.将生铁中的大部分碳反应除去得到的钢是纯净物
C.铁制品高温处理后,表面形成的致密氧化膜有防腐作用
D.日常生活中的废旧铁制品直接填埋处理
9.(2023河南驻马店十九中期末)如图为小李同学在实验室中模拟海水晒盐的过程,下列溶液中溶质质量分数最小的是 ( )
A.甲 B.乙 C.丙 D.丁
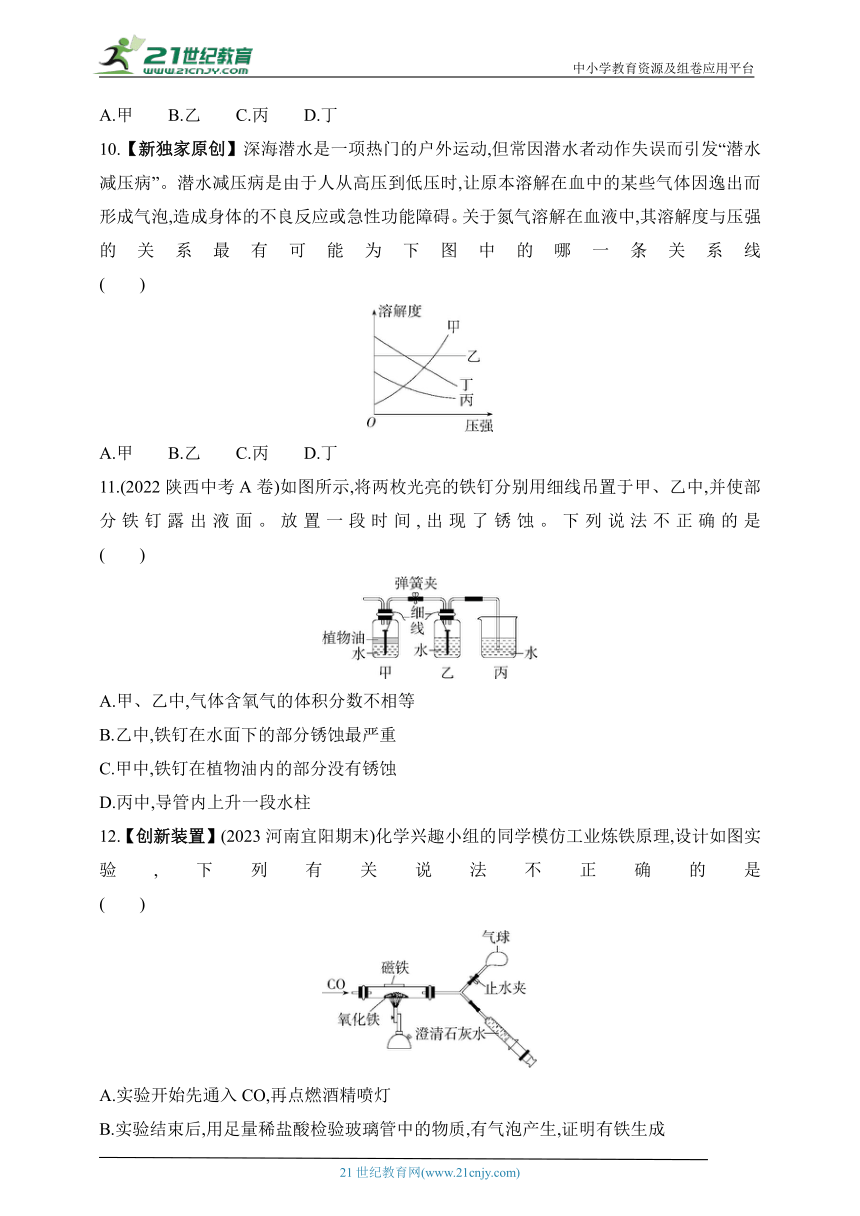
10.【新独家原创】深海潜水是一项热门的户外运动,但常因潜水者动作失误而引发“潜水减压病”。潜水减压病是由于人从高压到低压时,让原本溶解在血中的某些气体因逸出而形成气泡,造成身体的不良反应或急性功能障碍。关于氮气溶解在血液中,其溶解度与压强的关系最有可能为下图中的哪一条关系线 ( )
A.甲 B.乙 C.丙 D.丁
11.(2022陕西中考A卷)如图所示,将两枚光亮的铁钉分别用细线吊置于甲、乙中,并使部分铁钉露出液面。放置一段时间,出现了锈蚀。下列说法不正确的是 ( )
A.甲、乙中,气体含氧气的体积分数不相等
B.乙中,铁钉在水面下的部分锈蚀最严重
C.甲中,铁钉在植物油内的部分没有锈蚀
D.丙中,导管内上升一段水柱
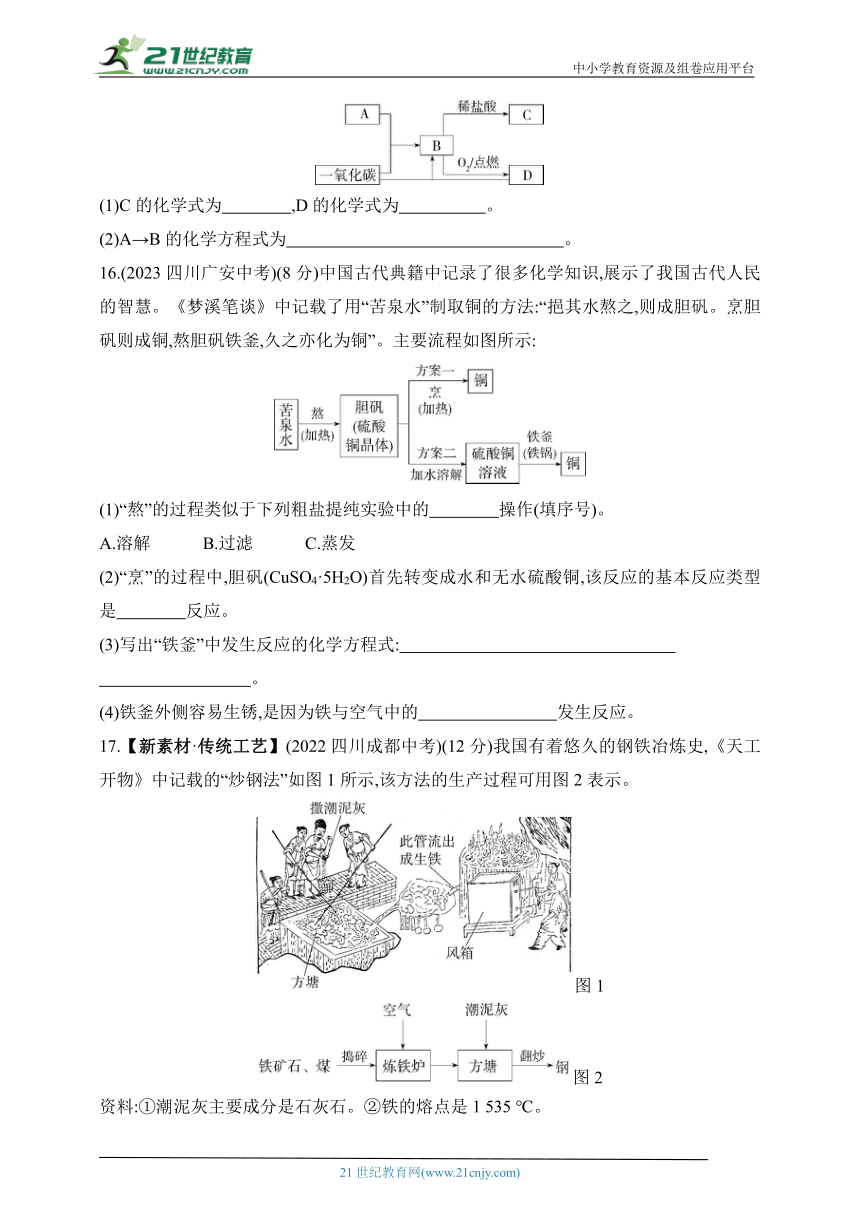
12.【创新装置】(2023河南宜阳期末)化学兴趣小组的同学模仿工业炼铁原理,设计如图实验,下列有关说法不正确的是 ( )
A.实验开始先通入CO,再点燃酒精喷灯
B.实验结束后,用足量稀盐酸检验玻璃管中的物质,有气泡产生,证明有铁生成
C.一段时间后注射器内溶液变浑浊
D.装置中气球的作用是收集CO2,防止污染空气
二、填空题(共42分)
13.[含评分说明](2023甘肃金昌中考)(6分)金属在生产和生活中应用极为广泛。
(1)生铁和钢是两种含碳量 的铁合金(填“相同”或“不同”)。
(2)下列生活用品利用金属良好导热性的是 (填序号)。
a.镀铬水龙头 b.铸铁暖气片
c.包糖果的铝箔
(3)焊接钢轨的反应原理是铝与氧化铁在高温条件下反应生成铁和氧化铝,该反应的化学方程式为 。
14.(2023山东滨州中考)(10分)下图为甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,请回答下列问题:
(1)当温度为 ℃时,甲物质的溶解度等于丙物质的溶解度;
(2)图中A点表示乙物质在t1 ℃时的 (填“饱和”或“不饱和”)溶液;
(3)若甲中含有少量乙时,可以采用 (填“降温结晶”或“蒸发结晶”)的方法提纯甲;
(4)将t2 ℃时接近饱和的丙溶液变成饱和溶液,下列方法不能达到目的的是 ;
A.蒸发溶剂 B.降低温度
C.增加溶质 D.升高温度
(5)将t2 ℃时甲的饱和溶液100 g稀释成溶质质量分数为25%的溶液,需加水的质量为 g。
15.【推断题】(2023四川自贡中考)(6分)A、B、C、D四种物质均含同一种金属元素,A为赤铁矿的主要成分,B为单质。它们之间的转化关系如下图所示(图中“—”表示物质间能相互发生反应,“→”表示物质间能发生一步转化,部分物质和反应条件已略去)。
(1)C的化学式为 ,D的化学式为 。
(2)A→B的化学方程式为 。
16.(2023四川广安中考)(8分)中国古代典籍中记录了很多化学知识,展示了我国古代人民的智慧。《梦溪笔谈》中记载了用“苦泉水”制取铜的方法:“挹其水熬之,则成胆矾。烹胆矾则成铜,熬胆矾铁釜,久之亦化为铜”。主要流程如图所示:
(1)“熬”的过程类似于下列粗盐提纯实验中的 操作(填序号)。
A.溶解 B.过滤 C.蒸发
(2)“烹”的过程中,胆矾(CuSO4·5H2O)首先转变成水和无水硫酸铜,该反应的基本反应类型是 反应。
(3)写出“铁釜”中发生反应的化学方程式: 。
(4)铁釜外侧容易生锈,是因为铁与空气中的 发生反应。
17.【新素材·传统工艺】(2022四川成都中考)(12分)我国有着悠久的钢铁冶炼史,《天工开物》中记载的“炒钢法”如图1所示,该方法的生产过程可用图2表示。
图1
图2
资料:①潮泥灰主要成分是石灰石。②铁的熔点是1 535 ℃。
根据图文回答下列问题。
(1)常见的铁矿石有赤铁矿和 (写一种)。
(2)不断鼓入空气的目的是 。
(3)炼铁炉中生成铁的化学方程式为 。
(4)撒入潮泥灰主要作用是 。不断翻炒液态生铁,是为了降低 元素的含量。
(5)钢的性能优良,如钢的熔点比纯铁 ,易于加工。
三、实验探究题(共12分)
18.(12分)为了研究物质的溶解现象,进行如下探究活动。
探究Ⅰ:将足量的碳酸钠、氯化钠和硝酸钾三种物质分别溶解在一定量的水中,溶解过程的温度变化如图所示。
探究Ⅱ:
① ② ③
固体溶解,形成紫红色溶液 固体溶解,形成紫红色溶液 固体几乎不溶解
探究Ⅲ:探究过程如图所示。
回答下列问题:
(1)探究Ⅰ中,溶解过程放出热量的物质是 。
(2)对探究Ⅱ中实验现象进行分析,需要做的对比是 。分析得出的结论之一是 (写一条即可)。
(3)探究Ⅲ中,所得溶液一定属于饱和溶液的是 。通过该探究得出的结论是 (答一点即可)。
(4)在上述探究的基础上,同学们想通过探究,比较氯化钠和氯化铵在水中的溶解度大小,探究方案应该是 。
四、计算题(共10分)
19.[含评分说明](2022青海中考)(10分)根据Fe3O4+4CO 3Fe+4CO2反应原理,工业上可用来冶炼铁。现用100 t含四氧化三铁为46.4%的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
(1)该铁矿石中含四氧化三铁质量是 。
(2)理论上可炼出含铁96%的生铁的质量是多少
答案全解全析
1.B 面粉、辣椒面放入水中形成不稳定的悬浊液;植物油放入水中形成不稳定的乳浊液;白糖放入水中形成均一、稳定的溶液,故选B。
2.B 铝能加工成铝箔,说明铝具有良好的延展性。
3.B 量取液体读数时,视线要与量筒内液体凹液面的最低处保持水平,B错误。
4.A 铝的表面有致密的氧化铝薄膜,能保护内部金属不被氧化,经常用钢丝球擦洗铝锅表面会破坏氧化膜,加速铝的腐蚀。
5.B 合金与其组分金属相比,具有硬度大、熔点低、抗腐蚀性强等特点,本题描述的是硬度大,故选B。
6.C 水是均一、稳定的液体,但不是溶液,A错误;饱和溶液的浓度不一定比不饱和溶液的浓度大,B错误;氢氧化钙的溶解度随温度的降低而增大,降低其饱和溶液的温度后,溶液变为不饱和溶液,但溶质的质量分数不变,D错误。
7.D 由题可知,X不与稀硫酸发生反应,Y、Z能与稀硫酸反应,则活动性:Y>X,Z>X;由题图分析可得,至完全反应,Z产生氢气所需时间短,则Z的金属活动性比Y强,故X、Y、Z的金属活动性顺序是Z>Y>X。故选D。
8.C 炼铁原理是用合适的物质将氧化铁(或其他铁的氧化物)转化为单质铁,A错误;钢是一种铁合金,属于混合物,B错误;废旧铁制品应回收利用,既能节约金属资源,又能减少环境污染,D错误。
9.A 甲蒸发水分得到乙,二者溶质质量相同,乙中溶剂质量减小,溶质质量分数:甲<乙;丙中含有未溶解的固体,丙过滤后得到丁,丙、丁为该温度下的饱和溶液,溶质质量分数:丙=丁;乙蒸发水分得到丙,有固体析出,所以乙可能恰好饱和,也可能是不饱和溶液,故溶质质量分数:乙≤丙,则溶质质量分数的关系是甲<乙≤丙=丁。
10.A 结合题给材料信息推断,气体在血液中的溶解度最有可能随压强的增大而增大,故A项符合题意。
11.B 铁的锈蚀过程消耗氧气,乙装置为密闭环境,铁锈蚀过程中会使氧气体积分数减小,而甲装置始终与空气连通,反应后瓶内气体成分与空气成分基本相同,氧气体积分数也基本不变,A正确;乙中铁钉在液面处锈蚀最严重,B不正确;铁钉在植物油内的部分不与水和氧气接触,不发生锈蚀,C正确;乙中消耗了氧气,装置内压强减小,在大气压的作用下丙烧杯内的水被压入导管,导管内会上升一段水柱,D正确。
12.D 实验开始先通入CO,再点燃酒精喷灯,目的是排尽装置中的空气,防止加热时发生爆炸,A正确;实验结束后,用足量稀盐酸检验玻璃管中的物质,有气泡产生,证明有铁生成,B正确;反应生成的二氧化碳能使澄清石灰水变浑浊,C正确;装置中气球的作用是收集CO,防止污染空气,D错误。
13.(1)不同 (2)b (3)2Al+Fe2O32Fe+Al2O3
【评分说明】(3)化学方程式未配平、未写反应条件扣1分,化学式写错不得分。
解析 (1)生铁的含碳量是2%~4.3%,钢的含碳量是0.03%~2%。(2)利用金属良好导热性的是铸铁暖气片。
14.(1)t1 (2)不饱和 (3)降温结晶 (4)B (5)100
解析 (1)分析溶解度曲线图可知,t1 ℃时甲、丙的溶解度曲线相交于A点,说明此时二者溶解度相等。(2)A点为t1 ℃时乙物质溶解度曲线下方的点,表示乙物质在t1 ℃时的不饱和溶液。(3)甲、乙的溶解度均随温度升高而增大,且甲的溶解度受温度变化影响较大,若甲中含有少量乙时,可采用降温结晶的方法提纯甲。(4)丙的溶解度随温度升高而减小,将t2 ℃时接近饱和的丙溶液变成饱和溶液可采用蒸发溶剂、增加溶质或升高温度的方法。(5)t2 ℃时甲物质的溶解度为100 g,因此100 g甲的饱和溶液中溶质质量为50 g、溶剂质量为50 g,根据溶液稀释前后溶质质量不变,得需加水的质量为50 g÷25%-100 g=100 g。
15.(1)FeCl2 Fe3O4 (2)Fe2O3+3CO2Fe+3CO2
解析 A、B、C、D四种物质中均含同一种金属元素,A为赤铁矿的主要成分,则A是氧化铁;B为单质,则B是铁;铁和稀盐酸反应生成氯化亚铁和氢气,铁在氧气中燃烧生成四氧化三铁,则C是氯化亚铁,D是四氧化三铁。
16.(1)C (2)分解 (3)Fe+CuSO4FeSO4+Cu (4)水蒸气、氧气(或H2O、O2)
解析 (1)从苦泉水中得到胆矾,类似于粗盐提纯实验中的蒸发操作,故选C。(2)胆矾转化为水和无水硫酸铜,符合“一变多”的特征,属于分解反应。(3)“铁釜”中发生的反应是铁与硫酸铜反应生成铜和硫酸亚铁。
17.(1)磁铁矿(合理即可) (2)提高炉温 (3)Fe2O3+3CO2Fe+3CO2(或Fe3O4+4CO3Fe+4CO2) (4)除杂 碳(或C) (5)低
解析 (1)常见的铁矿石有赤铁矿、磁铁矿和菱铁矿等。(2)不断鼓入空气的目的是使碳与氧气充分反应,提高炉温。(3)用赤铁矿炼铁时,反应的化学方程式为Fe2O3+3CO2Fe+3CO2;用磁铁矿炼铁时,反应的化学方程式为Fe3O4+4CO3Fe+4CO2。(4)生铁和钢的含碳量不同,不断翻炒液态生铁,目的是使生铁中的碳与氧气反应,降低碳元素的含量。(5)合金的熔点低于组成它的纯金属的熔点。
18.(1)碳酸钠 (2)将①③、②③分别对比 其他条件相同时,高锰酸钾在水中的溶解能力比在汽油中强(合理即可) (3)BDE 硝酸钾的溶解能力随温度升高而增大(合理即可) (4)20℃时,各取100g水于两只烧杯中,分别逐渐加入氯化铵、氯化钠,至不再溶解,称量两溶液的质量,溶液质量越大,该物质的溶解度越大
解析 (1)根据溶解过程的温度变化图可知,碳酸钠在溶于水的过程中放出热量。(3)由D中未溶解的固体通过升高温度使之溶解可知,硝酸钾的溶解能力随温度升高而增大。
19.(1)46.4t(3分)
(2)解:设可炼出纯铁的质量为x。 1分
Fe3O4+4CO 3Fe+4CO2 2分
232 168
46.4 t x
= 2分
x=33.6 t 1分
理论上可炼出含铁96%的生铁的质量为33.6 t÷96%=35 t 1分
答:理论上可炼出含铁96%的生铁的质量为35 t。
【评分说明】解、设、答共1分,化学方程式未配平、未写反应条件,扣1分;相对分子质量计算错误,但对应关系、比例关系均正确的,扣1分;其他解法,合理均给分。
解析 (1)100 t该铁矿石中含四氧化三铁的质量为100 t×46.4%=46.4 t。(2)根据化学方程式,由四氧化三铁的质量求得铁的质量,进而求得生铁的质量。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024北京课改化学九年级下学期
期中素养综合测试
(满分100分,限时60分钟)
一、选择题(每小题3分,共36分)
1.(2023辽宁抚顺、本溪、辽阳中考)厨房里的下列物质放入水中,能形成溶液的是 ( )
A.面粉 B.白糖
C.植物油 D.辣椒面
2.(2023北京东城二模)铝能加工成铝箔,说明铝具有良好的 ( )
A.导热性 B.延展性
C.导电性 D.抗腐蚀性
3.(2023湖北宜昌中考)实验室配制一定溶质质量分数的氯化钠溶液,下列操作错误的是( )
4.下列有关金属资源的利用与防护不合理的是 ( )
A.经常用钢丝球擦洗铝锅表面,保持洁净
B.在钢铁表面喷油漆可防止生锈
C.废旧金属的回收利用,是保护金属资源的有效途径之一
D.改变金属的组成和结构,铸造成合金材料可优化其性能
5.【跨学科·语文】《吕氏春秋》记载:“金(即铜单质)柔锡(即锡单质)柔,合两柔则为刚(即坚硬)。”这句话说明合金具有的特性是 ( )
A.合金的熔点一般比其组分金属低
B.合金的硬度一般比其组分金属大
C.合金的抗腐蚀性一般比其组分金属强
D.合金的耐磨性一般比其组分金属好
6.(2023湖南衡阳中考)溶液具有广泛的用途,与人们的生活息息相关。下列有关溶液的说法正确的是 ( )
A.凡是均一、稳定的液体一定是溶液
B.饱和溶液一定比不饱和溶液的浓度大
C.硝酸铵固体在溶于水形成溶液的过程中,吸收热量
D.降低饱和溶液的温度后,溶液中溶质的质量分数一定减小
7.(2023四川自贡中考)现有体积大小相同的三种金属X、Y、Z,分别放入三份溶质质量分数相等的足量稀硫酸中,X不发生反应,Y、Z反应生成氢气的质量与反应时间的关系如图所示。X、Y、Z的金属活动性顺序正确的是 ( )
A.X>Y>Z B.X>Z>Y C.Y>Z>X D.Z>Y>X
8.(2023江苏苏州中考)铁是应用最广泛的金属。下列有关说法正确的是 ( )
A.炼铁原理是用合适的物质将单质铁转化为氧化铁
B.将生铁中的大部分碳反应除去得到的钢是纯净物
C.铁制品高温处理后,表面形成的致密氧化膜有防腐作用
D.日常生活中的废旧铁制品直接填埋处理
9.(2023河南驻马店十九中期末)如图为小李同学在实验室中模拟海水晒盐的过程,下列溶液中溶质质量分数最小的是 ( )
A.甲 B.乙 C.丙 D.丁
10.【新独家原创】深海潜水是一项热门的户外运动,但常因潜水者动作失误而引发“潜水减压病”。潜水减压病是由于人从高压到低压时,让原本溶解在血中的某些气体因逸出而形成气泡,造成身体的不良反应或急性功能障碍。关于氮气溶解在血液中,其溶解度与压强的关系最有可能为下图中的哪一条关系线 ( )
A.甲 B.乙 C.丙 D.丁
11.(2022陕西中考A卷)如图所示,将两枚光亮的铁钉分别用细线吊置于甲、乙中,并使部分铁钉露出液面。放置一段时间,出现了锈蚀。下列说法不正确的是 ( )
A.甲、乙中,气体含氧气的体积分数不相等
B.乙中,铁钉在水面下的部分锈蚀最严重
C.甲中,铁钉在植物油内的部分没有锈蚀
D.丙中,导管内上升一段水柱
12.【创新装置】(2023河南宜阳期末)化学兴趣小组的同学模仿工业炼铁原理,设计如图实验,下列有关说法不正确的是 ( )
A.实验开始先通入CO,再点燃酒精喷灯
B.实验结束后,用足量稀盐酸检验玻璃管中的物质,有气泡产生,证明有铁生成
C.一段时间后注射器内溶液变浑浊
D.装置中气球的作用是收集CO2,防止污染空气
二、填空题(共42分)
13.[含评分说明](2023甘肃金昌中考)(6分)金属在生产和生活中应用极为广泛。
(1)生铁和钢是两种含碳量 的铁合金(填“相同”或“不同”)。
(2)下列生活用品利用金属良好导热性的是 (填序号)。
a.镀铬水龙头 b.铸铁暖气片
c.包糖果的铝箔
(3)焊接钢轨的反应原理是铝与氧化铁在高温条件下反应生成铁和氧化铝,该反应的化学方程式为 。
14.(2023山东滨州中考)(10分)下图为甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,请回答下列问题:
(1)当温度为 ℃时,甲物质的溶解度等于丙物质的溶解度;
(2)图中A点表示乙物质在t1 ℃时的 (填“饱和”或“不饱和”)溶液;
(3)若甲中含有少量乙时,可以采用 (填“降温结晶”或“蒸发结晶”)的方法提纯甲;
(4)将t2 ℃时接近饱和的丙溶液变成饱和溶液,下列方法不能达到目的的是 ;
A.蒸发溶剂 B.降低温度
C.增加溶质 D.升高温度
(5)将t2 ℃时甲的饱和溶液100 g稀释成溶质质量分数为25%的溶液,需加水的质量为 g。
15.【推断题】(2023四川自贡中考)(6分)A、B、C、D四种物质均含同一种金属元素,A为赤铁矿的主要成分,B为单质。它们之间的转化关系如下图所示(图中“—”表示物质间能相互发生反应,“→”表示物质间能发生一步转化,部分物质和反应条件已略去)。
(1)C的化学式为 ,D的化学式为 。
(2)A→B的化学方程式为 。
16.(2023四川广安中考)(8分)中国古代典籍中记录了很多化学知识,展示了我国古代人民的智慧。《梦溪笔谈》中记载了用“苦泉水”制取铜的方法:“挹其水熬之,则成胆矾。烹胆矾则成铜,熬胆矾铁釜,久之亦化为铜”。主要流程如图所示:
(1)“熬”的过程类似于下列粗盐提纯实验中的 操作(填序号)。
A.溶解 B.过滤 C.蒸发
(2)“烹”的过程中,胆矾(CuSO4·5H2O)首先转变成水和无水硫酸铜,该反应的基本反应类型是 反应。
(3)写出“铁釜”中发生反应的化学方程式: 。
(4)铁釜外侧容易生锈,是因为铁与空气中的 发生反应。
17.【新素材·传统工艺】(2022四川成都中考)(12分)我国有着悠久的钢铁冶炼史,《天工开物》中记载的“炒钢法”如图1所示,该方法的生产过程可用图2表示。
图1
图2
资料:①潮泥灰主要成分是石灰石。②铁的熔点是1 535 ℃。
根据图文回答下列问题。
(1)常见的铁矿石有赤铁矿和 (写一种)。
(2)不断鼓入空气的目的是 。
(3)炼铁炉中生成铁的化学方程式为 。
(4)撒入潮泥灰主要作用是 。不断翻炒液态生铁,是为了降低 元素的含量。
(5)钢的性能优良,如钢的熔点比纯铁 ,易于加工。
三、实验探究题(共12分)
18.(12分)为了研究物质的溶解现象,进行如下探究活动。
探究Ⅰ:将足量的碳酸钠、氯化钠和硝酸钾三种物质分别溶解在一定量的水中,溶解过程的温度变化如图所示。
探究Ⅱ:
① ② ③
固体溶解,形成紫红色溶液 固体溶解,形成紫红色溶液 固体几乎不溶解
探究Ⅲ:探究过程如图所示。
回答下列问题:
(1)探究Ⅰ中,溶解过程放出热量的物质是 。
(2)对探究Ⅱ中实验现象进行分析,需要做的对比是 。分析得出的结论之一是 (写一条即可)。
(3)探究Ⅲ中,所得溶液一定属于饱和溶液的是 。通过该探究得出的结论是 (答一点即可)。
(4)在上述探究的基础上,同学们想通过探究,比较氯化钠和氯化铵在水中的溶解度大小,探究方案应该是 。
四、计算题(共10分)
19.[含评分说明](2022青海中考)(10分)根据Fe3O4+4CO 3Fe+4CO2反应原理,工业上可用来冶炼铁。现用100 t含四氧化三铁为46.4%的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
(1)该铁矿石中含四氧化三铁质量是 。
(2)理论上可炼出含铁96%的生铁的质量是多少
答案全解全析
1.B 面粉、辣椒面放入水中形成不稳定的悬浊液;植物油放入水中形成不稳定的乳浊液;白糖放入水中形成均一、稳定的溶液,故选B。
2.B 铝能加工成铝箔,说明铝具有良好的延展性。
3.B 量取液体读数时,视线要与量筒内液体凹液面的最低处保持水平,B错误。
4.A 铝的表面有致密的氧化铝薄膜,能保护内部金属不被氧化,经常用钢丝球擦洗铝锅表面会破坏氧化膜,加速铝的腐蚀。
5.B 合金与其组分金属相比,具有硬度大、熔点低、抗腐蚀性强等特点,本题描述的是硬度大,故选B。
6.C 水是均一、稳定的液体,但不是溶液,A错误;饱和溶液的浓度不一定比不饱和溶液的浓度大,B错误;氢氧化钙的溶解度随温度的降低而增大,降低其饱和溶液的温度后,溶液变为不饱和溶液,但溶质的质量分数不变,D错误。
7.D 由题可知,X不与稀硫酸发生反应,Y、Z能与稀硫酸反应,则活动性:Y>X,Z>X;由题图分析可得,至完全反应,Z产生氢气所需时间短,则Z的金属活动性比Y强,故X、Y、Z的金属活动性顺序是Z>Y>X。故选D。
8.C 炼铁原理是用合适的物质将氧化铁(或其他铁的氧化物)转化为单质铁,A错误;钢是一种铁合金,属于混合物,B错误;废旧铁制品应回收利用,既能节约金属资源,又能减少环境污染,D错误。
9.A 甲蒸发水分得到乙,二者溶质质量相同,乙中溶剂质量减小,溶质质量分数:甲<乙;丙中含有未溶解的固体,丙过滤后得到丁,丙、丁为该温度下的饱和溶液,溶质质量分数:丙=丁;乙蒸发水分得到丙,有固体析出,所以乙可能恰好饱和,也可能是不饱和溶液,故溶质质量分数:乙≤丙,则溶质质量分数的关系是甲<乙≤丙=丁。
10.A 结合题给材料信息推断,气体在血液中的溶解度最有可能随压强的增大而增大,故A项符合题意。
11.B 铁的锈蚀过程消耗氧气,乙装置为密闭环境,铁锈蚀过程中会使氧气体积分数减小,而甲装置始终与空气连通,反应后瓶内气体成分与空气成分基本相同,氧气体积分数也基本不变,A正确;乙中铁钉在液面处锈蚀最严重,B不正确;铁钉在植物油内的部分不与水和氧气接触,不发生锈蚀,C正确;乙中消耗了氧气,装置内压强减小,在大气压的作用下丙烧杯内的水被压入导管,导管内会上升一段水柱,D正确。
12.D 实验开始先通入CO,再点燃酒精喷灯,目的是排尽装置中的空气,防止加热时发生爆炸,A正确;实验结束后,用足量稀盐酸检验玻璃管中的物质,有气泡产生,证明有铁生成,B正确;反应生成的二氧化碳能使澄清石灰水变浑浊,C正确;装置中气球的作用是收集CO,防止污染空气,D错误。
13.(1)不同 (2)b (3)2Al+Fe2O32Fe+Al2O3
【评分说明】(3)化学方程式未配平、未写反应条件扣1分,化学式写错不得分。
解析 (1)生铁的含碳量是2%~4.3%,钢的含碳量是0.03%~2%。(2)利用金属良好导热性的是铸铁暖气片。
14.(1)t1 (2)不饱和 (3)降温结晶 (4)B (5)100
解析 (1)分析溶解度曲线图可知,t1 ℃时甲、丙的溶解度曲线相交于A点,说明此时二者溶解度相等。(2)A点为t1 ℃时乙物质溶解度曲线下方的点,表示乙物质在t1 ℃时的不饱和溶液。(3)甲、乙的溶解度均随温度升高而增大,且甲的溶解度受温度变化影响较大,若甲中含有少量乙时,可采用降温结晶的方法提纯甲。(4)丙的溶解度随温度升高而减小,将t2 ℃时接近饱和的丙溶液变成饱和溶液可采用蒸发溶剂、增加溶质或升高温度的方法。(5)t2 ℃时甲物质的溶解度为100 g,因此100 g甲的饱和溶液中溶质质量为50 g、溶剂质量为50 g,根据溶液稀释前后溶质质量不变,得需加水的质量为50 g÷25%-100 g=100 g。
15.(1)FeCl2 Fe3O4 (2)Fe2O3+3CO2Fe+3CO2
解析 A、B、C、D四种物质中均含同一种金属元素,A为赤铁矿的主要成分,则A是氧化铁;B为单质,则B是铁;铁和稀盐酸反应生成氯化亚铁和氢气,铁在氧气中燃烧生成四氧化三铁,则C是氯化亚铁,D是四氧化三铁。
16.(1)C (2)分解 (3)Fe+CuSO4FeSO4+Cu (4)水蒸气、氧气(或H2O、O2)
解析 (1)从苦泉水中得到胆矾,类似于粗盐提纯实验中的蒸发操作,故选C。(2)胆矾转化为水和无水硫酸铜,符合“一变多”的特征,属于分解反应。(3)“铁釜”中发生的反应是铁与硫酸铜反应生成铜和硫酸亚铁。
17.(1)磁铁矿(合理即可) (2)提高炉温 (3)Fe2O3+3CO2Fe+3CO2(或Fe3O4+4CO3Fe+4CO2) (4)除杂 碳(或C) (5)低
解析 (1)常见的铁矿石有赤铁矿、磁铁矿和菱铁矿等。(2)不断鼓入空气的目的是使碳与氧气充分反应,提高炉温。(3)用赤铁矿炼铁时,反应的化学方程式为Fe2O3+3CO2Fe+3CO2;用磁铁矿炼铁时,反应的化学方程式为Fe3O4+4CO3Fe+4CO2。(4)生铁和钢的含碳量不同,不断翻炒液态生铁,目的是使生铁中的碳与氧气反应,降低碳元素的含量。(5)合金的熔点低于组成它的纯金属的熔点。
18.(1)碳酸钠 (2)将①③、②③分别对比 其他条件相同时,高锰酸钾在水中的溶解能力比在汽油中强(合理即可) (3)BDE 硝酸钾的溶解能力随温度升高而增大(合理即可) (4)20℃时,各取100g水于两只烧杯中,分别逐渐加入氯化铵、氯化钠,至不再溶解,称量两溶液的质量,溶液质量越大,该物质的溶解度越大
解析 (1)根据溶解过程的温度变化图可知,碳酸钠在溶于水的过程中放出热量。(3)由D中未溶解的固体通过升高温度使之溶解可知,硝酸钾的溶解能力随温度升高而增大。
19.(1)46.4t(3分)
(2)解:设可炼出纯铁的质量为x。 1分
Fe3O4+4CO 3Fe+4CO2 2分
232 168
46.4 t x
= 2分
x=33.6 t 1分
理论上可炼出含铁96%的生铁的质量为33.6 t÷96%=35 t 1分
答:理论上可炼出含铁96%的生铁的质量为35 t。
【评分说明】解、设、答共1分,化学方程式未配平、未写反应条件,扣1分;相对分子质量计算错误,但对应关系、比例关系均正确的,扣1分;其他解法,合理均给分。
解析 (1)100 t该铁矿石中含四氧化三铁的质量为100 t×46.4%=46.4 t。(2)根据化学方程式,由四氧化三铁的质量求得铁的质量,进而求得生铁的质量。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
