第6部分 第10章 第59讲 物质的检验与鉴别(基础课)(共43张PPT)-2024届高考化学一轮复习
文档属性
| 名称 | 第6部分 第10章 第59讲 物质的检验与鉴别(基础课)(共43张PPT)-2024届高考化学一轮复习 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-31 00:00:00 | ||
图片预览










文档简介
(共43张PPT)
第59讲 物质的检验与鉴别(基础课)
第六部分 化学实验基础
第十章 化学实验基础
1.了解常见气体的检验方法,了解常见离子的检验方法。 2.能对常见物质的组成进行鉴定、检验和分析。 3.了解常见物质的鉴别方法或鉴别方案的评价等。
知识点一 物质的检验
必备知识梳理
关键能力训练
01
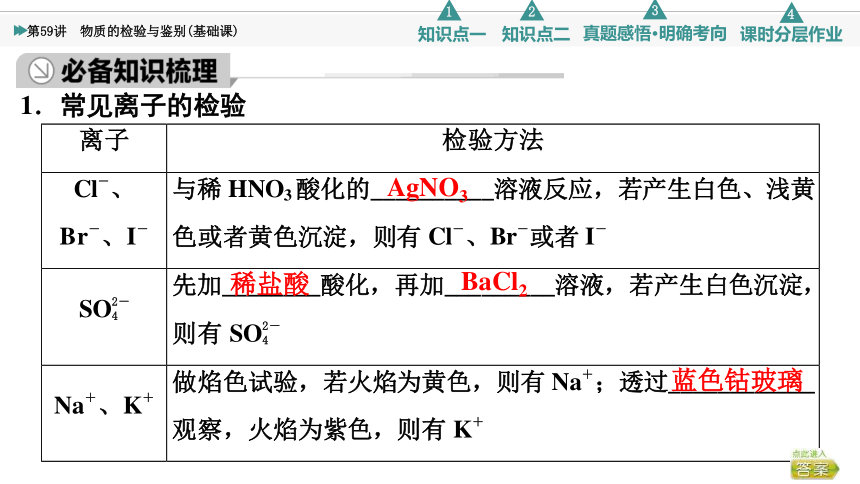
1.常见离子的检验
AgNO3
稀盐酸
BaCl2
蓝色钴玻璃
蓝
KSCN
K3[Fe(CN)6]
离子 检验方法
Fe3+ ①滴加KSCN溶液,若溶液变红色,则有Fe3+;②滴加苯酚溶液,若溶液变____色,则有Fe3+;③滴加NaOH溶液,若立即产生红褐色沉淀,则有Fe3+
紫
2.常见气体的检验
(1)酸性气体的检验
先变浑浊后变澄清
褪去
出现红色
(2)碱性气体的检验
白烟
蓝
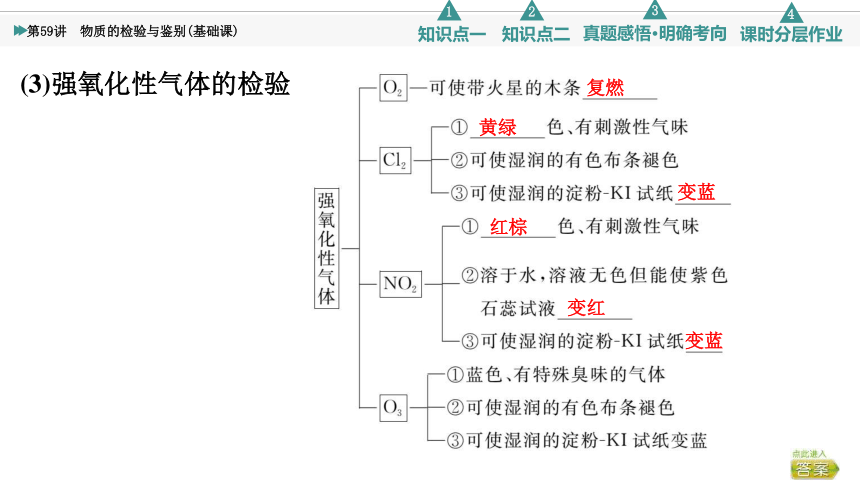
(3)强氧化性气体的检验
复燃
黄绿
变蓝
红棕
变红
变蓝
(4)还原性气体的检验
Cu和H2O
Cu和CO2
红棕色
3.常见有机物的检验
(2)含—CHO的有机物:
①碱性条件下与银氨溶液共热生成银镜。
②碱性条件下与新制Cu(OH)2共热生成砖红色沉淀。
(3)含酚羟基的物质:与FeCl3溶液发生显色反应,或与浓溴水反应生成沉淀。
(4)卤代烃:与碱的水溶液共热,加稀HNO3酸化,然后加AgNO3溶液,有沉淀生成。
(5)蛋白质:遇浓HNO3显黄色,灼烧有烧焦羽毛气味。
(6)淀粉:遇I2变蓝色。
常见物质的检验
1.(2022·唐山模拟)现有一瓶标签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合制剂,某同学为了确认其成分,取部分制剂作为试液,设计并完成了如下实验:
已知:控制溶液pH=4时,Fe(OH)3沉淀完全,Ca2+、Mg2+不沉淀。该同学得出的结论正确的是( )
A.根据现象1可推出该试液中含有Na+
B.根据现象2可推出该试液中不含有葡萄糖酸根
C.根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+
D.根据现象5可推出该试液中一定含有Fe2+
C [Na+的焰色试验呈黄色,但由于在检验过程中向试液中加入了Na+,故不能根据现象1判断原试液中含Na+,A项错误;葡萄糖酸根[CH2OH(CHOH)4COO-]中不含有醛基,不能发生银镜反应,因此不能通过银镜反应来判断葡萄糖酸根是否存在,B项错误;调节pH=4时Fe3+全部沉淀,此时滤液中可能存在的金属离子只有Ca2+和Mg2+,根据加入氨水后无沉淀生成可知滤液中无Mg2+,根据加入Na2CO3溶液后产生沉淀,可知存在Ca2+,C项正确;若原试液中只含有Fe3+,通过图示操作,也可出现现象5,即原试液中不一定含有Fe2+,D项错误。]
序号 A装置 B装置 C装置 判断通入的气体 尾气
处理
Ⅰ CuO由 黑色变 红色 无水硫酸铜变蓝 澄清石灰水变浑浊 ________ 点燃
Ⅱ 无水硫酸铜变蓝 无现象 ________ 点燃
Ⅲ 无现象 澄清石灰水变浑浊 ________ 点燃
Ⅳ ________ ________ NH3 用水吸收
①
②
③
④
⑤
[解析] 由于四种气体均有还原性,故A装置中的现象相同(黑色固体变为红色);四种气体中含氢元素的物质(H2、CH4、NH3)与氧化铜反应后,产物中含水蒸气,能使无水硫酸铜变蓝;四种气体中含碳元素的物质(CO、CH4)与氧化铜反应后,产物中含二氧化碳,能使澄清石灰水变浑浊;NH3极易溶于水,故通入饱和澄清石灰水时石灰水变浑浊;尾气能燃烧的可点燃或收集处理,而NH3则不需要另外处理,通入水中即可。
[答案] ①CH4 ②H2 ③CO ④无水硫酸铜变蓝 ⑤澄清石灰水变浑浊
物质检验的实验及其探究
3.中药材铁华粉的主要成分是醋酸亚铁,检测的流程如图。下列说法错误的是( )
A.气体X中含有醋酸蒸气
B.该铁华粉中可能含有铁单质
C.向滤液中滴入酸性KMnO4溶液,可用于证明Fe2+具有还原性
D.产生蓝色沉淀的反应为K++Fe2++[Fe(CN)6]3-===KFe[Fe(CN)6]↓
C [由图可知,铁华粉中加入稀硫酸,加热时醋酸亚铁与稀硫酸反应生成硫酸亚铁和醋酸蒸气;铁华粉中加入稀盐酸反应生成氢气说明铁华粉中可能还含有铁单质,过滤,向滤液中加入铁氰化钾溶液,溶液中亚铁离子与铁氰化钾反应生成铁氰化亚铁钾蓝色沉淀。滤液中含有氯离子,向滤液中滴入酸性高锰酸钾溶液,酸性条件下氯离子也能与高锰酸钾反应,使溶液褪色,则溶液褪色不能证明亚铁离子具有还原性,C错误。]
4.(2022·淄博模拟)探究甲烷的还原性并检验产物的实验设计如图。下列说法错误的是( )
A.D中可用无水硫酸铜
B.先通足量的甲烷气体,后点燃C处酒精灯
C.若D中盛装碱石灰,根据其质量变化可以推断甲烷组成
C [由题给装置图可知,探究甲烷的还原性并检验产物时应先通足量的甲烷气体排尽装置中的空气,然后点燃C处的酒精灯,装置D中盛有的无水硫酸铜用于检验水的生成,装置E中澄清石灰水用于检验二氧化碳的生成,装置F将未反应的甲烷尾气进行燃烧处理。若D中盛装碱石灰,碱石灰会吸收反应生成的二氧化碳和水,无法分别测定反应生成二氧化碳和水的质量,不能根据其质量变化推断甲烷组成,C错误。]
气体检验中干扰因素的排除
气体检验中干扰因素的排除方法一般是先检验出一种可能具有干扰的气体,并除去该气体,而且要确认该气体已经除尽,再检验其余气体。如在SO2存在的条件下检验CO2,可设计如下检验思路:品红溶液检验SO2→高锰酸钾溶液除去SO2→品红溶液检验SO2是否除尽→澄清石灰水检验CO2。与此类似的还有检验实验室制取的乙烯中含有SO2等。
知识点二 物质的鉴别
02
必备知识梳理
关键能力训练
1.物质鉴别的原则
操作简便 能用物理方法鉴别的不用化学方法,能用一种试剂鉴别的不用多种试剂
现象明显 使待鉴别的物质之间的现象对比度较大
防止干扰 区别Cl-和SO 时,只能用BaCl2溶液不能用AgNO3溶液
2.物质鉴别的方法
物 理 方 法 观察法 抓住物质的特殊颜色、状态等差异性进行区分。如铁和铜的鉴别
气味法 抓住物质的特殊气味进行区分。如氧气和氨气的鉴别
水溶法 抓住物质的溶解性及溶解后现象的差异进行区分。如硝酸铵和氢氧化钠的鉴别
化 学 方 法 加热法 抓住物质热稳定性差异进行区分。如KClO3和KCl的鉴别
指示 剂法 抓住物质的水溶液酸、碱性的差异用酸碱指示剂、pH试纸来区分物质。如HCl、NaOH、NaCl三种无色溶液的鉴别
气体法 抓住所加试剂与待鉴别物质间反应生成气体的差异来区分。如碳酸钠和氢氧化钠的鉴别
沉淀法 抓住所加试剂与待鉴别物质间反应生成沉淀的差异来区分。如硝酸银和硝酸钾的鉴别
3.物质鉴别选择试剂的分析思路
(1)先分析被鉴别物质的水溶性、密度、溶液的酸碱性,确定能否选用水或指示剂进行鉴别。如:a.用水鉴别Na2CO3和CaCO3两种白色粉末;b.用水鉴别苯、CCl4、酒精三种无色液体;c.用pH试纸鉴别NH4Cl、NaCl、Na2CO3三种无色溶液。
(2)在鉴别多种酸、碱、盐的溶液时,可依据“相反原理”确定试剂进行鉴别。即被鉴别的溶液多数呈酸性时,可选用碱或水解呈碱性的盐溶液作试剂;若被鉴别的溶液多数呈碱性时,可选用酸或水解呈酸性的盐溶液作试剂。如:a.用Ba(OH)2溶液鉴别NH4Cl、(NH4)2SO4、H2SO4三种无色溶液;b.用稀盐酸鉴别NaOH、Na2CO3、NaAlO2三种无色溶液。
4.不另加试剂鉴别的两种常见方法
(1)两两混合法:对多种溶液鉴别时,通过两两溶液混合所得现象的差异,分析确定。如Na2CO3溶液、BaCl2溶液和HNO3溶液,根据两两混合所得现象可以鉴别,有沉淀和气体的为Na2CO3,只有沉淀的为BaCl2,只有气体的为HNO3。
(2)顺序滴加法:当需鉴别的物质为两种时,可根据试剂滴加顺序得到的现象,鉴别两物质。如Na2CO3溶液与盐酸,AlCl3溶液与NaOH溶液,AgNO3溶液与氨水等。
1.下列实验可以实现鉴别目的的是( )
A.用澄清石灰水可以鉴别SO2和CO2
B.用湿润的KI 淀粉试纸鉴别Cl2与NO2
C.用酸性KMnO4溶液可以鉴别甲苯和环己烯
D.用新制的Cu(OH)2通过加热可以鉴别乙醛与乙酸
[答案] D
2.现有①NaOH、②Al2(SO4)3、③Ba(NO3)2、④FeCl3、⑤KCl五种溶液,不用任何试剂,被鉴别出来的物质的顺序依次是( )
A.①②③④⑤ B.④①②③⑤
C.②③①④⑤ D.①④②③⑤
B [FeCl3溶液为棕黄色,先鉴别出FeCl3,分别取其他四种溶液少许,滴加FeCl3溶液,反应生成红褐色沉淀的是NaOH;再分别取其他三种溶液少许,滴加NaOH溶液,先产生白色沉淀后溶解的是Al2(SO4)3,再利用Al2(SO4)3分别与剩余的两种溶液反应,生成白色沉淀的是Ba(NO3)2,无现象的是KCl,所以不加任何试剂就可鉴别出的物质的先后顺序为④①②③⑤。]
3.下列有关鉴别的说法正确的是________(填序号)。
①用水可以鉴别CCl4与苯
②用Ca(OH)2溶液鉴别Na2CO3与NaHCO3溶液
③不另外加试剂可以鉴别Al2(SO4)3与NaOH溶液
④不另外加试剂可以鉴别NaAlO2与盐酸溶液
⑤用紫色石蕊试液可以鉴别乙醇、乙酸和苯
⑥用溴水可以鉴别乙烯与甲醛
⑦不另外加试剂可以鉴别NaHCO3溶液、BaCl2溶液、H2SO4溶液
⑧用酸性KMnO4溶液可以鉴别FeCl2与FeCl3溶液
[答案] ①③④⑤⑦
真题感悟·明确考向
03
1.(2022·全国甲卷,T13)根据实验目的,下列实验及现象、结论都正确的是( )
1
3
2
选项 实验目的 实验及现象 结论
A 比较CH3COO-和HCO 的水解常数 分别测浓度均为0.1 mol·L-1的CH3COONH4 和NaHCO3溶液的pH,后者大于前者 Kh(CH3COO-)<
Kh(HCO )
1
3
2
1
3
2
选项 实验目的 实验及现象 结论
D 检验乙醇中是否含有水 向乙醇中加入一小粒金属钠,产生无色气体 乙醇中含有水
1
3
2
2.(2022·浙江1月选考,T25)下列方案设计、现象和结论有不正确的是( )
1
3
2
目的 方案设计 现象和结论
A 检验硫酸厂周边空气中是否含有二氧化硫 用注射器多次抽取空气,慢慢注入盛有酸性KMnO4稀溶液的同一试管中,观察溶液颜色变化 溶液不变色,说明空气中不含二氧化硫
B 鉴定某涂改液中是否存在含氯化合物 取涂改液与KOH溶液混合加热充分反应,取上层清液,硝酸酸化,加入硝酸银溶液,观察现象 出现白色沉淀,说明涂改液中存在含氯化合物
1
3
2
目的 方案设计 现象和结论
C 检验牙膏中是否含有甘油 将适量牙膏样品与蒸馏水混合,搅拌,静置一段时间,取上层清液,加入新制的Cu(OH)2,振荡,观察现象 溶液出现绛蓝色,说明牙膏中含有甘油
D 鉴别食盐与亚硝酸钠 各取少量固体加水溶解,分别滴加含淀粉的KI溶液,振荡,观察溶液颜色变化 溶液变蓝色的为亚硝酸钠;溶液不变蓝的为食盐
D [NaNO2和KI需在酸性条件下反应。]
3.(2022·山东等级考,T11)某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列物质组合不符合要求的是( )
1
3
2
选项 气体 液体 固体粉末
A CO2 饱和Na2CO3溶液 CaCO3
B Cl2 FeCl2溶液 Fe
C HCl Cu(NO3)2溶液 Cu
D NH3 H2O AgCl
1
3
2
谢谢观看 THANK YOU!
第59讲 物质的检验与鉴别(基础课)
第六部分 化学实验基础
第十章 化学实验基础
1.了解常见气体的检验方法,了解常见离子的检验方法。 2.能对常见物质的组成进行鉴定、检验和分析。 3.了解常见物质的鉴别方法或鉴别方案的评价等。
知识点一 物质的检验
必备知识梳理
关键能力训练
01
1.常见离子的检验
AgNO3
稀盐酸
BaCl2
蓝色钴玻璃
蓝
KSCN
K3[Fe(CN)6]
离子 检验方法
Fe3+ ①滴加KSCN溶液,若溶液变红色,则有Fe3+;②滴加苯酚溶液,若溶液变____色,则有Fe3+;③滴加NaOH溶液,若立即产生红褐色沉淀,则有Fe3+
紫
2.常见气体的检验
(1)酸性气体的检验
先变浑浊后变澄清
褪去
出现红色
(2)碱性气体的检验
白烟
蓝
(3)强氧化性气体的检验
复燃
黄绿
变蓝
红棕
变红
变蓝
(4)还原性气体的检验
Cu和H2O
Cu和CO2
红棕色
3.常见有机物的检验
(2)含—CHO的有机物:
①碱性条件下与银氨溶液共热生成银镜。
②碱性条件下与新制Cu(OH)2共热生成砖红色沉淀。
(3)含酚羟基的物质:与FeCl3溶液发生显色反应,或与浓溴水反应生成沉淀。
(4)卤代烃:与碱的水溶液共热,加稀HNO3酸化,然后加AgNO3溶液,有沉淀生成。
(5)蛋白质:遇浓HNO3显黄色,灼烧有烧焦羽毛气味。
(6)淀粉:遇I2变蓝色。
常见物质的检验
1.(2022·唐山模拟)现有一瓶标签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合制剂,某同学为了确认其成分,取部分制剂作为试液,设计并完成了如下实验:
已知:控制溶液pH=4时,Fe(OH)3沉淀完全,Ca2+、Mg2+不沉淀。该同学得出的结论正确的是( )
A.根据现象1可推出该试液中含有Na+
B.根据现象2可推出该试液中不含有葡萄糖酸根
C.根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+
D.根据现象5可推出该试液中一定含有Fe2+
C [Na+的焰色试验呈黄色,但由于在检验过程中向试液中加入了Na+,故不能根据现象1判断原试液中含Na+,A项错误;葡萄糖酸根[CH2OH(CHOH)4COO-]中不含有醛基,不能发生银镜反应,因此不能通过银镜反应来判断葡萄糖酸根是否存在,B项错误;调节pH=4时Fe3+全部沉淀,此时滤液中可能存在的金属离子只有Ca2+和Mg2+,根据加入氨水后无沉淀生成可知滤液中无Mg2+,根据加入Na2CO3溶液后产生沉淀,可知存在Ca2+,C项正确;若原试液中只含有Fe3+,通过图示操作,也可出现现象5,即原试液中不一定含有Fe2+,D项错误。]
序号 A装置 B装置 C装置 判断通入的气体 尾气
处理
Ⅰ CuO由 黑色变 红色 无水硫酸铜变蓝 澄清石灰水变浑浊 ________ 点燃
Ⅱ 无水硫酸铜变蓝 无现象 ________ 点燃
Ⅲ 无现象 澄清石灰水变浑浊 ________ 点燃
Ⅳ ________ ________ NH3 用水吸收
①
②
③
④
⑤
[解析] 由于四种气体均有还原性,故A装置中的现象相同(黑色固体变为红色);四种气体中含氢元素的物质(H2、CH4、NH3)与氧化铜反应后,产物中含水蒸气,能使无水硫酸铜变蓝;四种气体中含碳元素的物质(CO、CH4)与氧化铜反应后,产物中含二氧化碳,能使澄清石灰水变浑浊;NH3极易溶于水,故通入饱和澄清石灰水时石灰水变浑浊;尾气能燃烧的可点燃或收集处理,而NH3则不需要另外处理,通入水中即可。
[答案] ①CH4 ②H2 ③CO ④无水硫酸铜变蓝 ⑤澄清石灰水变浑浊
物质检验的实验及其探究
3.中药材铁华粉的主要成分是醋酸亚铁,检测的流程如图。下列说法错误的是( )
A.气体X中含有醋酸蒸气
B.该铁华粉中可能含有铁单质
C.向滤液中滴入酸性KMnO4溶液,可用于证明Fe2+具有还原性
D.产生蓝色沉淀的反应为K++Fe2++[Fe(CN)6]3-===KFe[Fe(CN)6]↓
C [由图可知,铁华粉中加入稀硫酸,加热时醋酸亚铁与稀硫酸反应生成硫酸亚铁和醋酸蒸气;铁华粉中加入稀盐酸反应生成氢气说明铁华粉中可能还含有铁单质,过滤,向滤液中加入铁氰化钾溶液,溶液中亚铁离子与铁氰化钾反应生成铁氰化亚铁钾蓝色沉淀。滤液中含有氯离子,向滤液中滴入酸性高锰酸钾溶液,酸性条件下氯离子也能与高锰酸钾反应,使溶液褪色,则溶液褪色不能证明亚铁离子具有还原性,C错误。]
4.(2022·淄博模拟)探究甲烷的还原性并检验产物的实验设计如图。下列说法错误的是( )
A.D中可用无水硫酸铜
B.先通足量的甲烷气体,后点燃C处酒精灯
C.若D中盛装碱石灰,根据其质量变化可以推断甲烷组成
C [由题给装置图可知,探究甲烷的还原性并检验产物时应先通足量的甲烷气体排尽装置中的空气,然后点燃C处的酒精灯,装置D中盛有的无水硫酸铜用于检验水的生成,装置E中澄清石灰水用于检验二氧化碳的生成,装置F将未反应的甲烷尾气进行燃烧处理。若D中盛装碱石灰,碱石灰会吸收反应生成的二氧化碳和水,无法分别测定反应生成二氧化碳和水的质量,不能根据其质量变化推断甲烷组成,C错误。]
气体检验中干扰因素的排除
气体检验中干扰因素的排除方法一般是先检验出一种可能具有干扰的气体,并除去该气体,而且要确认该气体已经除尽,再检验其余气体。如在SO2存在的条件下检验CO2,可设计如下检验思路:品红溶液检验SO2→高锰酸钾溶液除去SO2→品红溶液检验SO2是否除尽→澄清石灰水检验CO2。与此类似的还有检验实验室制取的乙烯中含有SO2等。
知识点二 物质的鉴别
02
必备知识梳理
关键能力训练
1.物质鉴别的原则
操作简便 能用物理方法鉴别的不用化学方法,能用一种试剂鉴别的不用多种试剂
现象明显 使待鉴别的物质之间的现象对比度较大
防止干扰 区别Cl-和SO 时,只能用BaCl2溶液不能用AgNO3溶液
2.物质鉴别的方法
物 理 方 法 观察法 抓住物质的特殊颜色、状态等差异性进行区分。如铁和铜的鉴别
气味法 抓住物质的特殊气味进行区分。如氧气和氨气的鉴别
水溶法 抓住物质的溶解性及溶解后现象的差异进行区分。如硝酸铵和氢氧化钠的鉴别
化 学 方 法 加热法 抓住物质热稳定性差异进行区分。如KClO3和KCl的鉴别
指示 剂法 抓住物质的水溶液酸、碱性的差异用酸碱指示剂、pH试纸来区分物质。如HCl、NaOH、NaCl三种无色溶液的鉴别
气体法 抓住所加试剂与待鉴别物质间反应生成气体的差异来区分。如碳酸钠和氢氧化钠的鉴别
沉淀法 抓住所加试剂与待鉴别物质间反应生成沉淀的差异来区分。如硝酸银和硝酸钾的鉴别
3.物质鉴别选择试剂的分析思路
(1)先分析被鉴别物质的水溶性、密度、溶液的酸碱性,确定能否选用水或指示剂进行鉴别。如:a.用水鉴别Na2CO3和CaCO3两种白色粉末;b.用水鉴别苯、CCl4、酒精三种无色液体;c.用pH试纸鉴别NH4Cl、NaCl、Na2CO3三种无色溶液。
(2)在鉴别多种酸、碱、盐的溶液时,可依据“相反原理”确定试剂进行鉴别。即被鉴别的溶液多数呈酸性时,可选用碱或水解呈碱性的盐溶液作试剂;若被鉴别的溶液多数呈碱性时,可选用酸或水解呈酸性的盐溶液作试剂。如:a.用Ba(OH)2溶液鉴别NH4Cl、(NH4)2SO4、H2SO4三种无色溶液;b.用稀盐酸鉴别NaOH、Na2CO3、NaAlO2三种无色溶液。
4.不另加试剂鉴别的两种常见方法
(1)两两混合法:对多种溶液鉴别时,通过两两溶液混合所得现象的差异,分析确定。如Na2CO3溶液、BaCl2溶液和HNO3溶液,根据两两混合所得现象可以鉴别,有沉淀和气体的为Na2CO3,只有沉淀的为BaCl2,只有气体的为HNO3。
(2)顺序滴加法:当需鉴别的物质为两种时,可根据试剂滴加顺序得到的现象,鉴别两物质。如Na2CO3溶液与盐酸,AlCl3溶液与NaOH溶液,AgNO3溶液与氨水等。
1.下列实验可以实现鉴别目的的是( )
A.用澄清石灰水可以鉴别SO2和CO2
B.用湿润的KI 淀粉试纸鉴别Cl2与NO2
C.用酸性KMnO4溶液可以鉴别甲苯和环己烯
D.用新制的Cu(OH)2通过加热可以鉴别乙醛与乙酸
[答案] D
2.现有①NaOH、②Al2(SO4)3、③Ba(NO3)2、④FeCl3、⑤KCl五种溶液,不用任何试剂,被鉴别出来的物质的顺序依次是( )
A.①②③④⑤ B.④①②③⑤
C.②③①④⑤ D.①④②③⑤
B [FeCl3溶液为棕黄色,先鉴别出FeCl3,分别取其他四种溶液少许,滴加FeCl3溶液,反应生成红褐色沉淀的是NaOH;再分别取其他三种溶液少许,滴加NaOH溶液,先产生白色沉淀后溶解的是Al2(SO4)3,再利用Al2(SO4)3分别与剩余的两种溶液反应,生成白色沉淀的是Ba(NO3)2,无现象的是KCl,所以不加任何试剂就可鉴别出的物质的先后顺序为④①②③⑤。]
3.下列有关鉴别的说法正确的是________(填序号)。
①用水可以鉴别CCl4与苯
②用Ca(OH)2溶液鉴别Na2CO3与NaHCO3溶液
③不另外加试剂可以鉴别Al2(SO4)3与NaOH溶液
④不另外加试剂可以鉴别NaAlO2与盐酸溶液
⑤用紫色石蕊试液可以鉴别乙醇、乙酸和苯
⑥用溴水可以鉴别乙烯与甲醛
⑦不另外加试剂可以鉴别NaHCO3溶液、BaCl2溶液、H2SO4溶液
⑧用酸性KMnO4溶液可以鉴别FeCl2与FeCl3溶液
[答案] ①③④⑤⑦
真题感悟·明确考向
03
1.(2022·全国甲卷,T13)根据实验目的,下列实验及现象、结论都正确的是( )
1
3
2
选项 实验目的 实验及现象 结论
A 比较CH3COO-和HCO 的水解常数 分别测浓度均为0.1 mol·L-1的CH3COONH4 和NaHCO3溶液的pH,后者大于前者 Kh(CH3COO-)<
Kh(HCO )
1
3
2
1
3
2
选项 实验目的 实验及现象 结论
D 检验乙醇中是否含有水 向乙醇中加入一小粒金属钠,产生无色气体 乙醇中含有水
1
3
2
2.(2022·浙江1月选考,T25)下列方案设计、现象和结论有不正确的是( )
1
3
2
目的 方案设计 现象和结论
A 检验硫酸厂周边空气中是否含有二氧化硫 用注射器多次抽取空气,慢慢注入盛有酸性KMnO4稀溶液的同一试管中,观察溶液颜色变化 溶液不变色,说明空气中不含二氧化硫
B 鉴定某涂改液中是否存在含氯化合物 取涂改液与KOH溶液混合加热充分反应,取上层清液,硝酸酸化,加入硝酸银溶液,观察现象 出现白色沉淀,说明涂改液中存在含氯化合物
1
3
2
目的 方案设计 现象和结论
C 检验牙膏中是否含有甘油 将适量牙膏样品与蒸馏水混合,搅拌,静置一段时间,取上层清液,加入新制的Cu(OH)2,振荡,观察现象 溶液出现绛蓝色,说明牙膏中含有甘油
D 鉴别食盐与亚硝酸钠 各取少量固体加水溶解,分别滴加含淀粉的KI溶液,振荡,观察溶液颜色变化 溶液变蓝色的为亚硝酸钠;溶液不变蓝的为食盐
D [NaNO2和KI需在酸性条件下反应。]
3.(2022·山东等级考,T11)某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列物质组合不符合要求的是( )
1
3
2
选项 气体 液体 固体粉末
A CO2 饱和Na2CO3溶液 CaCO3
B Cl2 FeCl2溶液 Fe
C HCl Cu(NO3)2溶液 Cu
D NH3 H2O AgCl
1
3
2
谢谢观看 THANK YOU!
同课章节目录
