第十单元 化学实验(2)物质的分离和提纯 精讲课件(共37张PPT)——2024届高考解锁大单元一轮复习
文档属性
| 名称 | 第十单元 化学实验(2)物质的分离和提纯 精讲课件(共37张PPT)——2024届高考解锁大单元一轮复习 |
|
|
| 格式 | pptx | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-01 00:00:00 | ||
图片预览






文档简介
(共37张PPT)
第十单元 化学实验
第二节 物质的分离和提纯
核心素养
科学探究与创新精神:掌握常见物质分离和提纯的方法。
分离、提纯
01
1.分离、提纯
(1)分离、提纯的区别
①物质的分离:根据混合物中各物质通过物理变化或化学变化,将彼此分开的过程,分开后各自要恢复到原来的状态。
②物质的提纯:把混合物中杂质除去,以得到纯净物的过程,如果杂质发生了化学变化,不必恢复为原来的状态。
(2)分类提纯的原则
分离、提纯混合物的常用物理方法
02
2.分离提纯混合物的常用物理方法
过滤
玻璃棒
防止液体溅出
或冲破滤纸
滤纸
漏斗
滤纸
玻璃棒
三层滤纸
烧杯内壁
蒸发
玻璃棒
防止局部温度过高而使液体飞溅
出现大量固体
升华
萃取和分液
远大于
互不相溶
密度差别
不反应
下口放出
上口倒出
(5)沉淀溶解平衡的应用
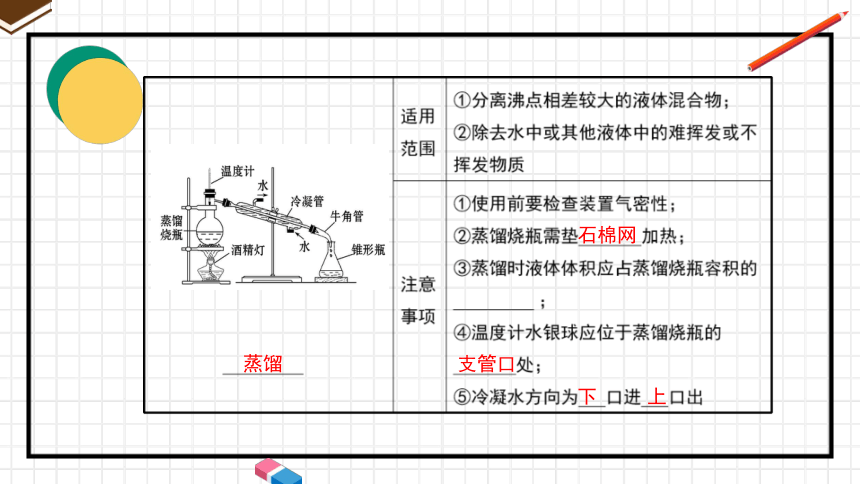
蒸馏
石棉网
支管口
下
上
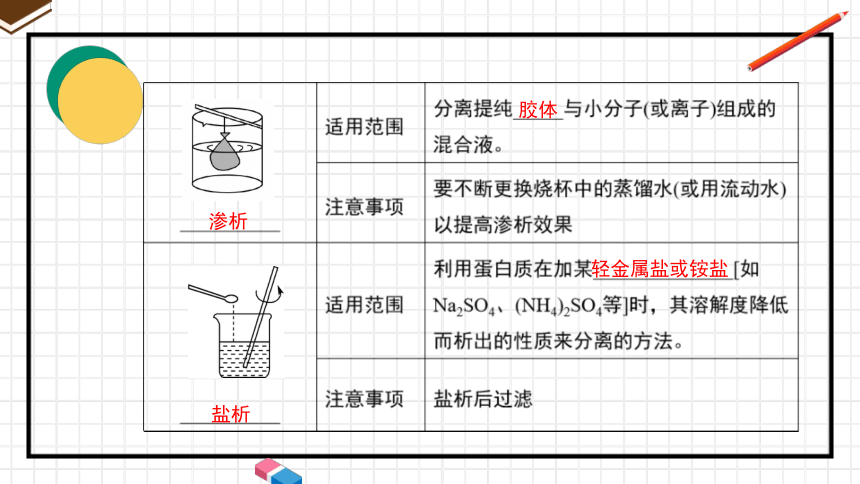
渗析
胶体
盐析
轻金属盐或铵盐
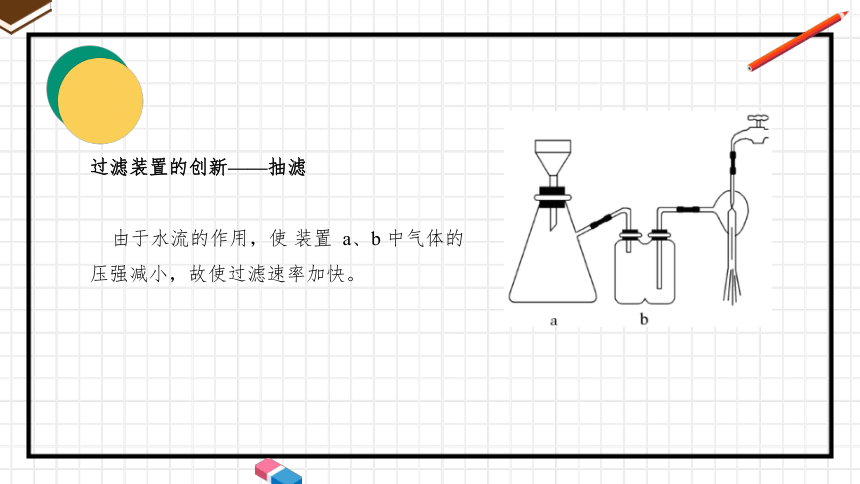
过滤装置的创新——抽滤
由于水流的作用,使 装置 a、b 中气体的压强减小,故使过滤速率加快。
蒸馏、冷凝装置的创新应用
由于冷凝管竖立,使液体混合物能冷凝回流,若以此容器做反应容器,可使反应物循环利用,提高了反应物的转化率。
洗气装置的创新——双耳球吸收法
由于双耳球上端球形容器的容积较大,能有效地防止倒吸。故该装置既能除去气体中的气态杂质,又能防止倒吸。
物质分离提纯常用的化学方法
03
3.物质分离、提纯常用的化学方法
高考常考物质的除杂方法
NaOH溶液
饱和的
NaHCO3溶液
饱和的食盐水
饱和的
NaHCO3溶液
过滤,加热
NaOH溶液
过滤,加热
稀盐酸
过滤
CO2
Cl2
Fe
溴水
新制CaO
蒸馏
NaOH溶液
洗气
饱和的
NaHCO3溶液
分液
基础测评
1.易错易混辨析(正确的画“√”,错误的画“ ”)。
(1)用长颈漏斗分离出乙酸与乙醇反应的产物 ( )
(2)将Cl2与HCl的混合气体通过饱和食盐水可得到纯净的Cl2 ( )
(3)除去Cu粉中混有的CuO:加入稀硝酸溶解、过滤、洗涤、干燥( )
(4)除去CO中的CO2:将混合气体通入NaOH溶液,导管进入洗气瓶时
“短进长出” ( )
(5)用坩埚蒸干NaCl溶液制备NaCl晶体 ( )
(6)用分液漏斗、烧杯、蒸馏水分离Br2和CCl4的混合物 ( )
2.请选用适当的分离方法,分离下列混合物(填序号)。
①过滤 ②蒸发 ③萃取 ④蒸馏 ⑤升华 ⑥分液 ⑦重结晶 ⑧盐析
②
③
①
⑤
④
⑧
⑥
⑦
解题技巧
分离、提纯混合物的物理方法的选择
分离、提纯混合物时,往往要根据混合物的状态、性质等角度选择最佳的方法。
(1)“固-固”混合物的分离提纯方法
解题技巧
(2)“固-液”混合物的分离提纯方法
(3)“液-液”混合物的分离提纯方法
3.物质分离提纯实验中的答题规范
(1)如何提取母液中的成分
①在粗盐的提纯实验中,过滤,舍去不溶性杂质(滤渣)后,怎样从母液中获取NaCl固体 ______________________________________________________。
②若母液是CuSO4饱和溶液,怎样获得CuSO4·5H2O晶体 ____________________________。
加热蒸发,当析出大量NaCl晶体时,停止加热,利用余热蒸干
加热蒸发,冷
却结晶,过滤
(2)需要滤渣时,如何得到纯净的滤渣
在测定Na2SO4和NaCl的混合物中Na2SO4的质量分数时,可以在混合物中
加入过量BaCl2溶液,沉淀S ,然后过滤、洗涤、烘干、称量得到BaSO
4的质量,试问:
①怎样判断S 是否沉淀完全 _______________________________________________________________________________________________。
②过滤完毕后,为什么要洗涤沉淀(即洗涤沉淀的目的) __________________________________________。
在上层清液中,再加入BaCl2溶液,若产生
白色沉淀,说明SO42- 未沉淀完全,反之则沉淀完全
洗去可溶性
杂质(Na+、Cl-等)
③沉淀的洗涤方法 ___________________________________________________________________。
④怎样判断沉淀是否洗净 ___________________________________________________________________________________________________。
沿玻璃棒向漏斗中注水至浸没沉淀,待水自
然流下后,再重复2~3次
取最后一次滤出液少许于试管中,滴加稀HNO3
酸化的AgNO3溶液,若产生白色沉淀,说明沉淀未洗净,反之已洗净
4.现有一瓶乙二醇和丙三醇的混合物,已知它们的性质如表所示,据此将
乙二醇和丙三醇互相分离的最佳方法是 ( )
D
A.萃取法 B.结晶法 C.分液法 D.蒸馏法
5.《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”“以
烧酒复烧二次……价值数倍也”。其方法与分离下列物质的实验方法
在原理上相同的是 ( )
A.甲苯和水
B.硝酸钾和氯化钠
C.乙酸乙酯和乙酸
D.食盐水和泥沙
C
6.实验室提纯含少量氯化钠杂质的硝酸钾的过程如图所示。
下列分析正确的是 ( )
A.操作Ⅰ是过滤,将固体分离除去
B.操作Ⅱ是加热浓缩,趁热过滤,除去杂
质氯化钠
C.操作Ⅲ是过滤、洗涤,将硝酸钾晶体
从溶液中分离出来
D.操作Ⅰ~Ⅲ总共需两次过滤
C
7.如图是分离混合物时常用的仪器,从左至右,对应的混合物分离操作方
法正确的是 ( )
A.蒸发、过滤、蒸馏、分液 B.蒸馏、分液、蒸发、过滤
C.蒸馏、过滤、蒸发、分液 D.蒸发、分液、蒸馏、过滤
B
8.将空气缓慢通过如图所示装置后,在试管中收集到少量稀有气体。空
气在通过a~d装置时,依次除去的气体是 ( )
B
A.O2、N2、H2O、CO2 B.CO2、H2O、O2、N2
C.H2O、CO2、N2、O2 D.N2、O2、CO2、H2O
真题演练
1.(2022·海南·高考真题)《医学入门》中记载我国传统中医提纯铜绿的方法:“水洗净,细研水飞,去石澄清,慢火熬干,”其中未涉及的操作是
A.洗涤 B.粉碎 C.萃取 D.蒸发
C
2.(2022·山东·高考真题)已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲苯、苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是
A.苯胺既可与盐酸也可与溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
C
3.(2021·浙江·高考真题)下列说法不正确的是
A.用纸层析法分离Fe3+和Cu2+,将滤纸上的试样点完全浸入展开剂可提高分离效果
B.将CoCl2·6H2O晶体溶于95%乙醇,加水稀释,溶液颜色由蓝色逐渐转变为粉红色
C.乙酰水杨酸粗产品中加入足量碳酸氢钠溶液,充分反应后过滤,可除去聚合物杂质
D.某些强氧化剂(如:氯酸钾、高锰酸钾)及其混合物不能研磨,否则可能引起爆炸
A
A
4.(2020·全国·高考真题)下列气体去除杂质的方法中,不能实现目的的是
THANKS
谢谢观看
第十单元 化学实验
第二节 物质的分离和提纯
核心素养
科学探究与创新精神:掌握常见物质分离和提纯的方法。
分离、提纯
01
1.分离、提纯
(1)分离、提纯的区别
①物质的分离:根据混合物中各物质通过物理变化或化学变化,将彼此分开的过程,分开后各自要恢复到原来的状态。
②物质的提纯:把混合物中杂质除去,以得到纯净物的过程,如果杂质发生了化学变化,不必恢复为原来的状态。
(2)分类提纯的原则
分离、提纯混合物的常用物理方法
02
2.分离提纯混合物的常用物理方法
过滤
玻璃棒
防止液体溅出
或冲破滤纸
滤纸
漏斗
滤纸
玻璃棒
三层滤纸
烧杯内壁
蒸发
玻璃棒
防止局部温度过高而使液体飞溅
出现大量固体
升华
萃取和分液
远大于
互不相溶
密度差别
不反应
下口放出
上口倒出
(5)沉淀溶解平衡的应用
蒸馏
石棉网
支管口
下
上
渗析
胶体
盐析
轻金属盐或铵盐
过滤装置的创新——抽滤
由于水流的作用,使 装置 a、b 中气体的压强减小,故使过滤速率加快。
蒸馏、冷凝装置的创新应用
由于冷凝管竖立,使液体混合物能冷凝回流,若以此容器做反应容器,可使反应物循环利用,提高了反应物的转化率。
洗气装置的创新——双耳球吸收法
由于双耳球上端球形容器的容积较大,能有效地防止倒吸。故该装置既能除去气体中的气态杂质,又能防止倒吸。
物质分离提纯常用的化学方法
03
3.物质分离、提纯常用的化学方法
高考常考物质的除杂方法
NaOH溶液
饱和的
NaHCO3溶液
饱和的食盐水
饱和的
NaHCO3溶液
过滤,加热
NaOH溶液
过滤,加热
稀盐酸
过滤
CO2
Cl2
Fe
溴水
新制CaO
蒸馏
NaOH溶液
洗气
饱和的
NaHCO3溶液
分液
基础测评
1.易错易混辨析(正确的画“√”,错误的画“ ”)。
(1)用长颈漏斗分离出乙酸与乙醇反应的产物 ( )
(2)将Cl2与HCl的混合气体通过饱和食盐水可得到纯净的Cl2 ( )
(3)除去Cu粉中混有的CuO:加入稀硝酸溶解、过滤、洗涤、干燥( )
(4)除去CO中的CO2:将混合气体通入NaOH溶液,导管进入洗气瓶时
“短进长出” ( )
(5)用坩埚蒸干NaCl溶液制备NaCl晶体 ( )
(6)用分液漏斗、烧杯、蒸馏水分离Br2和CCl4的混合物 ( )
2.请选用适当的分离方法,分离下列混合物(填序号)。
①过滤 ②蒸发 ③萃取 ④蒸馏 ⑤升华 ⑥分液 ⑦重结晶 ⑧盐析
②
③
①
⑤
④
⑧
⑥
⑦
解题技巧
分离、提纯混合物的物理方法的选择
分离、提纯混合物时,往往要根据混合物的状态、性质等角度选择最佳的方法。
(1)“固-固”混合物的分离提纯方法
解题技巧
(2)“固-液”混合物的分离提纯方法
(3)“液-液”混合物的分离提纯方法
3.物质分离提纯实验中的答题规范
(1)如何提取母液中的成分
①在粗盐的提纯实验中,过滤,舍去不溶性杂质(滤渣)后,怎样从母液中获取NaCl固体 ______________________________________________________。
②若母液是CuSO4饱和溶液,怎样获得CuSO4·5H2O晶体 ____________________________。
加热蒸发,当析出大量NaCl晶体时,停止加热,利用余热蒸干
加热蒸发,冷
却结晶,过滤
(2)需要滤渣时,如何得到纯净的滤渣
在测定Na2SO4和NaCl的混合物中Na2SO4的质量分数时,可以在混合物中
加入过量BaCl2溶液,沉淀S ,然后过滤、洗涤、烘干、称量得到BaSO
4的质量,试问:
①怎样判断S 是否沉淀完全 _______________________________________________________________________________________________。
②过滤完毕后,为什么要洗涤沉淀(即洗涤沉淀的目的) __________________________________________。
在上层清液中,再加入BaCl2溶液,若产生
白色沉淀,说明SO42- 未沉淀完全,反之则沉淀完全
洗去可溶性
杂质(Na+、Cl-等)
③沉淀的洗涤方法 ___________________________________________________________________。
④怎样判断沉淀是否洗净 ___________________________________________________________________________________________________。
沿玻璃棒向漏斗中注水至浸没沉淀,待水自
然流下后,再重复2~3次
取最后一次滤出液少许于试管中,滴加稀HNO3
酸化的AgNO3溶液,若产生白色沉淀,说明沉淀未洗净,反之已洗净
4.现有一瓶乙二醇和丙三醇的混合物,已知它们的性质如表所示,据此将
乙二醇和丙三醇互相分离的最佳方法是 ( )
D
A.萃取法 B.结晶法 C.分液法 D.蒸馏法
5.《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”“以
烧酒复烧二次……价值数倍也”。其方法与分离下列物质的实验方法
在原理上相同的是 ( )
A.甲苯和水
B.硝酸钾和氯化钠
C.乙酸乙酯和乙酸
D.食盐水和泥沙
C
6.实验室提纯含少量氯化钠杂质的硝酸钾的过程如图所示。
下列分析正确的是 ( )
A.操作Ⅰ是过滤,将固体分离除去
B.操作Ⅱ是加热浓缩,趁热过滤,除去杂
质氯化钠
C.操作Ⅲ是过滤、洗涤,将硝酸钾晶体
从溶液中分离出来
D.操作Ⅰ~Ⅲ总共需两次过滤
C
7.如图是分离混合物时常用的仪器,从左至右,对应的混合物分离操作方
法正确的是 ( )
A.蒸发、过滤、蒸馏、分液 B.蒸馏、分液、蒸发、过滤
C.蒸馏、过滤、蒸发、分液 D.蒸发、分液、蒸馏、过滤
B
8.将空气缓慢通过如图所示装置后,在试管中收集到少量稀有气体。空
气在通过a~d装置时,依次除去的气体是 ( )
B
A.O2、N2、H2O、CO2 B.CO2、H2O、O2、N2
C.H2O、CO2、N2、O2 D.N2、O2、CO2、H2O
真题演练
1.(2022·海南·高考真题)《医学入门》中记载我国传统中医提纯铜绿的方法:“水洗净,细研水飞,去石澄清,慢火熬干,”其中未涉及的操作是
A.洗涤 B.粉碎 C.萃取 D.蒸发
C
2.(2022·山东·高考真题)已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲苯、苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是
A.苯胺既可与盐酸也可与溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
C
3.(2021·浙江·高考真题)下列说法不正确的是
A.用纸层析法分离Fe3+和Cu2+,将滤纸上的试样点完全浸入展开剂可提高分离效果
B.将CoCl2·6H2O晶体溶于95%乙醇,加水稀释,溶液颜色由蓝色逐渐转变为粉红色
C.乙酰水杨酸粗产品中加入足量碳酸氢钠溶液,充分反应后过滤,可除去聚合物杂质
D.某些强氧化剂(如:氯酸钾、高锰酸钾)及其混合物不能研磨,否则可能引起爆炸
A
A
4.(2020·全国·高考真题)下列气体去除杂质的方法中,不能实现目的的是
THANKS
谢谢观看
同课章节目录
