8.1.2《石油炼制乙烯》巩固提升练(含解析)-苏教版高中化学必修第二册
文档属性
| 名称 | 8.1.2《石油炼制乙烯》巩固提升练(含解析)-苏教版高中化学必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 558.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-02 00:00:00 | ||
图片预览




文档简介
8.1.2《石油炼制乙烯》巩固提升练-苏教版高中化学必修第二册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列物质中,含有碳碳双键的是
A.乙烷 B.乙烯 C.乙醇 D.苯
2.为阿伏加德罗常数的值。下列说法正确的是
A.0.25molZn与一定量浓硫酸反应后完全溶解,生成气体的分子数小于
B.标准状况下,11.2L甲烷和乙烯的混合气体中含氢原子数目为
C.被完全还原为Fe时转移的电子数为
D.9.2g的乙醇中含极性共价键的数目为
3.防护口罩由三氟氯乙烯、聚丙烯或聚乙烯等制成的熔喷布及定位铝条等组成。下列相关化学用语错误的是
A.质子数与中子数相等的氟原子: B.Al的结构示意图:
C.聚乙烯的结构简式为: D.乙烯电子式:
4.下列叙述Ⅰ和叙述Ⅱ均正确并有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 乙醛使溴水褪色 乙醛与发生加成反应
B 氯水使红色布条褪色 氯气具有强氧化性
C 能使溴水褪色 具有漂白性
D 乙烯使酸性高锰酸钾溶液褪色 乙烯被高锰酸钾氧化
A.A B.B C.C D.D
5.工业上由G生产苯乙烯的原理为:。下列说法正确的是
A.G的结构简式中,Et表示丙基 B.苯乙烯与丙烯互为同系物
C.溴水可以鉴别G和苯乙烯 D.该反应类型为加成反应
6.为确定某纯净气体X的成分,进行了如下实验,其中正确的是
选项 操作(现象) 结论
A 将X通入酸性溶液中,溶液褪色 X一定是乙烯
B 将X通入澄清石灰水中,溶液变浑浊 X一定是
C 将X通入品红溶液中,溶液褪色,加热后溶液变红色 X一定是
D 将X通入滴有酚酞试液的溶液中,溶液褪色 X一定是
A.A B.B C.C D.D
7.NA是阿伏加德罗常数的值,下列说法正确的是
A.10g46%的乙醇水溶液所含氢原子的数目为0.6NA
B.5.6g乙烯和环丁烷(C4H8)的混合气体中含有碳原子数为0.4NA
C.1.8gNH中含有的电子数为1.1NA
D.标准状况下,80gSO3所占的体积约为22.4L
8.香茅醇(结构如图所示)是调配各种玫瑰系花香香精不可缺少的原料。下列关于香茅醇的叙述错误的是
A.分子式为C10H20O
B.能发生加成聚合反应
C.分子中所有原子可能共面
D.能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色,但褪色原理不同
9.除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是
选项 含杂质的物质 试剂 除杂方法
A 高锰酸钾溶液 洗气
B NaOH溶液 分液
C NaOH溶液 洗气
D 生石灰 蒸馏
A.A B.B C.C D.D
10.由乙烯的性质推测丙烯的性质,下列说法不正确的是
A.能发生加聚反应 B.燃烧时火焰明亮并伴有黑烟
C.不能使溴的四氯化碳溶液褪色 D.完全燃烧生成的和的物质的量相等
二、填空题
11.回答下列问题:
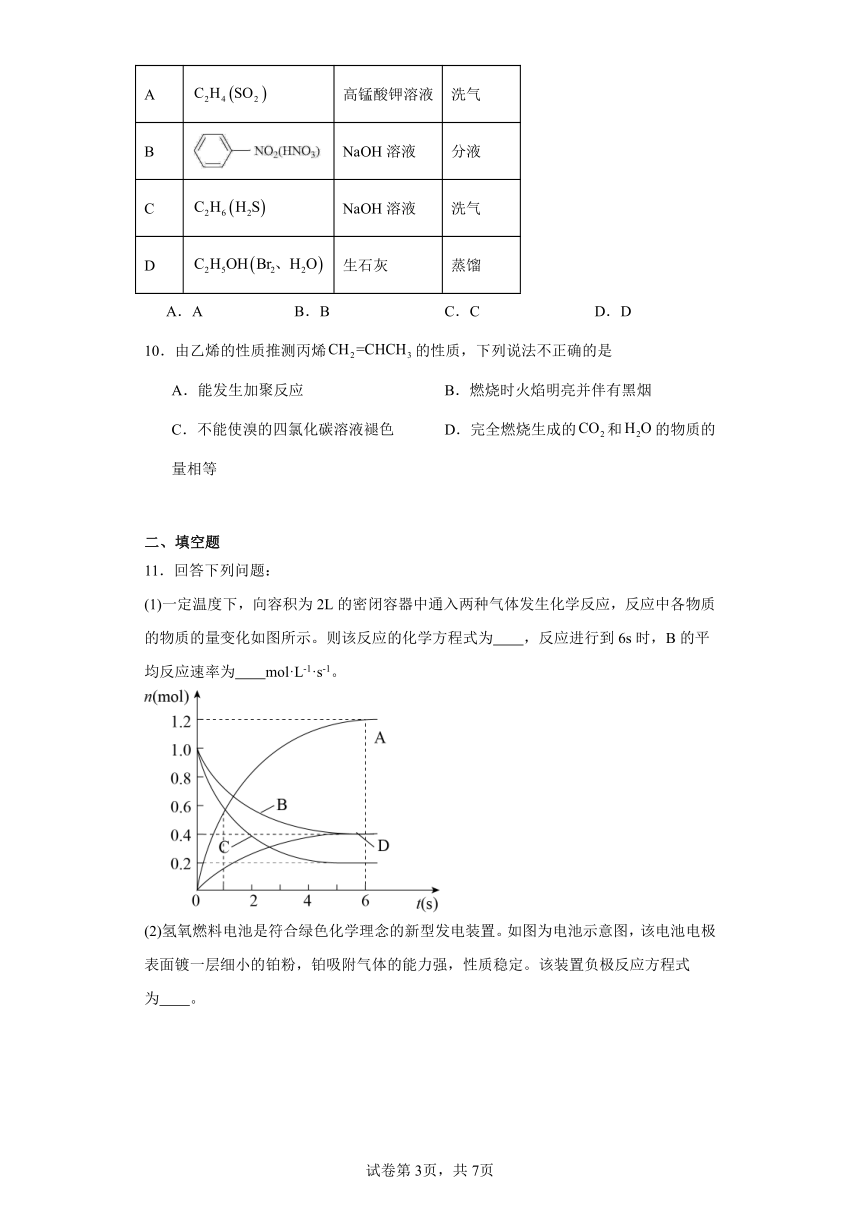
(1)一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则该反应的化学方程式为 ,反应进行到6s时,B的平均反应速率为 mol·L-1·s-1。
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。该装置负极反应方程式为 。
(3)写出乙烷和氯气反应生成一氯乙烷的化学方程式: ,该反应类型为 ;写出乙烯和溴的四氯化碳溶液反应的化学方程式: ,该反应类型为 。
12.已知以下信息:
①A的相对分子质量为28
②2RCH2CHO
A生成B 属于
13.塑料制品是人类日常生活中使用量最大的合成高分子材料,但也造成了严重的环境问题——白色污染。回答下列问题:
(1)石油裂解气是一种复杂的混合气体,含有乙烯、丙烯、丁二烯等不饱和烃,聚丙烯广泛用于服装、毛毯、医疗器械、汽车、自行车等,请写出工业上利用石油裂解气生产聚丙烯的化学方程式 。
(2)下列物质与乙烯互为同系物的是 。
a. b.
c. d.
(3)下列几组物质,可以用分液漏斗分离的是
a. 硝基苯与水 b. 溴的溶液 c. 乙醇与乙酸 d. 乙酸乙酯与溶液
(4)可以将废旧塑料隔绝空气加强热,使其变成氢气、甲烷、乙烯、苯……等有用物质,实验装置如图所示(加热装置略)。
①试管B收集到的产物的结构简式为 。
②锥形瓶中发生反应的方程式为 。
14.乙烯是一种重要化工原料,乙烯的产量可用来衡量一个国家的石油化工发展水平。请回答下列问题
(1)乙烯的结构式为 ,乙烯的空间构型为 ;
(2)将乙烯气体通入酸性高锰酸钾溶液中的现象为: ,乙烯可以在空气中燃烧,化学方程式为 。
(3)在一定条件下,乙烯可以与H2、HCl、Cl2、H2O等物质发生反应。请写出乙烯与水反应的化学方程式 。
15.Ⅰ.请用序号填空:
①13C 与 14C;②正丁烷与异丁烷;③CH3CH3 与 CH3CH2CH3;④和
(1)属于同位素的是 ;
(2)属于同系物的是 ;
(3)属于同分异构体的是 ;
(4)属于同一个物质的是 。
Ⅱ.已知甲烷、乙烯是常见的化工原料,按要求填空:(注意书写方程式的条件)
(5)写出甲烷和氯气光照条件下按分子数之比为 1:1 发生反应的化学方程式: ,该反应的类型为 反应(填有机反应类型,下同)。
(6)写出乙烯与氢气,在催化剂、加热条件下发生反应的化学方程式: ,该反应的类型为 反应。
(7)乙烯常用于制造聚乙烯塑料,在一定条件下该反应的化学方程式: ,该反应的类型为 反应。
16.乙烯
(1)物理性质:
(2)分子式: 结构式: 结构简式: 官能团: 分子构型:
17.H、C、N、O、S是重要的非金属元素,请按要求回答下列问题:
(1)C元素的一种氢化物(分子中含有6个原子)是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是 。(填序号)。
a.该氢化物分子中C原子采用sp2杂化
b.6个原子不在同一平面上
c.只含有4个sp2—sσ键和1个p—pπ键
d.属于含有极性键的非极性分子
(2)相同条件下CO2与SO2分子在水中的溶解度较大的是 (写分子式),理由是 。中的O—C—O键角 (填“>”“<”或“=”)中的O—S—O键角。
(3)已知(CN)2是直线形分子,且有对称性,则(CN)2分子的结构式为 ;其中π键与σ键的个数比为 。
(4)配位化合物[Cu(NH3)4(H2O)2]SO4中,的空间结构呈 ;阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是 (写化学式),判断理由是 。
18.根据要求回答下列有关问题:
Ⅰ.由乙烷和乙烯都能制得一氯乙烷。
(1)由乙烷制一氯乙烷的化学方程式为 ,反应类型为 。
(2)由乙烯制一氯乙烷的化学方程式为 ,反应类型为 。
(3)以上两种方法中 [填“(1)”或“(2)”]更合理,原因是 。
Ⅱ.分别用一个化学方程式解释下列问题。
(1)甲烷与氯气的混合物在漫射光下一段时间,出现白雾: 。
(2)溴水中通入乙烯颜色褪去: 。
(3)工业上通过乙烯水化获得乙醇:
19.常见的烃基
名称 甲基 乙基 正丙基 异丙基 乙烯基
结构简式
20.回答下列问题:
(1)有机气体A是一种植物生长调节剂,其相对分子质量为28。A通入溴水中,能使溴水褪色。A与溴水反应的化学方程式是 。
(2)同分异构现象的广泛存在是造成有机物种类繁多的重要原因之一。C4H10有两种同分异构体,其结构简式分别是 , 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】乙烷属于饱和烃,乙醇相当于乙烷中的一个氢被羟基取代,属于饱和一元醇,苯分子结构中不含碳碳双键,乙烯属于烯烃,含有碳碳双键,故选:B。
2.B
【详解】A.0.25molZn与一定量浓硫酸反应后完全溶解,Zn全部转化为Zn2+,转移电子0.5mol,无论生成SO2还是SO2和H2混合气体,根据得失电子守恒可知生成气体的物质的量为0.25mol,生成气体的分子数等于,故A错误;
B.每个甲烷分子和每个乙烯分子中均含4个H原子,标准状况下,11.2L甲烷和乙烯的混合气体为0.5mol,混合气体中含氢原子数目为,故B正确;
C.为0.5mol,被完全还原为Fe时转移的电子数,为,故C错误;
D.9.2g的乙醇为0.2mol,1个乙醇分子含有7个极性键,0.2mol乙醇中含极性共价键的数目为,故D错误;
故答案为B。
3.B
【详解】A.F为9号元素,质子数与中子数相等,则其质量数为18,其原子符号为,A正确;
B.Al的核外各层电子数目分别为2、8、3,其结构示意图为,B错误;
C.聚乙烯,由乙烯CH2=CH2加聚得到,其结构简式为,C正确;
D.乙烯的结构简式为CH2=CH2,碳和碳之间形成双键,碳和氢之间形成单键,其电子式为,D正确;
故选:B。
4.D
【详解】A.乙醛使溴水褪色是发生氧化反应,乙醛与发生加成反应,两者没有因果关系,A项错误;
B.氯水使红色布条褪色,是因为反应生成的次氯酸,结论错误,B项错误;
C.能使溴水褪色,是因为其具有还原性,结论错误,C项错误;
D.乙烯使酸性高锰酸钾溶液褪色,是因为酸性高锰酸钾溶液具有强氧化性,结论正确,D项正确;
答案选D。
5.C
【详解】A.根据原理方程式可知,G比苯乙烯多2个H,所以G的结构简式中,Et表示乙基,A错误;
B.同系物是指结构相似、分子组成相差若干个“CH2”原子团的有机化合物,苯乙烯分子式是C8H8,丙烯分子式C3H6,两者相差C5H2,因此苯乙烯与丙烯不是互为同系物,B错误;
C.苯乙烯可以使溴水褪色,而G不可以,可以签别,C正确;
D.该反应为消去反应,不是加成反应,D错误;
故选C。
6.C
【详解】A.将X通入酸性 KMnO4溶液中,溶液褪色,则X具有还原性,可以是乙烯,也可以是二氧化硫等,故A错误;
B.能使澄清石灰水变浑浊的可以是二氧化碳,也可以是二氧化硫,故B错误;
C.二氧化硫漂白具有可逆性,将X通入品红溶液中,溶液褪色,加热后溶液变红色,则X一定是 SO2,故C正确;
D.将X通入滴有酚酞试液的 NaOH 溶液中,溶液褪色,X不一定是氯气,也可能具有酸性,将NaOH中和,酚酞试液也会褪色,故D错误;
故选C。
7.B
【详解】A.10g 46%的乙醇水溶液中含有乙醇和水,所含氢原子数目为1.2NA,A错误;
B.乙烯和环丁烷的最简式相同,均是CH2,所以5.6g乙烯和环丁烷(C4H8)的混合气体可看作5.6gCH2,物质的量是0.4mol,含有碳原子数为0.4NA,B正确;
C.一个中含有10个电子,1.8g中含有的电子数为1.0NA,C错误;
D.SO3在标况下不是气体,不能利用气体摩尔体积求算物质的量,D错误;
故答案选B。
8.C
【详解】A.根据物质分子结构可知,物质分子中有10个C原子,1个O原子,不饱和度为1,故有20个H,分子式为C10H20O,A正确;
B.分子中含碳碳双键,故能发生加成聚合反应,B正确;
C.分子中含有8个饱和C原子,由于饱和C原子是四面体结构,因此分子中所有原子不可能共面,C错误;
D.分子中含有不饱和的碳碳双键,能够与溴的四氯化碳溶液发生加成反应而使溴的四氯化碳溶液褪色;使酸性高锰酸钾溶液褪色是由于发生氧化反应,故二者褪色原理不同,D正确;
故答案为C。
9.A
【详解】A.SO2和乙烯都能被高锰酸钾溶液氧化,所以不能用高锰酸钾溶液除去乙烯中的SO2,故A错误;
B.HNO3与NaOH溶液反应产生易溶于水的NaNO3,而硝基苯是难溶于水的液体,二者互不相溶,然后通过分液就可以分离除去,故B正确;
C.H2S与NaOH溶液发生中和反应生成Na2S和水,乙烷不能溶解,也不发生反应,因此通过洗气可以除去乙烷中的H2S,故C正确;
D.生石灰和水反应生成熟石灰,溴溶于碱中,而乙醇不和生石灰反应,所以可以在混有溴和水的乙醇中加入生石灰,然后蒸馏,将乙醇蒸出来,从而除去杂质溴和水,故D正确;
故选A。
10.C
【详解】A.丙烯中含有碳碳双键能发生加聚反应,生成聚丙烯,选项A正确;
B.丙烯与乙烯的含碳量相同,燃烧时有黑烟,选项B正确;
C.丙烯能与溴的四氯化碳溶液发生加成反应而褪色,选项C不正确;
D.乙烯和丙烯都仅含有C、H两种元素,它们在O2中完全燃烧的产物都是CO2和H2O,选项D正确;
答案选C。
11.(1) 3B+4C6A+2D 0.05
(2)H2 -2e- +2OH- =2H2O
(3) CH3CH3+Cl2 CH3CH2Cl +HCl 取代反应 CH2=CH2+Br2→CH3BrCH3Br 加成反应
【详解】(1)从图中可知,6s时反应达到平衡,A物质增加了1.2mol,D物质增加了0.4mol,B物质减少了0.6mol,C物质减少了0.8mol,改变量之比等于系数之比,则该反应的化学方程式为:3B+4C6A+2D;反应进行到6s时,B的平均反应速率为==0.05mol·L-1·s-1。
(2)该电池通入氢气的一极是负极,失去电子,发生氧化反应,以KOH溶液作电解质,则负极反应方程式为:H2 -2e- +2OH- =2H2O。正极是O2通入的一极,电极反应是:O2+4e-+5H2O=4OH-。
(3)乙烷和氯气发生取代反应,生成一氯乙烷,化学方程式:CH3CH3+Cl2 CH3CH2Cl +HCl,反应类型是取代反应;乙烯和溴的四氯化碳溶液发生加成反应,化学方程式:CH2=CH2+Br2→CH3BrCH3Br,反应类型是加成反应。
12.加成反应
【详解】A的相对分子质量为28,则A为CH2=CH2,乙烯与水在催化剂的作用下发生加成反应生成CH3CH2OH,因此A生成B属于加成反应。
13.(1)nCH3CH=CH2
(2)c
(3)ad
(4) CH2=CH2 + Br2 =
【解析】(1)
工业上利用石油裂解气中的丙烯通过加聚反应生产聚丙烯,其方程式为:nCH3CH=CH2
(2)
同系物必须具有相同的结构且分子组成上相差若干个CH2原子团的有机物,故乙烯的同系物只有c。
(3)
能用分液漏斗分离的的两种液体不能相溶,
a.硝基苯与水,不能相溶,可以用分液漏斗分离,a符合题意;
b.溴是有机物可以溶于有机溶剂四氯化碳,不可以用分液漏斗分离,b不符合题意;
c.乙醇和乙酸同是有机物,是相溶的,不可以用分液漏斗分离,c不符合题意;
d.乙酸乙酯是有机物,碳酸钠溶液为无机溶液,不能相溶,可以用分液漏斗分离,d符合题意;
故选ad。
(4)
①因为苯在常温下为液体,故废旧塑料加强热之后的产物中只有苯会被冷水冷凝下来,故B中收集到的为物质的结构简式为
②生成的乙烯使溴水褪色,其方程式为:CH2=CH2 + Br2 =
14.(1) 平面型
(2) 酸性高锰酸钾溶液褪色 C2H4+3O22CO2+2H2O
(3)CH2=CH2+H2OCH3CH2OH
【详解】(1)乙烯的结构式为;乙烯的空间构型为平面型。
(2)将乙烯气体通入酸性高锰酸钾溶液中,乙烯被氧化,酸性高锰酸钾溶液被还原,现象为:酸性高锰酸钾溶液褪色;乙烯可以在空气中燃烧,生成CO2和H2O,化学方程式为:C2H4+3O22CO2+2H2O。
(3)乙烯与水发生加成反应生成乙醇,化学方程式:CH2=CH2+H2OCH3CH2OH。
15.(1)①
(2)③
(3)②
(4)④
(5) CH4+Cl2CH3Cl+HCl 取代
(6) CH2=CH2+H2 CH3CH3 加成
(7) nCH2=CH2 加聚
【详解】(1)同位素是指质子数相同、中子数不同的原子,①13C 与 14C为碳的两种不同核素,两者互为同位素,故答案为:①;
(2)③CH3CH3 与 CH3CH2CH3的结构相似,组成上相差1个“CH2”,两者互为同系物,故答案为:③
(3)②正丁烷与异丁烷的分子式均为C4H10,但结构不同,两者互为同分异构体,故答案为:②;
(4)根据甲烷的正四面体结构可知,其二氯代物只有1种,即④和为同种物质,故答案为:④;
(5)甲烷和氯气光照条件下按分子数之比为 1:1 发生一氯取代反应,其化学方程式为:CH4+Cl2CH3Cl+HCl,其反应类型为取代反应;
(6)乙烯与氢气,在催化剂、加热条件下发生加成反应生成乙烷,其化学方程式为:CH2=CH2+H2 CH3CH3,该反应类型为加成反应;
(7)乙烯在催化剂作用下可发生加聚反应生成聚乙烯,其化学方程式为:nCH2=CH2,反应类型属于加聚反应。
16.(1)无色、稍有气味的气体,难溶于水,密度比空气略小
(2) C2H4 CH2=CH2 碳碳双键
【解析】略
17. ad SO2 SO2为极性分子,CO2为非极性分子,H2O为极性溶剂,极性分子易溶于极性溶剂 > N≡C—C≡N 4:3 四面体形 共价键和配位键 H2O H2O和Cu2+形成的配位键比NH3与Cu2+的弱
【详解】(1)碳元素一种氢化物是的产量作为衡量石油化工发展水平的标志,该氢化物为C2H4,
a.C原子呈1个C=C双键、2个C-H键,杂化轨道数为3,原子采用sp2杂化,选项a正确;
b. 乙烯分子是平面结构,乙烯分子中6个原子处于同一平面,选项b错误;
c.乙烯分子中含有1个C=C双键、4个C-H键,故含有4个sp2—sσ键、1个pσ—pσ键和1个p—pπ键,选项c错误;
d. 乙烯分子中含有1个C=C双键、4个C-H键,属于含有极性键的非极性分子,选项d正确;
答案选ad;
(2)在相同的条件下CO2、SO2在水中的溶解度较大的是,SO2;SO2是极性分子,CO2是非极性分子,水是极性分子,根据相似相溶原理:极性分子易溶于极性溶剂中,所以SO2在水中的溶解度比CO2的大;
故答案为:SO2;SO2为极性分子,CO2为非极性分子,H2O为极性溶剂,极性分子易溶于极性溶剂;
中中心原子C采用sp2杂化,平面型结构,键角是120°;中心原子的杂化方式为sp3杂化,空间构型为三角锥形,键角是107°18,故中的O—C—O键角>中的O—S—O键角;
(3)(CN)2是直线型分子,并有对称性,结构式为:N≡C-C≡N;(CN)2中π键和σ键的个数比为4:3;
(4)中价层电子对个数,4+(6+2-4×2)=4,所以为正四面体结构;
阳离子[Cu(NH3)4(H2O)2]2+中Cu2+与NH3、H2O存在配位键,N、H存极性共价键、H、O存在极性共价键,故阳离子中存在的化学键类型有共价键和配位键;
H2O和Cu2+形成的配位键比NH3与Cu2+的弱,故该化合物加热时首先失去的组分是H2O。
18. CH3CH3+Cl2CH3CH2Cl+HCl 取代反应 CH2=CH2+HClCH3CH2Cl 加成反应 (2) 没有副产物生成 CH4+Cl2CH3Cl+HCl CH2=CH2+Br2→CH2BrCH2Br CH2=CH2+H2OCH3CH2OH
【详解】Ⅰ.(1)乙烷与氯气在光照条件下反应生成一氯乙烷和HCl,反应的化学方程式为CH3CH3+Cl2CH3CH2Cl+HCl,故答案为:CH3CH3+Cl2CH3CH2Cl+HCl;取代反应;
(2)乙烯与HCl发生加成反应生成一氯乙烷,反应的化学方程式为CH2=CH2+HClCH3CH2Cl,故答案为:CH2=CH2+HClCH3CH2Cl;加成反应;
(3)以上两种方法中(2)更合理,反应(1)为烷烃的取代反应,副产物多,反应(2)无副产物,故答案为:(2);没有副产物生成;
Ⅱ. (1)甲烷与氯气在漫射光下一段时间发生取代反应,产物之一为HCl,HCl遇到空气中的水蒸气形成白雾,反应的化学方程式为CH4+Cl2CH3Cl+HCl,故答案为:CH4+Cl2CH3Cl+HCl;
(2)溴水中通入乙烯,乙烯和溴发生加成反应,溴水褪色,反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br,故答案为:CH2=CH2+Br2→CH2BrCH2Br;
(3)工业上通过乙烯水化获得乙醇的化学方程式为CH2=CH2+H2OCH3CH2OH,故答案为:CH2=CH2+H2OCH3CH2OH。
19. -CH3 -CH2CH3或-C2H5 -CH2CH2CH3 -CH(CH3)2 -CH=CH2
【详解】甲烷、乙烷、正丙烷、乙烯分别为CH4、CH3CH3或C2H6、CH3CH2CH3、CH2=CH2;则甲基、乙基、正丙基、异丙基、乙烯基分别为-CH3、-CH2CH3或-C2H5、-CH2CH2CH3、-CH(CH3)2、-CH=CH2。
20.(1)CH2=CH2+Br2→CH2Br-CH2Br
(2) CH3CH2CH2CH3 (CH3)2CHCH3
【解析】(1)
有机气体A是一种植物生长调节剂,其相对分子质量为28。A为乙烯,分子式为C2H4,A的结构简式是CH2=CH2,A通入溴水中,能使溴水褪色,发生加成反应。A与溴水反应的化学方程式是CH2=CH2+Br2→CH2Br-CH2Br。故答案为:CH2=CH2+Br2→CH2Br-CH2Br;
(2)
C4H10有两种同分异构体,有主链4个碳无支链,主链3个碳有1个支链两种异构体,其结构简式分别是CH3CH2CH2CH3,(CH3)2CHCH3,故答案为:CH3CH2CH2CH3;(CH3)2CHCH3。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列物质中,含有碳碳双键的是
A.乙烷 B.乙烯 C.乙醇 D.苯
2.为阿伏加德罗常数的值。下列说法正确的是
A.0.25molZn与一定量浓硫酸反应后完全溶解,生成气体的分子数小于
B.标准状况下,11.2L甲烷和乙烯的混合气体中含氢原子数目为
C.被完全还原为Fe时转移的电子数为
D.9.2g的乙醇中含极性共价键的数目为
3.防护口罩由三氟氯乙烯、聚丙烯或聚乙烯等制成的熔喷布及定位铝条等组成。下列相关化学用语错误的是
A.质子数与中子数相等的氟原子: B.Al的结构示意图:
C.聚乙烯的结构简式为: D.乙烯电子式:
4.下列叙述Ⅰ和叙述Ⅱ均正确并有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 乙醛使溴水褪色 乙醛与发生加成反应
B 氯水使红色布条褪色 氯气具有强氧化性
C 能使溴水褪色 具有漂白性
D 乙烯使酸性高锰酸钾溶液褪色 乙烯被高锰酸钾氧化
A.A B.B C.C D.D
5.工业上由G生产苯乙烯的原理为:。下列说法正确的是
A.G的结构简式中,Et表示丙基 B.苯乙烯与丙烯互为同系物
C.溴水可以鉴别G和苯乙烯 D.该反应类型为加成反应
6.为确定某纯净气体X的成分,进行了如下实验,其中正确的是
选项 操作(现象) 结论
A 将X通入酸性溶液中,溶液褪色 X一定是乙烯
B 将X通入澄清石灰水中,溶液变浑浊 X一定是
C 将X通入品红溶液中,溶液褪色,加热后溶液变红色 X一定是
D 将X通入滴有酚酞试液的溶液中,溶液褪色 X一定是
A.A B.B C.C D.D
7.NA是阿伏加德罗常数的值,下列说法正确的是
A.10g46%的乙醇水溶液所含氢原子的数目为0.6NA
B.5.6g乙烯和环丁烷(C4H8)的混合气体中含有碳原子数为0.4NA
C.1.8gNH中含有的电子数为1.1NA
D.标准状况下,80gSO3所占的体积约为22.4L
8.香茅醇(结构如图所示)是调配各种玫瑰系花香香精不可缺少的原料。下列关于香茅醇的叙述错误的是
A.分子式为C10H20O
B.能发生加成聚合反应
C.分子中所有原子可能共面
D.能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色,但褪色原理不同
9.除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是
选项 含杂质的物质 试剂 除杂方法
A 高锰酸钾溶液 洗气
B NaOH溶液 分液
C NaOH溶液 洗气
D 生石灰 蒸馏
A.A B.B C.C D.D
10.由乙烯的性质推测丙烯的性质,下列说法不正确的是
A.能发生加聚反应 B.燃烧时火焰明亮并伴有黑烟
C.不能使溴的四氯化碳溶液褪色 D.完全燃烧生成的和的物质的量相等
二、填空题
11.回答下列问题:
(1)一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则该反应的化学方程式为 ,反应进行到6s时,B的平均反应速率为 mol·L-1·s-1。
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。该装置负极反应方程式为 。
(3)写出乙烷和氯气反应生成一氯乙烷的化学方程式: ,该反应类型为 ;写出乙烯和溴的四氯化碳溶液反应的化学方程式: ,该反应类型为 。
12.已知以下信息:
①A的相对分子质量为28
②2RCH2CHO
A生成B 属于
13.塑料制品是人类日常生活中使用量最大的合成高分子材料,但也造成了严重的环境问题——白色污染。回答下列问题:
(1)石油裂解气是一种复杂的混合气体,含有乙烯、丙烯、丁二烯等不饱和烃,聚丙烯广泛用于服装、毛毯、医疗器械、汽车、自行车等,请写出工业上利用石油裂解气生产聚丙烯的化学方程式 。
(2)下列物质与乙烯互为同系物的是 。
a. b.
c. d.
(3)下列几组物质,可以用分液漏斗分离的是
a. 硝基苯与水 b. 溴的溶液 c. 乙醇与乙酸 d. 乙酸乙酯与溶液
(4)可以将废旧塑料隔绝空气加强热,使其变成氢气、甲烷、乙烯、苯……等有用物质,实验装置如图所示(加热装置略)。
①试管B收集到的产物的结构简式为 。
②锥形瓶中发生反应的方程式为 。
14.乙烯是一种重要化工原料,乙烯的产量可用来衡量一个国家的石油化工发展水平。请回答下列问题
(1)乙烯的结构式为 ,乙烯的空间构型为 ;
(2)将乙烯气体通入酸性高锰酸钾溶液中的现象为: ,乙烯可以在空气中燃烧,化学方程式为 。
(3)在一定条件下,乙烯可以与H2、HCl、Cl2、H2O等物质发生反应。请写出乙烯与水反应的化学方程式 。
15.Ⅰ.请用序号填空:
①13C 与 14C;②正丁烷与异丁烷;③CH3CH3 与 CH3CH2CH3;④和
(1)属于同位素的是 ;
(2)属于同系物的是 ;
(3)属于同分异构体的是 ;
(4)属于同一个物质的是 。
Ⅱ.已知甲烷、乙烯是常见的化工原料,按要求填空:(注意书写方程式的条件)
(5)写出甲烷和氯气光照条件下按分子数之比为 1:1 发生反应的化学方程式: ,该反应的类型为 反应(填有机反应类型,下同)。
(6)写出乙烯与氢气,在催化剂、加热条件下发生反应的化学方程式: ,该反应的类型为 反应。
(7)乙烯常用于制造聚乙烯塑料,在一定条件下该反应的化学方程式: ,该反应的类型为 反应。
16.乙烯
(1)物理性质:
(2)分子式: 结构式: 结构简式: 官能团: 分子构型:
17.H、C、N、O、S是重要的非金属元素,请按要求回答下列问题:
(1)C元素的一种氢化物(分子中含有6个原子)是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是 。(填序号)。
a.该氢化物分子中C原子采用sp2杂化
b.6个原子不在同一平面上
c.只含有4个sp2—sσ键和1个p—pπ键
d.属于含有极性键的非极性分子
(2)相同条件下CO2与SO2分子在水中的溶解度较大的是 (写分子式),理由是 。中的O—C—O键角 (填“>”“<”或“=”)中的O—S—O键角。
(3)已知(CN)2是直线形分子,且有对称性,则(CN)2分子的结构式为 ;其中π键与σ键的个数比为 。
(4)配位化合物[Cu(NH3)4(H2O)2]SO4中,的空间结构呈 ;阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是 (写化学式),判断理由是 。
18.根据要求回答下列有关问题:
Ⅰ.由乙烷和乙烯都能制得一氯乙烷。
(1)由乙烷制一氯乙烷的化学方程式为 ,反应类型为 。
(2)由乙烯制一氯乙烷的化学方程式为 ,反应类型为 。
(3)以上两种方法中 [填“(1)”或“(2)”]更合理,原因是 。
Ⅱ.分别用一个化学方程式解释下列问题。
(1)甲烷与氯气的混合物在漫射光下一段时间,出现白雾: 。
(2)溴水中通入乙烯颜色褪去: 。
(3)工业上通过乙烯水化获得乙醇:
19.常见的烃基
名称 甲基 乙基 正丙基 异丙基 乙烯基
结构简式
20.回答下列问题:
(1)有机气体A是一种植物生长调节剂,其相对分子质量为28。A通入溴水中,能使溴水褪色。A与溴水反应的化学方程式是 。
(2)同分异构现象的广泛存在是造成有机物种类繁多的重要原因之一。C4H10有两种同分异构体,其结构简式分别是 , 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】乙烷属于饱和烃,乙醇相当于乙烷中的一个氢被羟基取代,属于饱和一元醇,苯分子结构中不含碳碳双键,乙烯属于烯烃,含有碳碳双键,故选:B。
2.B
【详解】A.0.25molZn与一定量浓硫酸反应后完全溶解,Zn全部转化为Zn2+,转移电子0.5mol,无论生成SO2还是SO2和H2混合气体,根据得失电子守恒可知生成气体的物质的量为0.25mol,生成气体的分子数等于,故A错误;
B.每个甲烷分子和每个乙烯分子中均含4个H原子,标准状况下,11.2L甲烷和乙烯的混合气体为0.5mol,混合气体中含氢原子数目为,故B正确;
C.为0.5mol,被完全还原为Fe时转移的电子数,为,故C错误;
D.9.2g的乙醇为0.2mol,1个乙醇分子含有7个极性键,0.2mol乙醇中含极性共价键的数目为,故D错误;
故答案为B。
3.B
【详解】A.F为9号元素,质子数与中子数相等,则其质量数为18,其原子符号为,A正确;
B.Al的核外各层电子数目分别为2、8、3,其结构示意图为,B错误;
C.聚乙烯,由乙烯CH2=CH2加聚得到,其结构简式为,C正确;
D.乙烯的结构简式为CH2=CH2,碳和碳之间形成双键,碳和氢之间形成单键,其电子式为,D正确;
故选:B。
4.D
【详解】A.乙醛使溴水褪色是发生氧化反应,乙醛与发生加成反应,两者没有因果关系,A项错误;
B.氯水使红色布条褪色,是因为反应生成的次氯酸,结论错误,B项错误;
C.能使溴水褪色,是因为其具有还原性,结论错误,C项错误;
D.乙烯使酸性高锰酸钾溶液褪色,是因为酸性高锰酸钾溶液具有强氧化性,结论正确,D项正确;
答案选D。
5.C
【详解】A.根据原理方程式可知,G比苯乙烯多2个H,所以G的结构简式中,Et表示乙基,A错误;
B.同系物是指结构相似、分子组成相差若干个“CH2”原子团的有机化合物,苯乙烯分子式是C8H8,丙烯分子式C3H6,两者相差C5H2,因此苯乙烯与丙烯不是互为同系物,B错误;
C.苯乙烯可以使溴水褪色,而G不可以,可以签别,C正确;
D.该反应为消去反应,不是加成反应,D错误;
故选C。
6.C
【详解】A.将X通入酸性 KMnO4溶液中,溶液褪色,则X具有还原性,可以是乙烯,也可以是二氧化硫等,故A错误;
B.能使澄清石灰水变浑浊的可以是二氧化碳,也可以是二氧化硫,故B错误;
C.二氧化硫漂白具有可逆性,将X通入品红溶液中,溶液褪色,加热后溶液变红色,则X一定是 SO2,故C正确;
D.将X通入滴有酚酞试液的 NaOH 溶液中,溶液褪色,X不一定是氯气,也可能具有酸性,将NaOH中和,酚酞试液也会褪色,故D错误;
故选C。
7.B
【详解】A.10g 46%的乙醇水溶液中含有乙醇和水,所含氢原子数目为1.2NA,A错误;
B.乙烯和环丁烷的最简式相同,均是CH2,所以5.6g乙烯和环丁烷(C4H8)的混合气体可看作5.6gCH2,物质的量是0.4mol,含有碳原子数为0.4NA,B正确;
C.一个中含有10个电子,1.8g中含有的电子数为1.0NA,C错误;
D.SO3在标况下不是气体,不能利用气体摩尔体积求算物质的量,D错误;
故答案选B。
8.C
【详解】A.根据物质分子结构可知,物质分子中有10个C原子,1个O原子,不饱和度为1,故有20个H,分子式为C10H20O,A正确;
B.分子中含碳碳双键,故能发生加成聚合反应,B正确;
C.分子中含有8个饱和C原子,由于饱和C原子是四面体结构,因此分子中所有原子不可能共面,C错误;
D.分子中含有不饱和的碳碳双键,能够与溴的四氯化碳溶液发生加成反应而使溴的四氯化碳溶液褪色;使酸性高锰酸钾溶液褪色是由于发生氧化反应,故二者褪色原理不同,D正确;
故答案为C。
9.A
【详解】A.SO2和乙烯都能被高锰酸钾溶液氧化,所以不能用高锰酸钾溶液除去乙烯中的SO2,故A错误;
B.HNO3与NaOH溶液反应产生易溶于水的NaNO3,而硝基苯是难溶于水的液体,二者互不相溶,然后通过分液就可以分离除去,故B正确;
C.H2S与NaOH溶液发生中和反应生成Na2S和水,乙烷不能溶解,也不发生反应,因此通过洗气可以除去乙烷中的H2S,故C正确;
D.生石灰和水反应生成熟石灰,溴溶于碱中,而乙醇不和生石灰反应,所以可以在混有溴和水的乙醇中加入生石灰,然后蒸馏,将乙醇蒸出来,从而除去杂质溴和水,故D正确;
故选A。
10.C
【详解】A.丙烯中含有碳碳双键能发生加聚反应,生成聚丙烯,选项A正确;
B.丙烯与乙烯的含碳量相同,燃烧时有黑烟,选项B正确;
C.丙烯能与溴的四氯化碳溶液发生加成反应而褪色,选项C不正确;
D.乙烯和丙烯都仅含有C、H两种元素,它们在O2中完全燃烧的产物都是CO2和H2O,选项D正确;
答案选C。
11.(1) 3B+4C6A+2D 0.05
(2)H2 -2e- +2OH- =2H2O
(3) CH3CH3+Cl2 CH3CH2Cl +HCl 取代反应 CH2=CH2+Br2→CH3BrCH3Br 加成反应
【详解】(1)从图中可知,6s时反应达到平衡,A物质增加了1.2mol,D物质增加了0.4mol,B物质减少了0.6mol,C物质减少了0.8mol,改变量之比等于系数之比,则该反应的化学方程式为:3B+4C6A+2D;反应进行到6s时,B的平均反应速率为==0.05mol·L-1·s-1。
(2)该电池通入氢气的一极是负极,失去电子,发生氧化反应,以KOH溶液作电解质,则负极反应方程式为:H2 -2e- +2OH- =2H2O。正极是O2通入的一极,电极反应是:O2+4e-+5H2O=4OH-。
(3)乙烷和氯气发生取代反应,生成一氯乙烷,化学方程式:CH3CH3+Cl2 CH3CH2Cl +HCl,反应类型是取代反应;乙烯和溴的四氯化碳溶液发生加成反应,化学方程式:CH2=CH2+Br2→CH3BrCH3Br,反应类型是加成反应。
12.加成反应
【详解】A的相对分子质量为28,则A为CH2=CH2,乙烯与水在催化剂的作用下发生加成反应生成CH3CH2OH,因此A生成B属于加成反应。
13.(1)nCH3CH=CH2
(2)c
(3)ad
(4) CH2=CH2 + Br2 =
【解析】(1)
工业上利用石油裂解气中的丙烯通过加聚反应生产聚丙烯,其方程式为:nCH3CH=CH2
(2)
同系物必须具有相同的结构且分子组成上相差若干个CH2原子团的有机物,故乙烯的同系物只有c。
(3)
能用分液漏斗分离的的两种液体不能相溶,
a.硝基苯与水,不能相溶,可以用分液漏斗分离,a符合题意;
b.溴是有机物可以溶于有机溶剂四氯化碳,不可以用分液漏斗分离,b不符合题意;
c.乙醇和乙酸同是有机物,是相溶的,不可以用分液漏斗分离,c不符合题意;
d.乙酸乙酯是有机物,碳酸钠溶液为无机溶液,不能相溶,可以用分液漏斗分离,d符合题意;
故选ad。
(4)
①因为苯在常温下为液体,故废旧塑料加强热之后的产物中只有苯会被冷水冷凝下来,故B中收集到的为物质的结构简式为
②生成的乙烯使溴水褪色,其方程式为:CH2=CH2 + Br2 =
14.(1) 平面型
(2) 酸性高锰酸钾溶液褪色 C2H4+3O22CO2+2H2O
(3)CH2=CH2+H2OCH3CH2OH
【详解】(1)乙烯的结构式为;乙烯的空间构型为平面型。
(2)将乙烯气体通入酸性高锰酸钾溶液中,乙烯被氧化,酸性高锰酸钾溶液被还原,现象为:酸性高锰酸钾溶液褪色;乙烯可以在空气中燃烧,生成CO2和H2O,化学方程式为:C2H4+3O22CO2+2H2O。
(3)乙烯与水发生加成反应生成乙醇,化学方程式:CH2=CH2+H2OCH3CH2OH。
15.(1)①
(2)③
(3)②
(4)④
(5) CH4+Cl2CH3Cl+HCl 取代
(6) CH2=CH2+H2 CH3CH3 加成
(7) nCH2=CH2 加聚
【详解】(1)同位素是指质子数相同、中子数不同的原子,①13C 与 14C为碳的两种不同核素,两者互为同位素,故答案为:①;
(2)③CH3CH3 与 CH3CH2CH3的结构相似,组成上相差1个“CH2”,两者互为同系物,故答案为:③
(3)②正丁烷与异丁烷的分子式均为C4H10,但结构不同,两者互为同分异构体,故答案为:②;
(4)根据甲烷的正四面体结构可知,其二氯代物只有1种,即④和为同种物质,故答案为:④;
(5)甲烷和氯气光照条件下按分子数之比为 1:1 发生一氯取代反应,其化学方程式为:CH4+Cl2CH3Cl+HCl,其反应类型为取代反应;
(6)乙烯与氢气,在催化剂、加热条件下发生加成反应生成乙烷,其化学方程式为:CH2=CH2+H2 CH3CH3,该反应类型为加成反应;
(7)乙烯在催化剂作用下可发生加聚反应生成聚乙烯,其化学方程式为:nCH2=CH2,反应类型属于加聚反应。
16.(1)无色、稍有气味的气体,难溶于水,密度比空气略小
(2) C2H4 CH2=CH2 碳碳双键
【解析】略
17. ad SO2 SO2为极性分子,CO2为非极性分子,H2O为极性溶剂,极性分子易溶于极性溶剂 > N≡C—C≡N 4:3 四面体形 共价键和配位键 H2O H2O和Cu2+形成的配位键比NH3与Cu2+的弱
【详解】(1)碳元素一种氢化物是的产量作为衡量石油化工发展水平的标志,该氢化物为C2H4,
a.C原子呈1个C=C双键、2个C-H键,杂化轨道数为3,原子采用sp2杂化,选项a正确;
b. 乙烯分子是平面结构,乙烯分子中6个原子处于同一平面,选项b错误;
c.乙烯分子中含有1个C=C双键、4个C-H键,故含有4个sp2—sσ键、1个pσ—pσ键和1个p—pπ键,选项c错误;
d. 乙烯分子中含有1个C=C双键、4个C-H键,属于含有极性键的非极性分子,选项d正确;
答案选ad;
(2)在相同的条件下CO2、SO2在水中的溶解度较大的是,SO2;SO2是极性分子,CO2是非极性分子,水是极性分子,根据相似相溶原理:极性分子易溶于极性溶剂中,所以SO2在水中的溶解度比CO2的大;
故答案为:SO2;SO2为极性分子,CO2为非极性分子,H2O为极性溶剂,极性分子易溶于极性溶剂;
中中心原子C采用sp2杂化,平面型结构,键角是120°;中心原子的杂化方式为sp3杂化,空间构型为三角锥形,键角是107°18,故中的O—C—O键角>中的O—S—O键角;
(3)(CN)2是直线型分子,并有对称性,结构式为:N≡C-C≡N;(CN)2中π键和σ键的个数比为4:3;
(4)中价层电子对个数,4+(6+2-4×2)=4,所以为正四面体结构;
阳离子[Cu(NH3)4(H2O)2]2+中Cu2+与NH3、H2O存在配位键,N、H存极性共价键、H、O存在极性共价键,故阳离子中存在的化学键类型有共价键和配位键;
H2O和Cu2+形成的配位键比NH3与Cu2+的弱,故该化合物加热时首先失去的组分是H2O。
18. CH3CH3+Cl2CH3CH2Cl+HCl 取代反应 CH2=CH2+HClCH3CH2Cl 加成反应 (2) 没有副产物生成 CH4+Cl2CH3Cl+HCl CH2=CH2+Br2→CH2BrCH2Br CH2=CH2+H2OCH3CH2OH
【详解】Ⅰ.(1)乙烷与氯气在光照条件下反应生成一氯乙烷和HCl,反应的化学方程式为CH3CH3+Cl2CH3CH2Cl+HCl,故答案为:CH3CH3+Cl2CH3CH2Cl+HCl;取代反应;
(2)乙烯与HCl发生加成反应生成一氯乙烷,反应的化学方程式为CH2=CH2+HClCH3CH2Cl,故答案为:CH2=CH2+HClCH3CH2Cl;加成反应;
(3)以上两种方法中(2)更合理,反应(1)为烷烃的取代反应,副产物多,反应(2)无副产物,故答案为:(2);没有副产物生成;
Ⅱ. (1)甲烷与氯气在漫射光下一段时间发生取代反应,产物之一为HCl,HCl遇到空气中的水蒸气形成白雾,反应的化学方程式为CH4+Cl2CH3Cl+HCl,故答案为:CH4+Cl2CH3Cl+HCl;
(2)溴水中通入乙烯,乙烯和溴发生加成反应,溴水褪色,反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br,故答案为:CH2=CH2+Br2→CH2BrCH2Br;
(3)工业上通过乙烯水化获得乙醇的化学方程式为CH2=CH2+H2OCH3CH2OH,故答案为:CH2=CH2+H2OCH3CH2OH。
19. -CH3 -CH2CH3或-C2H5 -CH2CH2CH3 -CH(CH3)2 -CH=CH2
【详解】甲烷、乙烷、正丙烷、乙烯分别为CH4、CH3CH3或C2H6、CH3CH2CH3、CH2=CH2;则甲基、乙基、正丙基、异丙基、乙烯基分别为-CH3、-CH2CH3或-C2H5、-CH2CH2CH3、-CH(CH3)2、-CH=CH2。
20.(1)CH2=CH2+Br2→CH2Br-CH2Br
(2) CH3CH2CH2CH3 (CH3)2CHCH3
【解析】(1)
有机气体A是一种植物生长调节剂,其相对分子质量为28。A为乙烯,分子式为C2H4,A的结构简式是CH2=CH2,A通入溴水中,能使溴水褪色,发生加成反应。A与溴水反应的化学方程式是CH2=CH2+Br2→CH2Br-CH2Br。故答案为:CH2=CH2+Br2→CH2Br-CH2Br;
(2)
C4H10有两种同分异构体,有主链4个碳无支链,主链3个碳有1个支链两种异构体,其结构简式分别是CH3CH2CH2CH3,(CH3)2CHCH3,故答案为:CH3CH2CH2CH3;(CH3)2CHCH3。
答案第1页,共2页
答案第1页,共2页
