2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 学业练习题(含答案)
文档属性
| 名称 | 2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 学业练习题(含答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 383.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-03 00:00:00 | ||
图片预览




文档简介
2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 学业练习题(含答案)
鲁教版第五单元 定量研究化学反应
一、选择题。
1、下列变化中,属于化学变化,并且能用质量守恒定律解释的是( )
A. 5g水受热变成5g水蒸气
B. 5g食盐溶解在95g水中,成为100g食盐溶液
C. 100mL水加入100mL酒精,成为体积小于200mL的溶液
D. 木炭燃烧后质量减少
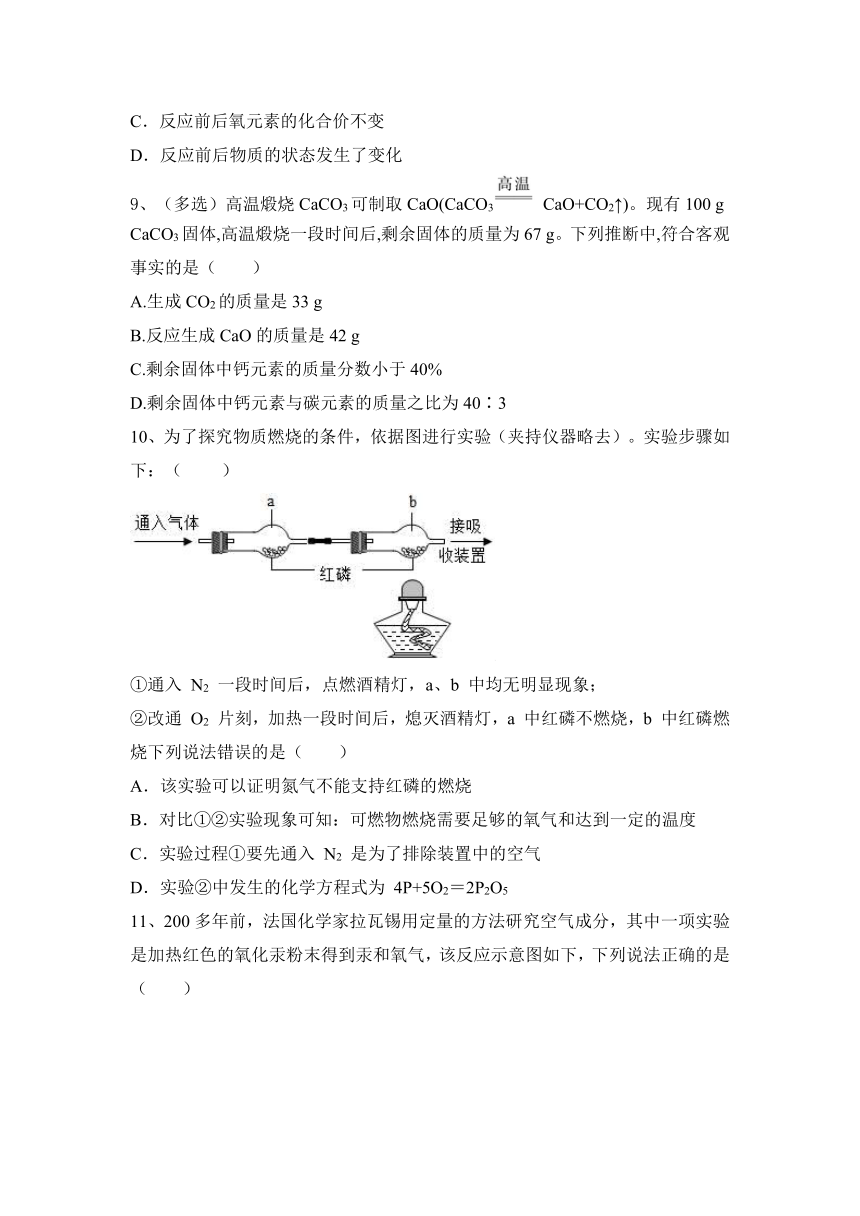
2、密闭容器中发生的某化学反应,各物质的分子数目随时间变化情况如图1所示,物质Y和Z的质量随时间变化情况如图2所示。下列说法正确的是( )
图1 图2
A.该反应属于分解反应 B.X与Z的质量变化比为9∶34
C.该反应前后分子总数保持不变 D.Z一定是化合物
3、我国已经研究出新型水处理剂ClO2的新制法,其反应的微观过程如下图所示。下列说法正确的是( )
A.乙中氯元素的化合价为+5
B.乙物质是氧化物
C.该反应符合质量守恒定律
D.该反应的化学方程式为
4、在反应A+3B 2C+2D中,28 g A与一定质量的B恰好完全反应,生成88 g C。若C、D的相对分子质量之比为22∶9,则A与B的相对分子质量之比为 ( )
A.7∶8 B.8∶7 C.7∶24 D.24∶7
5、某同学为探究物质燃烧条件,设计并完成如图所示实验,根据如图所示的实验现象,下列对此实验的判断与认识中不正确的是( )
A.物质燃烧必须要与氧气(或空气)接触
B.物质燃烧温度必须要达到着火点
C.烧杯中热水的作用只起提高温度的作用
D.铜片上的白磷与红磷的着火点不同,则现象不同
6、一定质量的某化合物完全燃烧,需要3.2g氧气,生成4.4g二氧化碳和1.8g水。下列判断错误的是( )
A.该化合物的质量为3.0g
B.该化合物一定含有碳、氢、氧三种元素
C.该化合物中碳、氢、氧的原子个数比为2:4:1
D.该化合物中碳元素的质量分数是40%
7、下列关于化学反应的说法,错误的是 ( )
A.化学反应前后,分子种类发生改变,原子种类不变
B.化学反应前后,分子数目发生改变,原子数目不变
C.化学反应前后,物质种类发生改变,元素种类不变
D.化学反应的过程就是参加反应的各物质的原子重新组合生成其他物质的过程
8、古代“银针验毒”的原理是: ,关于此反应的说法不正确的是( )
A.X的化学式为Ag2S
B.反应前后元素的种类不变
C.反应前后氧元素的化合价不变
D.反应前后物质的状态发生了变化
9、(多选)高温煅烧CaCO3可制取CaO(CaCO3 CaO+CO2↑)。现有100 g CaCO3固体,高温煅烧一段时间后,剩余固体的质量为67 g。下列推断中,符合客观事实的是( )
A.生成CO2的质量是33 g
B.反应生成CaO的质量是42 g
C.剩余固体中钙元素的质量分数小于40%
D.剩余固体中钙元素与碳元素的质量之比为40∶3
10、为了探究物质燃烧的条件,依据图进行实验(夹持仪器略去)。实验步骤如下:( )
①通入 N2 一段时间后,点燃酒精灯,a、b 中均无明显现象;
②改通 O2 片刻,加热一段时间后,熄灭酒精灯,a 中红磷不燃烧,b 中红磷燃烧下列说法错误的是( )
A.该实验可以证明氮气不能支持红磷的燃烧
B.对比①②实验现象可知:可燃物燃烧需要足够的氧气和达到一定的温度
C.实验过程①要先通入 N2 是为了排除装置中的空气
D.实验②中发生的化学方程式为 4P+5O2=2P2O5
11、200多年前,法国化学家拉瓦锡用定量的方法研究空气成分,其中一项实验是加热红色的氧化汞粉末得到汞和氧气,该反应示意图如下,下列说法正确的是( )
A.氧化汞分解过程中,原子个数没有发生改变
B.氧化汞分解过程中,分子的种类没有发生改变
C.氧化汞分子是该变化中最小的粒子
D.该反应既不是化合反应也不是分解反应
12、下列有关化学反应的认识,不正确的是 ( )
A.通过化学变化,改变世界上物质的种类,但不能改变物质的总质量
B.质量守恒定律揭示了化学变化中宏观物质之间的质量关系,其实质是分子的重新组合
C.质量守恒定律为定量揭示化学反应的规律提供了理论依据
D.人们研究物质的化学变化的意义在于实现物质和能量的转化
13、关于化学方程式2CO O22CO2的读法或叙述正确的是( )
A.一氧化碳加氧气点燃等于二氧化碳
B.两份一氧化碳与一份氧气反应后生成两份二氧化碳
C.一氧化碳、氧气、二氧化碳的质量比为 28:32:44
D.每 56 份质量的一氧化碳与 32 份质量的氧气完全反应,生成 88 份质量的二氧化碳
14、天然气的主要成分是甲烷(CH4)。当氧气不足时,甲烷燃烧会生成CO2、CO和H2O,若16 g甲烷燃烧生成CO2和CO的质量比为11∶7,则参加反应的O2的质量为 ( )
A.48 g B.56 g C.64 g D.72 g
15、通过下图所示实验得出的结论中正确的是( )
①既说明甲烷具有可燃性,又说明甲烷中含有碳、氢两种元素
②既说明二氧化碳密度比空气大,又说明二氧化碳不燃烧也不支持燃烧
③既说明水分解能产生氢气和氧气,又说明水是由H、O两种元素组成
④既可探究可燃物的燃烧条件,又说明白磷的着火点比红磷低
A.①②③ B.①③④ C.②③④ D.①②③④
16、在化学反应中,已知与恰好完全反应,生成C和D的质量比为,又知B的相对分子质量为32,则D的相对分子质量为( )
A.9 B.12 C.18 D.36
二、填空题。
17、小青和同学们一起完成了氢气燃烧的实验,并绘制了该反映的微观示意图。
请你和她讨论下列问题:
(1)图中①的微观实质是________ ,②的微观实质是________ 。
(2)图中方框内表示纯净物的是________(填字母序号).
18、硝酸()是高中化学将要学习的一种常见物质,硝酸中氮元素的化合价为 ,浓硝酸见光会发生分解反应,生成红棕色的气体和一种常见液体以及能供给呼吸的气体,写出该反应的化学方程式:
。
19、下列各组变化中,符合“1+1=2”的事实是(_____)
A、1L水与1L酒精混合后的体积等于2L
B、1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫
C、1g镁与1g氧气反应得到2g氧化镁
D、_________________
20、(1)天然气的化学式为: ,其燃烧的化学方程式为: ;
(2)氢气是最清洁的能源,用化学方程式表示: 。
21、一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
物质 A B C D
反应前质量/g 1.7 2.2 7.9 0.9
反应后质量/g 待测 6.6 0 2.7
则反应后A的质量为___________;该反应所属的基本反应类型是_____________;该反应中B和D两种物质变化的质量比为_________________。
三、综合应用题。
22、2017年5月18日,我国首次海域“可燃冰”试采成功,“可燃冰”的主要成分是甲烷。
(1)用金刚石做成的钻头开采海域“可燃冰”,利用了金刚石的______(填物理性质)。
(2)康康在实验室制取甲烷时用下图装置收集,则气体应该从_________通入(填“m”或“n”)。
(3)下图为甲烷与水反应的微观示意图。请写出对应的化学方程式:
______ 。
(4)运用燃烧法可确定甲烷的元素组成。
①请写出甲烷完全燃烧的化学方程式______ 。
②请写出确定甲烷元素组成的实验方案_______(简要写出实验操作、现象及结论)。
注意:若答对第(5)小题奖励4分,化学试卷总分不超过60分。
(5)“煤改气”可降低煤的消耗,减少空气污染,但也造成了今年的“气荒”,可燃冰的开采将会缓解这一状况。已知:1 kg甲烷完全燃烧放出热量55700 kJ,1 kg含硫5%的标准煤完全燃烧放出热量29000 kJ。请计算:
①1 kg甲烷完全燃烧放出的热量与______千克含硫5%的标准煤完全燃烧放出热量相等(保留小数点后两位)。
②完全燃烧1 kg甲烷,理论上可减少排放二氧化硫______千克。
四、实验探究题。
23、如图是初中化学中的一些重要实验。
(1)图1实验中,能证明可燃物燃烧跟温度有关的实验现象是:
。
(2)通过图2中A、B对比说明燃烧需要的条件是 。
(3)切割白磷时,应在水下进行。其原因是 。
五、计算类题。
24、科学研究中,常通过对实验数据的分析计算,得出某未知物质的相对分子质量,从而推测该物质的分子式。某科研小组经反复实验,发现2A+3B 2C+4D中,3.2 g A恰好和4.8 g B完全反应,生成4.4 g C。请问:
(1)同时生成D的质量为 g。
(2)若D的相对分子质量为18,求A的相对分子质量。
2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 学业练习题(含答案)
鲁教版第五单元 定量研究化学反应
一、选择题。
1、下列变化中,属于化学变化,并且能用质量守恒定律解释的是( )
A. 5g水受热变成5g水蒸气
B. 5g食盐溶解在95g水中,成为100g食盐溶液
C. 100mL水加入100mL酒精,成为体积小于200mL的溶液
D. 木炭燃烧后质量减少
【答案】D
2、密闭容器中发生的某化学反应,各物质的分子数目随时间变化情况如图1所示,物质Y和Z的质量随时间变化情况如图2所示。下列说法正确的是( )
图1 图2
A.该反应属于分解反应 B.X与Z的质量变化比为9∶34
C.该反应前后分子总数保持不变 D.Z一定是化合物
【答案】D
3、我国已经研究出新型水处理剂ClO2的新制法,其反应的微观过程如下图所示。下列说法正确的是( )
A.乙中氯元素的化合价为+5
B.乙物质是氧化物
C.该反应符合质量守恒定律
D.该反应的化学方程式为
【答案】C
4、在反应A+3B 2C+2D中,28 g A与一定质量的B恰好完全反应,生成88 g C。若C、D的相对分子质量之比为22∶9,则A与B的相对分子质量之比为 ( )
A.7∶8 B.8∶7 C.7∶24 D.24∶7
【答案】A
5、某同学为探究物质燃烧条件,设计并完成如图所示实验,根据如图所示的实验现象,下列对此实验的判断与认识中不正确的是( )
A.物质燃烧必须要与氧气(或空气)接触
B.物质燃烧温度必须要达到着火点
C.烧杯中热水的作用只起提高温度的作用
D.铜片上的白磷与红磷的着火点不同,则现象不同
【答案】C
6、一定质量的某化合物完全燃烧,需要3.2g氧气,生成4.4g二氧化碳和1.8g水。下列判断错误的是( )
A.该化合物的质量为3.0g
B.该化合物一定含有碳、氢、氧三种元素
C.该化合物中碳、氢、氧的原子个数比为2:4:1
D.该化合物中碳元素的质量分数是40%
【答案】C
7、下列关于化学反应的说法,错误的是 ( )
A.化学反应前后,分子种类发生改变,原子种类不变
B.化学反应前后,分子数目发生改变,原子数目不变
C.化学反应前后,物质种类发生改变,元素种类不变
D.化学反应的过程就是参加反应的各物质的原子重新组合生成其他物质的过程
【答案】B
8、古代“银针验毒”的原理是: ,关于此反应的说法不正确的是( )
A.X的化学式为Ag2S
B.反应前后元素的种类不变
C.反应前后氧元素的化合价不变
D.反应前后物质的状态发生了变化
【答案】C
9、(多选)高温煅烧CaCO3可制取CaO(CaCO3 CaO+CO2↑)。现有100 g CaCO3固体,高温煅烧一段时间后,剩余固体的质量为67 g。下列推断中,符合客观事实的是( )
A.生成CO2的质量是33 g
B.反应生成CaO的质量是42 g
C.剩余固体中钙元素的质量分数小于40%
D.剩余固体中钙元素与碳元素的质量之比为40∶3
【答案】ABD
10、为了探究物质燃烧的条件,依据图进行实验(夹持仪器略去)。实验步骤如下:( )
①通入 N2 一段时间后,点燃酒精灯,a、b 中均无明显现象;
②改通 O2 片刻,加热一段时间后,熄灭酒精灯,a 中红磷不燃烧,b 中红磷燃烧下列说法错误的是( )
A.该实验可以证明氮气不能支持红磷的燃烧
B.对比①②实验现象可知:可燃物燃烧需要足够的氧气和达到一定的温度
C.实验过程①要先通入 N2 是为了排除装置中的空气
D.实验②中发生的化学方程式为 4P+5O2=2P2O5
【答案】D
11、200多年前,法国化学家拉瓦锡用定量的方法研究空气成分,其中一项实验是加热红色的氧化汞粉末得到汞和氧气,该反应示意图如下,下列说法正确的是( )
A.氧化汞分解过程中,原子个数没有发生改变
B.氧化汞分解过程中,分子的种类没有发生改变
C.氧化汞分子是该变化中最小的粒子
D.该反应既不是化合反应也不是分解反应
【答案】A
12、下列有关化学反应的认识,不正确的是 ( )
A.通过化学变化,改变世界上物质的种类,但不能改变物质的总质量
B.质量守恒定律揭示了化学变化中宏观物质之间的质量关系,其实质是分子的重新组合
C.质量守恒定律为定量揭示化学反应的规律提供了理论依据
D.人们研究物质的化学变化的意义在于实现物质和能量的转化
【答案】B
13、关于化学方程式2CO O22CO2的读法或叙述正确的是( )
A.一氧化碳加氧气点燃等于二氧化碳
B.两份一氧化碳与一份氧气反应后生成两份二氧化碳
C.一氧化碳、氧气、二氧化碳的质量比为 28:32:44
D.每 56 份质量的一氧化碳与 32 份质量的氧气完全反应,生成 88 份质量的二氧化碳
【答案】D
14、天然气的主要成分是甲烷(CH4)。当氧气不足时,甲烷燃烧会生成CO2、CO和H2O,若16 g甲烷燃烧生成CO2和CO的质量比为11∶7,则参加反应的O2的质量为 ( )
A.48 g B.56 g C.64 g D.72 g
【答案】B
15、通过下图所示实验得出的结论中正确的是( )
①既说明甲烷具有可燃性,又说明甲烷中含有碳、氢两种元素
②既说明二氧化碳密度比空气大,又说明二氧化碳不燃烧也不支持燃烧
③既说明水分解能产生氢气和氧气,又说明水是由H、O两种元素组成
④既可探究可燃物的燃烧条件,又说明白磷的着火点比红磷低
A.①②③ B.①③④ C.②③④ D.①②③④
【答案】C
16、在化学反应中,已知与恰好完全反应,生成C和D的质量比为,又知B的相对分子质量为32,则D的相对分子质量为( )
A.9 B.12 C.18 D.36
【答案】C
二、填空题。
17、小青和同学们一起完成了氢气燃烧的实验,并绘制了该反映的微观示意图。
请你和她讨论下列问题:
(1)图中①的微观实质是________ ,②的微观实质是________ 。
(2)图中方框内表示纯净物的是________(填字母序号).
【答案】氢分子分解成氢原子,氧分子分解成氧原子
氢原子和氧原子结合成了水分子 C
18、硝酸()是高中化学将要学习的一种常见物质,硝酸中氮元素的化合价为 ,浓硝酸见光会发生分解反应,生成红棕色的气体和一种常见液体以及能供给呼吸的气体,写出该反应的化学方程式:
。
【答案】+5 ↑+↑
19、下列各组变化中,符合“1+1=2”的事实是(_____)
A、1L水与1L酒精混合后的体积等于2L
B、1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫
C、1g镁与1g氧气反应得到2g氧化镁
D、_________________
【答案】B 1g水与1g酒精混合后的质量等于2g
20、(1)天然气的化学式为: ,其燃烧的化学方程式为: ;
(2)氢气是最清洁的能源,用化学方程式表示: 。
【答案】(1)CH4;CH4 +2O2 CO2 +2H2O;
(2)2H2 + O22H2O
21、一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
物质 A B C D
反应前质量/g 1.7 2.2 7.9 0.9
反应后质量/g 待测 6.6 0 2.7
则反应后A的质量为___________;该反应所属的基本反应类型是_____________;该反应中B和D两种物质变化的质量比为_________________。
【答案】(1) 3.4g (2)分解反应 (3)22:9
三、综合应用题。
22、2017年5月18日,我国首次海域“可燃冰”试采成功,“可燃冰”的主要成分是甲烷。
(1)用金刚石做成的钻头开采海域“可燃冰”,利用了金刚石的______(填物理性质)。
(2)康康在实验室制取甲烷时用下图装置收集,则气体应该从_________通入(填“m”或“n”)。
(3)下图为甲烷与水反应的微观示意图。请写出对应的化学方程式:
______ 。
(4)运用燃烧法可确定甲烷的元素组成。
①请写出甲烷完全燃烧的化学方程式______ 。
②请写出确定甲烷元素组成的实验方案_______(简要写出实验操作、现象及结论)。
注意:若答对第(5)小题奖励4分,化学试卷总分不超过60分。
(5)“煤改气”可降低煤的消耗,减少空气污染,但也造成了今年的“气荒”,可燃冰的开采将会缓解这一状况。已知:1 kg甲烷完全燃烧放出热量55700 kJ,1 kg含硫5%的标准煤完全燃烧放出热量29000 kJ。请计算:
①1 kg甲烷完全燃烧放出的热量与______千克含硫5%的标准煤完全燃烧放出热量相等(保留小数点后两位)。
②完全燃烧1 kg甲烷,理论上可减少排放二氧化硫______千克。
【答案】(1)硬度大 (2)n (4)CH4+H2OCO+3H2
(4)CH4 + 2O2CO2 + 2H2O 验纯后,点燃甲烷,用干而冷的小烧杯罩住火焰,烧杯壁有水雾,说明含有氢元素,迅速倒转烧杯,加入少量澄清石灰水振荡,发现石灰水变浑浊,说明含有碳元素。(或其它合理答案)
(5)1.92 0.19
四、实验探究题。
23、如图是初中化学中的一些重要实验。
(1)图1实验中,能证明可燃物燃烧跟温度有关的实验现象是:
。
(2)通过图2中A、B对比说明燃烧需要的条件是 。
(3)切割白磷时,应在水下进行。其原因是 。
【答案】(1)铜片上的白磷燃烧,红磷不燃烧;
(2)燃烧需要氧气(或空气);
(3)防止在空气中切割时白磷自燃。
五、计算类题。
24、科学研究中,常通过对实验数据的分析计算,得出某未知物质的相对分子质量,从而推测该物质的分子式。某科研小组经反复实验,发现2A+3B 2C+4D中,3.2 g A恰好和4.8 g B完全反应,生成4.4 g C。请问:
(1)同时生成D的质量为 g。
(2)若D的相对分子质量为18,求A的相对分子质量。
【答案】(1)3.6; (2)32。
鲁教版第五单元 定量研究化学反应
一、选择题。
1、下列变化中,属于化学变化,并且能用质量守恒定律解释的是( )
A. 5g水受热变成5g水蒸气
B. 5g食盐溶解在95g水中,成为100g食盐溶液
C. 100mL水加入100mL酒精,成为体积小于200mL的溶液
D. 木炭燃烧后质量减少
2、密闭容器中发生的某化学反应,各物质的分子数目随时间变化情况如图1所示,物质Y和Z的质量随时间变化情况如图2所示。下列说法正确的是( )
图1 图2
A.该反应属于分解反应 B.X与Z的质量变化比为9∶34
C.该反应前后分子总数保持不变 D.Z一定是化合物
3、我国已经研究出新型水处理剂ClO2的新制法,其反应的微观过程如下图所示。下列说法正确的是( )
A.乙中氯元素的化合价为+5
B.乙物质是氧化物
C.该反应符合质量守恒定律
D.该反应的化学方程式为
4、在反应A+3B 2C+2D中,28 g A与一定质量的B恰好完全反应,生成88 g C。若C、D的相对分子质量之比为22∶9,则A与B的相对分子质量之比为 ( )
A.7∶8 B.8∶7 C.7∶24 D.24∶7
5、某同学为探究物质燃烧条件,设计并完成如图所示实验,根据如图所示的实验现象,下列对此实验的判断与认识中不正确的是( )
A.物质燃烧必须要与氧气(或空气)接触
B.物质燃烧温度必须要达到着火点
C.烧杯中热水的作用只起提高温度的作用
D.铜片上的白磷与红磷的着火点不同,则现象不同
6、一定质量的某化合物完全燃烧,需要3.2g氧气,生成4.4g二氧化碳和1.8g水。下列判断错误的是( )
A.该化合物的质量为3.0g
B.该化合物一定含有碳、氢、氧三种元素
C.该化合物中碳、氢、氧的原子个数比为2:4:1
D.该化合物中碳元素的质量分数是40%
7、下列关于化学反应的说法,错误的是 ( )
A.化学反应前后,分子种类发生改变,原子种类不变
B.化学反应前后,分子数目发生改变,原子数目不变
C.化学反应前后,物质种类发生改变,元素种类不变
D.化学反应的过程就是参加反应的各物质的原子重新组合生成其他物质的过程
8、古代“银针验毒”的原理是: ,关于此反应的说法不正确的是( )
A.X的化学式为Ag2S
B.反应前后元素的种类不变
C.反应前后氧元素的化合价不变
D.反应前后物质的状态发生了变化
9、(多选)高温煅烧CaCO3可制取CaO(CaCO3 CaO+CO2↑)。现有100 g CaCO3固体,高温煅烧一段时间后,剩余固体的质量为67 g。下列推断中,符合客观事实的是( )
A.生成CO2的质量是33 g
B.反应生成CaO的质量是42 g
C.剩余固体中钙元素的质量分数小于40%
D.剩余固体中钙元素与碳元素的质量之比为40∶3
10、为了探究物质燃烧的条件,依据图进行实验(夹持仪器略去)。实验步骤如下:( )
①通入 N2 一段时间后,点燃酒精灯,a、b 中均无明显现象;
②改通 O2 片刻,加热一段时间后,熄灭酒精灯,a 中红磷不燃烧,b 中红磷燃烧下列说法错误的是( )
A.该实验可以证明氮气不能支持红磷的燃烧
B.对比①②实验现象可知:可燃物燃烧需要足够的氧气和达到一定的温度
C.实验过程①要先通入 N2 是为了排除装置中的空气
D.实验②中发生的化学方程式为 4P+5O2=2P2O5
11、200多年前,法国化学家拉瓦锡用定量的方法研究空气成分,其中一项实验是加热红色的氧化汞粉末得到汞和氧气,该反应示意图如下,下列说法正确的是( )
A.氧化汞分解过程中,原子个数没有发生改变
B.氧化汞分解过程中,分子的种类没有发生改变
C.氧化汞分子是该变化中最小的粒子
D.该反应既不是化合反应也不是分解反应
12、下列有关化学反应的认识,不正确的是 ( )
A.通过化学变化,改变世界上物质的种类,但不能改变物质的总质量
B.质量守恒定律揭示了化学变化中宏观物质之间的质量关系,其实质是分子的重新组合
C.质量守恒定律为定量揭示化学反应的规律提供了理论依据
D.人们研究物质的化学变化的意义在于实现物质和能量的转化
13、关于化学方程式2CO O22CO2的读法或叙述正确的是( )
A.一氧化碳加氧气点燃等于二氧化碳
B.两份一氧化碳与一份氧气反应后生成两份二氧化碳
C.一氧化碳、氧气、二氧化碳的质量比为 28:32:44
D.每 56 份质量的一氧化碳与 32 份质量的氧气完全反应,生成 88 份质量的二氧化碳
14、天然气的主要成分是甲烷(CH4)。当氧气不足时,甲烷燃烧会生成CO2、CO和H2O,若16 g甲烷燃烧生成CO2和CO的质量比为11∶7,则参加反应的O2的质量为 ( )
A.48 g B.56 g C.64 g D.72 g
15、通过下图所示实验得出的结论中正确的是( )
①既说明甲烷具有可燃性,又说明甲烷中含有碳、氢两种元素
②既说明二氧化碳密度比空气大,又说明二氧化碳不燃烧也不支持燃烧
③既说明水分解能产生氢气和氧气,又说明水是由H、O两种元素组成
④既可探究可燃物的燃烧条件,又说明白磷的着火点比红磷低
A.①②③ B.①③④ C.②③④ D.①②③④
16、在化学反应中,已知与恰好完全反应,生成C和D的质量比为,又知B的相对分子质量为32,则D的相对分子质量为( )
A.9 B.12 C.18 D.36
二、填空题。
17、小青和同学们一起完成了氢气燃烧的实验,并绘制了该反映的微观示意图。
请你和她讨论下列问题:
(1)图中①的微观实质是________ ,②的微观实质是________ 。
(2)图中方框内表示纯净物的是________(填字母序号).
18、硝酸()是高中化学将要学习的一种常见物质,硝酸中氮元素的化合价为 ,浓硝酸见光会发生分解反应,生成红棕色的气体和一种常见液体以及能供给呼吸的气体,写出该反应的化学方程式:
。
19、下列各组变化中,符合“1+1=2”的事实是(_____)
A、1L水与1L酒精混合后的体积等于2L
B、1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫
C、1g镁与1g氧气反应得到2g氧化镁
D、_________________
20、(1)天然气的化学式为: ,其燃烧的化学方程式为: ;
(2)氢气是最清洁的能源,用化学方程式表示: 。
21、一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
物质 A B C D
反应前质量/g 1.7 2.2 7.9 0.9
反应后质量/g 待测 6.6 0 2.7
则反应后A的质量为___________;该反应所属的基本反应类型是_____________;该反应中B和D两种物质变化的质量比为_________________。
三、综合应用题。
22、2017年5月18日,我国首次海域“可燃冰”试采成功,“可燃冰”的主要成分是甲烷。
(1)用金刚石做成的钻头开采海域“可燃冰”,利用了金刚石的______(填物理性质)。
(2)康康在实验室制取甲烷时用下图装置收集,则气体应该从_________通入(填“m”或“n”)。
(3)下图为甲烷与水反应的微观示意图。请写出对应的化学方程式:
______ 。
(4)运用燃烧法可确定甲烷的元素组成。
①请写出甲烷完全燃烧的化学方程式______ 。
②请写出确定甲烷元素组成的实验方案_______(简要写出实验操作、现象及结论)。
注意:若答对第(5)小题奖励4分,化学试卷总分不超过60分。
(5)“煤改气”可降低煤的消耗,减少空气污染,但也造成了今年的“气荒”,可燃冰的开采将会缓解这一状况。已知:1 kg甲烷完全燃烧放出热量55700 kJ,1 kg含硫5%的标准煤完全燃烧放出热量29000 kJ。请计算:
①1 kg甲烷完全燃烧放出的热量与______千克含硫5%的标准煤完全燃烧放出热量相等(保留小数点后两位)。
②完全燃烧1 kg甲烷,理论上可减少排放二氧化硫______千克。
四、实验探究题。
23、如图是初中化学中的一些重要实验。
(1)图1实验中,能证明可燃物燃烧跟温度有关的实验现象是:
。
(2)通过图2中A、B对比说明燃烧需要的条件是 。
(3)切割白磷时,应在水下进行。其原因是 。
五、计算类题。
24、科学研究中,常通过对实验数据的分析计算,得出某未知物质的相对分子质量,从而推测该物质的分子式。某科研小组经反复实验,发现2A+3B 2C+4D中,3.2 g A恰好和4.8 g B完全反应,生成4.4 g C。请问:
(1)同时生成D的质量为 g。
(2)若D的相对分子质量为18,求A的相对分子质量。
2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 学业练习题(含答案)
鲁教版第五单元 定量研究化学反应
一、选择题。
1、下列变化中,属于化学变化,并且能用质量守恒定律解释的是( )
A. 5g水受热变成5g水蒸气
B. 5g食盐溶解在95g水中,成为100g食盐溶液
C. 100mL水加入100mL酒精,成为体积小于200mL的溶液
D. 木炭燃烧后质量减少
【答案】D
2、密闭容器中发生的某化学反应,各物质的分子数目随时间变化情况如图1所示,物质Y和Z的质量随时间变化情况如图2所示。下列说法正确的是( )
图1 图2
A.该反应属于分解反应 B.X与Z的质量变化比为9∶34
C.该反应前后分子总数保持不变 D.Z一定是化合物
【答案】D
3、我国已经研究出新型水处理剂ClO2的新制法,其反应的微观过程如下图所示。下列说法正确的是( )
A.乙中氯元素的化合价为+5
B.乙物质是氧化物
C.该反应符合质量守恒定律
D.该反应的化学方程式为
【答案】C
4、在反应A+3B 2C+2D中,28 g A与一定质量的B恰好完全反应,生成88 g C。若C、D的相对分子质量之比为22∶9,则A与B的相对分子质量之比为 ( )
A.7∶8 B.8∶7 C.7∶24 D.24∶7
【答案】A
5、某同学为探究物质燃烧条件,设计并完成如图所示实验,根据如图所示的实验现象,下列对此实验的判断与认识中不正确的是( )
A.物质燃烧必须要与氧气(或空气)接触
B.物质燃烧温度必须要达到着火点
C.烧杯中热水的作用只起提高温度的作用
D.铜片上的白磷与红磷的着火点不同,则现象不同
【答案】C
6、一定质量的某化合物完全燃烧,需要3.2g氧气,生成4.4g二氧化碳和1.8g水。下列判断错误的是( )
A.该化合物的质量为3.0g
B.该化合物一定含有碳、氢、氧三种元素
C.该化合物中碳、氢、氧的原子个数比为2:4:1
D.该化合物中碳元素的质量分数是40%
【答案】C
7、下列关于化学反应的说法,错误的是 ( )
A.化学反应前后,分子种类发生改变,原子种类不变
B.化学反应前后,分子数目发生改变,原子数目不变
C.化学反应前后,物质种类发生改变,元素种类不变
D.化学反应的过程就是参加反应的各物质的原子重新组合生成其他物质的过程
【答案】B
8、古代“银针验毒”的原理是: ,关于此反应的说法不正确的是( )
A.X的化学式为Ag2S
B.反应前后元素的种类不变
C.反应前后氧元素的化合价不变
D.反应前后物质的状态发生了变化
【答案】C
9、(多选)高温煅烧CaCO3可制取CaO(CaCO3 CaO+CO2↑)。现有100 g CaCO3固体,高温煅烧一段时间后,剩余固体的质量为67 g。下列推断中,符合客观事实的是( )
A.生成CO2的质量是33 g
B.反应生成CaO的质量是42 g
C.剩余固体中钙元素的质量分数小于40%
D.剩余固体中钙元素与碳元素的质量之比为40∶3
【答案】ABD
10、为了探究物质燃烧的条件,依据图进行实验(夹持仪器略去)。实验步骤如下:( )
①通入 N2 一段时间后,点燃酒精灯,a、b 中均无明显现象;
②改通 O2 片刻,加热一段时间后,熄灭酒精灯,a 中红磷不燃烧,b 中红磷燃烧下列说法错误的是( )
A.该实验可以证明氮气不能支持红磷的燃烧
B.对比①②实验现象可知:可燃物燃烧需要足够的氧气和达到一定的温度
C.实验过程①要先通入 N2 是为了排除装置中的空气
D.实验②中发生的化学方程式为 4P+5O2=2P2O5
【答案】D
11、200多年前,法国化学家拉瓦锡用定量的方法研究空气成分,其中一项实验是加热红色的氧化汞粉末得到汞和氧气,该反应示意图如下,下列说法正确的是( )
A.氧化汞分解过程中,原子个数没有发生改变
B.氧化汞分解过程中,分子的种类没有发生改变
C.氧化汞分子是该变化中最小的粒子
D.该反应既不是化合反应也不是分解反应
【答案】A
12、下列有关化学反应的认识,不正确的是 ( )
A.通过化学变化,改变世界上物质的种类,但不能改变物质的总质量
B.质量守恒定律揭示了化学变化中宏观物质之间的质量关系,其实质是分子的重新组合
C.质量守恒定律为定量揭示化学反应的规律提供了理论依据
D.人们研究物质的化学变化的意义在于实现物质和能量的转化
【答案】B
13、关于化学方程式2CO O22CO2的读法或叙述正确的是( )
A.一氧化碳加氧气点燃等于二氧化碳
B.两份一氧化碳与一份氧气反应后生成两份二氧化碳
C.一氧化碳、氧气、二氧化碳的质量比为 28:32:44
D.每 56 份质量的一氧化碳与 32 份质量的氧气完全反应,生成 88 份质量的二氧化碳
【答案】D
14、天然气的主要成分是甲烷(CH4)。当氧气不足时,甲烷燃烧会生成CO2、CO和H2O,若16 g甲烷燃烧生成CO2和CO的质量比为11∶7,则参加反应的O2的质量为 ( )
A.48 g B.56 g C.64 g D.72 g
【答案】B
15、通过下图所示实验得出的结论中正确的是( )
①既说明甲烷具有可燃性,又说明甲烷中含有碳、氢两种元素
②既说明二氧化碳密度比空气大,又说明二氧化碳不燃烧也不支持燃烧
③既说明水分解能产生氢气和氧气,又说明水是由H、O两种元素组成
④既可探究可燃物的燃烧条件,又说明白磷的着火点比红磷低
A.①②③ B.①③④ C.②③④ D.①②③④
【答案】C
16、在化学反应中,已知与恰好完全反应,生成C和D的质量比为,又知B的相对分子质量为32,则D的相对分子质量为( )
A.9 B.12 C.18 D.36
【答案】C
二、填空题。
17、小青和同学们一起完成了氢气燃烧的实验,并绘制了该反映的微观示意图。
请你和她讨论下列问题:
(1)图中①的微观实质是________ ,②的微观实质是________ 。
(2)图中方框内表示纯净物的是________(填字母序号).
【答案】氢分子分解成氢原子,氧分子分解成氧原子
氢原子和氧原子结合成了水分子 C
18、硝酸()是高中化学将要学习的一种常见物质,硝酸中氮元素的化合价为 ,浓硝酸见光会发生分解反应,生成红棕色的气体和一种常见液体以及能供给呼吸的气体,写出该反应的化学方程式:
。
【答案】+5 ↑+↑
19、下列各组变化中,符合“1+1=2”的事实是(_____)
A、1L水与1L酒精混合后的体积等于2L
B、1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫
C、1g镁与1g氧气反应得到2g氧化镁
D、_________________
【答案】B 1g水与1g酒精混合后的质量等于2g
20、(1)天然气的化学式为: ,其燃烧的化学方程式为: ;
(2)氢气是最清洁的能源,用化学方程式表示: 。
【答案】(1)CH4;CH4 +2O2 CO2 +2H2O;
(2)2H2 + O22H2O
21、一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
物质 A B C D
反应前质量/g 1.7 2.2 7.9 0.9
反应后质量/g 待测 6.6 0 2.7
则反应后A的质量为___________;该反应所属的基本反应类型是_____________;该反应中B和D两种物质变化的质量比为_________________。
【答案】(1) 3.4g (2)分解反应 (3)22:9
三、综合应用题。
22、2017年5月18日,我国首次海域“可燃冰”试采成功,“可燃冰”的主要成分是甲烷。
(1)用金刚石做成的钻头开采海域“可燃冰”,利用了金刚石的______(填物理性质)。
(2)康康在实验室制取甲烷时用下图装置收集,则气体应该从_________通入(填“m”或“n”)。
(3)下图为甲烷与水反应的微观示意图。请写出对应的化学方程式:
______ 。
(4)运用燃烧法可确定甲烷的元素组成。
①请写出甲烷完全燃烧的化学方程式______ 。
②请写出确定甲烷元素组成的实验方案_______(简要写出实验操作、现象及结论)。
注意:若答对第(5)小题奖励4分,化学试卷总分不超过60分。
(5)“煤改气”可降低煤的消耗,减少空气污染,但也造成了今年的“气荒”,可燃冰的开采将会缓解这一状况。已知:1 kg甲烷完全燃烧放出热量55700 kJ,1 kg含硫5%的标准煤完全燃烧放出热量29000 kJ。请计算:
①1 kg甲烷完全燃烧放出的热量与______千克含硫5%的标准煤完全燃烧放出热量相等(保留小数点后两位)。
②完全燃烧1 kg甲烷,理论上可减少排放二氧化硫______千克。
【答案】(1)硬度大 (2)n (4)CH4+H2OCO+3H2
(4)CH4 + 2O2CO2 + 2H2O 验纯后,点燃甲烷,用干而冷的小烧杯罩住火焰,烧杯壁有水雾,说明含有氢元素,迅速倒转烧杯,加入少量澄清石灰水振荡,发现石灰水变浑浊,说明含有碳元素。(或其它合理答案)
(5)1.92 0.19
四、实验探究题。
23、如图是初中化学中的一些重要实验。
(1)图1实验中,能证明可燃物燃烧跟温度有关的实验现象是:
。
(2)通过图2中A、B对比说明燃烧需要的条件是 。
(3)切割白磷时,应在水下进行。其原因是 。
【答案】(1)铜片上的白磷燃烧,红磷不燃烧;
(2)燃烧需要氧气(或空气);
(3)防止在空气中切割时白磷自燃。
五、计算类题。
24、科学研究中,常通过对实验数据的分析计算,得出某未知物质的相对分子质量,从而推测该物质的分子式。某科研小组经反复实验,发现2A+3B 2C+4D中,3.2 g A恰好和4.8 g B完全反应,生成4.4 g C。请问:
(1)同时生成D的质量为 g。
(2)若D的相对分子质量为18,求A的相对分子质量。
【答案】(1)3.6; (2)32。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
