江苏省南京市普通高中学业水平测试训练样题化学试题
文档属性
| 名称 | 江苏省南京市普通高中学业水平测试训练样题化学试题 |  | |
| 格式 | zip | ||
| 文件大小 | 369.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-03-16 15:25:44 | ||
图片预览



文档简介
2015年南京市普通高中学业水平测试训练样题
化学试题
本卷可能用到的相对原子质量 H:1 C:12 O:16 Na:23 Mg:24 Al:27 S:32 Cu:64
一.单项选择题:在每题的4个选项中,只有一个选项是符合要求的(本部分23题,每题3分,共69分)。
1.纪录片《穹顶之下》再次引起人们对大气环境的强烈关注。下列燃料中最环保的是
A.石油 B.煤 C.氢气 D.天然气
2. 2014年青奥会的吉祥物“砳砳”以雨花石为创意原型。雨花石的主要成分SiO2属于
A.氧化物 B.酸 C.碱 D.盐
3.下列物质含有离子键的是
A.N2 B.CO2 C.NaOH D.HCl
4.下列物质属于电解质的是
A.氯化钠 B.铜 C.蔗糖 D.乙醇
5.某溶液中存在大量的K+、OHˉ、CO32ˉ,该溶液中还可能大量存在的离子是
A. Al3+ B.NH4+ C.Fe3+ D.SO42ˉ
6.下列气体能使品红溶液褪色的是
A.O2 B.NH3 C.CO2 D.SO2
7.用NaCl固体配制100 mL 1.00 mol· L -1 NaCl溶液,不需要用到的仪器是
A.100 mL容量瓶 B.试管 C.玻璃棒 D.胶头滴管
8.下列食用品的有效成分正确的是
A.C6H12O6 B.Na2CO3 C.CH3COOH D.Al(OH)3
9.南京大屠杀死难者国家公祭鼎用青铜铸造。关于铜的一种核素Cu,下列说法正确的是
A.Cu的核电荷数为29
B.Cu的质子数为35
C.Cu的中子数为64
D.Cu的核外电子数为64
10.下列化学用语正确的是
A.乙醇分子的结构式:
B.氯原子的结构示意图:
C.过氧化氢分子的电子式:
D.硫酸钠的电离方程式:Na2SO4=Na2+ + SO42(
11.乙醇和乙酸是生活中两种常见的有机物。下列说法正确的是
A.乙醇、乙酸互为同分异构体
B.乙醇、乙酸都能与钠反应
C.乙醇、乙酸都能与NaOH溶液反应
D.乙醇、乙酸都能使紫色石蕊试液变红色
12.下列鉴别物质的方法能达到目的的是
A.用氨水鉴别MgCl2溶液和AlCl3溶液
B.用焰色反应鉴别Na2CO3固体和NaHCO3固体
C.用BaCl2溶液鉴别AgNO3溶液和Na2SO4溶液
D.用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体
13.下列物质的用途错误的是
A.铝制容器可以贮运稀硫酸
B.水玻璃可用作木材防火剂
C.过氧化钠可用作潜艇供氧剂
D.Fe2O3可用作红色涂料
14.下列变化属于物理变化的是
A.用石油分馏炼制汽油
B.用煤干馏制备焦炭
C.用铝土矿冶炼铝
D.用海带提取碘单质
15.下列反应的离子方程式正确的是
A.碳酸钙与盐酸反应 CO32ˉ+ 2H+ = CO2↑ + H2O
B.二氧化硫与氢氧化钠溶液反应 SO2 + 2OHˉ= SO42ˉ+ H2O
C.铁粉与氯化铁溶液反应 Fe + Fe3+ = 2Fe2+
D.氯气与氢氧化钠溶液反应 Cl2 + 2OHˉ = Clˉ+ ClOˉ+ H2O
16.一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:N2 + 3H2 2NH3(正反应是放热反应)。下列有关说法正确的是
A.降低温度可以加快反应速率
B.达到化学反应限度时,生成2mol NH3
C.向容器中再加入N2,可以加快反应速率
D.1mol N2 和3mol H2的总能量低于2mol NH3的总能量
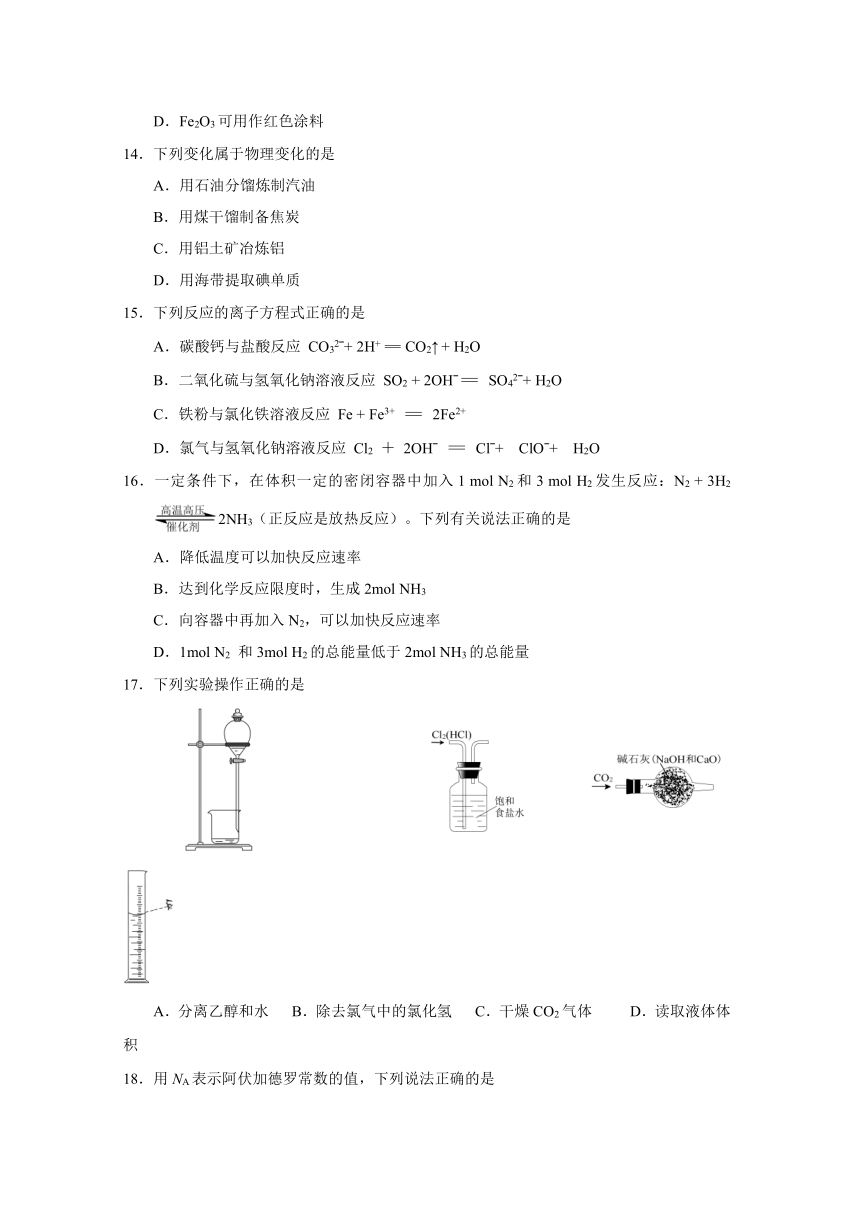
17.下列实验操作正确的是
A.分离乙醇和水 B.除去氯气中的氯化氢 C.干燥CO2气体 D.读取液体体积
18.用NA表示阿伏加德罗常数的值,下列说法正确的是
A.0.3 mol 氢气中含有氢原子的数目为0.3 NA
B.标准状况下,4.48 L水中含有水分子的数目为0.2 NA
C.0.2 mol· L -1 CaCl2溶液中含有氯离子的数目为0.4 NA
D.2.3 g 钠与足量水反应,生成钠离子的数目为0.1 NA
19.下列有机反应属于加成反应的是
A.
B.CH2=CH2 + HCl CH3CH2Cl
C.CH3COOH + CH3CH2OH CH3COOCH2CH3 + H2O
D.2CH3CH2OH + O2 2CH3CHO + 2H2O
20.某原电池反应原理示意图如右图。下列有关该原电池的说法正确的是
A.将电能转化为化学能
B.电子从锌片经导线流向铜片
C.一段时间后,铜片质量减轻
D.锌片发生还原反应
21.氮化铝(AlN)是一种新型陶瓷材料。可通过如下反应制备:Al2O3 + N2 + 3C 2AlN + 3CO 。关于该反应的说法正确的是
A.该反应是复分解反应
B.Al2O3 是氧化剂
C.N2发生还原反应
D.每反应1 mol N2转移3 mol电子
22.短周期主族元素W、R、X、Y、Z,原子序数依次增大。W、X、Y三种元素原子的最外层电子数之和为15, Y原子核电荷数等于W原子核电荷数的2倍,R原子最外层电子数与X原子最外层电子数相差1。下列叙述正确的是
A.R在化合物中显+1价
B.最高价氧化物的水化物的碱性:X>R
C.原子半径:X>Y>Z
D.简单气态氢化物的热稳定性:Y>W
23.铝碳酸镁[AlaMgb·(CO3)c·(OH)d·eH2O]用于治疗慢性胃炎。称取3.01 g铝碳酸镁样品,溶于50 mL
2 mol· L -1的盐酸(过量),收集到气体112 mL(标准状况);往所得溶液中加入40 mL 3 mol· L-1的NaOH溶液,过滤,将所得沉淀洗涤、干燥、称量得固体1.74 g;再将滤液稀释到100 mL,测得溶液中OHˉ的浓度为0.1 mol· L -1。由计算可以确定e的值为
A.4 B.5 C.7 D.8
二、非选择题(本部分3题,共31分)
24.(15分)本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A.《化学与生活》
(1)(3分)材料是人类赖以生存的物质基础。
①制造水泥、玻璃都要用到的原料是 ▲ (填字母)。
a.石灰石 b. 纯碱 c. 黏土
②不锈钢丝与棉纤维可织成一种防辐射布料。这种布料属于 ▲ (填字母)。
a.合金材料 b.复合材料 c.陶瓷材料
③天然橡胶的结构简式是 ▲ (填字母)。?
a. b. c.
(2)(5分)合理选择饮食,有益身体健康。小明家某次晚餐菜谱如右图所示。
①菜谱中富含脂肪的食物是 ▲ 。
②鸡蛋中的蛋白质在人体中会完全水解生成氨基酸,氨基酸的结构可表示为
,X的结构简式是 ▲ 。
③土豆泥中的主要营养物质水解生成葡萄糖的化学方程式为 ▲ 。
④青椒、西红柿等蔬菜富含维生素C。用淀粉溶液和碘水检验维生素C的还原性,有关实验操作和现象是 ▲ 。
(3)(7分)我国新修订的《环境保护法》,使环境保护有了更严格的法律依据。
①往燃煤中加入 ▲ (填化学式),可大大减少产物中的SO2。
②漂白粉用于生活用水的杀菌消毒,漂白粉的有效成份是 ▲ (填化学式)。治理废水中的重金属污染物可用沉淀法。例如,往含铬(Cr3+)废水中加入石灰乳使Cr3+转变为 ▲ (填化学式)沉淀而除去。
③回收的废钢铁因为易生锈不能长期在露天堆放,铁锈的化学式是 ▲ 。请举一种防止钢铁生锈的方法: ▲ 。
④将CO2和H2按物质的量1︰4混合,在适当条件下反应可获得CH4。写出该反应的化学方程式:
▲ 。
B.《有机化学基础》
(1)(3分)根据官能团可以对有机物进行分类、鉴别和除杂。
① 下列有机物属于烃的是 ▲ (填字母)。
a.乙炔 b.乙醇 c.乙酸
② 区分甲苯和苯酚,不可用的试剂是 ▲ (填字母)。
a. FeCl3 溶液 b.酸性KMnO4溶液 c.溴水
③ 除去乙酸乙酯中的乙酸,可用的试剂是 ▲ (填字母)。
a. NaOH溶液 b.NaCl溶液 c.饱和Na2CO3溶液
(2)(5分)异丙苯是一种重要的有机化工原料。异丙苯的结构简式为。
① 异丙苯中至少有 ▲ 个碳原子共平面。
② 异丙苯有多种同分异构体,其中一溴代物只有两种的芳香烃是 ▲ (填结构简式)。
③ 由异丙苯制备对溴异丙苯的化学方程式为 ▲ 。
(3)(7分)化合物III是一种合成医药的中间体,其合成路线如下:
Ⅰ Ⅱ Ⅲ
① 该合成路线中第二步反应属于 ▲ 反应(填反应类型)。
②I 、II、 III三种物质中,在一定条件下,能发生消去反应生成不含甲基产物的是 ▲ (填序号)。
③ Ⅲ的一种同分异构体X能发生银镜反应且能水解,X分子中有3种不同化学环境的氢。X的结构简式为 ▲ 。
④ 请写区分化合物Ⅰ和化合物Ⅱ的实验方法和现象 ▲ 。
25.(6分)有关物质的转化关系如下图所示(部分物质和条件已略去)。常温下A、C、D是常见气体, A是导致“温室效应”的主要物质,B是常见无色液体,C能使湿润的红色石蕊试纸变蓝,F是白色沉淀,G是红褐色沉淀。X加热生成A、B、C的物质的量之比为1︰1︰1。
请回答下列问题:
(1)C的电子式为 ▲ 。
(2)X的化学式为 ▲ 。
(3)写出反应①的离子方程式: ▲ 。
(4)写出反应②的化学方程式: ▲ 。
26.(10分)胆矾(CuSO4·5H2O)有广泛的用途。某研究性学习小组利用某次实验后的稀硫酸、稀硝酸混合液制备胆矾。实验流程如下:
请回答下列问题:
(1)操作X为 ▲ 。
(2)NO需要回收利用,写出NO与空气、H2O反应生成硝酸的化学方程式 ▲ 。
(3)现有48g含CuO质量分数为20%的铜粉,与一定量的稀硫酸、稀硝酸混合液恰好完全反应生成CuSO4。
①理论上生成胆矾的质量为多少? (写出计算过程)
②原混合液中硫酸和硝酸的物质的量之比为 ▲ 。
高二年级学业水平测试(必修科目)训练样题
化学参考答案及评分建议 2015.3
反应后溶液中:n(OHˉ)= 0.1 L×0.1 mol· L -1 =0.01 mol
反应后溶液中的溶质为NaCl、NaAlO2、NaOH。根据离子电荷守衡:
n(Clˉ)+ n(OHˉ)+ n(AlO2ˉ)= n(Na+)
0.1 mol+0.01 mol+ n(AlO2ˉ)= 0.12 mol
n(AlO2ˉ)= 0.01 mol
n(Al3+)︰n(Mg2+)︰n(CO32ˉ)= 0.01 mol︰0.03 mol︰0.005 mol=2︰6︰1
即AlaMgb·(CO3) c·(OH)d·eH2O中a=2,b = 6 c =1
根据分子中化合价代数和为零,得d =16
得化学式Al2Mg6·CO3·(OH)16 ·e H2O
Al2Mg6·CO3·(OH)16的相对分子质量为:530
3.01 g样品的物质的量是0.005 mol
m(结晶水)= 3.01 g –530 g·mol-1×0.005 mol = 0.36 g
n(结晶水)= 0.02 mol
可求出Al2Mg6·CO3·(OH)16 ·eH2O 中e=4
二、非选择题(本部分3题,共31分)
③ (2分)
(3)(7分)① 取代(1分)② Ⅰ Ⅱ(2分)③ (2分)
④ 取样,分别加入一小块金属钠,能反应产生无色气体的是化合物Ⅱ,不反应的是化合物I(2分)
25.(6分)
(1) (1分)
(2)NH4HCO3(1分)
(3)2Na2O2 + 2H2O = 4Na+ + 4OHˉ + O2↑(2分)
(4)4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3(2分)
化学试题
本卷可能用到的相对原子质量 H:1 C:12 O:16 Na:23 Mg:24 Al:27 S:32 Cu:64
一.单项选择题:在每题的4个选项中,只有一个选项是符合要求的(本部分23题,每题3分,共69分)。
1.纪录片《穹顶之下》再次引起人们对大气环境的强烈关注。下列燃料中最环保的是
A.石油 B.煤 C.氢气 D.天然气
2. 2014年青奥会的吉祥物“砳砳”以雨花石为创意原型。雨花石的主要成分SiO2属于
A.氧化物 B.酸 C.碱 D.盐
3.下列物质含有离子键的是
A.N2 B.CO2 C.NaOH D.HCl
4.下列物质属于电解质的是
A.氯化钠 B.铜 C.蔗糖 D.乙醇
5.某溶液中存在大量的K+、OHˉ、CO32ˉ,该溶液中还可能大量存在的离子是
A. Al3+ B.NH4+ C.Fe3+ D.SO42ˉ
6.下列气体能使品红溶液褪色的是
A.O2 B.NH3 C.CO2 D.SO2
7.用NaCl固体配制100 mL 1.00 mol· L -1 NaCl溶液,不需要用到的仪器是
A.100 mL容量瓶 B.试管 C.玻璃棒 D.胶头滴管
8.下列食用品的有效成分正确的是
A.C6H12O6 B.Na2CO3 C.CH3COOH D.Al(OH)3
9.南京大屠杀死难者国家公祭鼎用青铜铸造。关于铜的一种核素Cu,下列说法正确的是
A.Cu的核电荷数为29
B.Cu的质子数为35
C.Cu的中子数为64
D.Cu的核外电子数为64
10.下列化学用语正确的是
A.乙醇分子的结构式:
B.氯原子的结构示意图:
C.过氧化氢分子的电子式:
D.硫酸钠的电离方程式:Na2SO4=Na2+ + SO42(
11.乙醇和乙酸是生活中两种常见的有机物。下列说法正确的是
A.乙醇、乙酸互为同分异构体
B.乙醇、乙酸都能与钠反应
C.乙醇、乙酸都能与NaOH溶液反应
D.乙醇、乙酸都能使紫色石蕊试液变红色
12.下列鉴别物质的方法能达到目的的是
A.用氨水鉴别MgCl2溶液和AlCl3溶液
B.用焰色反应鉴别Na2CO3固体和NaHCO3固体
C.用BaCl2溶液鉴别AgNO3溶液和Na2SO4溶液
D.用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体
13.下列物质的用途错误的是
A.铝制容器可以贮运稀硫酸
B.水玻璃可用作木材防火剂
C.过氧化钠可用作潜艇供氧剂
D.Fe2O3可用作红色涂料
14.下列变化属于物理变化的是
A.用石油分馏炼制汽油
B.用煤干馏制备焦炭
C.用铝土矿冶炼铝
D.用海带提取碘单质
15.下列反应的离子方程式正确的是
A.碳酸钙与盐酸反应 CO32ˉ+ 2H+ = CO2↑ + H2O
B.二氧化硫与氢氧化钠溶液反应 SO2 + 2OHˉ= SO42ˉ+ H2O
C.铁粉与氯化铁溶液反应 Fe + Fe3+ = 2Fe2+
D.氯气与氢氧化钠溶液反应 Cl2 + 2OHˉ = Clˉ+ ClOˉ+ H2O
16.一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:N2 + 3H2 2NH3(正反应是放热反应)。下列有关说法正确的是
A.降低温度可以加快反应速率
B.达到化学反应限度时,生成2mol NH3
C.向容器中再加入N2,可以加快反应速率
D.1mol N2 和3mol H2的总能量低于2mol NH3的总能量
17.下列实验操作正确的是
A.分离乙醇和水 B.除去氯气中的氯化氢 C.干燥CO2气体 D.读取液体体积
18.用NA表示阿伏加德罗常数的值,下列说法正确的是
A.0.3 mol 氢气中含有氢原子的数目为0.3 NA
B.标准状况下,4.48 L水中含有水分子的数目为0.2 NA
C.0.2 mol· L -1 CaCl2溶液中含有氯离子的数目为0.4 NA
D.2.3 g 钠与足量水反应,生成钠离子的数目为0.1 NA
19.下列有机反应属于加成反应的是
A.
B.CH2=CH2 + HCl CH3CH2Cl
C.CH3COOH + CH3CH2OH CH3COOCH2CH3 + H2O
D.2CH3CH2OH + O2 2CH3CHO + 2H2O
20.某原电池反应原理示意图如右图。下列有关该原电池的说法正确的是
A.将电能转化为化学能
B.电子从锌片经导线流向铜片
C.一段时间后,铜片质量减轻
D.锌片发生还原反应
21.氮化铝(AlN)是一种新型陶瓷材料。可通过如下反应制备:Al2O3 + N2 + 3C 2AlN + 3CO 。关于该反应的说法正确的是
A.该反应是复分解反应
B.Al2O3 是氧化剂
C.N2发生还原反应
D.每反应1 mol N2转移3 mol电子
22.短周期主族元素W、R、X、Y、Z,原子序数依次增大。W、X、Y三种元素原子的最外层电子数之和为15, Y原子核电荷数等于W原子核电荷数的2倍,R原子最外层电子数与X原子最外层电子数相差1。下列叙述正确的是
A.R在化合物中显+1价
B.最高价氧化物的水化物的碱性:X>R
C.原子半径:X>Y>Z
D.简单气态氢化物的热稳定性:Y>W
23.铝碳酸镁[AlaMgb·(CO3)c·(OH)d·eH2O]用于治疗慢性胃炎。称取3.01 g铝碳酸镁样品,溶于50 mL
2 mol· L -1的盐酸(过量),收集到气体112 mL(标准状况);往所得溶液中加入40 mL 3 mol· L-1的NaOH溶液,过滤,将所得沉淀洗涤、干燥、称量得固体1.74 g;再将滤液稀释到100 mL,测得溶液中OHˉ的浓度为0.1 mol· L -1。由计算可以确定e的值为
A.4 B.5 C.7 D.8
二、非选择题(本部分3题,共31分)
24.(15分)本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A.《化学与生活》
(1)(3分)材料是人类赖以生存的物质基础。
①制造水泥、玻璃都要用到的原料是 ▲ (填字母)。
a.石灰石 b. 纯碱 c. 黏土
②不锈钢丝与棉纤维可织成一种防辐射布料。这种布料属于 ▲ (填字母)。
a.合金材料 b.复合材料 c.陶瓷材料
③天然橡胶的结构简式是 ▲ (填字母)。?
a. b. c.
(2)(5分)合理选择饮食,有益身体健康。小明家某次晚餐菜谱如右图所示。
①菜谱中富含脂肪的食物是 ▲ 。
②鸡蛋中的蛋白质在人体中会完全水解生成氨基酸,氨基酸的结构可表示为
,X的结构简式是 ▲ 。
③土豆泥中的主要营养物质水解生成葡萄糖的化学方程式为 ▲ 。
④青椒、西红柿等蔬菜富含维生素C。用淀粉溶液和碘水检验维生素C的还原性,有关实验操作和现象是 ▲ 。
(3)(7分)我国新修订的《环境保护法》,使环境保护有了更严格的法律依据。
①往燃煤中加入 ▲ (填化学式),可大大减少产物中的SO2。
②漂白粉用于生活用水的杀菌消毒,漂白粉的有效成份是 ▲ (填化学式)。治理废水中的重金属污染物可用沉淀法。例如,往含铬(Cr3+)废水中加入石灰乳使Cr3+转变为 ▲ (填化学式)沉淀而除去。
③回收的废钢铁因为易生锈不能长期在露天堆放,铁锈的化学式是 ▲ 。请举一种防止钢铁生锈的方法: ▲ 。
④将CO2和H2按物质的量1︰4混合,在适当条件下反应可获得CH4。写出该反应的化学方程式:
▲ 。
B.《有机化学基础》
(1)(3分)根据官能团可以对有机物进行分类、鉴别和除杂。
① 下列有机物属于烃的是 ▲ (填字母)。
a.乙炔 b.乙醇 c.乙酸
② 区分甲苯和苯酚,不可用的试剂是 ▲ (填字母)。
a. FeCl3 溶液 b.酸性KMnO4溶液 c.溴水
③ 除去乙酸乙酯中的乙酸,可用的试剂是 ▲ (填字母)。
a. NaOH溶液 b.NaCl溶液 c.饱和Na2CO3溶液
(2)(5分)异丙苯是一种重要的有机化工原料。异丙苯的结构简式为。
① 异丙苯中至少有 ▲ 个碳原子共平面。
② 异丙苯有多种同分异构体,其中一溴代物只有两种的芳香烃是 ▲ (填结构简式)。
③ 由异丙苯制备对溴异丙苯的化学方程式为 ▲ 。
(3)(7分)化合物III是一种合成医药的中间体,其合成路线如下:
Ⅰ Ⅱ Ⅲ
① 该合成路线中第二步反应属于 ▲ 反应(填反应类型)。
②I 、II、 III三种物质中,在一定条件下,能发生消去反应生成不含甲基产物的是 ▲ (填序号)。
③ Ⅲ的一种同分异构体X能发生银镜反应且能水解,X分子中有3种不同化学环境的氢。X的结构简式为 ▲ 。
④ 请写区分化合物Ⅰ和化合物Ⅱ的实验方法和现象 ▲ 。
25.(6分)有关物质的转化关系如下图所示(部分物质和条件已略去)。常温下A、C、D是常见气体, A是导致“温室效应”的主要物质,B是常见无色液体,C能使湿润的红色石蕊试纸变蓝,F是白色沉淀,G是红褐色沉淀。X加热生成A、B、C的物质的量之比为1︰1︰1。
请回答下列问题:
(1)C的电子式为 ▲ 。
(2)X的化学式为 ▲ 。
(3)写出反应①的离子方程式: ▲ 。
(4)写出反应②的化学方程式: ▲ 。
26.(10分)胆矾(CuSO4·5H2O)有广泛的用途。某研究性学习小组利用某次实验后的稀硫酸、稀硝酸混合液制备胆矾。实验流程如下:
请回答下列问题:
(1)操作X为 ▲ 。
(2)NO需要回收利用,写出NO与空气、H2O反应生成硝酸的化学方程式 ▲ 。
(3)现有48g含CuO质量分数为20%的铜粉,与一定量的稀硫酸、稀硝酸混合液恰好完全反应生成CuSO4。
①理论上生成胆矾的质量为多少? (写出计算过程)
②原混合液中硫酸和硝酸的物质的量之比为 ▲ 。
高二年级学业水平测试(必修科目)训练样题
化学参考答案及评分建议 2015.3
反应后溶液中:n(OHˉ)= 0.1 L×0.1 mol· L -1 =0.01 mol
反应后溶液中的溶质为NaCl、NaAlO2、NaOH。根据离子电荷守衡:
n(Clˉ)+ n(OHˉ)+ n(AlO2ˉ)= n(Na+)
0.1 mol+0.01 mol+ n(AlO2ˉ)= 0.12 mol
n(AlO2ˉ)= 0.01 mol
n(Al3+)︰n(Mg2+)︰n(CO32ˉ)= 0.01 mol︰0.03 mol︰0.005 mol=2︰6︰1
即AlaMgb·(CO3) c·(OH)d·eH2O中a=2,b = 6 c =1
根据分子中化合价代数和为零,得d =16
得化学式Al2Mg6·CO3·(OH)16 ·e H2O
Al2Mg6·CO3·(OH)16的相对分子质量为:530
3.01 g样品的物质的量是0.005 mol
m(结晶水)= 3.01 g –530 g·mol-1×0.005 mol = 0.36 g
n(结晶水)= 0.02 mol
可求出Al2Mg6·CO3·(OH)16 ·eH2O 中e=4
二、非选择题(本部分3题,共31分)
③ (2分)
(3)(7分)① 取代(1分)② Ⅰ Ⅱ(2分)③ (2分)
④ 取样,分别加入一小块金属钠,能反应产生无色气体的是化合物Ⅱ,不反应的是化合物I(2分)
25.(6分)
(1) (1分)
(2)NH4HCO3(1分)
(3)2Na2O2 + 2H2O = 4Na+ + 4OHˉ + O2↑(2分)
(4)4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3(2分)
同课章节目录
