3.4.2 羧酸衍生物课件(共33张PPT)2023-2024学年高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 3.4.2 羧酸衍生物课件(共33张PPT)2023-2024学年高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 20.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-05 00:00:00 | ||
图片预览











文档简介
(共33张PPT)
第三章 烃的衍生物 第四节 羧酸 羧酸衍生物
第2课时 羧酸衍生物
教学目标
1.认识羧酸衍生物(酯、油脂、酰胺和胺)的结构特点及应用。
2.通过探究乙酸乙酯的水解,熟悉控制变量法的应用,体验科学探究的一般过程。
3.能结合生产、生活实际了解羧酸衍生物对环境和健康可能产生的影响,关注羧酸衍生物的安全使用。
羧酸衍生物
定义:羧酸分子中羧基上的羟基被其他原子或原子团取代后的生成物。
乙酸分子中羧基上的羟基被乙氧基______________取代后生成_____________,
乙酸分子中羧基上的羟基被氨基_________取代后生成的____________。
例如
—OCH2CH3
乙酸乙酯
—NH2
乙酰胺
知识梳理
丁酸乙酯
戊酸戊酯
生活中的酯
邻氨基苯甲酸甲酯
—COOCH
—NH2
一、酯
CH3(CH2)3C—O—(CH2)4CH3
O
‖
CH3(CH2)2C—O—CH2CH3
O
‖
1.酯的概述
(1)定义:酯是羧酸分子羧基中的_________被_________取代后的产物,可简写为____________,其中R和R'可以相同,也可以不同。
—OH
—OR'
丁酸乙酯
乙酸异戊酯
某酸某酯
酯水解生成的酸和醇的名称
RCOOR'
—C—O—R
O
'
‖
CH3(CH2)2C—O—CH2CH3
O
‖
CH3C—O—(CH2)2CHCH3
O
‖
—
CH3
(2)官能团:酯基, —COO—或
(3)酯的命名:
许多酯也是常用的有机溶剂。
具有芳香气味的液体
密度一般比水小
易溶于有机溶剂
低级酯
2.酯的物理性质
乙酸乙酯的水解
【问题】 乙酸乙酯水解的速率与反应条件有着怎样的关系呢
【设计与实验】请你设计实验,探究乙酸乙酯在中性、酸性和碱性溶液中,以及不同温度下的水解速率。(提示:可以通过酯层消失的时间差异来 判断乙酸乙酯在不同条件下水解速率的差别。)
【实验方法】 控制变量法
探究
2.酯的化学性质
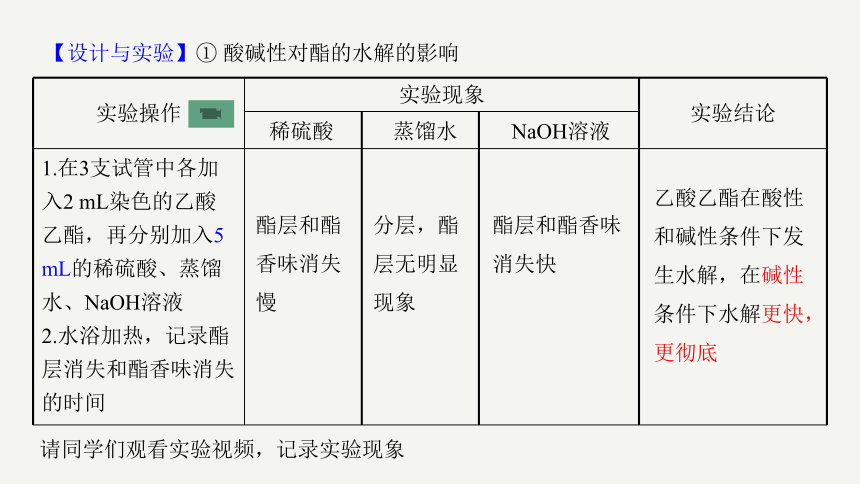
【设计与实验】① 酸碱性对酯的水解的影响
实验操作 实验现象 实验结论
乙酸乙酯在酸性和碱性条件下发生水解,在碱性条件下水解更快,更彻底
分层,酯层无明显现象
请同学们观看实验视频,记录实验现象
酯层和酯香味消失慢
稀硫酸
蒸馏水
酯层和酯香味消失快
NaOH溶液
1.在3支试管中各加入2 mL染色的乙酸乙酯,再分别加入5 mL的稀硫酸、蒸馏水、NaOH溶液
2.水浴加热,记录酯层消失和酯香味消失的时间
实验操作 实验现象 实验结论
酯层和酯香味消失慢
温度高的试管酯层消失得更快
常温
热水
酯层和酯香味消失快
5 min后
1.在两支试管中各加入2 mL染色的乙酸乙酯,再分别向试管中分别加入5 mL的氢氧化钠溶液
2.振荡均匀后,把2支试管分别置于常温和约60℃的水浴里加热
【设计与实验】② 温度对酯的水解的影响
请同学们观看乙酸乙酯水解的断成键过程
酯在无机酸或碱存在条件下,均能发生水解反应。在酸性条件下水解是可逆的。
在碱性条件下水解是不可逆的,可完全水解,水解速率较快。
【小结】酯的水解规律
酯+H2O 酸+醇
无机酸
△
酯+H2O 羧酸盐+醇
无机碱
△
【思考与讨论】利用化学平衡原理解释乙酸乙酯在碱性条件下水解程度大于酸性条件
乙酸乙酯的水解为可逆反应,在碱性条件下,碱与水解得到的乙酸反应生成乙酸钠,降低生成物乙酸的浓度,从而促进水解平衡向水解方向移动,使水解程度增大。
酯的酸性水解与酯化反应均为可逆反应和取代反应。
酯的碱性水解,由于生成了羧酸盐,水解反应不可逆,也属于取代反应。
【思考与讨论】对比酯化反应和酯的水解反应类型差异
(1)定义:油脂是重要的营养物质。日常生活中食用的油脂是由高级脂肪酸与甘油形成的酯,属于酯类化合物。
如:饱和的硬脂酸( )
饱和的软脂酸( )
不饱和的油酸( )
不饱和的亚油酸( )
C17H35COOH
C17H33COOH
C15H31COOH
C17H31COOH
二、油脂
1.油脂的概述
(2)结构: R、R'、R〞代表高级脂肪酸的烃基,可以相同也可以不同。组成油脂的高级脂肪酸的种类很多。
(3)油脂的分类
油
脂肪
常温呈液态的油脂
常温呈固态的油脂
如花生油、芝麻油、大豆油等植物油
如牛油、羊油等动物油脂
【思考与讨论】请写出硬脂酸、油酸分别与丙三醇反应的化学方程式。
浓硫酸
△
C17H35COOH +
3
CH2
OH
CH
OH
CH2
OH
+3H2O
硬脂酸甘油酯
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
C17H33COOH+
浓硫酸
△
3
CH2
OH
CH
OH
CH2
OH
+3H2O
油酸甘油酯
CH2
O
C
O
C17H33
CH
O
C
O
C17H33
CH2
O
C
O
C17H33
(1)水解反应
油脂是高级脂肪酸的甘油酯,化学性质与乙酸乙酯类似,在酸、碱等催化剂的作用下油脂可以发生水解反应。
C17H35COOH +
3
硬脂酸
甘油
CH2
OH
CH
OH
CH2
OH
稀硫酸
△
+3H2O
硬脂酸甘油酯
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
2.油脂的化学性质
C17H35COONa +
3
硬脂酸钠
油脂在碱性溶液中水解生成高级脂肪酸盐和甘油,又称皂化反应。
生成肥皂
甘油
CH2
OH
CH
OH
CH2
OH
+3NaOH
△
硬脂酸甘油酯
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
硬化油不易被空气氧化变质,便于储存和运输,可作为制造肥皂、人造奶油的原料。
不饱和程度较高、熔点较低的液态油
催化加氢
提高饱和度
半固态的脂肪
油脂的氢化,也称油脂的硬化
人造脂肪
硬化油
(2)油脂的氢化
△
催化剂
+3H2
油酸甘油酯
CH2
O
C
O
C17H33
CH
O
C
O
C17H33
CH2
O
C
O
C17H33
硬脂酸甘油酯
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
(加成反应)
(2)油脂的氢化
(1)定义:烃基取代氨分子中的氢原子而形成的化合物。
(2)结构:
(3)官能团:
胺也可看作是烃分子中的氢原子被氨基所替代得到的化合物
甲烷分子中的一个氢原子被一个氨基取代后,生成的化合物叫甲胺(CH3—NH2);
苯分子中的一个氢原子被一个氨基取代后,生成的化合物叫苯胺( ) 。
氨基(—NH2)
一般可写作R—NH2
三、酰胺
1.胺
用途:重要的化工原料,如甲胺和苯胺都是合成医药、农药和染料等的重要原料。
(4)胺的化学性质
胺类化合物具有碱性,能与盐酸、醋酸等反应。
如苯胺能与盐酸反应,生成可溶于水的苯胺盐酸盐。
NH2
NH3Cl
+HCl
苯胺 苯胺盐酸盐
2.酰胺
(1)定义:酰胺是羧酸分子中羟基被氨基所替代得到的化合物。
(2)结构:
(3)常见的物质有:
R
—C—
O
NH2
酰基
酰胺基
乙酰胺
CH3
—C—
O
NH2
苯甲酰胺
—C—
O
NH2
‖
N,N-二甲基甲酰胺
H
—C—
O
N(CH3)2
‖
与盐酸:
与氢氧化钠溶液:
(4)酰胺的化学性质
酰胺在酸或碱存在并加热的条件下可以发生水解反应。如果水解时加入碱,生成的酸就会变成盐,同时有氨气逸出。
RCONH2+H2O+HCl RCOOH+NH4Cl
RCONH2+NaOH RCOONa+NH3↑
(5)酰胺的用途: 酰胺常被用作溶剂和化工原料。
物质 氨 胺(甲胺) 酰胺(乙酰胺) 铵盐(NH4Cl)
组成元素 N、H C、N、H C、N、O、H N、H、Cl
结构特点
化学性质 具有碱性,与酸反应生成铵盐 具有碱性,与酸反应生成盐 在酸或碱存在并加热条件下可以发生水解反应 受热易分解,与碱共热产生氨气
用途 制冷剂,生产硝酸和尿素 合成医药、农药和染料 溶剂和化工原料 生产化肥和化工原料
含有氨基
含有酰胺基
NH3
三角锥形
R—NH2
R
C
O
NH2
含有铵根离子
【思考与讨论】请举例说明氨、胺、酰胺和铵盐这4类物质在组成、结构、性质和用途上的不同,并设计表格进行比较。
1.下列各组有机化合物中,互为同分异构体的是( )
A.甲酸和甲酸甲酯
B.乙酸和甲酸甲酯
C.乙酸和乙酸乙酯
D.甲酸和蚁酸
B
O
H—C—O—H CH2O2
O
H—C—O—CH3 C2H4O2
O
CH3—C—O—H C2H4O2
O
H—C—O—CH3 C2H4O2
O
CH3—C—O—H C2H4O2
O
CH3—C—O—CH2CH3 C4H8O2
O
H—C—O—H CH2O2
随堂练习
2.下列关于苯乙酸丁酯的描述错误的是( )
A.分子式为C12H16O2
B.有3种不同结构的苯乙酸丁酯
C.既能发生加成反应,又能发生取代反应
D.在酸、碱溶液中都能发生水解反应
B
【解析】据酯的命名原则知,苯乙酸丁酯是由苯乙酸 ( )和丁醇(C4H10O)反应生成的,其结构简式为 ,分子式为C12H16O2,A项正确;丁基(—C4H9)有4种结构,故有4种不同结构的苯乙酸丁酯,B项错误;苯乙酸丁酯中的苯环可与H2发生加成反应,也可与硝酸等发生取代反应,酯基在酸或碱溶液中都能发生水解反应,酯的水解反应也属于取代反应,C、D项正确。
3.下列属于油脂用途的是( )
①人类的营养物质 ②制取肥皂 ③制取甘油 ④制备高级脂肪酸 ⑤制备汽油
A.①②⑤ B.①③⑤
C.②③④⑤ D.①②③④
D
4.下列物质不属于酰胺的是( )
氨基酸
C
5.生活中常用烧碱来清洗抽油烟机上的油渍(主要成分是油脂),下列说法不正确的是( )
A.油脂属于天然高分子化合物
B.热的烧碱溶液去油渍效果更好
C.清洗时,油脂在碱性条件下发生水解反应
D.烧碱具有强腐蚀性,故清洗时必须戴防护手套
A
本节内容结束
第三章 烃的衍生物 第四节 羧酸 羧酸衍生物
第2课时 羧酸衍生物
教学目标
1.认识羧酸衍生物(酯、油脂、酰胺和胺)的结构特点及应用。
2.通过探究乙酸乙酯的水解,熟悉控制变量法的应用,体验科学探究的一般过程。
3.能结合生产、生活实际了解羧酸衍生物对环境和健康可能产生的影响,关注羧酸衍生物的安全使用。
羧酸衍生物
定义:羧酸分子中羧基上的羟基被其他原子或原子团取代后的生成物。
乙酸分子中羧基上的羟基被乙氧基______________取代后生成_____________,
乙酸分子中羧基上的羟基被氨基_________取代后生成的____________。
例如
—OCH2CH3
乙酸乙酯
—NH2
乙酰胺
知识梳理
丁酸乙酯
戊酸戊酯
生活中的酯
邻氨基苯甲酸甲酯
—COOCH
—NH2
一、酯
CH3(CH2)3C—O—(CH2)4CH3
O
‖
CH3(CH2)2C—O—CH2CH3
O
‖
1.酯的概述
(1)定义:酯是羧酸分子羧基中的_________被_________取代后的产物,可简写为____________,其中R和R'可以相同,也可以不同。
—OH
—OR'
丁酸乙酯
乙酸异戊酯
某酸某酯
酯水解生成的酸和醇的名称
RCOOR'
—C—O—R
O
'
‖
CH3(CH2)2C—O—CH2CH3
O
‖
CH3C—O—(CH2)2CHCH3
O
‖
—
CH3
(2)官能团:酯基, —COO—或
(3)酯的命名:
许多酯也是常用的有机溶剂。
具有芳香气味的液体
密度一般比水小
易溶于有机溶剂
低级酯
2.酯的物理性质
乙酸乙酯的水解
【问题】 乙酸乙酯水解的速率与反应条件有着怎样的关系呢
【设计与实验】请你设计实验,探究乙酸乙酯在中性、酸性和碱性溶液中,以及不同温度下的水解速率。(提示:可以通过酯层消失的时间差异来 判断乙酸乙酯在不同条件下水解速率的差别。)
【实验方法】 控制变量法
探究
2.酯的化学性质
【设计与实验】① 酸碱性对酯的水解的影响
实验操作 实验现象 实验结论
乙酸乙酯在酸性和碱性条件下发生水解,在碱性条件下水解更快,更彻底
分层,酯层无明显现象
请同学们观看实验视频,记录实验现象
酯层和酯香味消失慢
稀硫酸
蒸馏水
酯层和酯香味消失快
NaOH溶液
1.在3支试管中各加入2 mL染色的乙酸乙酯,再分别加入5 mL的稀硫酸、蒸馏水、NaOH溶液
2.水浴加热,记录酯层消失和酯香味消失的时间
实验操作 实验现象 实验结论
酯层和酯香味消失慢
温度高的试管酯层消失得更快
常温
热水
酯层和酯香味消失快
5 min后
1.在两支试管中各加入2 mL染色的乙酸乙酯,再分别向试管中分别加入5 mL的氢氧化钠溶液
2.振荡均匀后,把2支试管分别置于常温和约60℃的水浴里加热
【设计与实验】② 温度对酯的水解的影响
请同学们观看乙酸乙酯水解的断成键过程
酯在无机酸或碱存在条件下,均能发生水解反应。在酸性条件下水解是可逆的。
在碱性条件下水解是不可逆的,可完全水解,水解速率较快。
【小结】酯的水解规律
酯+H2O 酸+醇
无机酸
△
酯+H2O 羧酸盐+醇
无机碱
△
【思考与讨论】利用化学平衡原理解释乙酸乙酯在碱性条件下水解程度大于酸性条件
乙酸乙酯的水解为可逆反应,在碱性条件下,碱与水解得到的乙酸反应生成乙酸钠,降低生成物乙酸的浓度,从而促进水解平衡向水解方向移动,使水解程度增大。
酯的酸性水解与酯化反应均为可逆反应和取代反应。
酯的碱性水解,由于生成了羧酸盐,水解反应不可逆,也属于取代反应。
【思考与讨论】对比酯化反应和酯的水解反应类型差异
(1)定义:油脂是重要的营养物质。日常生活中食用的油脂是由高级脂肪酸与甘油形成的酯,属于酯类化合物。
如:饱和的硬脂酸( )
饱和的软脂酸( )
不饱和的油酸( )
不饱和的亚油酸( )
C17H35COOH
C17H33COOH
C15H31COOH
C17H31COOH
二、油脂
1.油脂的概述
(2)结构: R、R'、R〞代表高级脂肪酸的烃基,可以相同也可以不同。组成油脂的高级脂肪酸的种类很多。
(3)油脂的分类
油
脂肪
常温呈液态的油脂
常温呈固态的油脂
如花生油、芝麻油、大豆油等植物油
如牛油、羊油等动物油脂
【思考与讨论】请写出硬脂酸、油酸分别与丙三醇反应的化学方程式。
浓硫酸
△
C17H35COOH +
3
CH2
OH
CH
OH
CH2
OH
+3H2O
硬脂酸甘油酯
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
C17H33COOH+
浓硫酸
△
3
CH2
OH
CH
OH
CH2
OH
+3H2O
油酸甘油酯
CH2
O
C
O
C17H33
CH
O
C
O
C17H33
CH2
O
C
O
C17H33
(1)水解反应
油脂是高级脂肪酸的甘油酯,化学性质与乙酸乙酯类似,在酸、碱等催化剂的作用下油脂可以发生水解反应。
C17H35COOH +
3
硬脂酸
甘油
CH2
OH
CH
OH
CH2
OH
稀硫酸
△
+3H2O
硬脂酸甘油酯
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
2.油脂的化学性质
C17H35COONa +
3
硬脂酸钠
油脂在碱性溶液中水解生成高级脂肪酸盐和甘油,又称皂化反应。
生成肥皂
甘油
CH2
OH
CH
OH
CH2
OH
+3NaOH
△
硬脂酸甘油酯
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
硬化油不易被空气氧化变质,便于储存和运输,可作为制造肥皂、人造奶油的原料。
不饱和程度较高、熔点较低的液态油
催化加氢
提高饱和度
半固态的脂肪
油脂的氢化,也称油脂的硬化
人造脂肪
硬化油
(2)油脂的氢化
△
催化剂
+3H2
油酸甘油酯
CH2
O
C
O
C17H33
CH
O
C
O
C17H33
CH2
O
C
O
C17H33
硬脂酸甘油酯
CH2
O
C
O
C17H35
CH
O
C
O
C17H35
CH2
O
C
O
C17H35
(加成反应)
(2)油脂的氢化
(1)定义:烃基取代氨分子中的氢原子而形成的化合物。
(2)结构:
(3)官能团:
胺也可看作是烃分子中的氢原子被氨基所替代得到的化合物
甲烷分子中的一个氢原子被一个氨基取代后,生成的化合物叫甲胺(CH3—NH2);
苯分子中的一个氢原子被一个氨基取代后,生成的化合物叫苯胺( ) 。
氨基(—NH2)
一般可写作R—NH2
三、酰胺
1.胺
用途:重要的化工原料,如甲胺和苯胺都是合成医药、农药和染料等的重要原料。
(4)胺的化学性质
胺类化合物具有碱性,能与盐酸、醋酸等反应。
如苯胺能与盐酸反应,生成可溶于水的苯胺盐酸盐。
NH2
NH3Cl
+HCl
苯胺 苯胺盐酸盐
2.酰胺
(1)定义:酰胺是羧酸分子中羟基被氨基所替代得到的化合物。
(2)结构:
(3)常见的物质有:
R
—C—
O
NH2
酰基
酰胺基
乙酰胺
CH3
—C—
O
NH2
苯甲酰胺
—C—
O
NH2
‖
N,N-二甲基甲酰胺
H
—C—
O
N(CH3)2
‖
与盐酸:
与氢氧化钠溶液:
(4)酰胺的化学性质
酰胺在酸或碱存在并加热的条件下可以发生水解反应。如果水解时加入碱,生成的酸就会变成盐,同时有氨气逸出。
RCONH2+H2O+HCl RCOOH+NH4Cl
RCONH2+NaOH RCOONa+NH3↑
(5)酰胺的用途: 酰胺常被用作溶剂和化工原料。
物质 氨 胺(甲胺) 酰胺(乙酰胺) 铵盐(NH4Cl)
组成元素 N、H C、N、H C、N、O、H N、H、Cl
结构特点
化学性质 具有碱性,与酸反应生成铵盐 具有碱性,与酸反应生成盐 在酸或碱存在并加热条件下可以发生水解反应 受热易分解,与碱共热产生氨气
用途 制冷剂,生产硝酸和尿素 合成医药、农药和染料 溶剂和化工原料 生产化肥和化工原料
含有氨基
含有酰胺基
NH3
三角锥形
R—NH2
R
C
O
NH2
含有铵根离子
【思考与讨论】请举例说明氨、胺、酰胺和铵盐这4类物质在组成、结构、性质和用途上的不同,并设计表格进行比较。
1.下列各组有机化合物中,互为同分异构体的是( )
A.甲酸和甲酸甲酯
B.乙酸和甲酸甲酯
C.乙酸和乙酸乙酯
D.甲酸和蚁酸
B
O
H—C—O—H CH2O2
O
H—C—O—CH3 C2H4O2
O
CH3—C—O—H C2H4O2
O
H—C—O—CH3 C2H4O2
O
CH3—C—O—H C2H4O2
O
CH3—C—O—CH2CH3 C4H8O2
O
H—C—O—H CH2O2
随堂练习
2.下列关于苯乙酸丁酯的描述错误的是( )
A.分子式为C12H16O2
B.有3种不同结构的苯乙酸丁酯
C.既能发生加成反应,又能发生取代反应
D.在酸、碱溶液中都能发生水解反应
B
【解析】据酯的命名原则知,苯乙酸丁酯是由苯乙酸 ( )和丁醇(C4H10O)反应生成的,其结构简式为 ,分子式为C12H16O2,A项正确;丁基(—C4H9)有4种结构,故有4种不同结构的苯乙酸丁酯,B项错误;苯乙酸丁酯中的苯环可与H2发生加成反应,也可与硝酸等发生取代反应,酯基在酸或碱溶液中都能发生水解反应,酯的水解反应也属于取代反应,C、D项正确。
3.下列属于油脂用途的是( )
①人类的营养物质 ②制取肥皂 ③制取甘油 ④制备高级脂肪酸 ⑤制备汽油
A.①②⑤ B.①③⑤
C.②③④⑤ D.①②③④
D
4.下列物质不属于酰胺的是( )
氨基酸
C
5.生活中常用烧碱来清洗抽油烟机上的油渍(主要成分是油脂),下列说法不正确的是( )
A.油脂属于天然高分子化合物
B.热的烧碱溶液去油渍效果更好
C.清洗时,油脂在碱性条件下发生水解反应
D.烧碱具有强腐蚀性,故清洗时必须戴防护手套
A
本节内容结束
