2.2.1 烯烃课件(共35张PPT)2023-2024学年高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 2.2.1 烯烃课件(共35张PPT)2023-2024学年高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-05 00:00:00 | ||
图片预览






文档简介
(共35张PPT)
第二章 烃
第二节 烯烃 炔烃
第1课时 烯烃
自然界里存在许多烯烃,如番茄中的番茄红素、鲨鱼油中的角鲨烯都是烯烃。
乙烯是常见的烯烃。
番茄中存在番茄红素
新课导入
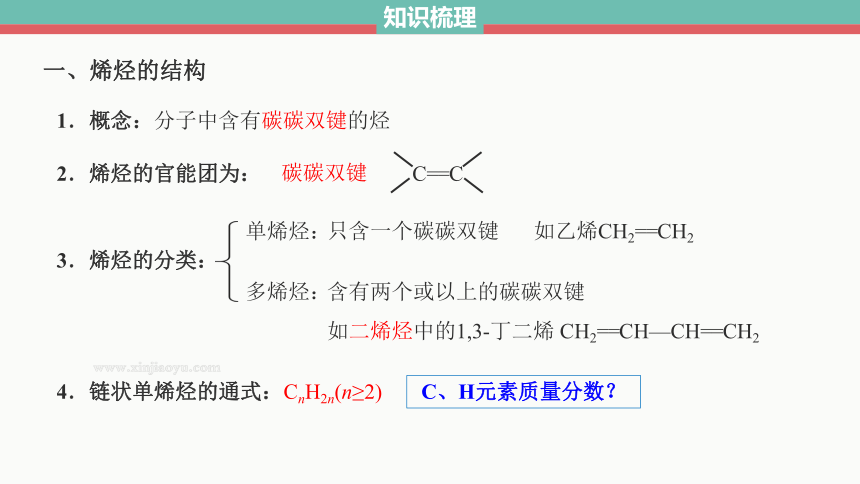
一、烯烃的结构
1.概念:分子中含有碳碳双键的烃
2.烯烃的官能团为:
碳碳双键
C==C
3.烯烃的分类:
单烯烃:
多烯烃:
只含一个碳碳双键
含有两个或以上的碳碳双键
如乙烯CH2==CH2
如二烯烃中的1,3-丁二烯 CH2==CH—CH==CH2
4.链状单烯烃的通式:
CnH2n(n≥2)
C、H元素质量分数?
知识梳理
(1)选择含碳碳双键的最长碳链为主链,称某烯;
(2)从靠近碳碳双键的一端编号,使双键位号最小;
(3)按照“取代基位号-取代基数目+名称-双键位号-某烯”写出名称。
CH3CH==CHCH-CHCH3
CH3
CH3
CH3CHCH==C—CHCH3
CH3
CH3
CH3
CH2==CHCH2CHCH3
CH3
5.烯烃的命名
最简单的烯烃——乙烯CH2==CH2
H× C ∷C×H
H H
·
·
·×
×·
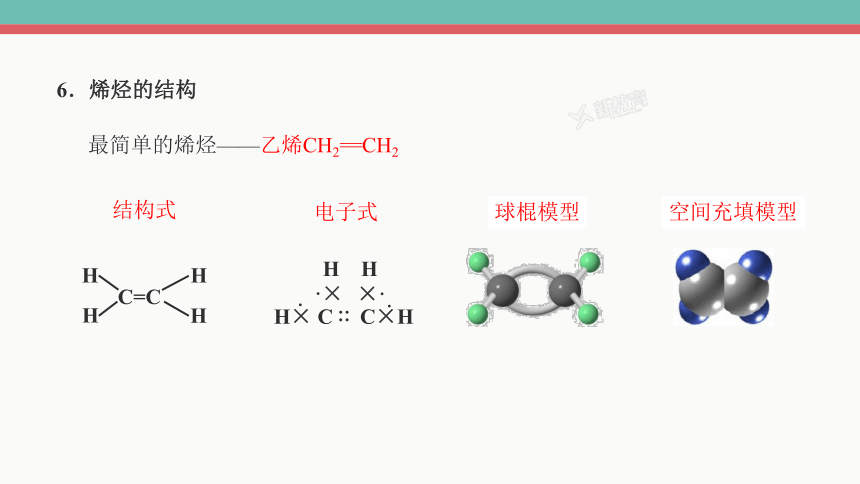
电子式
结构式
球棍模型
空间充填模型
C=C
H
H
H
H
6.烯烃的结构
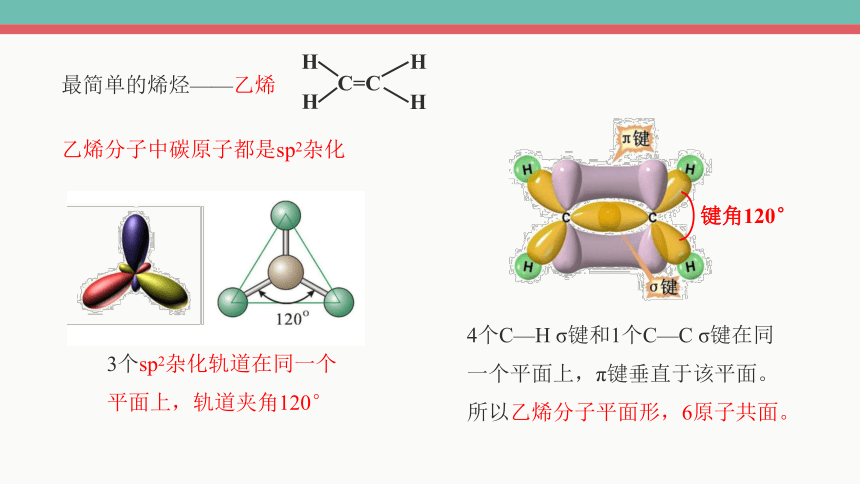
乙烯分子中碳原子都是sp2杂化
3个sp2杂化轨道在同一个平面上,轨道夹角120°
4个C—H σ键和1个C—C σ键在同一个平面上,π键垂直于该平面。
所以乙烯分子平面形,6原子共面。
键角120°
最简单的烯烃——乙烯
C=C
H
H
H
H
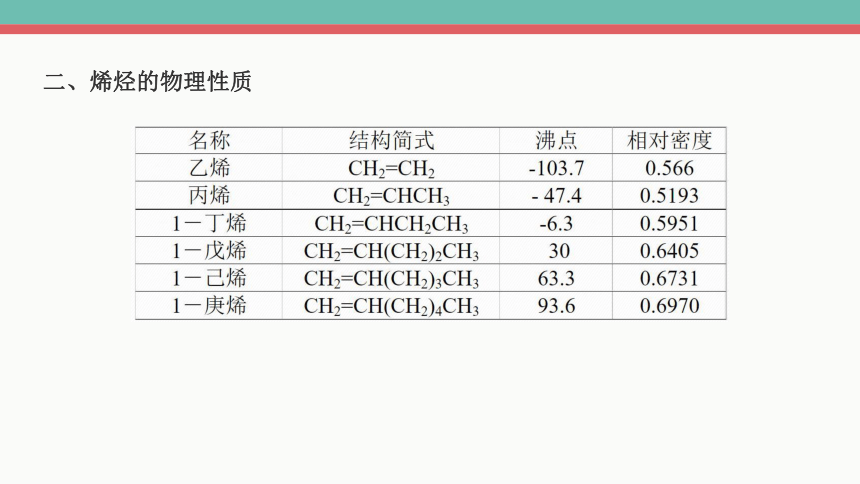
二、烯烃的物理性质
状态
熔沸点
溶解性
密度
随分子中碳原子数增加,熔沸点升高;碳原子数相同时,支链越多,沸点越低
C2 ~ C4的烯烃为气体,C5 ~ C18的烯烃为液体,其余固体
都难溶于水,易溶于有机溶剂
随分子中碳原子数增加,密度逐渐增大;烯烃密度都小于水
与烷烃的物理性质类似
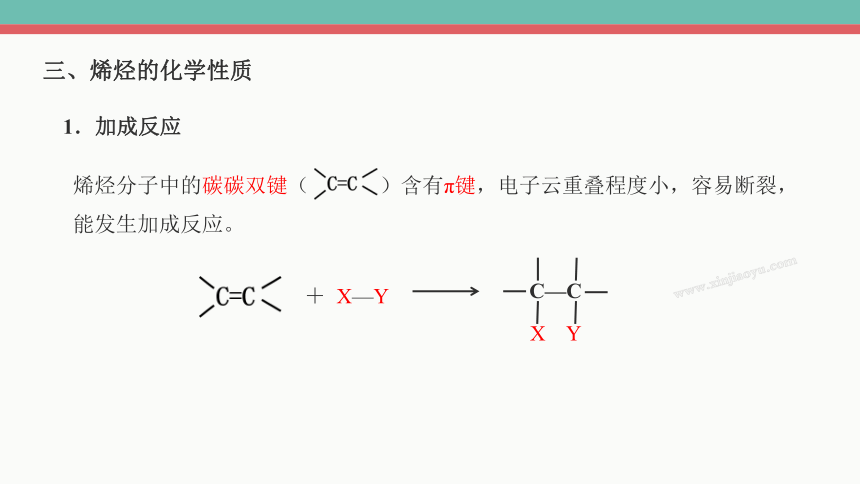
1.加成反应
烯烃分子中的碳碳双键( )含有π键,电子云重叠程度小,容易断裂,能发生加成反应。
+ X—Y
C—C
X Y
三、烯烃的化学性质
(1)与卤素单质加成
烯烃能使溴水或Br2的CCl4溶液褪色,可用于鉴别烯烃
将乙烯、丙烯分别通入溴水中有什么现象?
橙色褪去,有油状液体生成,液体分层,两层均为无色。
怎样命名?
若分别通入Br2/CCl4中,有什么现象?
橙红色褪去
CH2==CH—CH3+Br2→
CH2==CH2+Br2→CH2BrCH2Br
在铂催化剂、加热作用下烯烃与H2加成转为烷烃。
写出CH2==CH2 、 CH2==CHCH3 催化氢化的方程式:
CH2==CH2 +H2
催化剂
加热
CH3—CH3
CH3—CH==CH2+H2
催化剂
加热
CH3—CH2—CH3
工业上将植物油催化氢化得到人造黄油。
(2)与H2发生加成反应
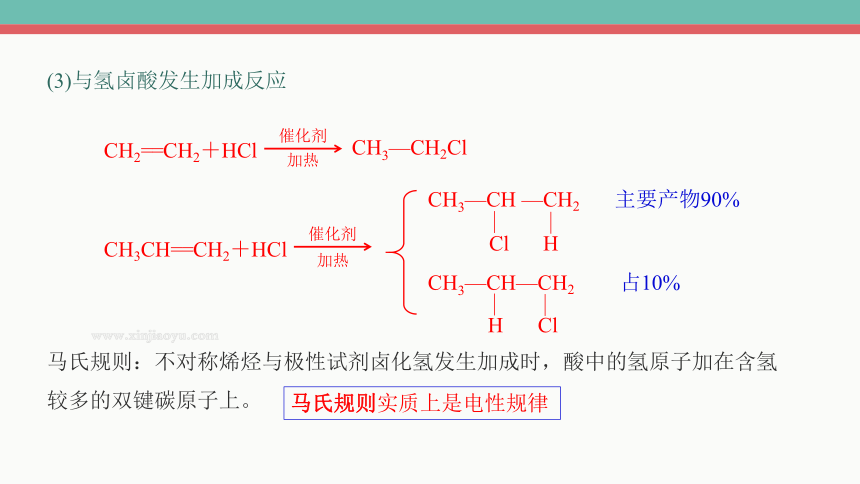
CH3CH==CH2+HCl
催化剂
加热
CH2==CH2+HCl
催化剂
加热
CH3—CH2Cl
主要产物90%
马氏规则:不对称烯烃与极性试剂卤化氢发生加成时,酸中的氢原子加在含氢较多的双键碳原子上。
马氏规则实质上是电性规律
占10%
(3)与氢卤酸发生加成反应
CH3—CH —CH2
—
H
—
Cl
CH3—CH—CH2
H
—
—
Cl
与HBr在过氧化物作用下发生加成反应:
CH3CH==CH2+HBr
过氧化物
光照
CH3—CH —CH2
H
—
—
Br
只能得到反马氏规则产物
丙烯与HBr在过氧化物作用下发生加成反应,生成正溴丙烷。
CH3CH==CH2+H2O
催化剂
加热加压
CH2==CH2+H2O
催化剂
加热加压
CH3—CH2—OH
CH3—CH—CH3
OH
—
2-丙醇(异丙醇)
(4)与H2O发生加成反应
CH3CH==CH2+H2SO4
CH2==CH2+H2SO4
CH3—CH2—OSO3H
CH3—CH—CH3
OSO3H
—
H—O—SO3H
加成产物硫酸氢酯与水加热,可水解成醇和硫酸,此法可用于制备醇。
(5)与浓H2SO4发生加成反应
在适当的温度、压强和催化剂存在的条件下,烯烃分子中碳碳双键中的一个键断裂,分子间通过碳原子相互结合形成很长的碳链,生成相对分子质量很大的聚合物。
乙烯CH2==CH2的加聚反应过程?
2.加聚反应
CH2==CH2+CH2==CH2+CH2==CH2+......
n CH2==CH2
[ CH2—CH2 ]n
催化剂
(聚乙烯)
链节
聚合度
单体
加聚反应的特点:
(1)反应物特征——含有不饱和键。
(2)生成物特征——与反应物具有相同的组成。
(3)反应特征——没有小分子化合物生成。
试写出丙烯(CH2==CHCH3)、苯乙烯( )、四氟乙烯(CF2==CF2)的加聚反应。
CH=CH2
链状单烯烃的燃烧通式:
乙烯燃烧的现象:
火焰明亮,并伴有黑烟
(可用燃烧法鉴别甲烷与乙烯)
3.氧化反应
CnH2n+nO2
点燃
nCO2 + nH2O
(1)燃烧
现象:溶液紫色褪去
CH2=CH2 CO2+H2O
KMnO4
反应化学方程式
5CH2==CH2+12KMnO4+18H2SO4→10CO2+28H2O+6K2SO4+12MnSO4
(2)乙烯气体通入酸性高锰酸钾溶液
【思考】
1.如何鉴别甲烷与乙烯?
2.除去甲烷中的乙烯能否用酸性KMnO4溶液 为什么
不能用酸性KMnO4溶液,因为酸性KMnO4将乙烯最终氧化为CO2,引入新杂质CO2。
①分别通入酸性高锰酸钾溶液
②燃烧法:观察燃烧时的火焰颜色
CH2==CHCH2CH2C==CHCH2CH3
CH3
烯烃结构不同,被酸性KMnO4溶液氧化的产物也不同,此反应可用于推测烯烃的结构。
酸性KMnO4
CO2
R-COOH
R1C=O
R2
CH2==
酸性KMnO4
RCH==
酸性KMnO4
R1C==
R2
酸性KMnO4
1.烯烃顺反异构产生的原因
两个双键碳原子之间不能自由旋转,导致所连接的原子或基团排列方式不同。
2.存在条件
双键碳原子分别连接两个不同的原子或基团。
C=C
a
b
a
b
反式
C=C
b
b
a
a
顺式
C=C
c
a
a
b
不存在顺反异构
四、烯烃的立体异构
C=C
H
H
CH3
CH3
C=C
CH3
H
CH3
H
顺-2-丁烯
反-2-丁烯
熔点/℃ -138.9 -105.5
沸点/℃ 3.7 0.9
相对密度 0.621 0.604
化学性质相同,物理性质有差异
2.链状二烯烃的通式:
3.二烯烃的分类:
CH2==C==CH2
CH2==CH—CH==CH2 (1,3-丁二烯)
CnH2n-2(n≥3)
累积二烯烃
共轭二烯烃
孤立二烯烃
CH2==CH—CH2—CH==CH2
(1,4-戊二烯)
五、二烯烃的结构
1.概念:分子中含有两个碳碳双键的烃
4.最简单的共轭二烯烃:1,3-丁二烯(CH2==CH—CH==CH2)
是一个平面形分子 。
CH2==C—CH==CH2
—
CH3
5.命名:
2-甲基-1,3-丁二烯(异戊二烯)
是天然橡胶的单体
六、二烯烃的化学性质
1.加成反应
CH2==CH—CH==CH2与Br2 按1∶1加成可能的反应:
CH2==CH—CH==CH2 + Br2
1,2-加成
1,4-加成
1,2-加成和1,4-加成是竞争反应,哪种反应占优势,取决于反应条件。
升高温度有利于1,4-加成,降低温度有利于1,2-加成。
CH2==CH—CH==CH2与过量Br2 可完全反应:
CH2==CH—CH==CH2 + 2Br2
CH2—CH—CH—CH2
—
Br
—
Br
—
Br
—
Br
2.加聚反应
n CH2==CH—CH==CH2
催化剂
CH2==C—CH==CH2
—
CH3
n
催化剂
CH2==C—CH==CH2
—
CH3
n
催化剂
+ n CH2==CH2
—CH2—CH==CH—CH2—
[ ]
n
—CH2—C==CH—CH2—
[ ]
n
—
CH3
1.有关乙烯与聚乙烯的说法正确的是( )
A.乙烯有一定的还原性
B.聚乙烯易溶于水
C.聚乙烯能使酸性高锰酸钾溶液褪色
D.乙烯与聚乙烯均能发生加成反应
随堂练习
A
B
2.有关烯烃的说法,不正确的是( )
A.常温下,大部分烯烃物质不是气体
B.所有烯烃的所有原子均共平面
C.1-丁烯与2-丁烯是同分异构体
D.能发生加聚反应,氧化反应
3.下列物质不存在顺反立体异构的是( )
B
A.CH3CH==CHCH3 B.CH2==C(CH3)2
C. D.BrCH==CHBr
4.有关苯乙烯 的说法,正确的是( )
A.用溴水可以除去苯中的苯乙烯
B.苯乙烯有顺反(立体)异构
C.苯乙烯的所有原子可以共平面
D.1 mol苯乙烯最多可以与1 mol H2发生加成反应
C
本节内容结束
第二章 烃
第二节 烯烃 炔烃
第1课时 烯烃
自然界里存在许多烯烃,如番茄中的番茄红素、鲨鱼油中的角鲨烯都是烯烃。
乙烯是常见的烯烃。
番茄中存在番茄红素
新课导入
一、烯烃的结构
1.概念:分子中含有碳碳双键的烃
2.烯烃的官能团为:
碳碳双键
C==C
3.烯烃的分类:
单烯烃:
多烯烃:
只含一个碳碳双键
含有两个或以上的碳碳双键
如乙烯CH2==CH2
如二烯烃中的1,3-丁二烯 CH2==CH—CH==CH2
4.链状单烯烃的通式:
CnH2n(n≥2)
C、H元素质量分数?
知识梳理
(1)选择含碳碳双键的最长碳链为主链,称某烯;
(2)从靠近碳碳双键的一端编号,使双键位号最小;
(3)按照“取代基位号-取代基数目+名称-双键位号-某烯”写出名称。
CH3CH==CHCH-CHCH3
CH3
CH3
CH3CHCH==C—CHCH3
CH3
CH3
CH3
CH2==CHCH2CHCH3
CH3
5.烯烃的命名
最简单的烯烃——乙烯CH2==CH2
H× C ∷C×H
H H
·
·
·×
×·
电子式
结构式
球棍模型
空间充填模型
C=C
H
H
H
H
6.烯烃的结构
乙烯分子中碳原子都是sp2杂化
3个sp2杂化轨道在同一个平面上,轨道夹角120°
4个C—H σ键和1个C—C σ键在同一个平面上,π键垂直于该平面。
所以乙烯分子平面形,6原子共面。
键角120°
最简单的烯烃——乙烯
C=C
H
H
H
H
二、烯烃的物理性质
状态
熔沸点
溶解性
密度
随分子中碳原子数增加,熔沸点升高;碳原子数相同时,支链越多,沸点越低
C2 ~ C4的烯烃为气体,C5 ~ C18的烯烃为液体,其余固体
都难溶于水,易溶于有机溶剂
随分子中碳原子数增加,密度逐渐增大;烯烃密度都小于水
与烷烃的物理性质类似
1.加成反应
烯烃分子中的碳碳双键( )含有π键,电子云重叠程度小,容易断裂,能发生加成反应。
+ X—Y
C—C
X Y
三、烯烃的化学性质
(1)与卤素单质加成
烯烃能使溴水或Br2的CCl4溶液褪色,可用于鉴别烯烃
将乙烯、丙烯分别通入溴水中有什么现象?
橙色褪去,有油状液体生成,液体分层,两层均为无色。
怎样命名?
若分别通入Br2/CCl4中,有什么现象?
橙红色褪去
CH2==CH—CH3+Br2→
CH2==CH2+Br2→CH2BrCH2Br
在铂催化剂、加热作用下烯烃与H2加成转为烷烃。
写出CH2==CH2 、 CH2==CHCH3 催化氢化的方程式:
CH2==CH2 +H2
催化剂
加热
CH3—CH3
CH3—CH==CH2+H2
催化剂
加热
CH3—CH2—CH3
工业上将植物油催化氢化得到人造黄油。
(2)与H2发生加成反应
CH3CH==CH2+HCl
催化剂
加热
CH2==CH2+HCl
催化剂
加热
CH3—CH2Cl
主要产物90%
马氏规则:不对称烯烃与极性试剂卤化氢发生加成时,酸中的氢原子加在含氢较多的双键碳原子上。
马氏规则实质上是电性规律
占10%
(3)与氢卤酸发生加成反应
CH3—CH —CH2
—
H
—
Cl
CH3—CH—CH2
H
—
—
Cl
与HBr在过氧化物作用下发生加成反应:
CH3CH==CH2+HBr
过氧化物
光照
CH3—CH —CH2
H
—
—
Br
只能得到反马氏规则产物
丙烯与HBr在过氧化物作用下发生加成反应,生成正溴丙烷。
CH3CH==CH2+H2O
催化剂
加热加压
CH2==CH2+H2O
催化剂
加热加压
CH3—CH2—OH
CH3—CH—CH3
OH
—
2-丙醇(异丙醇)
(4)与H2O发生加成反应
CH3CH==CH2+H2SO4
CH2==CH2+H2SO4
CH3—CH2—OSO3H
CH3—CH—CH3
OSO3H
—
H—O—SO3H
加成产物硫酸氢酯与水加热,可水解成醇和硫酸,此法可用于制备醇。
(5)与浓H2SO4发生加成反应
在适当的温度、压强和催化剂存在的条件下,烯烃分子中碳碳双键中的一个键断裂,分子间通过碳原子相互结合形成很长的碳链,生成相对分子质量很大的聚合物。
乙烯CH2==CH2的加聚反应过程?
2.加聚反应
CH2==CH2+CH2==CH2+CH2==CH2+......
n CH2==CH2
[ CH2—CH2 ]n
催化剂
(聚乙烯)
链节
聚合度
单体
加聚反应的特点:
(1)反应物特征——含有不饱和键。
(2)生成物特征——与反应物具有相同的组成。
(3)反应特征——没有小分子化合物生成。
试写出丙烯(CH2==CHCH3)、苯乙烯( )、四氟乙烯(CF2==CF2)的加聚反应。
CH=CH2
链状单烯烃的燃烧通式:
乙烯燃烧的现象:
火焰明亮,并伴有黑烟
(可用燃烧法鉴别甲烷与乙烯)
3.氧化反应
CnH2n+nO2
点燃
nCO2 + nH2O
(1)燃烧
现象:溶液紫色褪去
CH2=CH2 CO2+H2O
KMnO4
反应化学方程式
5CH2==CH2+12KMnO4+18H2SO4→10CO2+28H2O+6K2SO4+12MnSO4
(2)乙烯气体通入酸性高锰酸钾溶液
【思考】
1.如何鉴别甲烷与乙烯?
2.除去甲烷中的乙烯能否用酸性KMnO4溶液 为什么
不能用酸性KMnO4溶液,因为酸性KMnO4将乙烯最终氧化为CO2,引入新杂质CO2。
①分别通入酸性高锰酸钾溶液
②燃烧法:观察燃烧时的火焰颜色
CH2==CHCH2CH2C==CHCH2CH3
CH3
烯烃结构不同,被酸性KMnO4溶液氧化的产物也不同,此反应可用于推测烯烃的结构。
酸性KMnO4
CO2
R-COOH
R1C=O
R2
CH2==
酸性KMnO4
RCH==
酸性KMnO4
R1C==
R2
酸性KMnO4
1.烯烃顺反异构产生的原因
两个双键碳原子之间不能自由旋转,导致所连接的原子或基团排列方式不同。
2.存在条件
双键碳原子分别连接两个不同的原子或基团。
C=C
a
b
a
b
反式
C=C
b
b
a
a
顺式
C=C
c
a
a
b
不存在顺反异构
四、烯烃的立体异构
C=C
H
H
CH3
CH3
C=C
CH3
H
CH3
H
顺-2-丁烯
反-2-丁烯
熔点/℃ -138.9 -105.5
沸点/℃ 3.7 0.9
相对密度 0.621 0.604
化学性质相同,物理性质有差异
2.链状二烯烃的通式:
3.二烯烃的分类:
CH2==C==CH2
CH2==CH—CH==CH2 (1,3-丁二烯)
CnH2n-2(n≥3)
累积二烯烃
共轭二烯烃
孤立二烯烃
CH2==CH—CH2—CH==CH2
(1,4-戊二烯)
五、二烯烃的结构
1.概念:分子中含有两个碳碳双键的烃
4.最简单的共轭二烯烃:1,3-丁二烯(CH2==CH—CH==CH2)
是一个平面形分子 。
CH2==C—CH==CH2
—
CH3
5.命名:
2-甲基-1,3-丁二烯(异戊二烯)
是天然橡胶的单体
六、二烯烃的化学性质
1.加成反应
CH2==CH—CH==CH2与Br2 按1∶1加成可能的反应:
CH2==CH—CH==CH2 + Br2
1,2-加成
1,4-加成
1,2-加成和1,4-加成是竞争反应,哪种反应占优势,取决于反应条件。
升高温度有利于1,4-加成,降低温度有利于1,2-加成。
CH2==CH—CH==CH2与过量Br2 可完全反应:
CH2==CH—CH==CH2 + 2Br2
CH2—CH—CH—CH2
—
Br
—
Br
—
Br
—
Br
2.加聚反应
n CH2==CH—CH==CH2
催化剂
CH2==C—CH==CH2
—
CH3
n
催化剂
CH2==C—CH==CH2
—
CH3
n
催化剂
+ n CH2==CH2
—CH2—CH==CH—CH2—
[ ]
n
—CH2—C==CH—CH2—
[ ]
n
—
CH3
1.有关乙烯与聚乙烯的说法正确的是( )
A.乙烯有一定的还原性
B.聚乙烯易溶于水
C.聚乙烯能使酸性高锰酸钾溶液褪色
D.乙烯与聚乙烯均能发生加成反应
随堂练习
A
B
2.有关烯烃的说法,不正确的是( )
A.常温下,大部分烯烃物质不是气体
B.所有烯烃的所有原子均共平面
C.1-丁烯与2-丁烯是同分异构体
D.能发生加聚反应,氧化反应
3.下列物质不存在顺反立体异构的是( )
B
A.CH3CH==CHCH3 B.CH2==C(CH3)2
C. D.BrCH==CHBr
4.有关苯乙烯 的说法,正确的是( )
A.用溴水可以除去苯中的苯乙烯
B.苯乙烯有顺反(立体)异构
C.苯乙烯的所有原子可以共平面
D.1 mol苯乙烯最多可以与1 mol H2发生加成反应
C
本节内容结束
