专题4 生活中常用的有机物—烃的含氧衍生物 检测题(含解析) 2023-2024学年高二下学期化学苏教版(2019)选择性必修3
文档属性
| 名称 | 专题4 生活中常用的有机物—烃的含氧衍生物 检测题(含解析) 2023-2024学年高二下学期化学苏教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 810.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-05 00:00:00 | ||
图片预览


文档简介
专题4《生活中常用的有机物—烃的含氧衍生物》检测题
一、单选题
1.取代反应是一类重要的有机化学反应。下列反应属于取代反应的是
A.
B.
C.
D.nCH2=CH2
2.生活中有各式各样的油,下列油为醇类物质的是
A.煤油 B.汽油
C.柴油 D.甘油
3.研究表明,柠檬酸是需氧生物体内普遍存在的一种代谢中间体。柠檬酸的结构简式如图,关于柠檬酸的说法中不正确的是
A.柠檬酸的分子式是C6H8O7
B.柠檬酸中有2种不同的含氧官能团
C.1 mol柠檬酸能够和4 mol NaOH发生反应
D.柠檬酸可以用来清洗掉铁器表面的铁锈
4.下列关于乙酸和乙醇说法正确的是
A.都难溶于水 B.都能使石蕊试液变红
C.都能与钠反应 D.相互间不能发生反应
5.化学与生产和生活密切相关。下列有关说法正确的是
A.医用酒精中乙醇的体积分数为95%
B.生产N95口罩的“熔喷布”主要原料聚丙烯能使酸性高锰酸钾溶液褪色
C.聚氯乙烯塑料制品可用于食品包装
D.洗衣粉的主要成分之一是十二烷基苯磺酸钠,可由与NaOH溶液反应得到
6.下列实验能获得成功的是
A.苯、溴水、铁粉混合制成溴苯 B.加浓溴水,然后过滤可除去苯中少量苯酚
C.用高锰酸钾酸性溶液来区别甲烷和乙烯 D.可用分液漏斗分离乙醇和水
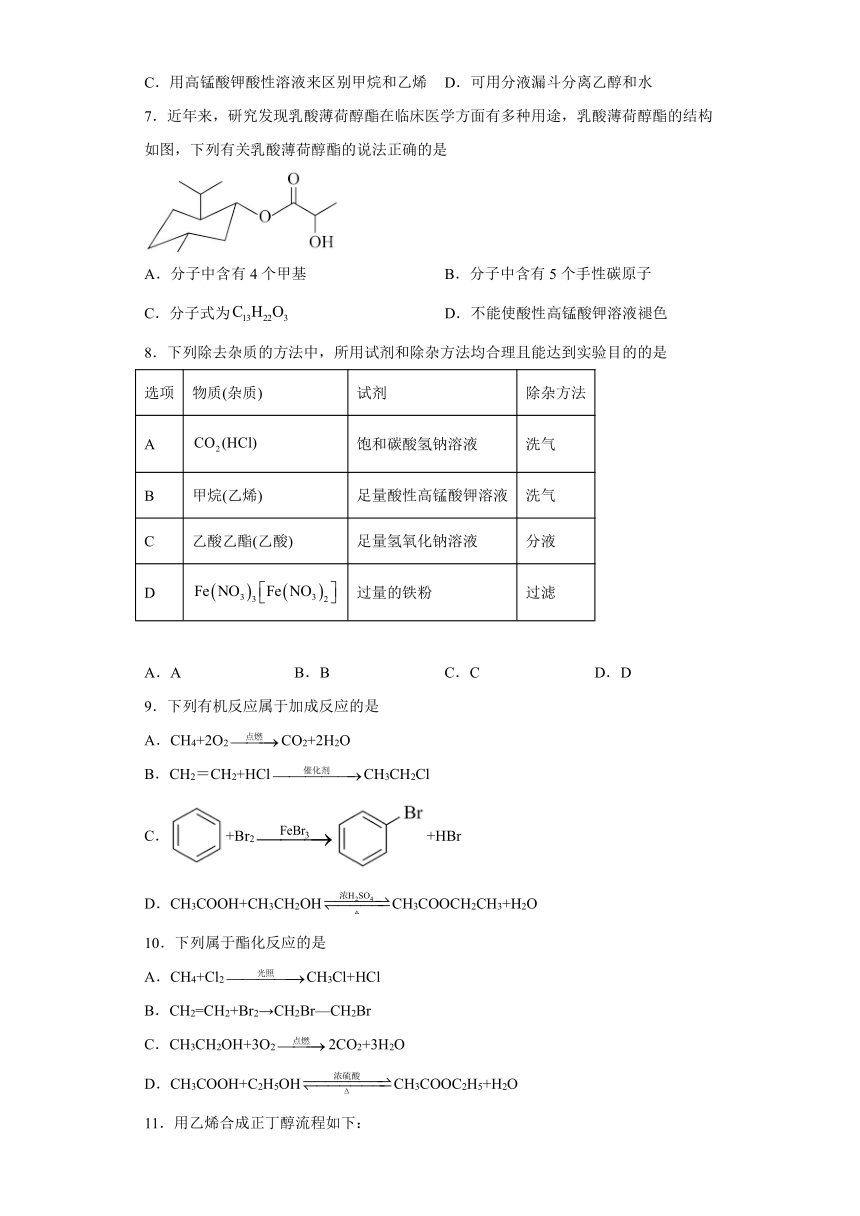
7.近年来,研究发现乳酸薄荷醇酯在临床医学方面有多种用途,乳酸薄荷醇酯的结构如图,下列有关乳酸薄荷醇酯的说法正确的是
A.分子中含有4个甲基 B.分子中含有5个手性碳原子
C.分子式为 D.不能使酸性高锰酸钾溶液褪色
8.下列除去杂质的方法中,所用试剂和除杂方法均合理且能达到实验目的的是
选项 物质(杂质) 试剂 除杂方法
A 饱和碳酸氢钠溶液 洗气
B 甲烷(乙烯) 足量酸性高锰酸钾溶液 洗气
C 乙酸乙酯(乙酸) 足量氢氧化钠溶液 分液
D 过量的铁粉 过滤
A.A B.B C.C D.D
9.下列有机反应属于加成反应的是
A.CH4+2O2CO2+2H2O
B.CH2=CH2+HClCH3CH2Cl
C.+Br2+HBr
D.CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
10.下列属于酯化反应的是
A.CH4+Cl2CH3Cl+HCl
B.CH2=CH2+Br2→CH2Br—CH2Br
C.CH3CH2OH+3O22CO2+3H2O
D.CH3COOH+C2H5OHCH3COOC2H5+H2O
11.用乙烯合成正丁醇流程如下:CH2=CH2CH3CH2OHCH3CHOCH3CH=CHCHOCH3CH2CH2CH2OH。下列说法错误的是
A.反应1是加成反应
B.反应2中,每生成1mol乙醛,转移2mol电子
C.检验反应3的生成物中含有碳碳双键,只需酸性KMnO4溶液
D.正丁醇的同分异构体中属于醇有3种
12.下列说法正确的是
A.体系的内能与温度等有关,只要温度不变,体系的内能不变
B.反应能自发进行,它的,
C.室温下,pH=4的醋酸溶液和pH=10的氢氧化钠溶液等体积混合后,所得溶液的pH大于7
D.水与丙酮能完全互溶的原因是两种分子间能形成氢键
13.某实验小组学习了乙醇的化学性质后,在老师的指导下设计了如下实验验证课堂所学的乙醇的化学性质。下列说法错误的是
A.甲、乙烧杯中均为78℃以上的热水 B.铜网降低了乙醇和氧气反应的活化能
C.试管a中得到的溶液可能使锌粒溶解 D.铜网上出现红色和黑色交替现象
14.下列甲、乙两组有机反应类型相同的是
选项 甲组 乙组
A 苯与氢气在催化剂、加热条件下反应 苯与液溴在FeBr3作用下反应
B 乙醇和钠反应 丙烯酸(CH2=CHCOOH)与乙醇在浓硫酸、加热条件下反应
C 乙醇与氧气在铜和加热条件下反应 丙烯(CH3CH=CH2)与溴的四氯化碳溶液反应
D 在酸性KMnO4溶液中滴加乙醇 在光照条件下甲烷与氯气发生反应
A.A B.B C.C D.D
15.利用下列实验装置完成对应的实验,能达到实验目的的是
选项 A B C D
目的 验证苯与液溴发生取代反应 探究酒精脱水生成乙烯 证明酸性:碳酸>苯酚 制备乙酸乙酯并提高产率
实验方案
A.A B.B C.C D.D
二、填空题
16.根据下列要求,从①H2O ②CH2=CH2 ③CH3COOH ④HNO3 ⑤CH3CH2OH中选择恰当的反应物,并写出对应的化学方程式,指出反应类型。
(1)得到乙醇的反应,化学方程式_______________;反应类型__________。
(2)与苯发生取代反应,化学方程式_______________;反应类型__________。
(3)炒菜时加入一些料酒和食醋,可使饭菜变得味香、可口的原因,化学方程式_______________;反应类型为酯化反应。
(4)由乙烯合成高分子化合物,化学方程式_______________;反应类型__________。
17.按要求填空
(1) 的名称为___________。
(2) 的名称为___________。
(3)1,3-二甲基-2-乙基苯 ___________。
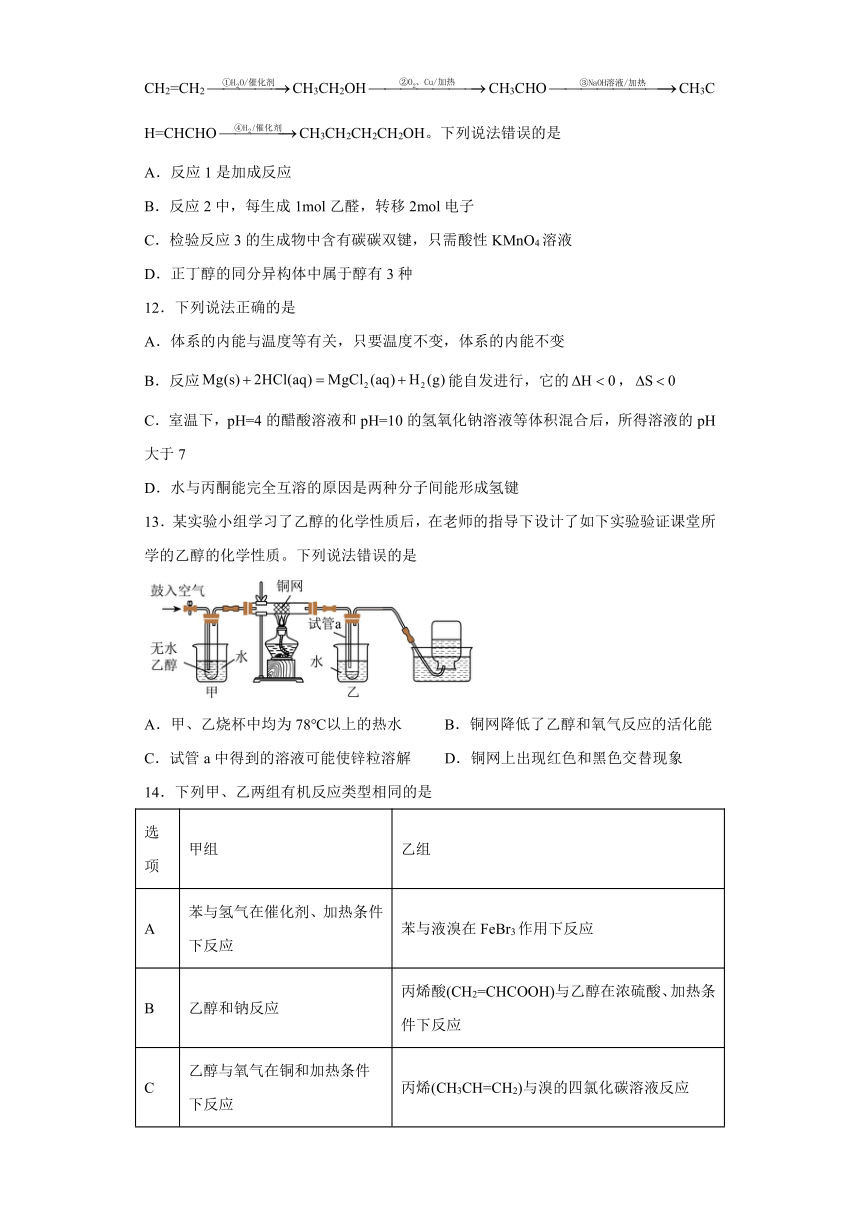
(4) 1mol该物质最多能与___________molBr2发生反应,最多能与___________molNaOH发生反应
18.B()有多种同分异构体,同时满足下列条件的同分异构体有___________种(不考虑立体异构)
①苯环上有2个取代基 ②能够发生银镜反应 ③与溶液发生显色发应
其中核磁共振氢谱有五组峰,且峰面积之比为6:2:2:1:1的结构简式为___________;
三、实验题
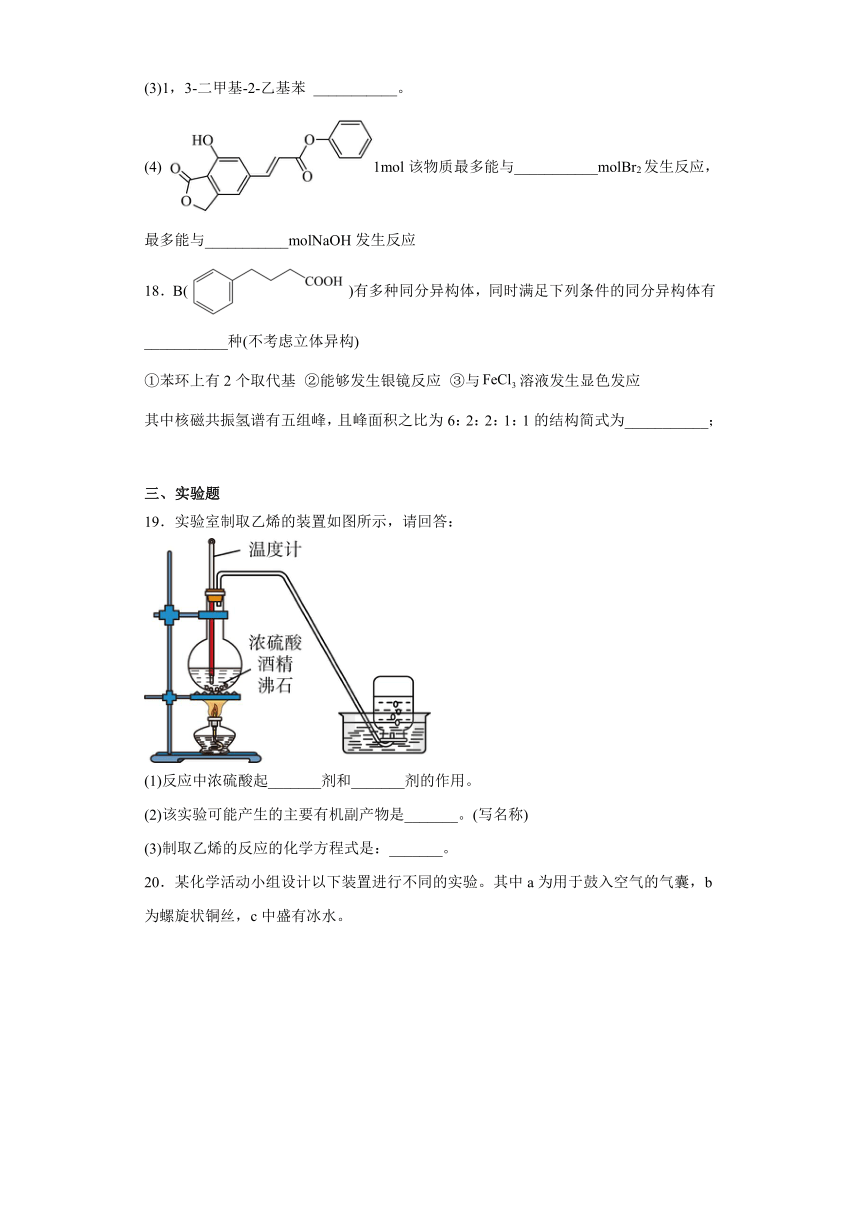
19.实验室制取乙烯的装置如图所示,请回答:
(1)反应中浓硫酸起_______剂和_______剂的作用。
(2)该实验可能产生的主要有机副产物是_______。(写名称)
(3)制取乙烯的反应的化学方程式是:_______。
20.某化学活动小组设计以下装置进行不同的实验。其中a为用于鼓入空气的气囊,b为螺旋状铜丝,c中盛有冰水。
(1)若用A装置做乙醇与乙酸的酯化反应实验,则还需连接的装置是___(填序号),该实验的反应原理是____。从实验安全角度考虑,A装置试管中除加入反应液外,还需加入固体物质,其目的是_____。
(2)该小组同学欲做乙醇氧化成乙醛的实验,则应选用的装置是____(填序号),再用制得的乙醛溶液进行银镜反应,正确的操作顺序是_____(填序号)。
①向试管中滴入3滴乙醛溶液
②一边振荡一边滴入2%的稀氨水,直至最初产生的沉淀恰好溶解为止
③振荡后放入热水中,水浴加热
④在洁净的试管中加入1mL2%的AgNO3溶液
银镜反应的化学反应方程式是______。
21.桂酸乙酯(3-苯基丙烯酸乙酯)能混溶于乙醇、乙醚,几乎不溶于甘油和水。实验室以肉桂酸( )为主要原料制取肉桂酸乙酯的实验装置如图所示。
已知:
物质 肉桂酸 肉桂酸乙酯 乙醇 环己烷 环己烷、乙醇和水形成的三元共沸物
沸点/℃(101kPa) 300 271.5 78.3 80.8 62.6
三元共沸物是指在恒定压力下沸腾时,其组分与沸点均保持不变的三组分液体混合物。
实验包含以下“步骤”:
①加料。操作甲后向装置M的圆底烧瓶中依次加入3.0g肉桂酸、15mL乙醇、15mL环己烷、1mL浓硫酸,连接装置。
②蒸馏。用无水氯化钙干燥至有机层澄清透明,过滤后转移入干燥的蒸馏装置,40℃水浴蒸馏蒸出乙醚。
③蒸馏。改为装置N,蒸馏出过量的乙醇和环己烷。
④中和。反应液稍冷后倒入盛有80mL水的烧杯中,分批加入固体碳酸钠,至溶液呈中性。
⑤分水回流。水浴回流约2-3h,当b(分水器)中下层液面接近其支管时进行操作乙,待下层共收集约3mL液体时停止加热。
⑥分液。液体转移至分液漏斗,静置片刻后分出有机层。水层用24mL乙醚分三次萃取,然后合并有机层。
⑦蒸馏。减压蒸馏,得粗产物。
回答下列问题:
(1)上述“步骤”正确的操作顺序是①___________⑦。
(2)写出制取肉桂酸乙酯的化学方程式___________。
(3)仪器a的名称为___________;实验中加入环己烷的作用是___________。
(4)操作甲是___________;操作乙是___________。
(5)用装置N(不考虑加热及夹持装置等)进行上述步骤③的操作,错误共有___________(填标号)。
A.2处 B.3处 C.4处 D.5处
(6)将粗产物进一步精馏干燥后,得到纯净产物2.2g,则肉桂酸乙酯的产率为___________%(保留三位有效数字)。
四、计算题
22.酒精溶液在抗击COVID-19中发挥了极为重要的作用,现有xg乙醇(C2H5OH)在一定量氧气中燃烧生成13.2gCO2、10.8gH2O及ygCO。回答下列问题:
(1)医用消毒酒精溶液的常用浓度(体积分数)是___________。
(2)生成物中CO2、H2O的分子个数比为___________,y=___________,写出该燃烧反应的化学方程式:___________。
(3)若使该乙醇完全燃烧,至少还需要___________LO2(标准状况)。
试卷第4页,共7页
参考答案:
1.A
【详解】A.乙醇和乙酸的酯化反应,酯化反应又是取代反应,A正确;
B.乙醇的催化氧化反应,属于氧化反应,B错误;
C.乙烯和溴化氢加成生成溴乙烷,属于加成反应,C错误;
D.乙烯能通过自身加聚反应生成聚乙烯,属于加聚反应,D错误;
故选A。
2.D
【详解】A.煤油是石油分馏的产品,主要成分仍为烃类物质,故A错误;
B.汽油是石油分馏的产品,主要成分仍为烃类物质,故B错误;
C.柴油是石油分馏的产品,主要成分仍为烃类物质,故C错误;
D.甘油是丙三醇,为醇类物质,故D正确;
故选D。
3.C
【分析】柠檬酸有3个羧基和1个醇羟基。
【详解】A.根据结构简式可知柠檬酸的分子式是C6H8O,故A正确;
B.柠檬酸中有3个羧基和1个醇羟基,即有2种不同的含氧官能团,故B正确;
C.柠檬酸中有3个羧基,即1 mol柠檬酸能够和3 mol NaOH发生反应,故C错误;
D.柠檬酸中有羧基,具有酸性,可以用来清洗掉铁器表面的铁锈,故D正确;
故答案为C。
4.C
【详解】A.都与水互溶,故A错误;
B.乙酸能使石蕊试液变红,乙醇不能,故B错误;
C.都能与钠反应,生成氢气,故C正确;
D.乙酸和乙醇能发生酯化反应,故D错误;
答案选C。
5.D
【详解】A.医用酒精中乙醇的体积分数为75%,故A错误;
B.生产N95口罩的“熔喷布”主要原料聚丙烯,聚丙烯不含碳碳双键,因此不能使酸性高锰酸钾溶液褪色,故B错误;
C.聚氯乙烯塑料制品有毒,不可用于食品包装,故C错误;
D.与NaOH溶液反应得到十二烷基苯磺酸钠和水,十二烷基苯磺酸钠是洗衣粉的主要成分之一,故D正确。
综上所述,答案为D。
6.C
【详解】A.苯与溴水不反应,苯、液溴、铁粉混合制成溴苯,故A错误;
B.三溴苯酚溶于苯中,加浓溴水与苯酚反应生成三溴苯酚,三溴苯酚与苯互溶,苯中引入新的杂质,故B错误;
C.乙烯能够被高锰酸钾酸性溶液氧化,使高锰酸钾酸性溶液褪色,而甲烷不能,可以用高锰酸钾酸性溶液来区别甲烷和乙烯,故C正确;
D.乙醇与水互溶,在分液漏斗中不分层,所以不能用分液漏斗分离乙醇和水,故D错误;
故选C。
7.A
【详解】A.该分子的结构简式为:,可知分子中含有4个甲基,A项正确;
B.将连有四个不同的原子或原子团的碳原子称为手性碳原子,如图所示,,可知分子中含有4个手性碳原子,B项错误;
C.根据结构图,可知分子式为C13H24O3,C项错误;
D.分子中含有羟基,能够被酸性高锰酸钾溶液氧化,所以能使酸性高锰酸钾溶液褪色,D项错误;
答案选A。
8.A
【详解】A.饱和碳酸氢钠溶液可吸收HCl并产生二氧化碳,符合除杂目的,A符合题意;
B.酸性高锰酸钾可将乙烯氧化,同时会产生,引入了新杂质,B项不符合题意;
C.乙酸乙酯中加入氢氧化钠溶液可除去乙酸,但同时乙酸乙酯在碱性条件下也会水解,C项不符合题意;
D.过量铁粉会将铁离子还原为亚铁离子,除杂试剂选用错误,D项不符合题意。
故选A。
9.B
【详解】A. 甲烷的燃烧反应属于氧化反应,不属于加成反应,故A不符合;
B. 具有双键的乙烯与氯化氢发生反应,生成饱和有机物氯乙烷,属于加成反应,故B符合;
C. 苯与液溴发生取代反应,故C不符合;
D. 乙醇与乙酸反应,生成乙酸乙酯和水,为酯化反应,也属于取代反应,不属于加成反应,故D不符合;
故选B。
10.D
【详解】A.CH4+Cl2CH3Cl+HCl表示甲烷和氯气的取代反应,故A不选;
B.CH2=CH2+Br2→CH2Br—CH2Br表示乙烯和溴单质的加成反应,故B不选;
C.CH3CH2OH+3O22CO2+3H2O表示乙醇的氧化反应,故C不选;
D.CH3COOH+C2H5OHCH3COOC2H5+H2O表示乙醇和乙酸的酯化反应,故D选;
正确答案是D。
11.C
【详解】A.由题干信息可知,反应1是CH2=CH2+H2OCH3CH2OH,属于加成反应,A正确;
B.由题干信息可知,反应2为2CH3CH2OH+O22CH3CHO+2H2O,故反应中每生成1mol乙醛,转移2mol电子,B正确;
C.由于醛基和碳碳双键均能使酸性高锰酸钾褪色,故检验反应3的生成物中含有碳碳双键,仅用酸性KMnO4溶液无法完成,可以仅用溴的四氯化碳溶液,C错误;
D.正丁醇即1-丁醇的同分异构体中除了其自身外属于醇有:2-丁醇CH3CH2CH(OH)CH3、2-甲基-1-丙醇(CH3)2CHCH2OH、2-甲基-2-丙醇(CH3)3COH等3种,D正确;
故答案为:C。
12.D
【详解】A.内能是体系内部能量的总和,与温度、体积、质量、状态等因素有关,A错误;
B.液体与固体反应生成气体,体系混乱程度增大,属于熵增过程,即△S>0,B错误;
C.由所给数据知,CH3COOH溶液中已经电离出的H+恰好将NaOH中和,而原醋酸溶液中大量CH3COOH未电离,故反应后,溶液中剩余大量醋酸,溶液显酸性,C错误;
D.丙酮中羰基氧与水分子中氢原子之间能形成分子间氢键,故丙酮与水互溶,D正确;
故答案选D。
13.A
【分析】该实验的原理为在铜的催化作用下,乙醇被氧气氧化成乙醛,乙醛可能继续被氧化成乙酸。甲烧杯内是高于乙醇沸点的热水,目的是使乙醇汽化,然后和氧气按照一定体积比混合,在硬质玻璃管中,铜被氧化成黑色CuO,CuO被乙醇还原成Cu,总体上铜作催化剂,降低了乙醇被氧气氧化成乙醛的活化能。反应生成的乙醛(可能含有乙酸及未被氧化的乙醇)进入置于乙烧杯冷水中的试管a中被冷凝,得到含有乙醛、可能含有乙酸及未被氧化的乙醇的溶液,乙酸和活泼金属Zn能反应;
【详解】A.甲烧杯内是高于乙醇沸点的热水,乙烧杯冷水,选项A错误;
B.铜网降低了乙醇和氧气反应的活化能,选项B正确;
C.反应生成的乙醛,可能含有乙酸,进入置于乙烧杯冷水中的试管a中可能使锌粒溶解,选项C正确;
D.铜被氧化成黑色CuO,CuO被乙醇还原成Cu,出现红色和黑色交替现象,选项D正确;
答案选A。
14.B
【详解】A.苯与氢气在催化剂、加热条件下发生加成反应,苯与液溴在FeBr3作用下发生取代反应,甲、乙两组有机反应类型不相同,故A不选;
B.乙醇和钠发生置换反应生成氢气,丙烯酸(CH2=CHCOOH)与乙醇在浓硫酸、加热条件下发生取代(酯化)反应,甲、乙两组有机反应类型相同,故B选;
C.乙醇与氧气在铜和加热条件下发生催化氧化反应,丙烯(CH3CH=CH2)与溴的四氯化碳溶液发生加成反应,甲、乙两组有机反应类型不相同,故C不选;
D.在酸性KMnO4溶液中滴加乙醇发生氧化反应,在光照条件下甲烷与氯气发生取代反应,甲、乙两组有机反应类型不相同,故D不选;
故选B。
15.D
【详解】A.苯与液溴在铁作催化剂发生取代反应:+Br2+HBr,该反应为放热反应,产生的HBr气体中混有Br2蒸气,Br2蒸气溶于硝酸银溶液中也产生淡黄色沉淀AgBr,对HBr的检验产生干扰,题中缺少除去Br2蒸气的装置,HBr极易溶于水,题中缺少防倒吸装置,故A错误;
B.乙醇发生消去反应:CH3CH2OHCH2=CH2↑+H2O,浓硫酸具有脱水性,将酒精脱水炭化,产生的碳单质与浓硫酸反应生成CO2、SO2,产生的乙烯中混有SO2和挥发出的乙醇,SO2和乙醇也能使酸性高锰酸钾溶液褪色,题中缺少除去SO2和乙醇的装置,故B错误;
C.浓盐酸具有挥发性,烧瓶中产生CO2中混有HCl(g),HCl(g)也能与苯酚钠反应产生苯酚,对碳酸、苯酚酸性强弱对比产生干扰,题中缺少除去CO2中HCl(g)的操作,故C错误;
D.乙酸和乙醇发生酯化反应CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O,乙醇、乙酸、乙酸乙酯蒸气在冷凝管中遇冷,回流到三口烧瓶中,增加乙酸、乙醇的利用率,提高乙酸乙酯的产率,同时利用分水器可以做到乙酸乙酯与水的分离,故D正确;
答案为D。
16.(1) CH2=CH2+H2O→CH3-CH2OH 加成反应
(2) 取代反应
(3)CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O
(4) nCH2=CH2→; 加聚反应
【详解】(1)乙烯与水发生加成反应生成乙醇,化学方程式为:CH2=CH2+H2O→CH3-CH2OH;故答案为CH2=CH2+H2O→CH3-CH2OH;加成反应。
(2)苯与硝酸在浓硫酸、加热条件下发生取代反应,生成硝基苯,化学方程式为:;故答案为;取代反应。
(3)乙酸和乙醇在一定条件下发生酯化反应,化学方程式为:CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O;故答案为CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O。
(4)乙烯在一定条件下发生加聚反应生成聚乙烯,化学方程式为:
nCH2=CH2→;故答案为nCH2=CH2→;加聚反应。
17. 3,3-二甲基-2-丁醇 2 -甲基 -1,3 -丁二烯 3 4
【详解】(1)该物质中含有羟基,属于醇,与羟基相连的最长碳链上有4个碳,从靠近羟基的一端编号,2号碳上有羟基,3号碳上有两个甲基,所以名称为3,3-二甲基-2-丁醇;
(2)该物质中含有两个碳碳双键,属于二烯烃,双键所在最长碳链有4个碳,由于双键位于主链两端,所以从靠近支链的一端开始编号,1、3号碳上有双键,2号碳上有一个甲基,所以名称为2 甲基 1,3 丁二烯;
(3)1,3-二甲基-2-乙基苯的母体为苯,任取苯环上一个碳原子开始编号,1、3号碳上各有一个甲基,2号碳上有一个乙基,所以结构简式为;
(4)碳碳双键可以和溴发生加成反应,酚羟基的邻、对位有空位,可以发生取代反应,所以1mol该物质最多能与3molBr2发生反应;酚羟基、两个酯基水解生成的羧基可以和NaOH反应,其中一个酯基水解后还生成酚羟基,也能与NaOH反应,所以1mol该物质最多与4molNaOH发生反应。
18. 15
【详解】的同分异构体满足:①能发生银镜反应,说明结构中存在醛基,②与FeCl3溶液发生显色发应,说明含有酚羟基,同时满足苯环上有2个取代基,酚羟基需占据苯环上的1个取代位置,支链上苯环连接方式(红色点标记):、 共五种,因此一共有5×3=15种结构;其中核磁共振氢谱有五组峰,因酚羟基和醛基均无对称结构,因此峰面积之比为6:2:2:1:1的结构简式一定具有对称性(否则苯环上的氢原子不等效),即苯环上取代基位于对位,核磁共振氢谱中峰面积比为6的氢原子位于与同一碳原子相连的两个甲基上,因此该同分异构的结构简式为。
19.(1) 催化 脱水
(2)乙醚
(3)CH3CH2OHCH2=CH2↑+H2O
【分析】乙醇在浓硫酸做作催化剂和脱水剂条件下迅速加热到170℃发生消去反应生成乙烯,反应方程式为: CH3CH2OHCH2=CH2↑+H2O,实验应注意温度应控制在170℃,在140℃时容易发生副反应生成乙醚, 据此分析解答。
【详解】(1)乙醇在浓硫酸做催化剂和脱水剂条件下发生消去反应生成乙烯;因此浓硫酸在该反应中的作用是脱水剂和催化剂;
(2)实验室制备乙烯反应温度应控制在170℃,若反应温度在140℃,会发生乙醇分子之间的取代反应产生有机副产物乙醚;
(3)乙醇在浓硫酸作催化剂和脱水剂条件下迅速加热到170℃,乙醇会发生消去反应生成乙烯,该反应的化学方程式为:CH3CH2OH CH2=CH2↑+H2O。
。
20. D CH3COOH+C2H5OHCH3COOC2H5+H2O 防止暴沸 ABC ④②①③ CH3CHO+2Ag(NH3)2OHCH3COONH4+3NH3↑+2Ag↓+H2O
【分析】若用A装置做乙醇与乙酸的酯化反应实验,需要连接D装置吸收乙醇,中和乙酸,降低乙酸乙酯溶解度,防止倒吸,A装置液体加热沸腾需要加入碎瓷片或沸石防止暴沸,以此解答。
【详解】(1)若用A装置做乙醇与乙酸的酯化反应实验,需要连接D装置,该实验的反应原理是:CH3COOH+C2H5OHCH3COOC2H5+H2O;A装置液体加热沸腾需要加入碎瓷片或沸石防止暴沸,故答案为:D;CH3COOH+C2H5OHCH3COOC2H5+H2O;防止暴沸;
(2)做乙醇氧化成乙醛的实验,需要提供乙醇蒸气和氧气在催化剂作用下氧化反应生成乙醛,反应的化学方程式为:2CH3CH2OH+O22CH3CHO+2H2O,冷却得到液体乙醛,装置连接为A、B、C;乙醛溶液进行银镜反应,先制取银氨溶液,向硝酸银溶液中滴入氨水至变色沉淀全部溶解得到银氨溶液,滴入乙醛溶液在水浴中加热反应观察银镜现象,实验顺序是④②①③,银镜反应的化学反应方程式是:CH3CHO+2Ag(NH3)2OHCH3COONH4+3NH3+2Ag↓+H2O,故答案为:ABC;④②①③;CH3CHO+2Ag(NH3)2OHCH3COONH4+3NH3↑+2Ag↓+H2O。
21.(1)⑤③④⑥②
(2)
(3) 球形冷凝管 形成共沸物,将产物水带出,使得平衡正向移动,提高产率
(4) 检查装置的气密性 打开分水器下端的活塞,使下层的水放出到量筒中
(5)B
(6)61.7
【分析】酸和醇在浓硫酸催化作用下生成酯,反应后得到酯蒸馏除去过量的乙醇和环己烷,加入碳酸钠除去酸,分液、萃取分液分离出有机层后,再次蒸馏得到粗品;
【详解】(1)根据分析可知,实验的过程为:①加料,并连接装置;⑤分水回流,制取得到酯;③蒸馏,利用物质沸点不同蒸馏出过量的乙醇和环己烷;④中和,加入碳酸钠固体除去酸;⑥分液,分离出有机层;②蒸馏,除去萃取剂乙醚;⑦减压蒸馏,得粗产物;故正确的操作顺序是①⑤③④⑥②⑦;
(2)肉桂酸和乙醇加热在浓硫酸催化作用下生成肉桂酸乙酯:;
(3)仪器a的名称为球形冷凝管;环己烷沸点较低,实验中加入环己烷的作用是形成共沸物,将产物水带出,使得平衡正向移动,提高产率;
(4)反应中涉及蒸馏回流操作,需要较好的装置气密性,故操作甲是检查装置的气密性;当b(分水器)中下层液面接近其支管时,需要排出其下层过量的水,保留上层的馏分,故操作乙是打开分水器下端的活塞,使下层的水放出到量筒中;
(5)蒸馏时温度计应该在支管口处;冷凝水应该下进上出;承接馏分的装置应该为敞口装置,使得馏分顺利滴下;故共3处错误,故选B;
(6)3.0g肉桂酸为,则理论生成肉桂酸乙酯的质量为,故肉桂酸乙酯的产率为。
22. 75% 1:2 2.8 1.12
【详解】(1)医用消毒酒精溶液的常用浓度(体积分数)是75%,低于75%消毒效果不理想,浓度太大会使蛋白质表面形成硬膜,阻止乙醇分子破坏病毒内部蛋白质,无法杀死病毒;
(2) xg乙醇(C2H5OH)在一定量氧气中燃烧生成13.2gCO2、10.8gH2O及ygCO,13.2gCO2的物质的量为=0.3mol,10.8gH2O的物质的量为=0.6mol,因此生成物中CO2、H2O的分子个数比为0.3:0.6=1:2,0.6molH2O中含有1.2molH,1mol C2H5OH含有6molH,则含1.2molH的乙醇的物质的量为=0.2mol,含碳原子的物质的量为0.4mol,根据碳原子守恒,反应生成的一氧化碳的物质的量为0.1mol,其质量y=0.1molx28g/mol=2.8g;该反应中C2H5OH、CO2、CO、H2O的物质的量之比为0.2:0.3:0.1:0.6=2:3:1:6,则反应的化学方程式:;
(3)一氧化碳燃烧的化学方程式为:2CO+O22CO2,由此可知,0.1mol的CO完全燃烧需要消耗0.05molO2,则这些氧气标况下的体积为0.05molx22.4L/mol=1.12L,则使该乙醇完全燃烧,至少还需要1.12LO2(标准状况)
一、单选题
1.取代反应是一类重要的有机化学反应。下列反应属于取代反应的是
A.
B.
C.
D.nCH2=CH2
2.生活中有各式各样的油,下列油为醇类物质的是
A.煤油 B.汽油
C.柴油 D.甘油
3.研究表明,柠檬酸是需氧生物体内普遍存在的一种代谢中间体。柠檬酸的结构简式如图,关于柠檬酸的说法中不正确的是
A.柠檬酸的分子式是C6H8O7
B.柠檬酸中有2种不同的含氧官能团
C.1 mol柠檬酸能够和4 mol NaOH发生反应
D.柠檬酸可以用来清洗掉铁器表面的铁锈
4.下列关于乙酸和乙醇说法正确的是
A.都难溶于水 B.都能使石蕊试液变红
C.都能与钠反应 D.相互间不能发生反应
5.化学与生产和生活密切相关。下列有关说法正确的是
A.医用酒精中乙醇的体积分数为95%
B.生产N95口罩的“熔喷布”主要原料聚丙烯能使酸性高锰酸钾溶液褪色
C.聚氯乙烯塑料制品可用于食品包装
D.洗衣粉的主要成分之一是十二烷基苯磺酸钠,可由与NaOH溶液反应得到
6.下列实验能获得成功的是
A.苯、溴水、铁粉混合制成溴苯 B.加浓溴水,然后过滤可除去苯中少量苯酚
C.用高锰酸钾酸性溶液来区别甲烷和乙烯 D.可用分液漏斗分离乙醇和水
7.近年来,研究发现乳酸薄荷醇酯在临床医学方面有多种用途,乳酸薄荷醇酯的结构如图,下列有关乳酸薄荷醇酯的说法正确的是
A.分子中含有4个甲基 B.分子中含有5个手性碳原子
C.分子式为 D.不能使酸性高锰酸钾溶液褪色
8.下列除去杂质的方法中,所用试剂和除杂方法均合理且能达到实验目的的是
选项 物质(杂质) 试剂 除杂方法
A 饱和碳酸氢钠溶液 洗气
B 甲烷(乙烯) 足量酸性高锰酸钾溶液 洗气
C 乙酸乙酯(乙酸) 足量氢氧化钠溶液 分液
D 过量的铁粉 过滤
A.A B.B C.C D.D
9.下列有机反应属于加成反应的是
A.CH4+2O2CO2+2H2O
B.CH2=CH2+HClCH3CH2Cl
C.+Br2+HBr
D.CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
10.下列属于酯化反应的是
A.CH4+Cl2CH3Cl+HCl
B.CH2=CH2+Br2→CH2Br—CH2Br
C.CH3CH2OH+3O22CO2+3H2O
D.CH3COOH+C2H5OHCH3COOC2H5+H2O
11.用乙烯合成正丁醇流程如下:CH2=CH2CH3CH2OHCH3CHOCH3CH=CHCHOCH3CH2CH2CH2OH。下列说法错误的是
A.反应1是加成反应
B.反应2中,每生成1mol乙醛,转移2mol电子
C.检验反应3的生成物中含有碳碳双键,只需酸性KMnO4溶液
D.正丁醇的同分异构体中属于醇有3种
12.下列说法正确的是
A.体系的内能与温度等有关,只要温度不变,体系的内能不变
B.反应能自发进行,它的,
C.室温下,pH=4的醋酸溶液和pH=10的氢氧化钠溶液等体积混合后,所得溶液的pH大于7
D.水与丙酮能完全互溶的原因是两种分子间能形成氢键
13.某实验小组学习了乙醇的化学性质后,在老师的指导下设计了如下实验验证课堂所学的乙醇的化学性质。下列说法错误的是
A.甲、乙烧杯中均为78℃以上的热水 B.铜网降低了乙醇和氧气反应的活化能
C.试管a中得到的溶液可能使锌粒溶解 D.铜网上出现红色和黑色交替现象
14.下列甲、乙两组有机反应类型相同的是
选项 甲组 乙组
A 苯与氢气在催化剂、加热条件下反应 苯与液溴在FeBr3作用下反应
B 乙醇和钠反应 丙烯酸(CH2=CHCOOH)与乙醇在浓硫酸、加热条件下反应
C 乙醇与氧气在铜和加热条件下反应 丙烯(CH3CH=CH2)与溴的四氯化碳溶液反应
D 在酸性KMnO4溶液中滴加乙醇 在光照条件下甲烷与氯气发生反应
A.A B.B C.C D.D
15.利用下列实验装置完成对应的实验,能达到实验目的的是
选项 A B C D
目的 验证苯与液溴发生取代反应 探究酒精脱水生成乙烯 证明酸性:碳酸>苯酚 制备乙酸乙酯并提高产率
实验方案
A.A B.B C.C D.D
二、填空题
16.根据下列要求,从①H2O ②CH2=CH2 ③CH3COOH ④HNO3 ⑤CH3CH2OH中选择恰当的反应物,并写出对应的化学方程式,指出反应类型。
(1)得到乙醇的反应,化学方程式_______________;反应类型__________。
(2)与苯发生取代反应,化学方程式_______________;反应类型__________。
(3)炒菜时加入一些料酒和食醋,可使饭菜变得味香、可口的原因,化学方程式_______________;反应类型为酯化反应。
(4)由乙烯合成高分子化合物,化学方程式_______________;反应类型__________。
17.按要求填空
(1) 的名称为___________。
(2) 的名称为___________。
(3)1,3-二甲基-2-乙基苯 ___________。
(4) 1mol该物质最多能与___________molBr2发生反应,最多能与___________molNaOH发生反应
18.B()有多种同分异构体,同时满足下列条件的同分异构体有___________种(不考虑立体异构)
①苯环上有2个取代基 ②能够发生银镜反应 ③与溶液发生显色发应
其中核磁共振氢谱有五组峰,且峰面积之比为6:2:2:1:1的结构简式为___________;
三、实验题
19.实验室制取乙烯的装置如图所示,请回答:
(1)反应中浓硫酸起_______剂和_______剂的作用。
(2)该实验可能产生的主要有机副产物是_______。(写名称)
(3)制取乙烯的反应的化学方程式是:_______。
20.某化学活动小组设计以下装置进行不同的实验。其中a为用于鼓入空气的气囊,b为螺旋状铜丝,c中盛有冰水。
(1)若用A装置做乙醇与乙酸的酯化反应实验,则还需连接的装置是___(填序号),该实验的反应原理是____。从实验安全角度考虑,A装置试管中除加入反应液外,还需加入固体物质,其目的是_____。
(2)该小组同学欲做乙醇氧化成乙醛的实验,则应选用的装置是____(填序号),再用制得的乙醛溶液进行银镜反应,正确的操作顺序是_____(填序号)。
①向试管中滴入3滴乙醛溶液
②一边振荡一边滴入2%的稀氨水,直至最初产生的沉淀恰好溶解为止
③振荡后放入热水中,水浴加热
④在洁净的试管中加入1mL2%的AgNO3溶液
银镜反应的化学反应方程式是______。
21.桂酸乙酯(3-苯基丙烯酸乙酯)能混溶于乙醇、乙醚,几乎不溶于甘油和水。实验室以肉桂酸( )为主要原料制取肉桂酸乙酯的实验装置如图所示。
已知:
物质 肉桂酸 肉桂酸乙酯 乙醇 环己烷 环己烷、乙醇和水形成的三元共沸物
沸点/℃(101kPa) 300 271.5 78.3 80.8 62.6
三元共沸物是指在恒定压力下沸腾时,其组分与沸点均保持不变的三组分液体混合物。
实验包含以下“步骤”:
①加料。操作甲后向装置M的圆底烧瓶中依次加入3.0g肉桂酸、15mL乙醇、15mL环己烷、1mL浓硫酸,连接装置。
②蒸馏。用无水氯化钙干燥至有机层澄清透明,过滤后转移入干燥的蒸馏装置,40℃水浴蒸馏蒸出乙醚。
③蒸馏。改为装置N,蒸馏出过量的乙醇和环己烷。
④中和。反应液稍冷后倒入盛有80mL水的烧杯中,分批加入固体碳酸钠,至溶液呈中性。
⑤分水回流。水浴回流约2-3h,当b(分水器)中下层液面接近其支管时进行操作乙,待下层共收集约3mL液体时停止加热。
⑥分液。液体转移至分液漏斗,静置片刻后分出有机层。水层用24mL乙醚分三次萃取,然后合并有机层。
⑦蒸馏。减压蒸馏,得粗产物。
回答下列问题:
(1)上述“步骤”正确的操作顺序是①___________⑦。
(2)写出制取肉桂酸乙酯的化学方程式___________。
(3)仪器a的名称为___________;实验中加入环己烷的作用是___________。
(4)操作甲是___________;操作乙是___________。
(5)用装置N(不考虑加热及夹持装置等)进行上述步骤③的操作,错误共有___________(填标号)。
A.2处 B.3处 C.4处 D.5处
(6)将粗产物进一步精馏干燥后,得到纯净产物2.2g,则肉桂酸乙酯的产率为___________%(保留三位有效数字)。
四、计算题
22.酒精溶液在抗击COVID-19中发挥了极为重要的作用,现有xg乙醇(C2H5OH)在一定量氧气中燃烧生成13.2gCO2、10.8gH2O及ygCO。回答下列问题:
(1)医用消毒酒精溶液的常用浓度(体积分数)是___________。
(2)生成物中CO2、H2O的分子个数比为___________,y=___________,写出该燃烧反应的化学方程式:___________。
(3)若使该乙醇完全燃烧,至少还需要___________LO2(标准状况)。
试卷第4页,共7页
参考答案:
1.A
【详解】A.乙醇和乙酸的酯化反应,酯化反应又是取代反应,A正确;
B.乙醇的催化氧化反应,属于氧化反应,B错误;
C.乙烯和溴化氢加成生成溴乙烷,属于加成反应,C错误;
D.乙烯能通过自身加聚反应生成聚乙烯,属于加聚反应,D错误;
故选A。
2.D
【详解】A.煤油是石油分馏的产品,主要成分仍为烃类物质,故A错误;
B.汽油是石油分馏的产品,主要成分仍为烃类物质,故B错误;
C.柴油是石油分馏的产品,主要成分仍为烃类物质,故C错误;
D.甘油是丙三醇,为醇类物质,故D正确;
故选D。
3.C
【分析】柠檬酸有3个羧基和1个醇羟基。
【详解】A.根据结构简式可知柠檬酸的分子式是C6H8O,故A正确;
B.柠檬酸中有3个羧基和1个醇羟基,即有2种不同的含氧官能团,故B正确;
C.柠檬酸中有3个羧基,即1 mol柠檬酸能够和3 mol NaOH发生反应,故C错误;
D.柠檬酸中有羧基,具有酸性,可以用来清洗掉铁器表面的铁锈,故D正确;
故答案为C。
4.C
【详解】A.都与水互溶,故A错误;
B.乙酸能使石蕊试液变红,乙醇不能,故B错误;
C.都能与钠反应,生成氢气,故C正确;
D.乙酸和乙醇能发生酯化反应,故D错误;
答案选C。
5.D
【详解】A.医用酒精中乙醇的体积分数为75%,故A错误;
B.生产N95口罩的“熔喷布”主要原料聚丙烯,聚丙烯不含碳碳双键,因此不能使酸性高锰酸钾溶液褪色,故B错误;
C.聚氯乙烯塑料制品有毒,不可用于食品包装,故C错误;
D.与NaOH溶液反应得到十二烷基苯磺酸钠和水,十二烷基苯磺酸钠是洗衣粉的主要成分之一,故D正确。
综上所述,答案为D。
6.C
【详解】A.苯与溴水不反应,苯、液溴、铁粉混合制成溴苯,故A错误;
B.三溴苯酚溶于苯中,加浓溴水与苯酚反应生成三溴苯酚,三溴苯酚与苯互溶,苯中引入新的杂质,故B错误;
C.乙烯能够被高锰酸钾酸性溶液氧化,使高锰酸钾酸性溶液褪色,而甲烷不能,可以用高锰酸钾酸性溶液来区别甲烷和乙烯,故C正确;
D.乙醇与水互溶,在分液漏斗中不分层,所以不能用分液漏斗分离乙醇和水,故D错误;
故选C。
7.A
【详解】A.该分子的结构简式为:,可知分子中含有4个甲基,A项正确;
B.将连有四个不同的原子或原子团的碳原子称为手性碳原子,如图所示,,可知分子中含有4个手性碳原子,B项错误;
C.根据结构图,可知分子式为C13H24O3,C项错误;
D.分子中含有羟基,能够被酸性高锰酸钾溶液氧化,所以能使酸性高锰酸钾溶液褪色,D项错误;
答案选A。
8.A
【详解】A.饱和碳酸氢钠溶液可吸收HCl并产生二氧化碳,符合除杂目的,A符合题意;
B.酸性高锰酸钾可将乙烯氧化,同时会产生,引入了新杂质,B项不符合题意;
C.乙酸乙酯中加入氢氧化钠溶液可除去乙酸,但同时乙酸乙酯在碱性条件下也会水解,C项不符合题意;
D.过量铁粉会将铁离子还原为亚铁离子,除杂试剂选用错误,D项不符合题意。
故选A。
9.B
【详解】A. 甲烷的燃烧反应属于氧化反应,不属于加成反应,故A不符合;
B. 具有双键的乙烯与氯化氢发生反应,生成饱和有机物氯乙烷,属于加成反应,故B符合;
C. 苯与液溴发生取代反应,故C不符合;
D. 乙醇与乙酸反应,生成乙酸乙酯和水,为酯化反应,也属于取代反应,不属于加成反应,故D不符合;
故选B。
10.D
【详解】A.CH4+Cl2CH3Cl+HCl表示甲烷和氯气的取代反应,故A不选;
B.CH2=CH2+Br2→CH2Br—CH2Br表示乙烯和溴单质的加成反应,故B不选;
C.CH3CH2OH+3O22CO2+3H2O表示乙醇的氧化反应,故C不选;
D.CH3COOH+C2H5OHCH3COOC2H5+H2O表示乙醇和乙酸的酯化反应,故D选;
正确答案是D。
11.C
【详解】A.由题干信息可知,反应1是CH2=CH2+H2OCH3CH2OH,属于加成反应,A正确;
B.由题干信息可知,反应2为2CH3CH2OH+O22CH3CHO+2H2O,故反应中每生成1mol乙醛,转移2mol电子,B正确;
C.由于醛基和碳碳双键均能使酸性高锰酸钾褪色,故检验反应3的生成物中含有碳碳双键,仅用酸性KMnO4溶液无法完成,可以仅用溴的四氯化碳溶液,C错误;
D.正丁醇即1-丁醇的同分异构体中除了其自身外属于醇有:2-丁醇CH3CH2CH(OH)CH3、2-甲基-1-丙醇(CH3)2CHCH2OH、2-甲基-2-丙醇(CH3)3COH等3种,D正确;
故答案为:C。
12.D
【详解】A.内能是体系内部能量的总和,与温度、体积、质量、状态等因素有关,A错误;
B.液体与固体反应生成气体,体系混乱程度增大,属于熵增过程,即△S>0,B错误;
C.由所给数据知,CH3COOH溶液中已经电离出的H+恰好将NaOH中和,而原醋酸溶液中大量CH3COOH未电离,故反应后,溶液中剩余大量醋酸,溶液显酸性,C错误;
D.丙酮中羰基氧与水分子中氢原子之间能形成分子间氢键,故丙酮与水互溶,D正确;
故答案选D。
13.A
【分析】该实验的原理为在铜的催化作用下,乙醇被氧气氧化成乙醛,乙醛可能继续被氧化成乙酸。甲烧杯内是高于乙醇沸点的热水,目的是使乙醇汽化,然后和氧气按照一定体积比混合,在硬质玻璃管中,铜被氧化成黑色CuO,CuO被乙醇还原成Cu,总体上铜作催化剂,降低了乙醇被氧气氧化成乙醛的活化能。反应生成的乙醛(可能含有乙酸及未被氧化的乙醇)进入置于乙烧杯冷水中的试管a中被冷凝,得到含有乙醛、可能含有乙酸及未被氧化的乙醇的溶液,乙酸和活泼金属Zn能反应;
【详解】A.甲烧杯内是高于乙醇沸点的热水,乙烧杯冷水,选项A错误;
B.铜网降低了乙醇和氧气反应的活化能,选项B正确;
C.反应生成的乙醛,可能含有乙酸,进入置于乙烧杯冷水中的试管a中可能使锌粒溶解,选项C正确;
D.铜被氧化成黑色CuO,CuO被乙醇还原成Cu,出现红色和黑色交替现象,选项D正确;
答案选A。
14.B
【详解】A.苯与氢气在催化剂、加热条件下发生加成反应,苯与液溴在FeBr3作用下发生取代反应,甲、乙两组有机反应类型不相同,故A不选;
B.乙醇和钠发生置换反应生成氢气,丙烯酸(CH2=CHCOOH)与乙醇在浓硫酸、加热条件下发生取代(酯化)反应,甲、乙两组有机反应类型相同,故B选;
C.乙醇与氧气在铜和加热条件下发生催化氧化反应,丙烯(CH3CH=CH2)与溴的四氯化碳溶液发生加成反应,甲、乙两组有机反应类型不相同,故C不选;
D.在酸性KMnO4溶液中滴加乙醇发生氧化反应,在光照条件下甲烷与氯气发生取代反应,甲、乙两组有机反应类型不相同,故D不选;
故选B。
15.D
【详解】A.苯与液溴在铁作催化剂发生取代反应:+Br2+HBr,该反应为放热反应,产生的HBr气体中混有Br2蒸气,Br2蒸气溶于硝酸银溶液中也产生淡黄色沉淀AgBr,对HBr的检验产生干扰,题中缺少除去Br2蒸气的装置,HBr极易溶于水,题中缺少防倒吸装置,故A错误;
B.乙醇发生消去反应:CH3CH2OHCH2=CH2↑+H2O,浓硫酸具有脱水性,将酒精脱水炭化,产生的碳单质与浓硫酸反应生成CO2、SO2,产生的乙烯中混有SO2和挥发出的乙醇,SO2和乙醇也能使酸性高锰酸钾溶液褪色,题中缺少除去SO2和乙醇的装置,故B错误;
C.浓盐酸具有挥发性,烧瓶中产生CO2中混有HCl(g),HCl(g)也能与苯酚钠反应产生苯酚,对碳酸、苯酚酸性强弱对比产生干扰,题中缺少除去CO2中HCl(g)的操作,故C错误;
D.乙酸和乙醇发生酯化反应CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O,乙醇、乙酸、乙酸乙酯蒸气在冷凝管中遇冷,回流到三口烧瓶中,增加乙酸、乙醇的利用率,提高乙酸乙酯的产率,同时利用分水器可以做到乙酸乙酯与水的分离,故D正确;
答案为D。
16.(1) CH2=CH2+H2O→CH3-CH2OH 加成反应
(2) 取代反应
(3)CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O
(4) nCH2=CH2→; 加聚反应
【详解】(1)乙烯与水发生加成反应生成乙醇,化学方程式为:CH2=CH2+H2O→CH3-CH2OH;故答案为CH2=CH2+H2O→CH3-CH2OH;加成反应。
(2)苯与硝酸在浓硫酸、加热条件下发生取代反应,生成硝基苯,化学方程式为:;故答案为;取代反应。
(3)乙酸和乙醇在一定条件下发生酯化反应,化学方程式为:CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O;故答案为CH3CH2OH+CH3COOHCH3COOCH2CH3+H2O。
(4)乙烯在一定条件下发生加聚反应生成聚乙烯,化学方程式为:
nCH2=CH2→;故答案为nCH2=CH2→;加聚反应。
17. 3,3-二甲基-2-丁醇 2 -甲基 -1,3 -丁二烯 3 4
【详解】(1)该物质中含有羟基,属于醇,与羟基相连的最长碳链上有4个碳,从靠近羟基的一端编号,2号碳上有羟基,3号碳上有两个甲基,所以名称为3,3-二甲基-2-丁醇;
(2)该物质中含有两个碳碳双键,属于二烯烃,双键所在最长碳链有4个碳,由于双键位于主链两端,所以从靠近支链的一端开始编号,1、3号碳上有双键,2号碳上有一个甲基,所以名称为2 甲基 1,3 丁二烯;
(3)1,3-二甲基-2-乙基苯的母体为苯,任取苯环上一个碳原子开始编号,1、3号碳上各有一个甲基,2号碳上有一个乙基,所以结构简式为;
(4)碳碳双键可以和溴发生加成反应,酚羟基的邻、对位有空位,可以发生取代反应,所以1mol该物质最多能与3molBr2发生反应;酚羟基、两个酯基水解生成的羧基可以和NaOH反应,其中一个酯基水解后还生成酚羟基,也能与NaOH反应,所以1mol该物质最多与4molNaOH发生反应。
18. 15
【详解】的同分异构体满足:①能发生银镜反应,说明结构中存在醛基,②与FeCl3溶液发生显色发应,说明含有酚羟基,同时满足苯环上有2个取代基,酚羟基需占据苯环上的1个取代位置,支链上苯环连接方式(红色点标记):、 共五种,因此一共有5×3=15种结构;其中核磁共振氢谱有五组峰,因酚羟基和醛基均无对称结构,因此峰面积之比为6:2:2:1:1的结构简式一定具有对称性(否则苯环上的氢原子不等效),即苯环上取代基位于对位,核磁共振氢谱中峰面积比为6的氢原子位于与同一碳原子相连的两个甲基上,因此该同分异构的结构简式为。
19.(1) 催化 脱水
(2)乙醚
(3)CH3CH2OHCH2=CH2↑+H2O
【分析】乙醇在浓硫酸做作催化剂和脱水剂条件下迅速加热到170℃发生消去反应生成乙烯,反应方程式为: CH3CH2OHCH2=CH2↑+H2O,实验应注意温度应控制在170℃,在140℃时容易发生副反应生成乙醚, 据此分析解答。
【详解】(1)乙醇在浓硫酸做催化剂和脱水剂条件下发生消去反应生成乙烯;因此浓硫酸在该反应中的作用是脱水剂和催化剂;
(2)实验室制备乙烯反应温度应控制在170℃,若反应温度在140℃,会发生乙醇分子之间的取代反应产生有机副产物乙醚;
(3)乙醇在浓硫酸作催化剂和脱水剂条件下迅速加热到170℃,乙醇会发生消去反应生成乙烯,该反应的化学方程式为:CH3CH2OH CH2=CH2↑+H2O。
。
20. D CH3COOH+C2H5OHCH3COOC2H5+H2O 防止暴沸 ABC ④②①③ CH3CHO+2Ag(NH3)2OHCH3COONH4+3NH3↑+2Ag↓+H2O
【分析】若用A装置做乙醇与乙酸的酯化反应实验,需要连接D装置吸收乙醇,中和乙酸,降低乙酸乙酯溶解度,防止倒吸,A装置液体加热沸腾需要加入碎瓷片或沸石防止暴沸,以此解答。
【详解】(1)若用A装置做乙醇与乙酸的酯化反应实验,需要连接D装置,该实验的反应原理是:CH3COOH+C2H5OHCH3COOC2H5+H2O;A装置液体加热沸腾需要加入碎瓷片或沸石防止暴沸,故答案为:D;CH3COOH+C2H5OHCH3COOC2H5+H2O;防止暴沸;
(2)做乙醇氧化成乙醛的实验,需要提供乙醇蒸气和氧气在催化剂作用下氧化反应生成乙醛,反应的化学方程式为:2CH3CH2OH+O22CH3CHO+2H2O,冷却得到液体乙醛,装置连接为A、B、C;乙醛溶液进行银镜反应,先制取银氨溶液,向硝酸银溶液中滴入氨水至变色沉淀全部溶解得到银氨溶液,滴入乙醛溶液在水浴中加热反应观察银镜现象,实验顺序是④②①③,银镜反应的化学反应方程式是:CH3CHO+2Ag(NH3)2OHCH3COONH4+3NH3+2Ag↓+H2O,故答案为:ABC;④②①③;CH3CHO+2Ag(NH3)2OHCH3COONH4+3NH3↑+2Ag↓+H2O。
21.(1)⑤③④⑥②
(2)
(3) 球形冷凝管 形成共沸物,将产物水带出,使得平衡正向移动,提高产率
(4) 检查装置的气密性 打开分水器下端的活塞,使下层的水放出到量筒中
(5)B
(6)61.7
【分析】酸和醇在浓硫酸催化作用下生成酯,反应后得到酯蒸馏除去过量的乙醇和环己烷,加入碳酸钠除去酸,分液、萃取分液分离出有机层后,再次蒸馏得到粗品;
【详解】(1)根据分析可知,实验的过程为:①加料,并连接装置;⑤分水回流,制取得到酯;③蒸馏,利用物质沸点不同蒸馏出过量的乙醇和环己烷;④中和,加入碳酸钠固体除去酸;⑥分液,分离出有机层;②蒸馏,除去萃取剂乙醚;⑦减压蒸馏,得粗产物;故正确的操作顺序是①⑤③④⑥②⑦;
(2)肉桂酸和乙醇加热在浓硫酸催化作用下生成肉桂酸乙酯:;
(3)仪器a的名称为球形冷凝管;环己烷沸点较低,实验中加入环己烷的作用是形成共沸物,将产物水带出,使得平衡正向移动,提高产率;
(4)反应中涉及蒸馏回流操作,需要较好的装置气密性,故操作甲是检查装置的气密性;当b(分水器)中下层液面接近其支管时,需要排出其下层过量的水,保留上层的馏分,故操作乙是打开分水器下端的活塞,使下层的水放出到量筒中;
(5)蒸馏时温度计应该在支管口处;冷凝水应该下进上出;承接馏分的装置应该为敞口装置,使得馏分顺利滴下;故共3处错误,故选B;
(6)3.0g肉桂酸为,则理论生成肉桂酸乙酯的质量为,故肉桂酸乙酯的产率为。
22. 75% 1:2 2.8 1.12
【详解】(1)医用消毒酒精溶液的常用浓度(体积分数)是75%,低于75%消毒效果不理想,浓度太大会使蛋白质表面形成硬膜,阻止乙醇分子破坏病毒内部蛋白质,无法杀死病毒;
(2) xg乙醇(C2H5OH)在一定量氧气中燃烧生成13.2gCO2、10.8gH2O及ygCO,13.2gCO2的物质的量为=0.3mol,10.8gH2O的物质的量为=0.6mol,因此生成物中CO2、H2O的分子个数比为0.3:0.6=1:2,0.6molH2O中含有1.2molH,1mol C2H5OH含有6molH,则含1.2molH的乙醇的物质的量为=0.2mol,含碳原子的物质的量为0.4mol,根据碳原子守恒,反应生成的一氧化碳的物质的量为0.1mol,其质量y=0.1molx28g/mol=2.8g;该反应中C2H5OH、CO2、CO、H2O的物质的量之比为0.2:0.3:0.1:0.6=2:3:1:6,则反应的化学方程式:;
(3)一氧化碳燃烧的化学方程式为:2CO+O22CO2,由此可知,0.1mol的CO完全燃烧需要消耗0.05molO2,则这些氧气标况下的体积为0.05molx22.4L/mol=1.12L,则使该乙醇完全燃烧,至少还需要1.12LO2(标准状况)
