2.2.2 氯气的实验室制法 教学设计 2023-2024学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 2.2.2 氯气的实验室制法 教学设计 2023-2024学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 645.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-06 00:00:00 | ||
图片预览



文档简介
《氯气的实验室制法》教学设计
课程基本信息
学科 化学 年级 高一 课型 新授课 课时 40min
课题 氯气的实验室制法
教材 化学必修第一册 第二章 第二节 氯及其化合物(第三课时)
教学目标
教 学 目 标 通过阅读氯气的发现史,感受科学家的探究精神,培养学生科学态度与社会责任的化学学科核心素养。 通过实验室制备氯气实验装置的选择,掌握实验室气体制备装置的选择原则和方案设计,能够根据实验室气体制备的实验原理选择合适的实验装置,培养学生科学探究与创新意识的化学学科核心素养。 通过归纳实验室气体制备装置的连接顺序和选择原则,建立实验室气体制备装置的思维模型,培养学生证据推理与模型认知的化学学科核心素养。
评 价 目 标 通过让学生阅读氯气发现史并写出舍勒发现氯气的化学方程式,诊断学生对氧化还原反应相关知识的掌握情况。 通过让学生小组合作选择实验室制备氯气各部分装置,诊断学生分析解决问题的能力。 通过让学生小组合作根据高锰酸钾和浓盐酸反应制备氯气的原理,选择并拼接出合适的实验装置,诊断学生对实验室气体制备装置思维模型的掌握情况。
教学内容分析
课 标 分 析 《普通高中化学课程标准(2017年版2020年修订)》,在《主题1:化学科学与实验探究》和《主题2:常见无机物及其应用》中都提到了氯气的实验室制法的相关要求,可以总结为以下两点: 理解并掌握氯气的实验室制法。 能根据反应原理选取装置制取物质。
教 材 分 析 这部分是教材新增加的内容。初中已经学过O2、CO2、H2等气体的实验室制法,氯气的制法是在这些气体制备的基础上引入的。教材中引入了实验室制取气体的装置的设计的方法导引,使学生在原来气体的制备装置的选择上认识更加系统和全面。 本部分内容难度不大,但是知识的应用很广泛。实验题中气体的制备、性质检验是高考的高频考点,因此氯气的实验室制法的学习为后面其他气体的制法的学习奠定了基础。
教学 重难点 重点:氯气的实验室制备装置的分析和选择 难点:实验室气体制备装置的思维模型
学 情 分 析 学生在初中学过实验室制备O2、CO2、H2 等气体,对氯气的物理性质和化学性质也有比较完整的认识,已经具备定的实验基本操作和实验设计的能力。 但还未建立实验室制取气体的基本思维模型,综合运用所学知识进行原理分析、实验设计的能力不足,全面分析、解决实验过程中可能出现的问题存在困难。
教学方法
教学 方法 讲授法、实验法、讨论法、合作探究法
教学 用具 多媒体课件、导学案、实验装置卡片(自制)、实验仪器、黑板等
教学过程
新 课 导 入 资料1:1774年,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。直到1810年,英国化学家戴维确认这种黄绿色气体是一种新元素组成的单质——氯气。 [学生活动] 阅读氯气发现史,感受科学家的探究精神。
环节一:探究氯气实验室制备的原理 【活动1】探究氯气实验室制备的原理 [学生活动] 根据舍勒发现氯气的史料和氧化还原反应的知识,写出产生氯气的化学方程式(已知:在该反应中MnO2被还原为MnCl2)。找出方程式中的氧化剂、还原剂、氧化产物和还原产物。 [教师活动] 引导学生思考,组织学生交流,对学生的学习成果进行评价。
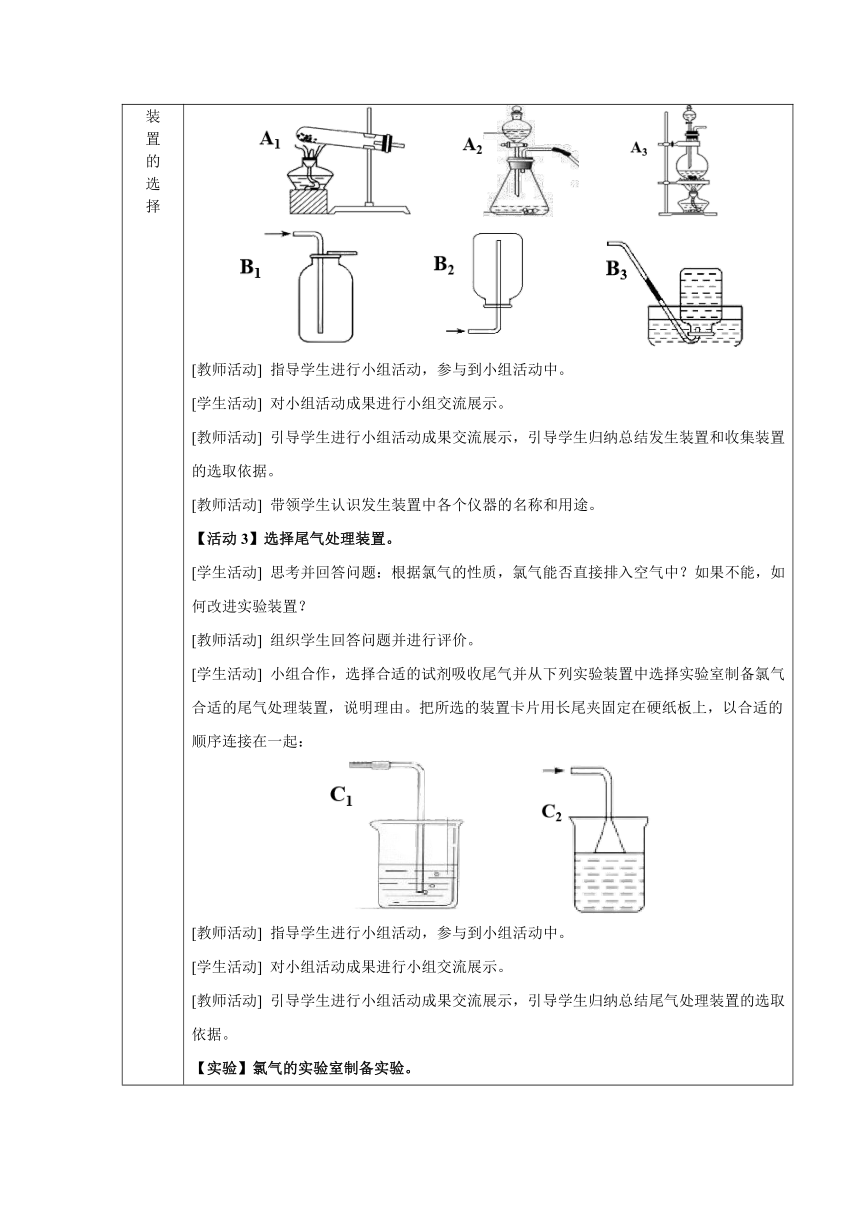
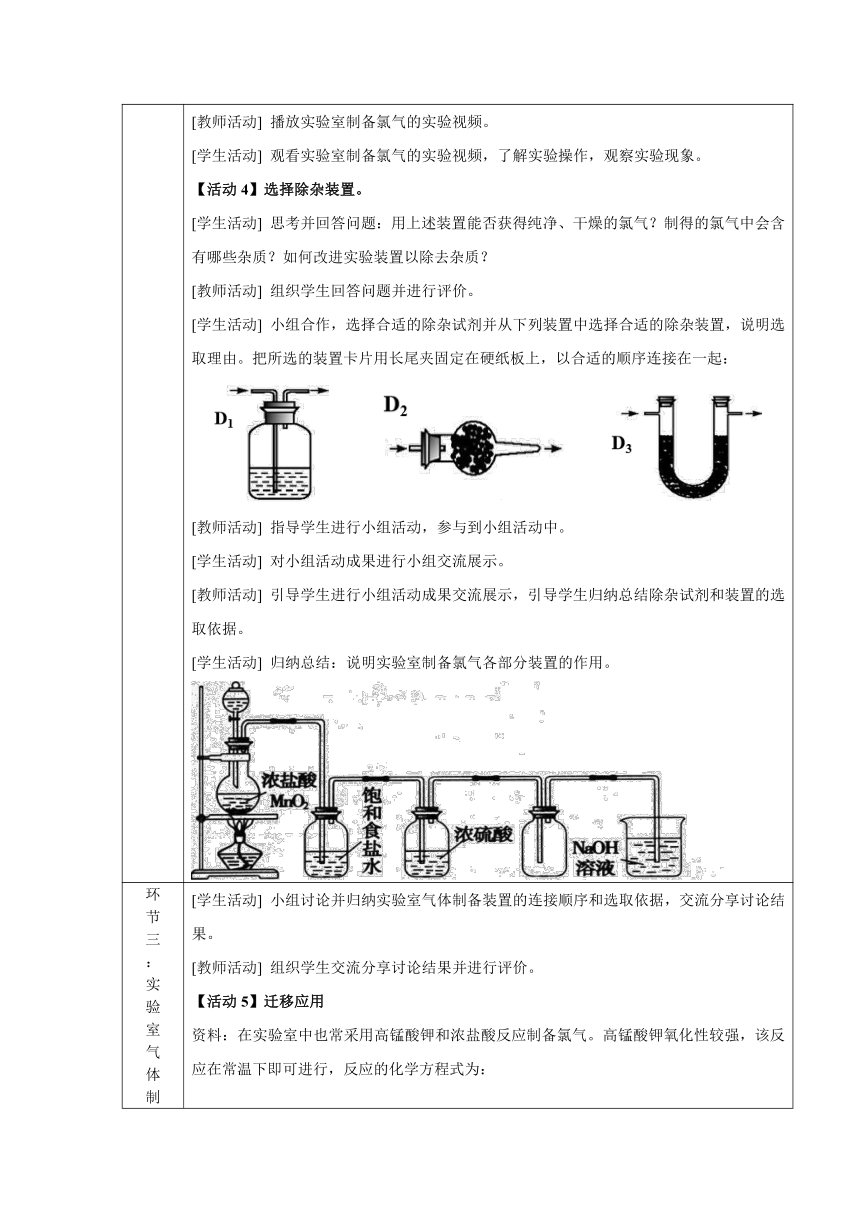
环 节 二 : 实 验 室 制 备 氯 气 装 置 的 选 择 结合初中所学的O2、CO2等气体的实验室制备原理和装置图,依据实验室制备氯气的原理,选择合适的实验室制备氯气的实验装置。 【活动2】选择发生装置和收集装置。 [学生活动] 小组合作从下列实验装置中选择实验室制备氯气合适的发生装置和收集装置。把所选装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起,并说明选择的理由: [教师活动] 指导学生进行小组活动,参与到小组活动中。 [学生活动] 对小组活动成果进行小组交流展示。 [教师活动] 引导学生进行小组活动成果交流展示,引导学生归纳总结发生装置和收集装置的选取依据。 [教师活动] 带领学生认识发生装置中各个仪器的名称和用途。 【活动3】选择尾气处理装置。 [学生活动] 思考并回答问题:根据氯气的性质,氯气能否直接排入空气中?如果不能,如何改进实验装置? [教师活动] 组织学生回答问题并进行评价。 [学生活动] 小组合作,选择合适的试剂吸收尾气并从下列实验装置中选择实验室制备氯气合适的尾气处理装置,说明理由。把所选的装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起: [教师活动] 指导学生进行小组活动,参与到小组活动中。 [学生活动] 对小组活动成果进行小组交流展示。 [教师活动] 引导学生进行小组活动成果交流展示,引导学生归纳总结尾气处理装置的选取依据。 【实验】氯气的实验室制备实验。 [教师活动] 播放实验室制备氯气的实验视频。 [学生活动] 观看实验室制备氯气的实验视频,了解实验操作,观察实验现象。 【活动4】选择除杂装置。 [学生活动] 思考并回答问题:用上述装置能否获得纯净、干燥的氯气?制得的氯气中会含有哪些杂质?如何改进实验装置以除去杂质? [教师活动] 组织学生回答问题并进行评价。 [学生活动] 小组合作,选择合适的除杂试剂并从下列装置中选择合适的除杂装置,说明选取理由。把所选的装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起: [教师活动] 指导学生进行小组活动,参与到小组活动中。 [学生活动] 对小组活动成果进行小组交流展示。 [教师活动] 引导学生进行小组活动成果交流展示,引导学生归纳总结除杂试剂和装置的选取依据。 [学生活动] 归纳总结:说明实验室制备氯气各部分装置的作用。
环 节 三 : 实 验 室 气 体 制 备 装 置 的 思 维 模 型 [学生活动] 小组讨论并归纳实验室气体制备装置的连接顺序和选取依据,交流分享讨论结果。 [教师活动] 组织学生交流分享讨论结果并进行评价。 【活动5】迁移应用 资料:在实验室中也常采用高锰酸钾和浓盐酸反应制备氯气。高锰酸钾氧化性较强,该反应在常温下即可进行,反应的化学方程式为: 2KMnO4 + 16HCl(浓)== 2MnCl2 + 2KCl + 5Cl2 ↑ + 8H2O [学生活动] 小组合作,依据以上反应原理,选择并拼接出合适的实验装置。 [教师活动] 指导学生进行小组活动,参与到小组活动中。 [学生活动] 对小组活动成果进行小组交流展示。 [教师活动] 引导学生进行小组活动成果交流展示,并进行分析评价。
课 堂 小 结 氯气的实验室制法 1.制备原理: 2.实验装置:发生装置→除杂装置→收集装置→尾气处理装置
课 堂 检 测 1.二氧化锰跟浓盐酸反应制备干燥纯净的氯气。 (1)连接上述仪器的正确顺序(填各接口处的字母):___接___;___接___;___接___;___接___。 (2)装置中,饱和食盐水的作用是____________;NaOH溶液的作用是_______________。 (3)写出下列化学反应的化学方程式: ①气体发生装置中:________________________________________________。 ②NaOH溶液中:__________________________________________________。 参考答案: E; C; D; A; B; H; G; F 除Cl2中的HCl;吸收过量的氯气。 MnO2+4HCl(浓) == MnCl2+Cl2↑ + 2H2O; 2NaOH+Cl2 = NaCl+NaClO+H2O
板书设计
2.2.1 氯气的实验室制法 1.制备原理: 2.实验装置:发生装置→除杂装置→收集装置→尾气处理装置
作业布置
完成学习任务单上的作业练习。
《氯气的实验室制法》学习任务单
课程基本信息
学科 化学 年级 高一 课型 新授课 课时 40min
课题 氯气的实验室制法
教材 化学必修第一册 第二章 第二节 氯及其化合物(第三课时)
教学目标
教 学 目 标 通过阅读氯气的发现史,感受科学家的探究精神,培养学生科学态度与社会责任的化学学科核心素养。 通过实验室制备氯气实验装置的选择,掌握实验室气体制备装置的选择原则和方案设计,能够根据实验室气体制备的实验原理选择合适的实验装置,培养学生科学探究与创新意识的化学学科核心素养。 通过归纳实验室气体制备装置的连接顺序和选择原则,建立实验室气体制备装置的思维模型,培养学生证据推理与模型认知的化学学科核心素养。
评 价 目 标 通过让学生阅读氯气发现史并写出舍勒发现氯气的化学方程式,检验学生对氧化还原反应相关知识的掌握情况。 通过让学生小组合作选择实验室制备氯气各部分装置,检验学生分析解决问题的能力。 通过让学生小组合作根据高锰酸钾和浓盐酸反应制备氯气的原理,选择并拼接出合适的实验装置,检验学生对实验室气体制备装置思维模型的掌握情况。
学习任务
任 务 一: 探 究 氯 气 实 验 室 制 备 的 原 理 资料1:1774年,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。直到1810年,英国化学家戴维确认这种黄绿色气体是一种新元素组成的单质——氯气。 【活动1】试根据舍勒发现氯气的史料和氧化还原反应的知识,写出产生氯气的化学方程式(已知:在该反应中MnO2被还原为MnCl2): 在该反应中,氧化剂是 ,还原剂是 ;氧化产物是 ,还原产物是 。浓盐酸在该反应中表现出了哪些性质 。
任 务 二 : 实 验 室 制 备 氯 气 装 置 的 选 择 结合初中所学的O2、CO2等气体的实验室制备原理和装置图,依据实验室制备氯气的原理,选择合适的实验室制备氯气的实验装置。 【活动2】发生装置和收集装置的选择。小组合作从下列实验装置中选择实验室制备氯气合适的发生装置和收集装置。把所选的装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起: 你们小组选择的发生装置是 ,选择此装置的原因 。 你们小组选择的收集装置是 ,选择此装置的原因 。 【思考】根据氯气的性质,氯气能否直接排入空气中?如果不能,如何改进实验装置? 【活动3】尾气处理装置的选择。小组合作,选择合适的试剂吸收尾气并从下列实验装置中选择实验室制备氯气合适的尾气处理装置,说明理由。把所选的装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起: 你们小组使用 试剂吸收尾气,选择的尾气处理装置是 ,选择以上试剂和装置的原因 。 【思考】用上述装置能否获得纯净、干燥的氯气? 制得的氯气中会含有哪些杂质?如何改进实验装置以除去杂质? 资料2:(1)氯化氢极易溶于水,氯气在饱和食盐水中溶解度较小。(2)常见干燥剂:浓硫酸、碱石灰、NaOH(S)、CaO、无水CaCl2 等。 【活动4】除杂装置的选择。小组合作,选择合适的除杂试剂并从下列装置中选择合适的除杂装置。把所选的装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起: 杂质① (填杂质名称或化学式)用 试剂除去,选用的装置为 ,选择以上试剂和装置的原因 。 杂质② (填杂质名称或化学式)用 试剂除去,选用的装置为 ,选择以上试剂和装置的原因 。
任 务 三 : 实 验 室 气 体 制 备 装 置 的 思 维 模 型 【归纳】实验室气体制备装置的连接顺序和选取依据: 连接顺序 选取依据 【活动5】迁移应用:在实验室中也常采用高锰酸钾和浓盐酸反应制备氯气。高锰酸钾氧化性较强,该反应在常温下即可进行,反应的化学方程式为: 2KMnO4 + 16HCl(浓)== 2MnCl2 + 2KCl + 5Cl2 ↑ + 8H2O 请小组合作,依据以上反应原理,选择并拼接合适的实验装置。
课 堂 检 测 1.二氧化锰跟浓盐酸反应制备干燥纯净的氯气。 (1)连接上述仪器的正确顺序(填各接口处的字母):___接___;___接___;___接___;___接___。 (2)装置中,饱和食盐水的作用是____________;NaOH溶液的作用是_______________。 (3)写出下列化学反应的化学方程式: ①气体发生装置中:________________________________________________。 ②NaOH溶液中:__________________________________________________。
作业练习
1.一个国家的氯产量常被看做是化学工业发展水平的重要标志。实验室制取氯气的原理或装置不能达到实验目的的是 A.用装置甲制备氯气 B.用装置乙除去Cl2中的HCl气体 C.用装置丙干燥氯气 D.用装置丁吸收多余的氯气 2.实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气设计了如下实验装置: 仪器X的名称为 A.分液漏斗 B.圆底烧瓶 C.蒸馏烧瓶 D.长颈漏斗 3.利用下列装置能达到实验目的的是 A.利用甲装置除去氯气中混有的少量HCl B.利用乙装置稀释浓硫酸 C.利用丙装置进行喷泉实验 D.利用丁装置进行蒸发结晶 4.实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气,设计了如图实验装置。 请回答下列问题: 实验室制取Cl2的化学方程式为 。 向烧瓶里加入少量 粉末,分液漏斗中注入 。 A中盛放的是 ,其作用为 。 B中盛放的是 ,其作用为 。 D中盛放的是 ,其作用为 。
参 考 答 案 课堂检测: E; C; D; A; B; H; G; F 除Cl2中的HCl;吸收过量的氯气。 MnO2+4HCl(浓) == MnCl2+Cl2↑ + H2O; 2NaOH+Cl2 = NaCl+NaClO+H2O 作业练习: A A A 4.(1)MnO2+4HCl(浓) == MnCl2+Cl2↑ +2 H2O; (2)二氧化锰;浓盐酸。 (3)饱和食盐水;出去氯气中的氯化氢杂质。 (4)浓硫酸;干燥氯气。 (5)氢氧化钠溶液;吸收多余的氯气。
课程基本信息
学科 化学 年级 高一 课型 新授课 课时 40min
课题 氯气的实验室制法
教材 化学必修第一册 第二章 第二节 氯及其化合物(第三课时)
教学目标
教 学 目 标 通过阅读氯气的发现史,感受科学家的探究精神,培养学生科学态度与社会责任的化学学科核心素养。 通过实验室制备氯气实验装置的选择,掌握实验室气体制备装置的选择原则和方案设计,能够根据实验室气体制备的实验原理选择合适的实验装置,培养学生科学探究与创新意识的化学学科核心素养。 通过归纳实验室气体制备装置的连接顺序和选择原则,建立实验室气体制备装置的思维模型,培养学生证据推理与模型认知的化学学科核心素养。
评 价 目 标 通过让学生阅读氯气发现史并写出舍勒发现氯气的化学方程式,诊断学生对氧化还原反应相关知识的掌握情况。 通过让学生小组合作选择实验室制备氯气各部分装置,诊断学生分析解决问题的能力。 通过让学生小组合作根据高锰酸钾和浓盐酸反应制备氯气的原理,选择并拼接出合适的实验装置,诊断学生对实验室气体制备装置思维模型的掌握情况。
教学内容分析
课 标 分 析 《普通高中化学课程标准(2017年版2020年修订)》,在《主题1:化学科学与实验探究》和《主题2:常见无机物及其应用》中都提到了氯气的实验室制法的相关要求,可以总结为以下两点: 理解并掌握氯气的实验室制法。 能根据反应原理选取装置制取物质。
教 材 分 析 这部分是教材新增加的内容。初中已经学过O2、CO2、H2等气体的实验室制法,氯气的制法是在这些气体制备的基础上引入的。教材中引入了实验室制取气体的装置的设计的方法导引,使学生在原来气体的制备装置的选择上认识更加系统和全面。 本部分内容难度不大,但是知识的应用很广泛。实验题中气体的制备、性质检验是高考的高频考点,因此氯气的实验室制法的学习为后面其他气体的制法的学习奠定了基础。
教学 重难点 重点:氯气的实验室制备装置的分析和选择 难点:实验室气体制备装置的思维模型
学 情 分 析 学生在初中学过实验室制备O2、CO2、H2 等气体,对氯气的物理性质和化学性质也有比较完整的认识,已经具备定的实验基本操作和实验设计的能力。 但还未建立实验室制取气体的基本思维模型,综合运用所学知识进行原理分析、实验设计的能力不足,全面分析、解决实验过程中可能出现的问题存在困难。
教学方法
教学 方法 讲授法、实验法、讨论法、合作探究法
教学 用具 多媒体课件、导学案、实验装置卡片(自制)、实验仪器、黑板等
教学过程
新 课 导 入 资料1:1774年,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。直到1810年,英国化学家戴维确认这种黄绿色气体是一种新元素组成的单质——氯气。 [学生活动] 阅读氯气发现史,感受科学家的探究精神。
环节一:探究氯气实验室制备的原理 【活动1】探究氯气实验室制备的原理 [学生活动] 根据舍勒发现氯气的史料和氧化还原反应的知识,写出产生氯气的化学方程式(已知:在该反应中MnO2被还原为MnCl2)。找出方程式中的氧化剂、还原剂、氧化产物和还原产物。 [教师活动] 引导学生思考,组织学生交流,对学生的学习成果进行评价。
环 节 二 : 实 验 室 制 备 氯 气 装 置 的 选 择 结合初中所学的O2、CO2等气体的实验室制备原理和装置图,依据实验室制备氯气的原理,选择合适的实验室制备氯气的实验装置。 【活动2】选择发生装置和收集装置。 [学生活动] 小组合作从下列实验装置中选择实验室制备氯气合适的发生装置和收集装置。把所选装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起,并说明选择的理由: [教师活动] 指导学生进行小组活动,参与到小组活动中。 [学生活动] 对小组活动成果进行小组交流展示。 [教师活动] 引导学生进行小组活动成果交流展示,引导学生归纳总结发生装置和收集装置的选取依据。 [教师活动] 带领学生认识发生装置中各个仪器的名称和用途。 【活动3】选择尾气处理装置。 [学生活动] 思考并回答问题:根据氯气的性质,氯气能否直接排入空气中?如果不能,如何改进实验装置? [教师活动] 组织学生回答问题并进行评价。 [学生活动] 小组合作,选择合适的试剂吸收尾气并从下列实验装置中选择实验室制备氯气合适的尾气处理装置,说明理由。把所选的装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起: [教师活动] 指导学生进行小组活动,参与到小组活动中。 [学生活动] 对小组活动成果进行小组交流展示。 [教师活动] 引导学生进行小组活动成果交流展示,引导学生归纳总结尾气处理装置的选取依据。 【实验】氯气的实验室制备实验。 [教师活动] 播放实验室制备氯气的实验视频。 [学生活动] 观看实验室制备氯气的实验视频,了解实验操作,观察实验现象。 【活动4】选择除杂装置。 [学生活动] 思考并回答问题:用上述装置能否获得纯净、干燥的氯气?制得的氯气中会含有哪些杂质?如何改进实验装置以除去杂质? [教师活动] 组织学生回答问题并进行评价。 [学生活动] 小组合作,选择合适的除杂试剂并从下列装置中选择合适的除杂装置,说明选取理由。把所选的装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起: [教师活动] 指导学生进行小组活动,参与到小组活动中。 [学生活动] 对小组活动成果进行小组交流展示。 [教师活动] 引导学生进行小组活动成果交流展示,引导学生归纳总结除杂试剂和装置的选取依据。 [学生活动] 归纳总结:说明实验室制备氯气各部分装置的作用。
环 节 三 : 实 验 室 气 体 制 备 装 置 的 思 维 模 型 [学生活动] 小组讨论并归纳实验室气体制备装置的连接顺序和选取依据,交流分享讨论结果。 [教师活动] 组织学生交流分享讨论结果并进行评价。 【活动5】迁移应用 资料:在实验室中也常采用高锰酸钾和浓盐酸反应制备氯气。高锰酸钾氧化性较强,该反应在常温下即可进行,反应的化学方程式为: 2KMnO4 + 16HCl(浓)== 2MnCl2 + 2KCl + 5Cl2 ↑ + 8H2O [学生活动] 小组合作,依据以上反应原理,选择并拼接出合适的实验装置。 [教师活动] 指导学生进行小组活动,参与到小组活动中。 [学生活动] 对小组活动成果进行小组交流展示。 [教师活动] 引导学生进行小组活动成果交流展示,并进行分析评价。
课 堂 小 结 氯气的实验室制法 1.制备原理: 2.实验装置:发生装置→除杂装置→收集装置→尾气处理装置
课 堂 检 测 1.二氧化锰跟浓盐酸反应制备干燥纯净的氯气。 (1)连接上述仪器的正确顺序(填各接口处的字母):___接___;___接___;___接___;___接___。 (2)装置中,饱和食盐水的作用是____________;NaOH溶液的作用是_______________。 (3)写出下列化学反应的化学方程式: ①气体发生装置中:________________________________________________。 ②NaOH溶液中:__________________________________________________。 参考答案: E; C; D; A; B; H; G; F 除Cl2中的HCl;吸收过量的氯气。 MnO2+4HCl(浓) == MnCl2+Cl2↑ + 2H2O; 2NaOH+Cl2 = NaCl+NaClO+H2O
板书设计
2.2.1 氯气的实验室制法 1.制备原理: 2.实验装置:发生装置→除杂装置→收集装置→尾气处理装置
作业布置
完成学习任务单上的作业练习。
《氯气的实验室制法》学习任务单
课程基本信息
学科 化学 年级 高一 课型 新授课 课时 40min
课题 氯气的实验室制法
教材 化学必修第一册 第二章 第二节 氯及其化合物(第三课时)
教学目标
教 学 目 标 通过阅读氯气的发现史,感受科学家的探究精神,培养学生科学态度与社会责任的化学学科核心素养。 通过实验室制备氯气实验装置的选择,掌握实验室气体制备装置的选择原则和方案设计,能够根据实验室气体制备的实验原理选择合适的实验装置,培养学生科学探究与创新意识的化学学科核心素养。 通过归纳实验室气体制备装置的连接顺序和选择原则,建立实验室气体制备装置的思维模型,培养学生证据推理与模型认知的化学学科核心素养。
评 价 目 标 通过让学生阅读氯气发现史并写出舍勒发现氯气的化学方程式,检验学生对氧化还原反应相关知识的掌握情况。 通过让学生小组合作选择实验室制备氯气各部分装置,检验学生分析解决问题的能力。 通过让学生小组合作根据高锰酸钾和浓盐酸反应制备氯气的原理,选择并拼接出合适的实验装置,检验学生对实验室气体制备装置思维模型的掌握情况。
学习任务
任 务 一: 探 究 氯 气 实 验 室 制 备 的 原 理 资料1:1774年,瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。直到1810年,英国化学家戴维确认这种黄绿色气体是一种新元素组成的单质——氯气。 【活动1】试根据舍勒发现氯气的史料和氧化还原反应的知识,写出产生氯气的化学方程式(已知:在该反应中MnO2被还原为MnCl2): 在该反应中,氧化剂是 ,还原剂是 ;氧化产物是 ,还原产物是 。浓盐酸在该反应中表现出了哪些性质 。
任 务 二 : 实 验 室 制 备 氯 气 装 置 的 选 择 结合初中所学的O2、CO2等气体的实验室制备原理和装置图,依据实验室制备氯气的原理,选择合适的实验室制备氯气的实验装置。 【活动2】发生装置和收集装置的选择。小组合作从下列实验装置中选择实验室制备氯气合适的发生装置和收集装置。把所选的装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起: 你们小组选择的发生装置是 ,选择此装置的原因 。 你们小组选择的收集装置是 ,选择此装置的原因 。 【思考】根据氯气的性质,氯气能否直接排入空气中?如果不能,如何改进实验装置? 【活动3】尾气处理装置的选择。小组合作,选择合适的试剂吸收尾气并从下列实验装置中选择实验室制备氯气合适的尾气处理装置,说明理由。把所选的装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起: 你们小组使用 试剂吸收尾气,选择的尾气处理装置是 ,选择以上试剂和装置的原因 。 【思考】用上述装置能否获得纯净、干燥的氯气? 制得的氯气中会含有哪些杂质?如何改进实验装置以除去杂质? 资料2:(1)氯化氢极易溶于水,氯气在饱和食盐水中溶解度较小。(2)常见干燥剂:浓硫酸、碱石灰、NaOH(S)、CaO、无水CaCl2 等。 【活动4】除杂装置的选择。小组合作,选择合适的除杂试剂并从下列装置中选择合适的除杂装置。把所选的装置卡片用长尾夹固定在硬纸板上,以合适的顺序连接在一起: 杂质① (填杂质名称或化学式)用 试剂除去,选用的装置为 ,选择以上试剂和装置的原因 。 杂质② (填杂质名称或化学式)用 试剂除去,选用的装置为 ,选择以上试剂和装置的原因 。
任 务 三 : 实 验 室 气 体 制 备 装 置 的 思 维 模 型 【归纳】实验室气体制备装置的连接顺序和选取依据: 连接顺序 选取依据 【活动5】迁移应用:在实验室中也常采用高锰酸钾和浓盐酸反应制备氯气。高锰酸钾氧化性较强,该反应在常温下即可进行,反应的化学方程式为: 2KMnO4 + 16HCl(浓)== 2MnCl2 + 2KCl + 5Cl2 ↑ + 8H2O 请小组合作,依据以上反应原理,选择并拼接合适的实验装置。
课 堂 检 测 1.二氧化锰跟浓盐酸反应制备干燥纯净的氯气。 (1)连接上述仪器的正确顺序(填各接口处的字母):___接___;___接___;___接___;___接___。 (2)装置中,饱和食盐水的作用是____________;NaOH溶液的作用是_______________。 (3)写出下列化学反应的化学方程式: ①气体发生装置中:________________________________________________。 ②NaOH溶液中:__________________________________________________。
作业练习
1.一个国家的氯产量常被看做是化学工业发展水平的重要标志。实验室制取氯气的原理或装置不能达到实验目的的是 A.用装置甲制备氯气 B.用装置乙除去Cl2中的HCl气体 C.用装置丙干燥氯气 D.用装置丁吸收多余的氯气 2.实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气设计了如下实验装置: 仪器X的名称为 A.分液漏斗 B.圆底烧瓶 C.蒸馏烧瓶 D.长颈漏斗 3.利用下列装置能达到实验目的的是 A.利用甲装置除去氯气中混有的少量HCl B.利用乙装置稀释浓硫酸 C.利用丙装置进行喷泉实验 D.利用丁装置进行蒸发结晶 4.实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气,设计了如图实验装置。 请回答下列问题: 实验室制取Cl2的化学方程式为 。 向烧瓶里加入少量 粉末,分液漏斗中注入 。 A中盛放的是 ,其作用为 。 B中盛放的是 ,其作用为 。 D中盛放的是 ,其作用为 。
参 考 答 案 课堂检测: E; C; D; A; B; H; G; F 除Cl2中的HCl;吸收过量的氯气。 MnO2+4HCl(浓) == MnCl2+Cl2↑ + H2O; 2NaOH+Cl2 = NaCl+NaClO+H2O 作业练习: A A A 4.(1)MnO2+4HCl(浓) == MnCl2+Cl2↑ +2 H2O; (2)二氧化锰;浓盐酸。 (3)饱和食盐水;出去氯气中的氯化氢杂质。 (4)浓硫酸;干燥氯气。 (5)氢氧化钠溶液;吸收多余的氯气。
