第九单元《溶液课题2溶解度》练习题(含解析)九年级化学下册人教版
文档属性
| 名称 | 第九单元《溶液课题2溶解度》练习题(含解析)九年级化学下册人教版 |

|
|
| 格式 | docx | ||
| 文件大小 | 296.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-07 00:00:00 | ||
图片预览


文档简介
课题2 溶解度
基础闯关全练
拓展训练
1.t ℃时有一杯接近饱和的硝酸钾溶液,下列做法一定不能使其变为饱和溶液的是( )
A.恒温蒸发溶剂
B.降低溶液的温度
C.向溶液中加入硝酸钾固体
D.向溶液中加入t ℃时的硝酸钾饱和溶液
2.(2018山东菏泽东明一模)下图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息错误的是( )
A.t1 ℃时甲、乙、丙三者的溶解度相等
B.甲的溶解度受温度的影响最大
C.要使t1 ℃时甲的饱和溶液变成不饱和溶液可以采取升高温度的方法
D.t2 ℃时,往100 g水中加入90 g甲,充分搅拌后得到190 g甲的溶液
能力提升全练
拓展训练
1.已知:在温度不变时,发生如下变化:
甲溶液 乙溶液 丙溶液
下列叙述中不正确的是( )
A.乙溶液不一定是饱和溶液
B.丙溶液一定是饱和溶液
C.乙和丙溶液可能都是饱和溶液
D.将丙溶液再蒸发10 g水,析出晶体的质量一定是5 g
2.根据表中的数据,回答下列问题。
温度/℃ 0 20 40 60 80 100
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4 39.8
KNO3 13.3 31.6 63.9 110 169 246
(1)20 ℃时,称取31.6 g KNO3固体加入盛有100 g水的烧杯中,充分溶解形成的溶液是 (填“饱和”或“不饱和”)溶液。
(2)当KNO3中混有少量NaCl时,提纯KNO3所采用的方法为 。
三年模拟全练
拓展训练
1.(2018陕西西安高新一中八模,20,★★☆)40 ℃时,取等质量的a、b、c三种物质的饱和溶液于三个烧杯中,再分别蒸发同质量的水,将温度降到30 ℃,固体溶解情况如图1所示;图2为a、b、c三种物质的溶解度曲线,仔细读图,回答下列问题。
图1
图2
(1)三种物质溶解度关系为b>a>c时的温度为t,则t的取值范围是 。
(2)烧杯甲里是 物质的溶液,烧杯乙里是 物质的溶液。
(3)40 ℃时,烧杯 里溶液中水量最少。
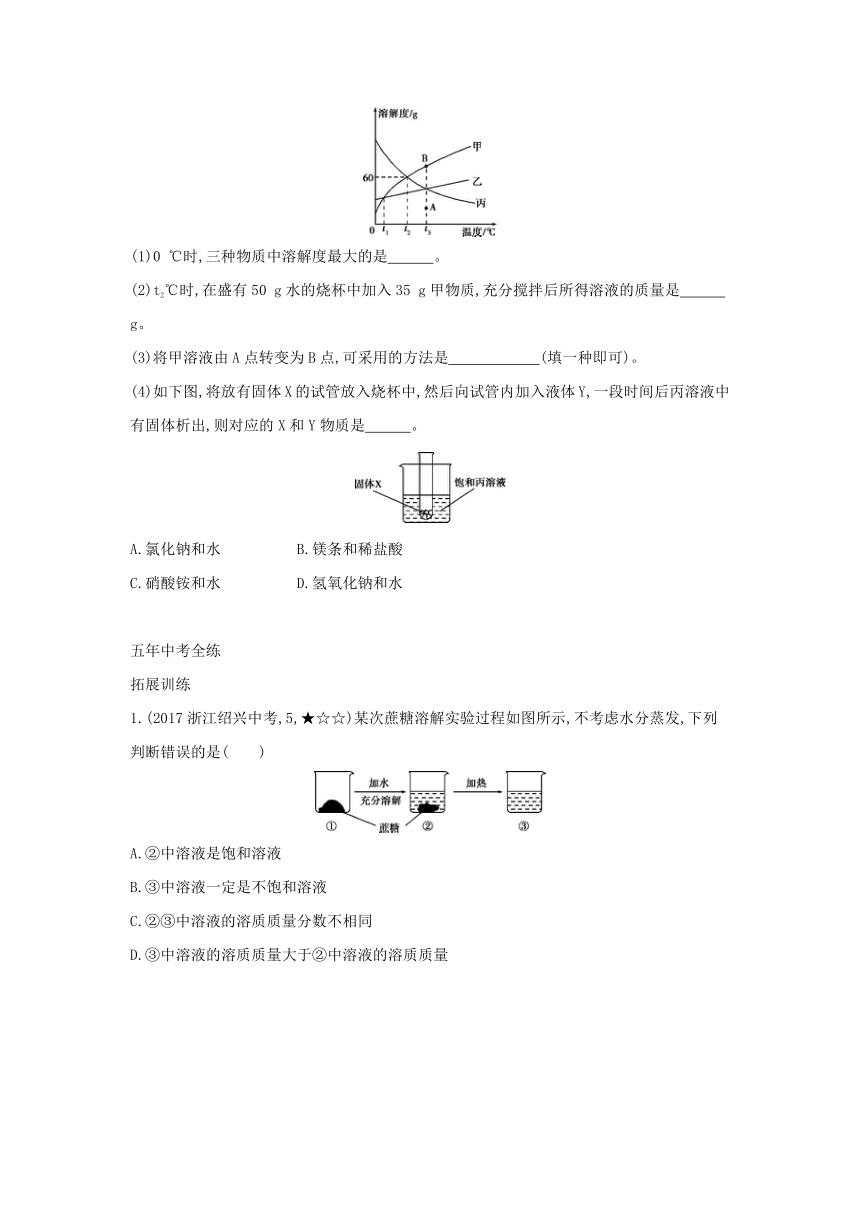
2.(2017广西南宁第八中学一模,23,★★☆)甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答:
(1)0 ℃时,三种物质中溶解度最大的是 。
(2)t2℃时,在盛有50 g水的烧杯中加入35 g甲物质,充分搅拌后所得溶液的质量是 g。
(3)将甲溶液由A点转变为B点,可采用的方法是 (填一种即可)。
(4)如下图,将放有固体X的试管放入烧杯中,然后向试管内加入液体Y,一段时间后丙溶液中有固体析出,则对应的X和Y物质是 。
A.氯化钠和水 B.镁条和稀盐酸
C.硝酸铵和水 D.氢氧化钠和水
五年中考全练
拓展训练
1.(2017浙江绍兴中考,5,★☆☆)某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是( )
A.②中溶液是饱和溶液
B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
2.(2018广东中考,18,★★☆)下图为两物质的溶解度曲线。请回答:
(1)50 ℃时Na2Cr2O7的溶解度为 g,60 ℃时溶解度:Na2Cr2O7 Na2SO4 (填“<”“=”或“>”)。
(2)在50 ℃时,把210 g Na2Cr2O7饱和溶液降温到10 ℃,析出Na2Cr2O7 g(假设不含结晶水)。
核心素养全练
拓展训练
1.科学课中,采用如下实验探究气体在水中的溶解能力。
(1)将注射器活塞拉到40 mL刻度的位置,用橡胶塞封口,慢慢推动活塞,松手后观察到 ,说明该装置气密性良好。
(2)轻轻开启一瓶汽水,用注射器吸出约13 mL汽水,再用橡胶塞封口,慢慢地往外拉注射器的活塞,观察到液体中有大量无色气泡逸出。由此实验得出的结论是
。
2.下图是一个趣味实验,请参与实验并回答问题:
将分液漏斗里适量的水加入大试管中,使足够量的氢氧化钠固体完全溶解后,能观察到的现象是 ;请解释产生上述现象的主要原因: 。
课题2 溶解度
基础闯关全练
拓展训练
1.答案 D 恒温蒸发溶剂,因溶剂减少而使不饱和溶液达到饱和;硝酸钾的溶解度随温度升高而增大,所以降低温度,可使接近饱和的硝酸钾溶液变为饱和溶液;加入一些硝酸钾固体能够使接近饱和的硝酸钾溶液变成饱和溶液;由于原溶液处于不饱和状态,加入同温度下的硝酸钾饱和溶液后,溶液仍然处于不饱和状态。
2.答案 D t1 ℃时,三种物质的溶解度曲线交于一点,所以在该温度下三种物质的溶解度相等;甲的溶解度曲线相对其他两物质更陡,所以受温度影响最大;要使t1 ℃时甲的饱和溶液变成不饱和溶液可以采取升高温度、增加溶剂等方法;t2 ℃时,甲物质的溶解度是80 g,所以在100 g水中加入90 g甲物质时,有10 g甲物质剩余,因此得到180 g溶液。
能力提升全练
拓展训练
1.答案 D 如果乙溶液是该温度下的饱和溶液,将丙溶液再蒸发10 g水,析出晶体的质量是5 g;如果乙溶液是不饱和溶液,则将丙溶液再蒸发10 g水,析出晶体的质量多于5 g,D项不正确。
2.答案 (1)饱和 (2)降温结晶(或冷却热饱和溶液)
解析 (1)根据表格中数据可知,20 ℃时,硝酸钾的溶解度为31.6 g,故称取31.6 g KNO3固体加入盛有100 g水的烧杯中,充分溶解形成的溶液是饱和溶液。(2)由于硝酸钾的溶解度受温度影响大,而氯化钠的溶解度受温度影响不大,所以提纯KNO3所采用的方法为降温结晶或冷却热饱和溶液。
三年模拟全练
拓展训练
1.答案 (1)20 ℃解析 40 ℃时,取等质量的a、b、c三种物质的饱和溶液于三个烧杯中,分别蒸发同质量的水,将温度降到30 ℃,丙中析出晶体最多,乙中没有析出晶体,结合图2可知,甲中溶液里的溶质为b,乙中溶液里的溶质为c,丙中溶液里的溶质为a。(1)由a、b、c三种物质的溶解度曲线可知,三种物质溶解度关系为b>a>c时,温度取值范围是20 ℃2.答案 (1)丙 (2)80 (3)增加溶质或恒温蒸发溶剂 (4)BD
解析 (1)结合溶解度曲线可知,0 ℃时,三种物质中溶解度最大的是丙物质。(2)t2 ℃时,甲物质的溶解度是60 g,50 g水中最多溶解30 g甲物质,故在盛有50 g水的烧杯中加入35 g甲物质,充分搅拌后所得溶液的质量是80 g。(3)A点表示t3 ℃时甲的不饱和溶液,B点表示相同温度下甲的饱和溶液,可通过增加溶质或恒温蒸发溶剂的方法将甲溶液由A点转变为B点。(4)丙物质的溶解度随温度的升高而减小,一段时间后饱和丙溶液中有固体析出,应该是X与Y混合后温度升高所致,所以选B和D。
五年中考全练
拓展训练
1.答案 B ②中有未溶解的物质,一定是饱和溶液;③中溶液可能是饱和溶液,也可能是不饱和溶液;②中溶质比③中溶质少,故②③中溶液的溶质质量分数不同;③比②中溶解的溶质多,所以③中溶液的溶质质量大于②中溶液的溶质质量。
2.答案 (1)110 > (2)50
解析 (1)据图可以看出,在50 ℃时Na2Cr2O7的溶解度为110 g,60 ℃时Na2Cr2O7的溶解度大于Na2SO4的溶解度。(2)10 ℃时Na2Cr2O7的溶解度为60 g,在50 ℃时,把210 g Na2Cr2O7饱和溶液降温到10 ℃,析出Na2Cr2O7的质量为110 g-60 g=50 g。
核心素养全练
拓展训练
1.答案 (1)活塞恢复至原位置
(2)压强减小,气体的溶解度减小
解析 本题通过一个简易装置对气体溶解性影响因素进行探究,考查了能根据实验目的,设计简单的实验,并能完成实验操作的核心素养。(1)检查装置气密性时,将注射器活塞拉到40 mL刻度的位置,用橡胶塞封口,慢慢推动活塞,松手后观察到注射器活塞回到原位置,说明气密性良好。(2)慢慢地往外拉注射器的活塞,注射器内压强减小,观察到液体中有大量无色气泡逸出,说明压强减小,气体的溶解度减小。
2.答案 U形管内a液面下降,b液面上升;烧杯内晶体减少 氢氧化钠溶于水放热,温度升高,气体压强变大
解析 本题通过对实验过程的简单分析,考查了具有实验探究精神与创新意识的核心素养。因为氢氧化钠固体溶于水要放热,所以试管中气体压强增大,大于外界大气压,所以a液面下降,b液面上升;此时硝酸钾饱和溶液的温度也升高,又因为硝酸钾溶解度随温度升高而增大,所以该溶液能继续溶解硝酸钾,故硝酸钾晶体会减少。
基础闯关全练
拓展训练
1.t ℃时有一杯接近饱和的硝酸钾溶液,下列做法一定不能使其变为饱和溶液的是( )
A.恒温蒸发溶剂
B.降低溶液的温度
C.向溶液中加入硝酸钾固体
D.向溶液中加入t ℃时的硝酸钾饱和溶液
2.(2018山东菏泽东明一模)下图是甲、乙、丙三种物质的溶解度曲线,从图中获得的信息错误的是( )
A.t1 ℃时甲、乙、丙三者的溶解度相等
B.甲的溶解度受温度的影响最大
C.要使t1 ℃时甲的饱和溶液变成不饱和溶液可以采取升高温度的方法
D.t2 ℃时,往100 g水中加入90 g甲,充分搅拌后得到190 g甲的溶液
能力提升全练
拓展训练
1.已知:在温度不变时,发生如下变化:
甲溶液 乙溶液 丙溶液
下列叙述中不正确的是( )
A.乙溶液不一定是饱和溶液
B.丙溶液一定是饱和溶液
C.乙和丙溶液可能都是饱和溶液
D.将丙溶液再蒸发10 g水,析出晶体的质量一定是5 g
2.根据表中的数据,回答下列问题。
温度/℃ 0 20 40 60 80 100
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4 39.8
KNO3 13.3 31.6 63.9 110 169 246
(1)20 ℃时,称取31.6 g KNO3固体加入盛有100 g水的烧杯中,充分溶解形成的溶液是 (填“饱和”或“不饱和”)溶液。
(2)当KNO3中混有少量NaCl时,提纯KNO3所采用的方法为 。
三年模拟全练
拓展训练
1.(2018陕西西安高新一中八模,20,★★☆)40 ℃时,取等质量的a、b、c三种物质的饱和溶液于三个烧杯中,再分别蒸发同质量的水,将温度降到30 ℃,固体溶解情况如图1所示;图2为a、b、c三种物质的溶解度曲线,仔细读图,回答下列问题。
图1
图2
(1)三种物质溶解度关系为b>a>c时的温度为t,则t的取值范围是 。
(2)烧杯甲里是 物质的溶液,烧杯乙里是 物质的溶液。
(3)40 ℃时,烧杯 里溶液中水量最少。
2.(2017广西南宁第八中学一模,23,★★☆)甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答:
(1)0 ℃时,三种物质中溶解度最大的是 。
(2)t2℃时,在盛有50 g水的烧杯中加入35 g甲物质,充分搅拌后所得溶液的质量是 g。
(3)将甲溶液由A点转变为B点,可采用的方法是 (填一种即可)。
(4)如下图,将放有固体X的试管放入烧杯中,然后向试管内加入液体Y,一段时间后丙溶液中有固体析出,则对应的X和Y物质是 。
A.氯化钠和水 B.镁条和稀盐酸
C.硝酸铵和水 D.氢氧化钠和水
五年中考全练
拓展训练
1.(2017浙江绍兴中考,5,★☆☆)某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是( )
A.②中溶液是饱和溶液
B.③中溶液一定是不饱和溶液
C.②③中溶液的溶质质量分数不相同
D.③中溶液的溶质质量大于②中溶液的溶质质量
2.(2018广东中考,18,★★☆)下图为两物质的溶解度曲线。请回答:
(1)50 ℃时Na2Cr2O7的溶解度为 g,60 ℃时溶解度:Na2Cr2O7 Na2SO4 (填“<”“=”或“>”)。
(2)在50 ℃时,把210 g Na2Cr2O7饱和溶液降温到10 ℃,析出Na2Cr2O7 g(假设不含结晶水)。
核心素养全练
拓展训练
1.科学课中,采用如下实验探究气体在水中的溶解能力。
(1)将注射器活塞拉到40 mL刻度的位置,用橡胶塞封口,慢慢推动活塞,松手后观察到 ,说明该装置气密性良好。
(2)轻轻开启一瓶汽水,用注射器吸出约13 mL汽水,再用橡胶塞封口,慢慢地往外拉注射器的活塞,观察到液体中有大量无色气泡逸出。由此实验得出的结论是
。
2.下图是一个趣味实验,请参与实验并回答问题:
将分液漏斗里适量的水加入大试管中,使足够量的氢氧化钠固体完全溶解后,能观察到的现象是 ;请解释产生上述现象的主要原因: 。
课题2 溶解度
基础闯关全练
拓展训练
1.答案 D 恒温蒸发溶剂,因溶剂减少而使不饱和溶液达到饱和;硝酸钾的溶解度随温度升高而增大,所以降低温度,可使接近饱和的硝酸钾溶液变为饱和溶液;加入一些硝酸钾固体能够使接近饱和的硝酸钾溶液变成饱和溶液;由于原溶液处于不饱和状态,加入同温度下的硝酸钾饱和溶液后,溶液仍然处于不饱和状态。
2.答案 D t1 ℃时,三种物质的溶解度曲线交于一点,所以在该温度下三种物质的溶解度相等;甲的溶解度曲线相对其他两物质更陡,所以受温度影响最大;要使t1 ℃时甲的饱和溶液变成不饱和溶液可以采取升高温度、增加溶剂等方法;t2 ℃时,甲物质的溶解度是80 g,所以在100 g水中加入90 g甲物质时,有10 g甲物质剩余,因此得到180 g溶液。
能力提升全练
拓展训练
1.答案 D 如果乙溶液是该温度下的饱和溶液,将丙溶液再蒸发10 g水,析出晶体的质量是5 g;如果乙溶液是不饱和溶液,则将丙溶液再蒸发10 g水,析出晶体的质量多于5 g,D项不正确。
2.答案 (1)饱和 (2)降温结晶(或冷却热饱和溶液)
解析 (1)根据表格中数据可知,20 ℃时,硝酸钾的溶解度为31.6 g,故称取31.6 g KNO3固体加入盛有100 g水的烧杯中,充分溶解形成的溶液是饱和溶液。(2)由于硝酸钾的溶解度受温度影响大,而氯化钠的溶解度受温度影响不大,所以提纯KNO3所采用的方法为降温结晶或冷却热饱和溶液。
三年模拟全练
拓展训练
1.答案 (1)20 ℃
解析 (1)结合溶解度曲线可知,0 ℃时,三种物质中溶解度最大的是丙物质。(2)t2 ℃时,甲物质的溶解度是60 g,50 g水中最多溶解30 g甲物质,故在盛有50 g水的烧杯中加入35 g甲物质,充分搅拌后所得溶液的质量是80 g。(3)A点表示t3 ℃时甲的不饱和溶液,B点表示相同温度下甲的饱和溶液,可通过增加溶质或恒温蒸发溶剂的方法将甲溶液由A点转变为B点。(4)丙物质的溶解度随温度的升高而减小,一段时间后饱和丙溶液中有固体析出,应该是X与Y混合后温度升高所致,所以选B和D。
五年中考全练
拓展训练
1.答案 B ②中有未溶解的物质,一定是饱和溶液;③中溶液可能是饱和溶液,也可能是不饱和溶液;②中溶质比③中溶质少,故②③中溶液的溶质质量分数不同;③比②中溶解的溶质多,所以③中溶液的溶质质量大于②中溶液的溶质质量。
2.答案 (1)110 > (2)50
解析 (1)据图可以看出,在50 ℃时Na2Cr2O7的溶解度为110 g,60 ℃时Na2Cr2O7的溶解度大于Na2SO4的溶解度。(2)10 ℃时Na2Cr2O7的溶解度为60 g,在50 ℃时,把210 g Na2Cr2O7饱和溶液降温到10 ℃,析出Na2Cr2O7的质量为110 g-60 g=50 g。
核心素养全练
拓展训练
1.答案 (1)活塞恢复至原位置
(2)压强减小,气体的溶解度减小
解析 本题通过一个简易装置对气体溶解性影响因素进行探究,考查了能根据实验目的,设计简单的实验,并能完成实验操作的核心素养。(1)检查装置气密性时,将注射器活塞拉到40 mL刻度的位置,用橡胶塞封口,慢慢推动活塞,松手后观察到注射器活塞回到原位置,说明气密性良好。(2)慢慢地往外拉注射器的活塞,注射器内压强减小,观察到液体中有大量无色气泡逸出,说明压强减小,气体的溶解度减小。
2.答案 U形管内a液面下降,b液面上升;烧杯内晶体减少 氢氧化钠溶于水放热,温度升高,气体压强变大
解析 本题通过对实验过程的简单分析,考查了具有实验探究精神与创新意识的核心素养。因为氢氧化钠固体溶于水要放热,所以试管中气体压强增大,大于外界大气压,所以a液面下降,b液面上升;此时硝酸钾饱和溶液的温度也升高,又因为硝酸钾溶解度随温度升高而增大,所以该溶液能继续溶解硝酸钾,故硝酸钾晶体会减少。
同课章节目录
