2023—2024学年人教版(五四学制)化学九年级全一册第3单元 酸和碱 期中训练(含答案)
文档属性
| 名称 | 2023—2024学年人教版(五四学制)化学九年级全一册第3单元 酸和碱 期中训练(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 364.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-07 00:00:00 | ||
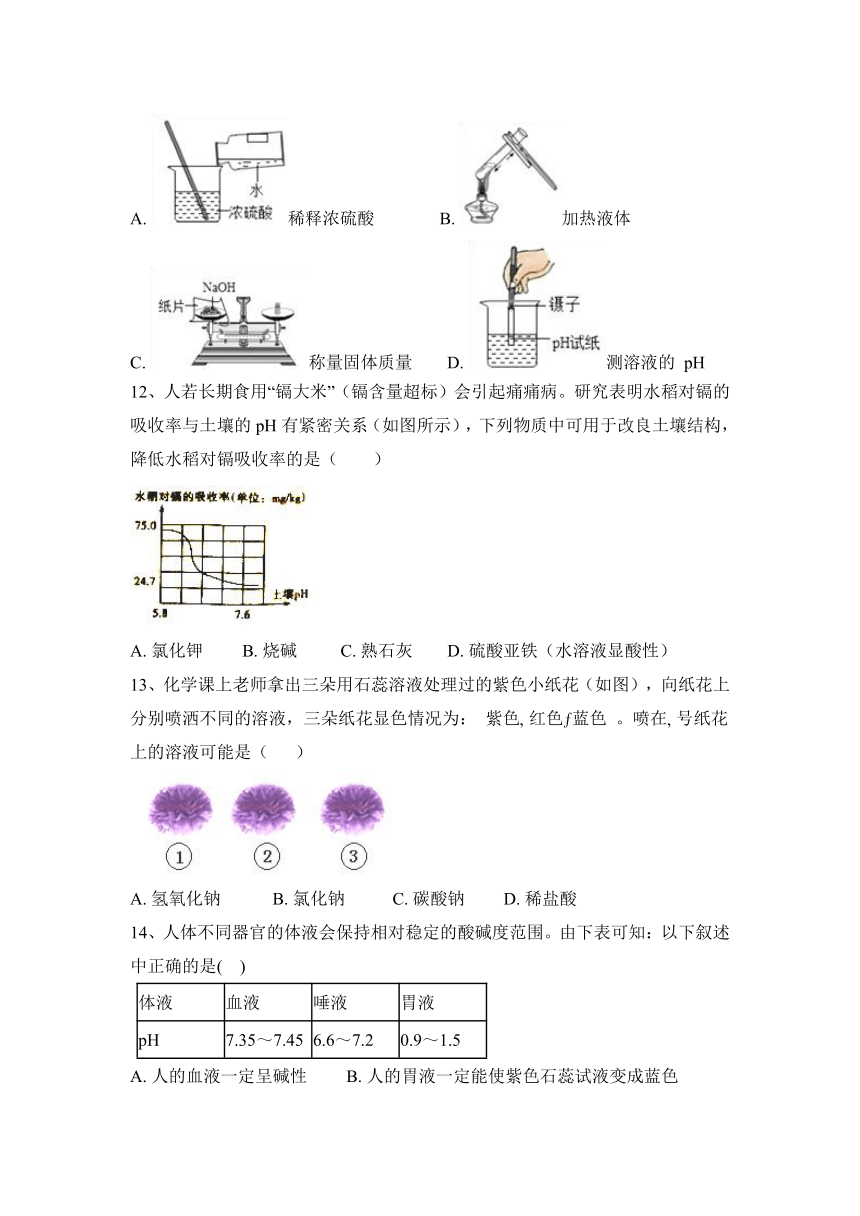
图片预览




文档简介
2023—2024学年人教版(五四学制)化学九年级全一册第3单元 酸和碱 期中训练含答案
人教版(五四学制)第3单元 酸和碱
一、选择题。
1、下列物质发生的变化与空气的成分无关的是( )
A. 钢铁在空气中生锈 B. 生石灰在空气中变质
C. 烧碱固体在空气中潮解、变质 D. 碳酸氢铵露置在空气中质量减少
2、某学生在检验某溶液是否显酸性时,取出少量该溶液进行如下实验,其中错误的做法是( )
A. 滴入紫色的石蕊试液 B. 用嘴品尝
C. 滴入Na2CO3溶液 D. 加入锌粒
3、下列物质分别放入水里,滴加无色酚酞试液能变红的是( )
A. 生石灰 B. 食盐 C. 硫酸铜 D. 氢氧化铜
4、下列叙述中正确的是( )
A. 能使石蕊试液变蓝的溶液一定是碱溶液
B. 可用酚酞试液鉴别酸性溶液和中性溶液
C. pH小于7的溶液是酸的溶液
D. 碱溶液一定是碱性溶液
5、下列关于氢氧化钠的描述中错误的是( )
A. 易溶于水,溶解时放出大量的热 B. 对皮肤具有强烈的腐蚀作用
C. 水溶液能使石蕊溶液变红 D. 能去油污,可作炉具清洁剂
6、用焊锡进行焊接时,为了清除金属表面的锈,焊接处要滴几滴( )
A. 食盐 B. 盐酸 C. 蒸馏水 D. 烧碱
7、生活中常见的物质pH大于7的是( )
A. 蔗糖溶液 B. 肥皂水 C. 食醋 D. 食盐水
8、某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的关系如图,下列说法正确的是( )
A. HCl和MgCl2一定存在
B. NaOH、H2SO4和MgCl2一定不存在
C. HCl和H2SO4一定存在
D. HCl一定存在,NaOH、H2SO4一定不存在,MgCl2可能存在
9、下列实验操作中,正确的是( )
A. 闻气味 B. 滴加液体
C. 加热液体 D. 测溶液pH
10、多数食品容易吸收空气的水分变潮湿,并与空气的氧气反应而腐败:生产上多在食品中放入一小包CaO[CaO+H2O=Ca(OH)2]或铁粉(包在多孔泡沫中),铁粉吸收水分和氧气变为铁锈,从而保护食品。下列说法不正确的是( )
A. 两种干燥剂袋上都要有明显的“勿食”字样
B. 铁粉干燥剂能和水与氧气发生化学反应
C. CaO干燥剂在空气中只与水发生反应
D. 生成的铁锈是一种混合物
11、下图实验操作中,正确的是( )
A. 稀释浓硫酸 B. 加热液体
C. 称量固体质量 D. 测溶液的 pH
12、人若长期食用“镉大米”(镉含量超标)会引起痛痛病。研究表明水稻对镉的吸收率与土壤的pH有紧密关系(如图所示),下列物质中可用于改良土壤结构,降低水稻对镉吸收率的是( )
A. 氯化钾 B. 烧碱 C. 熟石灰 D. 硫酸亚铁(水溶液显酸性)
13、化学课上老师拿出三朵用石蕊溶液处理过的紫色小纸花(如图),向纸花上分别喷洒不同的溶液,三朵纸花显色情况为: 紫色 红色 蓝色 。喷在 号纸花上的溶液可能是( )
A. 氢氧化钠 B. 氯化钠 C. 碳酸钠 D. 稀盐酸
14、人体不同器官的体液会保持相对稳定的酸碱度范围。由下表可知:以下叙述中正确的是( )
体液 血液 唾液 胃液
pH 7.35~7.45 6.6~7.2 0.9~1.5
A. 人的血液一定呈碱性 B. 人的胃液一定能使紫色石蕊试液变成蓝色
C. 人的唾液一定呈酸性 D. 用pH试纸能精确测定以上体液的pH
15、小明同学取生活中的四种物质,测得其pH如下表所示,其中酸性最强的是( )
物质 矿泉水 雨水 橙汁 蔗糖水
PH 7.3 5.8 3.6 7.0
A. 矿泉水 B. 雨水 C. 橙汁 D. 蔗糖水
*16、下列物质露置在空气中一段时间后,质量不会发生变化的是( )
A. 生石灰 B. 氯化钠 C. 浓硫酸 D. 浓盐酸
二、填空题。
17、结合NaOH、Ca(OH)2的相关知识,回答下列问题:
(1)可用来改变酸性土壤的固体是________ ;
(2)从微观角度看,它们的溶液具有相似化学性质的原因是________ ;
(3)除去NaOH溶液中混有的少量Ca(OH)2,可选用的试剂是________ 。
18、在清洗餐具时常加入少量洗涤剂,这是因为洗涤剂具有________功能;碱性洗发水易去油污,但对头发有损坏,于是人们通常用洗发水洗净头发后,再用护发素护理,由此可知护发素的pH________ 7。(填“>”、“<”或“=”)
19、氢氧化钠溶液逐滴滴入硫酸铜、硫酸混合溶液中,生成沉淀随滴入氢氧化钠溶液的变化如图所示。
(1)OA 段溶液中溶质是________ 。
(2)AB 段溶液中溶质是________ 。
(3)BC 段溶液中溶质是________ 。
20、实验兴趣小组同学要测定某土壤的酸碱性。
(1)取土壤样品,加入足量的水搅拌,静置后过滤。在实验室里过滤需要用到的玻璃仪器有________、漏斗和玻璃棒。
(2)用玻璃棒蘸取少量待测液滴在pH试纸上,与比色卡对照后得出pH<7,则该片土壤显________性,为调节土壤的酸碱性,可以向土壤中撒适量的________。
21、选择H、C、Cl、S 、O、Ca六种元素中的适当元素,组成符合下列要求的物质,将化学式填在空格中:
(1)相对分子质量最小的氧化物
(2)用于改良酸性土壤的碱
(3)实验室中用来干燥CO2气体的干燥剂
三、推断题。
22、如图所示,“﹣”表示相连物质之间能发生化学反应,请回答下列问题。
(1)反应③的现象是 。
(2)反应①的基本反应类型是 。
(3)H2SO4可以直接转化为CuSO4,写出转化的化学方程式:
。(写一个即可)
(4)反应④可证明Fe的活动性比Cu强,选用下列各组试剂进行实验时,不能验证此结论的是 (填字母)
A Cu、FeCl2溶液 B Fe、Cu、稀盐酸
C Fe、Cu、ZnSO4溶液 D Fe、CuCl2溶液
四、实验题。
23、实验中学同学开展了如下“溶液酸碱性的检验”的实验活动,根据图1、图2回答下列问题:
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
溶液 白醋 盐酸 食盐水 草木灰水 石灰水
加入紫薯汁后的颜色 红色 红色 紫色 绿色 绿色
①据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是________。
②若将盐酸逐滴滴入滴有紫薯汁的石灰水中直至过量,你看到的溶液颜色变化过程是________ ,发生反应的化学方程式为________ 。
(2)图2是三位同学分别测定土壤酸碱度的操作示意图,可能导致所测溶液pH数值发生改变的错误操作是(填“A”、“B”或“C”)________。
五、科学探究题。
24、中和反应是化学核心概念之一。某化学兴趣小组欲对“NaOH溶液与稀盐酸是否会发生反应”进行探究,设计并完成了如下实验:
【实验步骤】
步骤一:取一定量稀氢氧化钠溶液于烧杯中,滴加2滴酚酞溶液,溶液呈红色,如图1所示。
步骤二:用滴管吸取稀盐酸向烧杯中逐滴加入,边滴加边用玻璃棒搅拌,红色刚刚褪去,停止滴加。
步骤三:取适量烧杯中的无色溶液,加热蒸发得到白色固体。
【实验分析】
(1)实验中酚酞溶液的作用是___________,小明认为实验过程中不宜用紫色石蕊溶液代替酚酞溶液,可能原因是___________。
(2)兴趣小组中有同学认为也可能是滴入的稀盐酸将溶液中的酚酞反应掉,于是他们又取烧杯中的无色溶液,滴加___________ ,消除了该同学的疑惑。
(3)为确认步骤三中的白色固体是氯化钠而不是氢氧化钠,进行如下实验:
步骤 现象 结论
将白色固体溶于水形成溶液,均分成两等份 向其中一份滴加________溶液,振荡、静置 无蓝色沉淀生成 白色固体不是NaOH
向另一份滴加AgNO3溶液,振荡、静置 出现白色沉淀 白色固体是NaCl
写出上述过程中发生中和反应的化学方程式_____________。
(4)电导率是衡量溶液导电能力大小的物理量,在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比,兴趣小组用电导率传感器测氢氧化钠溶液中滴加稀盐酸的电导率变化(如图2)
【分析与讨论】
①OM段曲线下降的原因是___________
___________
___________ 。
②上述图2中的反应在___________点停止。
③N点时溶液中的离子数___________(填“小于”、“等于”或“大于”)P点时溶液中的离子数。
2023—2024学年人教版(五四学制)化学九年级全一册第3单元 酸和碱 期中训练含答案
人教版(五四学制)第3单元 酸和碱
一、选择题。
1、下列物质发生的变化与空气的成分无关的是( )
A. 钢铁在空气中生锈 B. 生石灰在空气中变质
C. 烧碱固体在空气中潮解、变质 D. 碳酸氢铵露置在空气中质量减少
【答案】D
2、某学生在检验某溶液是否显酸性时,取出少量该溶液进行如下实验,其中错误的做法是( )
A. 滴入紫色的石蕊试液 B. 用嘴品尝
C. 滴入Na2CO3溶液 D. 加入锌粒
【答案】B
3、下列物质分别放入水里,滴加无色酚酞试液能变红的是( )
A. 生石灰 B. 食盐 C. 硫酸铜 D. 氢氧化铜
【答案】A
4、下列叙述中正确的是( )
A. 能使石蕊试液变蓝的溶液一定是碱溶液
B. 可用酚酞试液鉴别酸性溶液和中性溶液
C. pH小于7的溶液是酸的溶液
D. 碱溶液一定是碱性溶液
【答案】 D
5、下列关于氢氧化钠的描述中错误的是( )
A. 易溶于水,溶解时放出大量的热 B. 对皮肤具有强烈的腐蚀作用
C. 水溶液能使石蕊溶液变红 D. 能去油污,可作炉具清洁剂
【答案】C
6、用焊锡进行焊接时,为了清除金属表面的锈,焊接处要滴几滴( )
A. 食盐 B. 盐酸 C. 蒸馏水 D. 烧碱
【答案】B
7、生活中常见的物质pH大于7的是( )
A. 蔗糖溶液 B. 肥皂水 C. 食醋 D. 食盐水
【答案】B
8、某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的关系如图,下列说法正确的是( )
A. HCl和MgCl2一定存在
B. NaOH、H2SO4和MgCl2一定不存在
C. HCl和H2SO4一定存在
D. HCl一定存在,NaOH、H2SO4一定不存在,MgCl2可能存在
【答案】A
9、下列实验操作中,正确的是( )
A. 闻气味 B. 滴加液体
C. 加热液体 D. 测溶液pH
【答案】C
10、多数食品容易吸收空气的水分变潮湿,并与空气的氧气反应而腐败:生产上多在食品中放入一小包CaO[CaO+H2O=Ca(OH)2]或铁粉(包在多孔泡沫中),铁粉吸收水分和氧气变为铁锈,从而保护食品。下列说法不正确的是( )
A. 两种干燥剂袋上都要有明显的“勿食”字样
B. 铁粉干燥剂能和水与氧气发生化学反应
C. CaO干燥剂在空气中只与水发生反应
D. 生成的铁锈是一种混合物
【答案】C
11、下图实验操作中,正确的是( )
A. 稀释浓硫酸 B. 加热液体
C. 称量固体质量 D. 测溶液的 pH
【答案】B
12、人若长期食用“镉大米”(镉含量超标)会引起痛痛病。研究表明水稻对镉的吸收率与土壤的pH有紧密关系(如图所示),下列物质中可用于改良土壤结构,降低水稻对镉吸收率的是( )
A. 氯化钾 B. 烧碱 C. 熟石灰 D. 硫酸亚铁(水溶液显酸性)
【答案】C
13、化学课上老师拿出三朵用石蕊溶液处理过的紫色小纸花(如图),向纸花上分别喷洒不同的溶液,三朵纸花显色情况为: 紫色 红色 蓝色 。喷在 号纸花上的溶液可能是( )
A. 氢氧化钠 B. 氯化钠 C. 碳酸钠 D. 稀盐酸
【答案】D
14、人体不同器官的体液会保持相对稳定的酸碱度范围。由下表可知:以下叙述中正确的是( )
体液 血液 唾液 胃液
pH 7.35~7.45 6.6~7.2 0.9~1.5
A. 人的血液一定呈碱性 B. 人的胃液一定能使紫色石蕊试液变成蓝色
C. 人的唾液一定呈酸性 D. 用pH试纸能精确测定以上体液的pH
【答案】A
15、小明同学取生活中的四种物质,测得其pH如下表所示,其中酸性最强的是( )
物质 矿泉水 雨水 橙汁 蔗糖水
PH 7.3 5.8 3.6 7.0
A. 矿泉水 B. 雨水 C. 橙汁 D. 蔗糖水
【答案】C
*16、下列物质露置在空气中一段时间后,质量不会发生变化的是( )
A. 生石灰 B. 氯化钠 C. 浓硫酸 D. 浓盐酸
【答案】B
二、填空题。
17、结合NaOH、Ca(OH)2的相关知识,回答下列问题:
(1)可用来改变酸性土壤的固体是________ ;
(2)从微观角度看,它们的溶液具有相似化学性质的原因是________ ;
(3)除去NaOH溶液中混有的少量Ca(OH)2,可选用的试剂是________ 。
【答案】氢氧化钙;都含有氢氧根离子;碳酸钠
18、在清洗餐具时常加入少量洗涤剂,这是因为洗涤剂具有________功能;碱性洗发水易去油污,但对头发有损坏,于是人们通常用洗发水洗净头发后,再用护发素护理,由此可知护发素的pH________ 7。(填“>”、“<”或“=”)
【答案】乳化;<
19、氢氧化钠溶液逐滴滴入硫酸铜、硫酸混合溶液中,生成沉淀随滴入氢氧化钠溶液的变化如图所示。
(1)OA 段溶液中溶质是________ 。
(2)AB 段溶液中溶质是________ 。
(3)BC 段溶液中溶质是________ 。
【答案】(1)Na2SO4、CuSO4、H2SO4
(2)Na2SO4、CuSO4 (3)Na2SO4、NaOH
20、实验兴趣小组同学要测定某土壤的酸碱性。
(1)取土壤样品,加入足量的水搅拌,静置后过滤。在实验室里过滤需要用到的玻璃仪器有________、漏斗和玻璃棒。
(2)用玻璃棒蘸取少量待测液滴在pH试纸上,与比色卡对照后得出pH<7,则该片土壤显________性,为调节土壤的酸碱性,可以向土壤中撒适量的________。
【答案】(1)烧杯 (2)酸;消石灰
21、选择H、C、Cl、S 、O、Ca六种元素中的适当元素,组成符合下列要求的物质,将化学式填在空格中:
(1)相对分子质量最小的氧化物
(2)用于改良酸性土壤的碱
(3)实验室中用来干燥CO2气体的干燥剂
【答案】H2O Ca(OH)2 H2SO4
三、推断题。
22、如图所示,“﹣”表示相连物质之间能发生化学反应,请回答下列问题。
(1)反应③的现象是 。
(2)反应①的基本反应类型是 。
(3)H2SO4可以直接转化为CuSO4,写出转化的化学方程式:
。(写一个即可)
(4)反应④可证明Fe的活动性比Cu强,选用下列各组试剂进行实验时,不能验证此结论的是 (填字母)
A Cu、FeCl2溶液 B Fe、Cu、稀盐酸
C Fe、Cu、ZnSO4溶液 D Fe、CuCl2溶液
【答案】生成蓝色沉淀 置换反应 CuO+H2SO4=CuSO4+H2O C
四、实验题。
23、实验中学同学开展了如下“溶液酸碱性的检验”的实验活动,根据图1、图2回答下列问题:
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
溶液 白醋 盐酸 食盐水 草木灰水 石灰水
加入紫薯汁后的颜色 红色 红色 紫色 绿色 绿色
①据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是________。
②若将盐酸逐滴滴入滴有紫薯汁的石灰水中直至过量,你看到的溶液颜色变化过程是________ ,发生反应的化学方程式为________ 。
(2)图2是三位同学分别测定土壤酸碱度的操作示意图,可能导致所测溶液pH数值发生改变的错误操作是(填“A”、“B”或“C”)________。
【答案】(1)红色;溶液由绿色变为紫色,最后变为红色;
Ca(OH)2+2HCl=CaCl2+2H2O
(2)C
五、科学探究题。
24、中和反应是化学核心概念之一。某化学兴趣小组欲对“NaOH溶液与稀盐酸是否会发生反应”进行探究,设计并完成了如下实验:
【实验步骤】
步骤一:取一定量稀氢氧化钠溶液于烧杯中,滴加2滴酚酞溶液,溶液呈红色,如图1所示。
步骤二:用滴管吸取稀盐酸向烧杯中逐滴加入,边滴加边用玻璃棒搅拌,红色刚刚褪去,停止滴加。
步骤三:取适量烧杯中的无色溶液,加热蒸发得到白色固体。
【实验分析】
(1)实验中酚酞溶液的作用是___________,小明认为实验过程中不宜用紫色石蕊溶液代替酚酞溶液,可能原因是___________。
(2)兴趣小组中有同学认为也可能是滴入的稀盐酸将溶液中的酚酞反应掉,于是他们又取烧杯中的无色溶液,滴加___________ ,消除了该同学的疑惑。
(3)为确认步骤三中的白色固体是氯化钠而不是氢氧化钠,进行如下实验:
步骤 现象 结论
将白色固体溶于水形成溶液,均分成两等份 向其中一份滴加________溶液,振荡、静置 无蓝色沉淀生成 白色固体不是NaOH
向另一份滴加AgNO3溶液,振荡、静置 出现白色沉淀 白色固体是NaCl
写出上述过程中发生中和反应的化学方程式_____________。
(4)电导率是衡量溶液导电能力大小的物理量,在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比,兴趣小组用电导率传感器测氢氧化钠溶液中滴加稀盐酸的电导率变化(如图2)
【分析与讨论】
①OM段曲线下降的原因是___________
___________
___________ 。
②上述图2中的反应在___________点停止。
③N点时溶液中的离子数___________(填“小于”、“等于”或“大于”)P点时溶液中的离子数。
【答案】(1)便于观察反应的进程(或通过酚酞试剂颜色的变化可以指示中和反应的发生)
石蕊溶液在碱性溶液中呈蓝色,在中性溶液中呈紫色,颜色变化不明显
(2)氢氧化钠溶液,溶液又变红色
(3)CuCl2(CuSO4、Cu(NO3)2等易溶于水的铜盐都可以)
(4)氢氧化钠溶液与盐酸反应的过程中氢氧根离子和氢离子结合生成水分子,在向氢氧化钠溶液中滴加稀盐酸的过程中,由于每反应1个OH-就会有1个C1-增加,因此离子数目不变,但溶液体积增大,使得溶液中离子的浓度降低,所以溶液电导率降低,曲线下降(合理即可)
M 大于
人教版(五四学制)第3单元 酸和碱
一、选择题。
1、下列物质发生的变化与空气的成分无关的是( )
A. 钢铁在空气中生锈 B. 生石灰在空气中变质
C. 烧碱固体在空气中潮解、变质 D. 碳酸氢铵露置在空气中质量减少
2、某学生在检验某溶液是否显酸性时,取出少量该溶液进行如下实验,其中错误的做法是( )
A. 滴入紫色的石蕊试液 B. 用嘴品尝
C. 滴入Na2CO3溶液 D. 加入锌粒
3、下列物质分别放入水里,滴加无色酚酞试液能变红的是( )
A. 生石灰 B. 食盐 C. 硫酸铜 D. 氢氧化铜
4、下列叙述中正确的是( )
A. 能使石蕊试液变蓝的溶液一定是碱溶液
B. 可用酚酞试液鉴别酸性溶液和中性溶液
C. pH小于7的溶液是酸的溶液
D. 碱溶液一定是碱性溶液
5、下列关于氢氧化钠的描述中错误的是( )
A. 易溶于水,溶解时放出大量的热 B. 对皮肤具有强烈的腐蚀作用
C. 水溶液能使石蕊溶液变红 D. 能去油污,可作炉具清洁剂
6、用焊锡进行焊接时,为了清除金属表面的锈,焊接处要滴几滴( )
A. 食盐 B. 盐酸 C. 蒸馏水 D. 烧碱
7、生活中常见的物质pH大于7的是( )
A. 蔗糖溶液 B. 肥皂水 C. 食醋 D. 食盐水
8、某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的关系如图,下列说法正确的是( )
A. HCl和MgCl2一定存在
B. NaOH、H2SO4和MgCl2一定不存在
C. HCl和H2SO4一定存在
D. HCl一定存在,NaOH、H2SO4一定不存在,MgCl2可能存在
9、下列实验操作中,正确的是( )
A. 闻气味 B. 滴加液体
C. 加热液体 D. 测溶液pH
10、多数食品容易吸收空气的水分变潮湿,并与空气的氧气反应而腐败:生产上多在食品中放入一小包CaO[CaO+H2O=Ca(OH)2]或铁粉(包在多孔泡沫中),铁粉吸收水分和氧气变为铁锈,从而保护食品。下列说法不正确的是( )
A. 两种干燥剂袋上都要有明显的“勿食”字样
B. 铁粉干燥剂能和水与氧气发生化学反应
C. CaO干燥剂在空气中只与水发生反应
D. 生成的铁锈是一种混合物
11、下图实验操作中,正确的是( )
A. 稀释浓硫酸 B. 加热液体
C. 称量固体质量 D. 测溶液的 pH
12、人若长期食用“镉大米”(镉含量超标)会引起痛痛病。研究表明水稻对镉的吸收率与土壤的pH有紧密关系(如图所示),下列物质中可用于改良土壤结构,降低水稻对镉吸收率的是( )
A. 氯化钾 B. 烧碱 C. 熟石灰 D. 硫酸亚铁(水溶液显酸性)
13、化学课上老师拿出三朵用石蕊溶液处理过的紫色小纸花(如图),向纸花上分别喷洒不同的溶液,三朵纸花显色情况为: 紫色 红色 蓝色 。喷在 号纸花上的溶液可能是( )
A. 氢氧化钠 B. 氯化钠 C. 碳酸钠 D. 稀盐酸
14、人体不同器官的体液会保持相对稳定的酸碱度范围。由下表可知:以下叙述中正确的是( )
体液 血液 唾液 胃液
pH 7.35~7.45 6.6~7.2 0.9~1.5
A. 人的血液一定呈碱性 B. 人的胃液一定能使紫色石蕊试液变成蓝色
C. 人的唾液一定呈酸性 D. 用pH试纸能精确测定以上体液的pH
15、小明同学取生活中的四种物质,测得其pH如下表所示,其中酸性最强的是( )
物质 矿泉水 雨水 橙汁 蔗糖水
PH 7.3 5.8 3.6 7.0
A. 矿泉水 B. 雨水 C. 橙汁 D. 蔗糖水
*16、下列物质露置在空气中一段时间后,质量不会发生变化的是( )
A. 生石灰 B. 氯化钠 C. 浓硫酸 D. 浓盐酸
二、填空题。
17、结合NaOH、Ca(OH)2的相关知识,回答下列问题:
(1)可用来改变酸性土壤的固体是________ ;
(2)从微观角度看,它们的溶液具有相似化学性质的原因是________ ;
(3)除去NaOH溶液中混有的少量Ca(OH)2,可选用的试剂是________ 。
18、在清洗餐具时常加入少量洗涤剂,这是因为洗涤剂具有________功能;碱性洗发水易去油污,但对头发有损坏,于是人们通常用洗发水洗净头发后,再用护发素护理,由此可知护发素的pH________ 7。(填“>”、“<”或“=”)
19、氢氧化钠溶液逐滴滴入硫酸铜、硫酸混合溶液中,生成沉淀随滴入氢氧化钠溶液的变化如图所示。
(1)OA 段溶液中溶质是________ 。
(2)AB 段溶液中溶质是________ 。
(3)BC 段溶液中溶质是________ 。
20、实验兴趣小组同学要测定某土壤的酸碱性。
(1)取土壤样品,加入足量的水搅拌,静置后过滤。在实验室里过滤需要用到的玻璃仪器有________、漏斗和玻璃棒。
(2)用玻璃棒蘸取少量待测液滴在pH试纸上,与比色卡对照后得出pH<7,则该片土壤显________性,为调节土壤的酸碱性,可以向土壤中撒适量的________。
21、选择H、C、Cl、S 、O、Ca六种元素中的适当元素,组成符合下列要求的物质,将化学式填在空格中:
(1)相对分子质量最小的氧化物
(2)用于改良酸性土壤的碱
(3)实验室中用来干燥CO2气体的干燥剂
三、推断题。
22、如图所示,“﹣”表示相连物质之间能发生化学反应,请回答下列问题。
(1)反应③的现象是 。
(2)反应①的基本反应类型是 。
(3)H2SO4可以直接转化为CuSO4,写出转化的化学方程式:
。(写一个即可)
(4)反应④可证明Fe的活动性比Cu强,选用下列各组试剂进行实验时,不能验证此结论的是 (填字母)
A Cu、FeCl2溶液 B Fe、Cu、稀盐酸
C Fe、Cu、ZnSO4溶液 D Fe、CuCl2溶液
四、实验题。
23、实验中学同学开展了如下“溶液酸碱性的检验”的实验活动,根据图1、图2回答下列问题:
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
溶液 白醋 盐酸 食盐水 草木灰水 石灰水
加入紫薯汁后的颜色 红色 红色 紫色 绿色 绿色
①据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是________。
②若将盐酸逐滴滴入滴有紫薯汁的石灰水中直至过量,你看到的溶液颜色变化过程是________ ,发生反应的化学方程式为________ 。
(2)图2是三位同学分别测定土壤酸碱度的操作示意图,可能导致所测溶液pH数值发生改变的错误操作是(填“A”、“B”或“C”)________。
五、科学探究题。
24、中和反应是化学核心概念之一。某化学兴趣小组欲对“NaOH溶液与稀盐酸是否会发生反应”进行探究,设计并完成了如下实验:
【实验步骤】
步骤一:取一定量稀氢氧化钠溶液于烧杯中,滴加2滴酚酞溶液,溶液呈红色,如图1所示。
步骤二:用滴管吸取稀盐酸向烧杯中逐滴加入,边滴加边用玻璃棒搅拌,红色刚刚褪去,停止滴加。
步骤三:取适量烧杯中的无色溶液,加热蒸发得到白色固体。
【实验分析】
(1)实验中酚酞溶液的作用是___________,小明认为实验过程中不宜用紫色石蕊溶液代替酚酞溶液,可能原因是___________。
(2)兴趣小组中有同学认为也可能是滴入的稀盐酸将溶液中的酚酞反应掉,于是他们又取烧杯中的无色溶液,滴加___________ ,消除了该同学的疑惑。
(3)为确认步骤三中的白色固体是氯化钠而不是氢氧化钠,进行如下实验:
步骤 现象 结论
将白色固体溶于水形成溶液,均分成两等份 向其中一份滴加________溶液,振荡、静置 无蓝色沉淀生成 白色固体不是NaOH
向另一份滴加AgNO3溶液,振荡、静置 出现白色沉淀 白色固体是NaCl
写出上述过程中发生中和反应的化学方程式_____________。
(4)电导率是衡量溶液导电能力大小的物理量,在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比,兴趣小组用电导率传感器测氢氧化钠溶液中滴加稀盐酸的电导率变化(如图2)
【分析与讨论】
①OM段曲线下降的原因是___________
___________
___________ 。
②上述图2中的反应在___________点停止。
③N点时溶液中的离子数___________(填“小于”、“等于”或“大于”)P点时溶液中的离子数。
2023—2024学年人教版(五四学制)化学九年级全一册第3单元 酸和碱 期中训练含答案
人教版(五四学制)第3单元 酸和碱
一、选择题。
1、下列物质发生的变化与空气的成分无关的是( )
A. 钢铁在空气中生锈 B. 生石灰在空气中变质
C. 烧碱固体在空气中潮解、变质 D. 碳酸氢铵露置在空气中质量减少
【答案】D
2、某学生在检验某溶液是否显酸性时,取出少量该溶液进行如下实验,其中错误的做法是( )
A. 滴入紫色的石蕊试液 B. 用嘴品尝
C. 滴入Na2CO3溶液 D. 加入锌粒
【答案】B
3、下列物质分别放入水里,滴加无色酚酞试液能变红的是( )
A. 生石灰 B. 食盐 C. 硫酸铜 D. 氢氧化铜
【答案】A
4、下列叙述中正确的是( )
A. 能使石蕊试液变蓝的溶液一定是碱溶液
B. 可用酚酞试液鉴别酸性溶液和中性溶液
C. pH小于7的溶液是酸的溶液
D. 碱溶液一定是碱性溶液
【答案】 D
5、下列关于氢氧化钠的描述中错误的是( )
A. 易溶于水,溶解时放出大量的热 B. 对皮肤具有强烈的腐蚀作用
C. 水溶液能使石蕊溶液变红 D. 能去油污,可作炉具清洁剂
【答案】C
6、用焊锡进行焊接时,为了清除金属表面的锈,焊接处要滴几滴( )
A. 食盐 B. 盐酸 C. 蒸馏水 D. 烧碱
【答案】B
7、生活中常见的物质pH大于7的是( )
A. 蔗糖溶液 B. 肥皂水 C. 食醋 D. 食盐水
【答案】B
8、某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的关系如图,下列说法正确的是( )
A. HCl和MgCl2一定存在
B. NaOH、H2SO4和MgCl2一定不存在
C. HCl和H2SO4一定存在
D. HCl一定存在,NaOH、H2SO4一定不存在,MgCl2可能存在
【答案】A
9、下列实验操作中,正确的是( )
A. 闻气味 B. 滴加液体
C. 加热液体 D. 测溶液pH
【答案】C
10、多数食品容易吸收空气的水分变潮湿,并与空气的氧气反应而腐败:生产上多在食品中放入一小包CaO[CaO+H2O=Ca(OH)2]或铁粉(包在多孔泡沫中),铁粉吸收水分和氧气变为铁锈,从而保护食品。下列说法不正确的是( )
A. 两种干燥剂袋上都要有明显的“勿食”字样
B. 铁粉干燥剂能和水与氧气发生化学反应
C. CaO干燥剂在空气中只与水发生反应
D. 生成的铁锈是一种混合物
【答案】C
11、下图实验操作中,正确的是( )
A. 稀释浓硫酸 B. 加热液体
C. 称量固体质量 D. 测溶液的 pH
【答案】B
12、人若长期食用“镉大米”(镉含量超标)会引起痛痛病。研究表明水稻对镉的吸收率与土壤的pH有紧密关系(如图所示),下列物质中可用于改良土壤结构,降低水稻对镉吸收率的是( )
A. 氯化钾 B. 烧碱 C. 熟石灰 D. 硫酸亚铁(水溶液显酸性)
【答案】C
13、化学课上老师拿出三朵用石蕊溶液处理过的紫色小纸花(如图),向纸花上分别喷洒不同的溶液,三朵纸花显色情况为: 紫色 红色 蓝色 。喷在 号纸花上的溶液可能是( )
A. 氢氧化钠 B. 氯化钠 C. 碳酸钠 D. 稀盐酸
【答案】D
14、人体不同器官的体液会保持相对稳定的酸碱度范围。由下表可知:以下叙述中正确的是( )
体液 血液 唾液 胃液
pH 7.35~7.45 6.6~7.2 0.9~1.5
A. 人的血液一定呈碱性 B. 人的胃液一定能使紫色石蕊试液变成蓝色
C. 人的唾液一定呈酸性 D. 用pH试纸能精确测定以上体液的pH
【答案】A
15、小明同学取生活中的四种物质,测得其pH如下表所示,其中酸性最强的是( )
物质 矿泉水 雨水 橙汁 蔗糖水
PH 7.3 5.8 3.6 7.0
A. 矿泉水 B. 雨水 C. 橙汁 D. 蔗糖水
【答案】C
*16、下列物质露置在空气中一段时间后,质量不会发生变化的是( )
A. 生石灰 B. 氯化钠 C. 浓硫酸 D. 浓盐酸
【答案】B
二、填空题。
17、结合NaOH、Ca(OH)2的相关知识,回答下列问题:
(1)可用来改变酸性土壤的固体是________ ;
(2)从微观角度看,它们的溶液具有相似化学性质的原因是________ ;
(3)除去NaOH溶液中混有的少量Ca(OH)2,可选用的试剂是________ 。
【答案】氢氧化钙;都含有氢氧根离子;碳酸钠
18、在清洗餐具时常加入少量洗涤剂,这是因为洗涤剂具有________功能;碱性洗发水易去油污,但对头发有损坏,于是人们通常用洗发水洗净头发后,再用护发素护理,由此可知护发素的pH________ 7。(填“>”、“<”或“=”)
【答案】乳化;<
19、氢氧化钠溶液逐滴滴入硫酸铜、硫酸混合溶液中,生成沉淀随滴入氢氧化钠溶液的变化如图所示。
(1)OA 段溶液中溶质是________ 。
(2)AB 段溶液中溶质是________ 。
(3)BC 段溶液中溶质是________ 。
【答案】(1)Na2SO4、CuSO4、H2SO4
(2)Na2SO4、CuSO4 (3)Na2SO4、NaOH
20、实验兴趣小组同学要测定某土壤的酸碱性。
(1)取土壤样品,加入足量的水搅拌,静置后过滤。在实验室里过滤需要用到的玻璃仪器有________、漏斗和玻璃棒。
(2)用玻璃棒蘸取少量待测液滴在pH试纸上,与比色卡对照后得出pH<7,则该片土壤显________性,为调节土壤的酸碱性,可以向土壤中撒适量的________。
【答案】(1)烧杯 (2)酸;消石灰
21、选择H、C、Cl、S 、O、Ca六种元素中的适当元素,组成符合下列要求的物质,将化学式填在空格中:
(1)相对分子质量最小的氧化物
(2)用于改良酸性土壤的碱
(3)实验室中用来干燥CO2气体的干燥剂
【答案】H2O Ca(OH)2 H2SO4
三、推断题。
22、如图所示,“﹣”表示相连物质之间能发生化学反应,请回答下列问题。
(1)反应③的现象是 。
(2)反应①的基本反应类型是 。
(3)H2SO4可以直接转化为CuSO4,写出转化的化学方程式:
。(写一个即可)
(4)反应④可证明Fe的活动性比Cu强,选用下列各组试剂进行实验时,不能验证此结论的是 (填字母)
A Cu、FeCl2溶液 B Fe、Cu、稀盐酸
C Fe、Cu、ZnSO4溶液 D Fe、CuCl2溶液
【答案】生成蓝色沉淀 置换反应 CuO+H2SO4=CuSO4+H2O C
四、实验题。
23、实验中学同学开展了如下“溶液酸碱性的检验”的实验活动,根据图1、图2回答下列问题:
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
溶液 白醋 盐酸 食盐水 草木灰水 石灰水
加入紫薯汁后的颜色 红色 红色 紫色 绿色 绿色
①据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是________。
②若将盐酸逐滴滴入滴有紫薯汁的石灰水中直至过量,你看到的溶液颜色变化过程是________ ,发生反应的化学方程式为________ 。
(2)图2是三位同学分别测定土壤酸碱度的操作示意图,可能导致所测溶液pH数值发生改变的错误操作是(填“A”、“B”或“C”)________。
【答案】(1)红色;溶液由绿色变为紫色,最后变为红色;
Ca(OH)2+2HCl=CaCl2+2H2O
(2)C
五、科学探究题。
24、中和反应是化学核心概念之一。某化学兴趣小组欲对“NaOH溶液与稀盐酸是否会发生反应”进行探究,设计并完成了如下实验:
【实验步骤】
步骤一:取一定量稀氢氧化钠溶液于烧杯中,滴加2滴酚酞溶液,溶液呈红色,如图1所示。
步骤二:用滴管吸取稀盐酸向烧杯中逐滴加入,边滴加边用玻璃棒搅拌,红色刚刚褪去,停止滴加。
步骤三:取适量烧杯中的无色溶液,加热蒸发得到白色固体。
【实验分析】
(1)实验中酚酞溶液的作用是___________,小明认为实验过程中不宜用紫色石蕊溶液代替酚酞溶液,可能原因是___________。
(2)兴趣小组中有同学认为也可能是滴入的稀盐酸将溶液中的酚酞反应掉,于是他们又取烧杯中的无色溶液,滴加___________ ,消除了该同学的疑惑。
(3)为确认步骤三中的白色固体是氯化钠而不是氢氧化钠,进行如下实验:
步骤 现象 结论
将白色固体溶于水形成溶液,均分成两等份 向其中一份滴加________溶液,振荡、静置 无蓝色沉淀生成 白色固体不是NaOH
向另一份滴加AgNO3溶液,振荡、静置 出现白色沉淀 白色固体是NaCl
写出上述过程中发生中和反应的化学方程式_____________。
(4)电导率是衡量溶液导电能力大小的物理量,在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比,兴趣小组用电导率传感器测氢氧化钠溶液中滴加稀盐酸的电导率变化(如图2)
【分析与讨论】
①OM段曲线下降的原因是___________
___________
___________ 。
②上述图2中的反应在___________点停止。
③N点时溶液中的离子数___________(填“小于”、“等于”或“大于”)P点时溶液中的离子数。
【答案】(1)便于观察反应的进程(或通过酚酞试剂颜色的变化可以指示中和反应的发生)
石蕊溶液在碱性溶液中呈蓝色,在中性溶液中呈紫色,颜色变化不明显
(2)氢氧化钠溶液,溶液又变红色
(3)CuCl2(CuSO4、Cu(NO3)2等易溶于水的铜盐都可以)
(4)氢氧化钠溶液与盐酸反应的过程中氢氧根离子和氢离子结合生成水分子,在向氢氧化钠溶液中滴加稀盐酸的过程中,由于每反应1个OH-就会有1个C1-增加,因此离子数目不变,但溶液体积增大,使得溶液中离子的浓度降低,所以溶液电导率降低,曲线下降(合理即可)
M 大于
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
